 香菇论文.docx
香菇论文.docx
- 文档编号:9919299
- 上传时间:2023-02-07
- 格式:DOCX
- 页数:16
- 大小:104.38KB
香菇论文.docx
《香菇论文.docx》由会员分享,可在线阅读,更多相关《香菇论文.docx(16页珍藏版)》请在冰豆网上搜索。
香菇论文
发酵涉及到微生物学、生物化学及发酵工艺学知识。
要想获得高产,对生产菌的生活规律要充分了解。
除了生产经验外,还需要科学的检测手段。
一、按投料方式分
微生物培养有三种方式,分批、连续培养和分批补料。
二、按菌体生长与产物形成关系分微生物发酵过程中的动力学类型
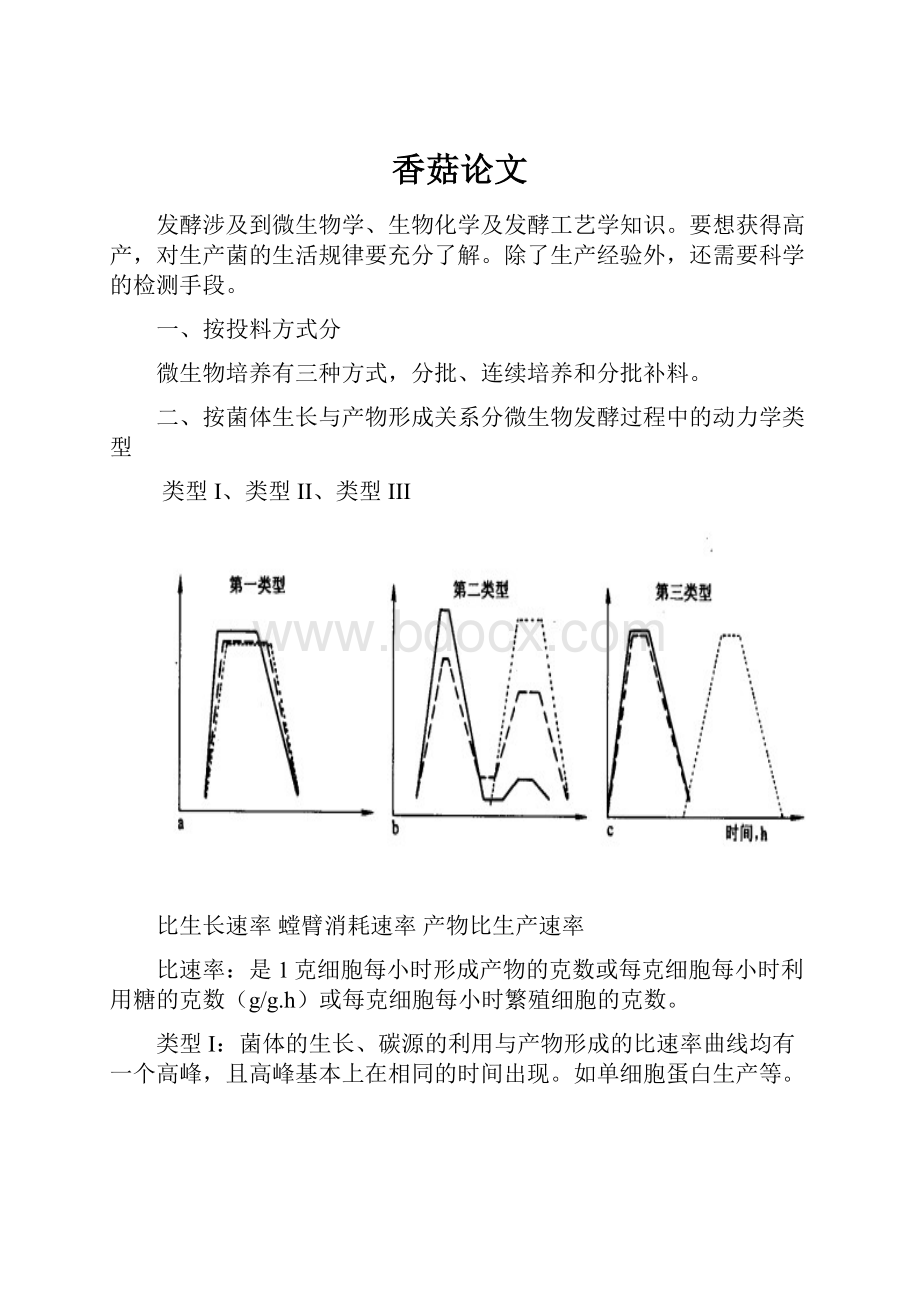
类型I、类型II、类型III
比生长速率螳臂消耗速率产物比生产速率
比速率:
是1克细胞每小时形成产物的克数或每克细胞每小时利用糖的克数(g/g.h)或每克细胞每小时繁殖细胞的克数。
类型I:
菌体的生长、碳源的利用与产物形成的比速率曲线均有一个高峰,且高峰基本上在相同的时间出现。
如单细胞蛋白生产等。
类型II:
可粗略的分为两个节段,在发酵的第一期菌体迅速生长,产物形成很少或全无,在第二个阶段产物高速形成,菌体生长和糖耗也相应增加。
如柠檬酸和某些氨基酸发酵。
类型III:
生长和产物是来自两个代谢途径,而不是来自分解代谢途径,在基质消耗和菌体生长之后,菌体利用中间代谢反应来形成产物,也就是,初级代谢和产物形成是完全分开的,如许多抗生素发酵。
工厂设备越先进,产品附加值越高,检测的参数就越多。
但工厂生产讲究越简单越好。
发酵控制一般分为物理、化学、生物三类。
一、物理参数
1.温度:
最适生长温度,它与酶反应速率,氧的溶解、产物合成都有关。
①如四环素生产菌在30℃时合成金霉素,35℃时,只产生四环素,合成方向会改变。
②生长温度与合成温度不同。
如青霉素,生长30℃,合成24.7℃。
2.压力(Pa,帕斯卡)。
98070Pa=1Kg/cm2
1Mpa﹦103Kpa=106Pa。
灭菌压力1Kg/cm2=0.11Mpa。
发酵罐压一般为0.02~0.05Mpa。
3.搅拌转速(r/min)。
罐体积转速(r/min)通风量(m3/m3.min)
50L5501:
0.6
50000L1101:
0.12
一般来说,假如小罐与大罐的几何相同。
但为什么转速会相差这么大?
原因大罐气液接触时间长,氧的溶解率高,搅拌和通气均可小些。
4.搅拌功率(KW)P/VKW/m3
生产上:
一般用瓦特计直接测量电动机的耗用功率,从中减去各项传动摩擦所损耗的功率。
对小罐,误差较大。
用电阻应变式动力计测量。
5. 通气量(V/V.min)
气体流量用转子流量计测量。
用m3/m3.min,指每分钟每立方米发酵液通进1立方米空气,用1︰1表示。
如柠檬酸1︰0.15,而青霉素1︰1。
6.粘度Pa·s(秒)Pa=1N/m2
是细胞生长和细胞形态的一项标志,它的大小可改变氧传递的阻力,又可表示相对菌体的浓度。
7.浊度:
反映单细胞生长状况的参数。
如大肠杆菌,用光密度650nm上检测或计数板计数。
8.料液流量(L/min)这是控制流体进料的参数。
1.菌丝形态:
观察菌丝形态是生产中最常用的方法。
每隔8小时镜检,
能及时发现异常染菌。
如青霉素生产,生产菌生长分为I.孢子发芽,
II.菌丝增殖,III.菌丝分枝旺盛,出现脂肪颗粒,IV.菌丝生长减缓,细胞内出现小气泡,V.气泡增大,颗粒消失,产物形成,VI.气泡延伸菌丝自溶。
2.菌体浓度:
测定方法有三种:
A.湿重法:
量100ml发酵液,进行过滤,滤后菌体用水洗净,然后用吸水纸将水分挤干,直接称量。
B.干重法:
上述步骤菌丝放85℃烘干至恒重。
C.体积法:
取样品10ml放于刻度离心管内,用转速为3000转/分离10min,计算%(V/V)。
固体原料也在其中,但如培养基组成不变条件下,具有相对准确性。
第三节菌体及基质浓度对发酵的影响及控制
3.1菌体浓度
对初级产品来说,菌浓愈大,产量愈高,但菌浓符合生长曲线。
象柠檬酸生产由糖转化成酸。
次级产品如菌浓过大,由于代谢产物的积累,会影响产量。
因其产品与原料并非对应(或底物抑制,分介产物抑制等)。
3.2基质浓度
①C源,青霉素生产中葡萄糖和乳糖利用。
因此工业上培养基中含有迅速和缓慢利用的混合C源。
如为聚合物,利用缓慢。
②N源,也有迅速利用和缓慢利用,前者有氨基酸、硫酸铵、尿素和玉米浆,后者有黄豆饼粉、花生、棉子饼粉等蛋白质。
前者菌生长快,但产量低,选用快、慢混合氮源很重要。
生产上可补加有机或无机氮源。
③磷酸盐:
P是核酸,许多辅酶,ATP,组成部分,P对微生物生长、代谢有重要作用。
工业多以供应KH2PO4、K2HPO4为磷源,配料时,KH2PO4计算,每克KH2PO4理论磷含量227毫克,如将其溶在1L水中,就是227ppm。
用链霉菌生产四环素时,菌体生长最适磷为65-70ppm,合成为25-30ppm。
测定方法:
磷与钼酸铵(NH4)2M0O4作用,生成磷钼酸铵,在酸性条件下,用VC还原,生成钼蓝,然后比色
3.3基质浓度的控制
分批补料培养(fed-batchculture,简称FBC),是指在分批培养过程中,间歇和连续地补加一种或多种成分的新鲜培养基的培养方法。
有报道四环素发酵不补料的话,培养72-96h,发酵单位5500-7000单位/mL,而补糖的批号,发酵周期延长到120-130h,单位提高到10000-12000u/ml。
中间补料的机理
①避免一次投料,菌丝生长过盛。
②延长次级代谢产物的分泌期,提高产量。
FBC的内容
①补碳源、氮源(无机和有机),如蛋白胨、玉米浆、硫酸铵、尿素。
②无机盐,微量元素,前体和促进剂。
③补全料和补水,总之视情况不同,补单项还是全部。
补料的时间和方式
补料的时间很重要,有人研究加糖时间对四环素发酵单位的影响。
接种20h45h62h
产量6000u/ml10000u/ml5000u/ml
一般认为,过早补糖,可能刺激菌丝生成,加速糖的利用,过迟补糖,可能菌丝的内在质量已受到一定损害,补糖只是干扰代谢并不能提高产量。
补料的方式:
①小量间隙多次补入。
②小量连续滴加补入。
③大量多次补入或大量少次补入等。
补料的实例:
如庆大霉素生产,大罐总体积20吨,第一次装料7吨,接种后15h一次性补5吨,然后在30-60h中小量间隙多次补入6吨料(全料),视生长情况决定是否在80h补适量水。
总周期120-130h。
微生物对氧的需求:
1、C6H12O6+6O2→6CO2+6H2O+能量
从分子式看出,180g葡萄糖完全氧化需190克O2。
2、构成细胞成分含有氧,如酵母细胞元素组成为C3.95N6.5O1.94。
O2在水中的溶解度很低。
如在25℃,1个大气压下O2溶解在水中的量为0.2mmol/L,或6.4mg/L。
而微生物需氧量20—50mmol/L.h,正常情况下,只能维持20—50秒钟,水中氧消耗完。
怎么供氧呢?
用纯O2输入发酵罐,效果好,但O2在水中的溶解度较低,大多跑了,成本高,没有实用价值。
基本概念:
1、微生物摄氧率(γ)mmolO2/(L.h)
单位体积培养液每小时消耗的氧量。
2、呼吸强度(Qo2)mmolo2/[g(干菌体).h]
单位重量的干菌体每小时消耗的氧量。
两者关系γ=Qo2.X
X—发酵液中菌体密度(g/L)。
3.临界氧浓度:
微生物对发酵液中溶解氧浓度有一个
最低要求,这个浓度叫临界氧浓度。
呼吸强度与溶氧的关系
①不同微生物C临界不同,见下表:
菌种温度.℃C临界(mg/L)
大肠杆菌37.80.26
酵母菌34.80.15
产黄青霉240.7
表明青霉菌摄氧率高,发酵时空气通气量大。
②同一种菌生长不同阶段C临界不同。
如幼龄菌大于老龄菌
另外一般生产菌都是:
生长期大于合成期的临界氧浓度。
饱和浓度:
气体与液体相接触,气体分子就会溶解于液体之中。
经过一段时间的接触,气体分子在气液两相中的浓度就会达到动态平衡。
溶解氧的饱和浓度(C*)的单位可用mmolo2/L、ppm、和mgo2/L。
影响氧饱和浓度的主要因素有:
(一)温度:
工业产品大多是随着温度升高,溶解度增加,;利用这个特点得到晶体。
如柠檬酸、葡萄糖等。
而O2正相反,温度增加,C降低。
(二)溶液的性质:
氧在不同性质的溶液中的溶解度是不同的。
同一种溶液由于其中溶质含量不同,氧的溶解度也不同。
盐酸0.5mol1mol2mol
1.211.161.12
溶质含量越高,氧的溶解度就越小。
(三)氧分压;亨利公式:
C*=H-1×Po2
C*—在平衡状态下液体中氧的溶解度(mmolo2/L)
Po2—氧分压MPa
H—亨利常数MPa×L/mmolo2
从公式中可知C*与Po2成正比。
气相中氧的浓度取决大气压和①纯氧;②罐压提高,Po2提高。
C*增大,但不能太高,纯氧也可提高。
③利用吸氮装置,减少空气中的氮气,增加氧含量。
理论上,发酵过程中:
温度越低,C*越高,
溶质越稀,C*越高,
罐压越高,C*越大。
但工业上应用都受到限制。
•N=KLa(C*—CL)
•式中
•N——氧的传递速率,mmolO2/h;
•C*——溶液中饱和溶氧浓度,mmolO2/L;
•CL——溶液主流中的溶氧浓度,mmolO2/L;
•KLa——以浓度差为推动力的氧传质系数,1/h;
•a——比表面积(单位体积溶液中所含有的气液接触面积m2/m3)。
因为a很难测定,所以将L当成一项,称为液相体积氧传递系数,1/h
•N=KLa(C*—CL)
•双膜理论:
•是气体吸收的基本理论:
P—空气中的分压;Pi—界面处氧分压;
P—Pi称为推动力(气相)
Ci—界面处氧的浓度;CL—液相中氧的浓度;
Ci—CL为液相推动力。
‘
双模的理论的气液接触
在稳定传质过程中通过双膜的传氧速率N应相等。
N=KGa(P—Pi)=KLa(Ci—CL)
由于Pi和Ci无法测量,因此改为
N=KGa(P—P*)=KLa(C*—CL)
N=KLa(C*—CL)
氧的传递速率N=KLa×(C*-CL)
影响氧传递推动力的因素:
C*-CL
1.提高C*,因素有温度、溶液、氧分压,三点都有局限性。
在抗生素生产中有时需要补水,原理使溶液稀释,C*提高。
2.降低发酵液中的CL
如降低通气量和搅拌速度可降低CL,但发酵过程中发酵液的CL不能低于C临界,否则就会影响微生物的呼吸。
影响KLa的因素
经过长时间的研究和生产实践证实,影响发酵设备的KLa。
主要因素有搅拌效率、空气流速、发酵液的物理化学性质、泡沫状态、空气分布器形状和发酵罐的结构等。
(1)搅拌的作用
A.把大气泡打碎,增加气液两相的接触面积,KLa增加;
B.降低液膜厚度,KLa增加;
C.减少菌丝结团,减少菌周围液膜阻力,并有利于排出废气;
搅拌速度(r/min)KLa摄氧率
30040576
500169720
700216864
KLa与空气流速(V)有关。
V增加KLa增加。
但当V增加到一定值后KLa便不增加,因存在所谓气泛现象,即空气流速过大时,气流形成大气泡在轴的周围逸出。
KLa与粘度成反比。
在发酵过程中,由于粘度变化,而使发酵液呈多种流变学性质(液体的湍动性和液膜的阻力)。
一般细菌、酵母发酵液粘度为一常数。
放线菌、霉菌粘度不是一个常数。
复膜氧电极的原理
溶氧电极可以看作是一种电解电池,它有两只具有不同电性的电极,一只是银丝做成的阴极,另一只是铅皮卷成的阳极。
这对电极装置在两端开口的细的玻璃套管内,在靠近阴极的一端用一种耐热的、只允许气体透过而不透过水及离子的半渗透塑料膜覆盖,形成一个有一定容积的电池,在电池中加入数毫升的电解质溶液(5molHAC+0.5molNaAC十0.1molPbAC2)。
这就在两极之间产生了一个电位,使阳极的铅变成铅离子Pb++进入电解质溶液,同时放出的电子在阴极上把透过半透膜进入电池的氧立即还原成OH—(见图)
铅阳极银阴极电极端部组装示意
复膜氧电极操作:
在实罐灭菌时将电极装入,灭菌后电流表指示为最低值,这时通气保压、搅拌、降温,溶氧CL会达到最大值,电流表指示为100%。
一般在抗生素生产时,接种后11个小时电流值保持一定,12小时后开始下降,43小时为最低值,随后电流值便上升。
菌的生长所需要的氧应略高于临界值。
控制溶氧浓度的方法有:
1.搅拌转速
2.进气量
3.适当降温、补水和加泡敌来改善溶氧水平。
5.1pH值对菌生长和代谢产物形成的影响。
①不同菌生长pH值不同
②改变发酵方向黑曲霉pH2-3时产柠檬酸,pH7时生成草酸。
③生长和合成pH不同如链霉素产生菌生长的最适pH为6.3-6.9,而合成pH6.7-7.3。
①改变菌膜电荷。
②直接影响酶的活性。
③影响培养基中营养物质和中间代谢产物的介离。
该物质都在水中解离,氢离子浓度对这些物质
的解离影响很大,从而影响微生物的营养吸收、
酶的活性等。
(1)调节发酵过程中由于营养物质的分解,菌的代谢等,pH值会发生变化。
调节的方法有:
①H2SO4和NaOH直接控制
②用补硫酸铵和氨水控制PH较高时补加硫酸铵。
当pH较低时补加氨水。
③可以通过补加糖或油来调节pH
(2)控制最适pH在微生物生长和产物形成的关系中有四种情况。
①比生长速率(u)和产物比生产
速率(Qp)最适pH范围较宽,
生产较易控制。
②u、Qp二者一个较宽,一个
较窄。
③二者都较窄,pH又相同。
④二者都较窄,pH又不同。
在发酵过程中,产热的因素有生物热(Q生物)和搅拌热(Q搅拌);散热因素有蒸发热(Q蒸发)、辐射热(Q辐射)。
产生的热能减去散失的热能,所得的净热量就是发酵热[Q发酵,kJ/(m3.h)],
即Q发酵=Q生物+Q搅拌-Q蒸发-Q辐射。
6.1发酵热发酵过程中产生的热能减去散失的热能,所得的净热量就是发酵热。
①生物热(Q生物)
C6H12O6+12O6→6CO+6H2O+热量,除了用于合成外,其余部分则以热的形式散发出来。
对数生长期产热量多。
热量的单位(KJ/m3.h)
②搅拌热(Q搅拌)液体与搅拌设备之间的摩擦产生的热量。
Q搅拌=P/V×3600。
(KW/m3×KJ/Kw.h)3600为热功当量。
③蒸发热(Q蒸发)通气时,引起发酵液水分的蒸发被冷空气和蒸发水分带走的热量叫蒸发热。
④辐射热(Q辐射)因发酵液温度与罐外温度不同,发酵液中有部分热通过罐体向外辐射。
由于Q生物及Q蒸发在发酵过程中是随着时间变化的,因此发酵热在整个过程中也随时间变化,发酵罐操作也需要降温、加温控制。
①通过测量一定时间内冷却水的流量和冷却水进出口温度,用下式计算:
Q发酵=G.c(t1-t2)/V单位千卡/m3.h
G—冷却水c—水的比热t1、t2—进出的冷却水温度(℃)。
V—发酵液体积(m3)
一般抗生素发酵过程中的最大发酵热均为3000-5000千卡/立方米.小时
抗生素生产,菌的生长和合成需不同温度。
有人试验青霉素变温发酵,起初5小时,维持在30℃,以后降到25℃培养35h,再降到20℃培养85h,最后又提高到25℃,培养40小时,放罐。
青霉素产量比在25℃恒温培养提高14.7%。
因此生长的温度和合成的温度并不一致。
CO2的来源和影响
CO2浓度高对微生物生长不利。
1.当细胞膜的脂质相中的CO2浓度偏高,细胞膜运输受到阻碍,生长受到抑制
2.使发酵液pH降低,影响菌生长和产物合成。
但某些菌又需要适量的CO2。
栽培金针菇菌最明显。
动物细胞培养需要CO2培养箱。
CO2能合成某些小分子前体物质如:
①丙酮酸+CO2+ATP→草酰乙酸+ADP+Pi。
②再如脂肪酸生物合成也需,如乙酰CoA+CO2→丙二酰CoA→长链脂肪酸。
8.1 泡沫的性质:
泡沫是气体分散在液体中的一种胶体系统,气泡间被一层液膜隔开而彼此不相连通。
8.2 泡沫的危害:
①造成大量的逃液,而使装料系数减少。
②泡沫从轴封中渗出,增加染菌机会。
③妨碍菌的呼吸和生长,使产量下降。
8.3泡沫产生的因素:
①与高速搅拌及大空气流量有关,发酵时前期要注意空气流量,先小后逐步加大
②培养基成份有关:
蛋白胨、玉米浆、黄豆饼粉等,高蛋白,易起泡。
③菌种不同,如有的生长慢,易起泡。
8.4泡沫的消除:
①机械消沫:
在罐内装消沫浆。
但作用不大。
②化学消沫:
A.消泡剂有天然油,豆油,菜子油等,它还作为碳源被菌利用。
B.高分子物质如聚氧乙烯氧丙烯甘油,(GPE)又叫泡敌。
消泡能力比植物油60-80倍强。
目前工业上已取代油。
8.5消泡的原理:
①.泡沫表面层存在着极性的表面活性物质,而形成双电层时,可加入另一种有相反电荷的表面活性剂,可降低其机械强度,促使其破裂。
②.泡沫表面粘度较大时,可加入某些分子内聚力较小的物质,以降低其表面粘度而使其破裂。
8.6 控制泡沫的方法
(一)减少泡沫形成的机会。
①原料配比。
②补料:
如基础料被抽出一部分蛋白质原料,在菌丝长浓后再加入。
③灭菌前加.
(二)消除已形成的泡沫。
起泡时加。
加量一般为培养基总体积的0.02%-0.002%。
多加对菌生长不利。
所谓发酵染菌是指在发酵过程中,生产菌以外的其他微生物侵入了发酵系统,从而造成生产损失。
据报道,国内的青霉素发酵染菌率2%,链霉素、红霉素和四环素发酵染菌率5%,谷氨酸发酵噬菌体感染率1%~2%。
染菌对发酵生产率、提取率、得率、产品质量和三废治理等都有很大的影响。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 香菇 论文
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《JAVA编程基础》课程标准软件16级.docx
《JAVA编程基础》课程标准软件16级.docx
