 山东省度中考一模化学试题B卷.docx
山东省度中考一模化学试题B卷.docx
- 文档编号:9763205
- 上传时间:2023-02-06
- 格式:DOCX
- 页数:12
- 大小:161.04KB
山东省度中考一模化学试题B卷.docx
《山东省度中考一模化学试题B卷.docx》由会员分享,可在线阅读,更多相关《山东省度中考一模化学试题B卷.docx(12页珍藏版)》请在冰豆网上搜索。
山东省度中考一模化学试题B卷
山东省2019-2020年度中考一模化学试题B卷
姓名:
________班级:
________成绩:
________
一、单选题
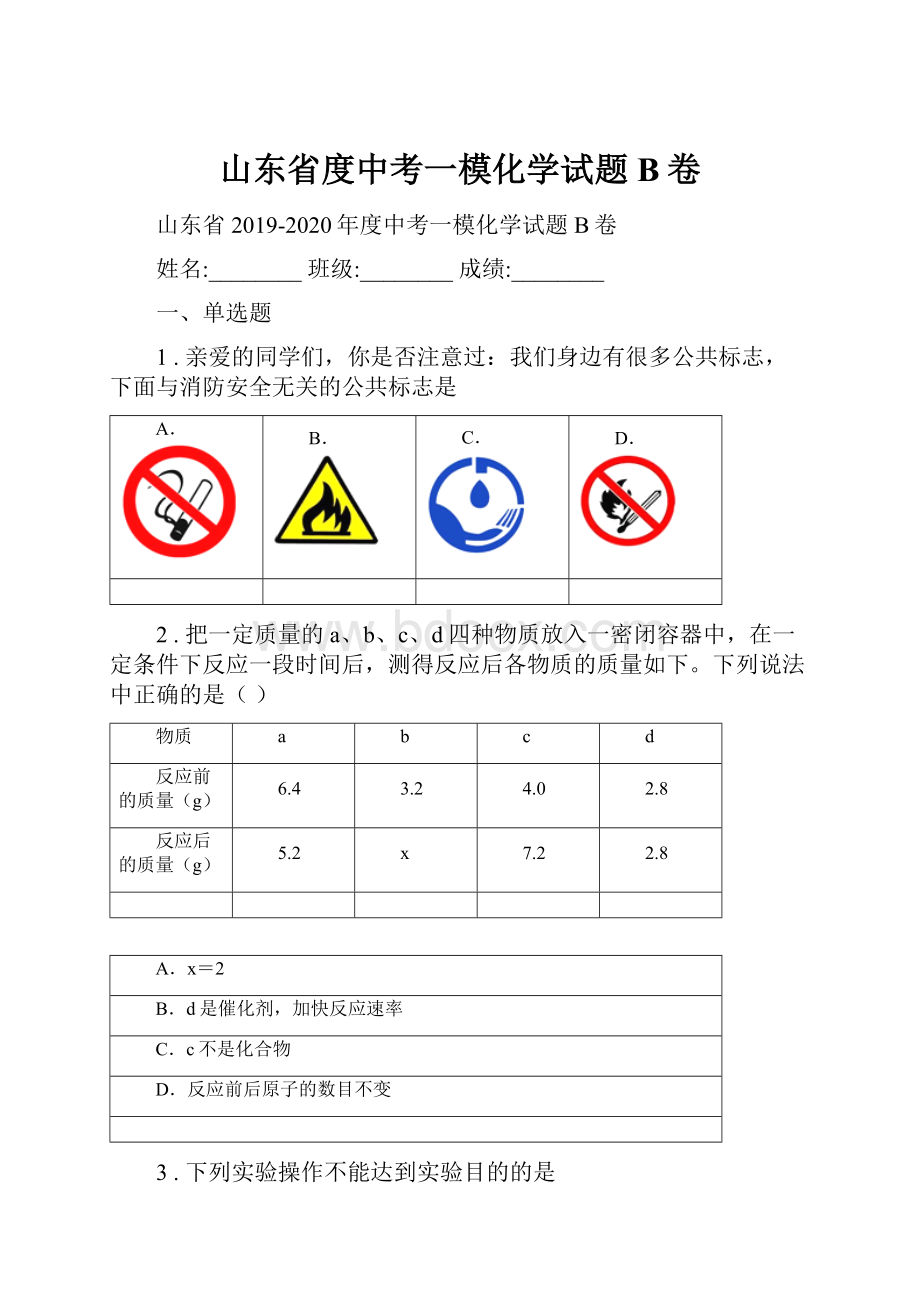
1.亲爱的同学们,你是否注意过:
我们身边有很多公共标志,下面与消防安全无关的公共标志是
A.
B.
C.
D.
2.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下。
下列说法中正确的是()
物质
a
b
c
d
反应前的质量(g)
6.4
3.2
4.0
2.8
反应后的质量(g)
5.2
x
7.2
2.8
A.x=2
B.d是催化剂,加快反应速率
C.c不是化合物
D.反应前后原子的数目不变
3.下列实验操作不能达到实验目的的是
选项
实验目的
实验操作
A
除去氮气中的少量氧气
将气体缓缓通过炽热的铜网
B
区分硝酸铵与氢氧化钠
分别取样,加入适量水
C
检验氢氧化钠溶液是否变质
取样,滴入几滴酚酞溶液
D
提纯含有少量氯化钠的硝酸钾
冷却热的饱和溶液,过滤,洗涤,干燥
A.A
B.B
C.C
D.D
4.从冰箱取出的瓶装饮料放在空气中,不久瓶的外壁出现水珠,这说明空气中含有
A.水蒸气
B.氮气
C.二氧化碳
D.氧气
5.下列各组物质是按单质、混合物的顺序排列的是
A.石墨、空气
B.水、氯酸钾
C.干冰、食盐
D.氧气、碳酸钙
6.在加热条件下,K2CrmO7[学名:
重铬酸钾,其中铬Cr的化合价为+6价]可分解为氧化铬(其中Cr为+3价]、氧化钾和另一种非金属单质x。
取一定质量的重铬酸钾固体充分加热至完全分解,测得反应后生成氧化铬、氧化钾的质量分别为15.2g和9.4g.则下列说法不正确的是
A.m=2
B.X的化学式为O2
C.生成X的质量为4.8g
D.该反应方程式中氧化铬和X的化学计量数之比为3:
2
7.下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是()
选项
实验目的
所加物质或方法
A
提纯硫酸钠中的硝酸钠
溶解、加适量的氯化钡溶液,过滤,蒸发
B
除去氧化铜中的碳粉
在足量的空气中灼烧
C
除去CO2中少量的HCl
将混合气体通入饱和碳酸氢钠溶液、再通入浓硫酸
D
鉴别NH4NO3固体和NaOH固体
加水溶解
A.A
B.B
C.C
D.D
8.生活中一些食品或用品的近似pH如下表,下列说法正确的是
食品或用品
食醋
泡菜
牙膏
草木灰
pH
2~3
3~4
8~9
10~11
A.牙膏是酸性物质
B.胃酸过多的人不宜吃泡菜
C.草木灰可降低土壤碱性
D.食醋的酸性比泡菜弱
9.下列实验操作叙述正确的是()
A.过滤时,漏斗中液面低于滤纸的边缘
B.加热蒸发过程中,当溶液蒸干时停止加热
C.酒精灯内添加的酒精量一般为1/5至4/5
D.倾倒液体时,试剂瓶口紧挨着试管口快速倒入
10.化学概念在逻辑上存在如图所示关系,对下列概念间的关系说法正确的是
A.纯净物与混合物属于包含关系
B.原子与元素属于交叉关系
C.物理变化与化学变化属于并列关系
D.氧化反应与化合反应属于并列关系
11.下列有关物质的性质与用途具有对应关系的是
A.铬耐磨、耐腐蚀,可镀在钢铁制品表面防生锈
B.石墨很软,有光泽和滑腻感,可用于制作电极
C.乙醇易挥发、易溶于水,可掺入汽油中作燃料
D.聚四氟乙烯塑料密度小,可用作不粘锅的内衬
12.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:
X
Y
Z
Q
反应前的质量/g
10
2
32
3
反应后的质量/g
2
13
待测
0
下列推理中不正确的是()
A.该反应是分解反应
B.参加反应X与Q的质量比为8:
3
C.反应中生成Y的质量为11g
D.Z不一定是该反应的催化剂
13.物质的组成和结构决定性质,性质决定用途。
下列叙述正确的是
A.生铁坚硬,可以作医疗手术器械
B.洗洁精可以加速油污溶解,可以除去油污
C.农业生产中通常用氢氧化钙改良酸性土壤
D.NH4NO3、HNO3、NH4HCO3中都含有氮元素,可用作氮肥
14.下列说法正确的是()
A.二氧化硫不会造成大气污染
B.近年来,我国许多城市禁止汽车使用含铅汽油的目的是缓解铅资源短缺
C.杜绝污染源属于“绿色化学”治理环境污染的有效措施
D.将废纸、汽水瓶等收集起来,一次性焚烧
二、填空题
15.如图所示是医院常用的药瓶和注射器,请你据图回答:
(1)含有金属材料的是______(写一种即可,下同),属于有机合成材料是______。
(2)注射器洗净后可以用于家庭小实验,可以代替______仪器使用。
(3)钢针一般用不锈钢制造,主要是由于其不容易生锈,请你写出生活中防止铁制品生锈的方法(一条即可)______。
(4)铝的金属活性比铁强,请写出铝放入硫酸亚铁溶液中反应的化学方程式______。
16.如图是五种粒子的结构示意图。
(1)A~D中,位于第一周期的元素是______________________________(填序号)
(2)A~D中,具有相对稳定结构的粒子是_____________________________(填化学符号)。
(3)C中元素的相对原子质量为23,则该元素的一个原子中微粒总数为_______________________________;
(4)E中,若m≠10+n,则n=______________________________。
17.请用化学用语填空
(1)两个氦原子_____;
(2)2个镁离子_____;
(3)保持氢气化学性质的粒子_____;
(4)碳可以与浓硫酸在加热的条件下发生如下反应:
C+2H2SO4(浓)
CO2+2X+2H2O其中X的化学式_____。
(5)汽车尾气催化转化器中发生的反应可减少有害气体排放,其反应的微观示意图如图。
从图中可知:
以上四种物质中,属于单质的是_____(用化学式表示)写出上述反应的化学方程式_____。
18.哈尔滨至大连的高铁运行已经近三个月了,为我们的出行提供了方便,也加快了速度.动车走的轨道都是无缝锰钢轨道,是因为锰钢具有 的物理性质,动车是在高电压环境下运行,其运行过程中的能量转化是 ,动车中的玻璃餐桌上玻璃花纹的雕刻原理是利用氢氟酸(HF)与玻璃中的二氧化硅(SiO2)反应,生成气态的四氟化硅和一种常见的氧化物,从而使玻璃上产生美丽图案的痕迹,请写出此反应的化学方程式 ,该反应的基本反应类型是 .
三、实验题
19.现有下图所示的实验装置,请回答问题:
(1)反应容器a的仪器名称是__________________。
(2)实验室用过氧化氢溶液和MnO2粉末制取氧气,制取装置应选用___________。
(填字母序号)
(3)在加入药品前,检查氧气制取装置气密性的方法是_____________。
(4)用过氧化氢和二氧化锰制取氧气的反应化学方程式____________________________,属于(________)反应类型。
(5)检验一瓶气体是氧气的方法是________________________________________________。
(6)甲烷(CH4)是一种无色、无味、密度比空气小且难溶于水的气体。
实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,应选择的发生装置是(填字母序号)_________,收集较为干燥的甲烷气体的收集装置是(填字母序号)__________。
20.实验室用铁片或铁粉、氧化铜、稀硫酸为原料制取铜,可选用的装置如下图所示。
科技小组同学设计了两个实验方案:
方案一:
方案二:
请回答:
①写出上图中仪器a、b的名称。
a_________________、b_________________。
②若用方案一实验,应选用图中的_________________装置(填序号);该方法制取的铜中可能含有的杂质可加_________除去。
若用方案二,氢气制取可以控制的实验装置,应选用图中的__________(填序号)。
方案一用铁粉,方案二用铁片的原因是__________________________________________。
③若用上述两个实验方案,获得相同质量的铜,则铁、氧化铜、稀硫酸三种原料中,消耗量相同的是___________,理由是__________________________________________。
四、简答题
21.回答下列与含碳物质有关的问题.
(1)金刚石和石墨物理性质不同是因为_________不同;
(2)能将CO和CO2区别开的溶液是_____;有关反应的化学方程式为________。
(3)炼铁时高炉内发生如下反应:
Fe2O3+3CO
2Fe+3CO2,其中___发生了氧化反应.
五、推断题
22.A﹣G是初中化学中的常见物质。
它们之间的关系如图所示(“→”表示物质间的转化关系,“一”表示两端的物质能发生化学反应)。
A俗称纯碱,B是光合作用不可缺少的物质,E、G是黑色粉末,F是未来最理想的清洁能源,请回答下列问题:
(1)写出化学式:
D_______。
(2)若C物质有三种元素组成,写出物质A和物质C反应的化学方程式是_______,基本类型是_______。
(3)写出测定A物质酸碱度的方法:
_______。
六、科学探究题
23.某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题。
部分钙、镁化合物溶解性表(20℃)
OH-
CO32-
HCO3-
Ca2+
微溶
不溶
可溶
Mg2+
不溶
微溶
可溶
(查阅资料)天然水中含有
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢(主要成分为碳酸盐和碱)。
有关物质的溶解性见下表:
(提出猜想)水垢的主要成分一定有CaCO3和_____(填化学式),可能含有Ca(OH)2和_____。
(设计方案)
实验1确定水垢中是否含有Ca(OH)2
实验步骤
现象
结论
在少量研体的水垢中,加入适量的蒸馏水充分搅拌、过滤,在滤液中加入Na2CO3溶液
___________
一定不含Ca(OH)2
实验2:
确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究。
其主要实验步骤如下:
称量D、E装置总质量为200.0g,按上图组装后,将2.5g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为201.25g(碱石灰主要分为CaO和NaOH,不考虑装置内空气对实验的影响)。
(实验讨论)
(1)反应结束后打开止水夹K,缓缓鼓入空气的目的是___________。
A、B装置之间__________设置干燥装置。
(填“要”或“不要”)其理由是____________。
(2)装置B盛放稀盐酸的仪器作用是_________________。
(3)装置B中生成气体的反应的化学方程式为_______________。
(4)装置B中生成CO2的质量为_________g,通过计算说明水垢中_________含MgCO3(填字母)。
A一定不 B一定 C可能 D无法确定
计算过程(已知CaCO3相对分子质量为100。
MgCO3相对分子质量为84):
___________
实验3:
确定水垢中是否有Mg(OH)2
(5)另取质量为1.25g水垢,加入3.65%稀盐酸与之反应,测得消耗稀盐酸mg,结合上述实验,判断当m的值满足____________条件时,水垢中一定含有Mg(OH)2。
写出计算过程。
七、计算题
24.H2在加热的条件下可以还原CuO()
。
某兴趣小组同学在一份资料中了解到:
铜有CuO和Cu2O(红色)两种常见的氧化物,Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。
(1)该小组同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为 。
(2)该小组在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g。
此红色固体中氧元素的质量为 ,以此推得Cu2O的质量为 。
(3)将
(2)中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:
Cu2O+2HCl═CuCl2+Cu+H2O),充分搅拌,除有红色固体外,还发现溶液变成蓝绿。
试计算此蓝色溶液中CuCl2的质量分数(精确到0.01%)。
25.苏丹红一号(C16H12NO)和苏丹红二号(C18H16N2O)都是工业合成的红色染色剂,世界上多数国家都不允许把其作为食用色素使用。
试回答:
(1)两种物质都是由 种元素组成;
(2)苏丹红一号中的C、H、N、O的原子个数比是 。
(3)计算234g苏丹红一号中氮元素质量(写出计算式,计算结果精确到0.1g)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 山东省 中考 化学试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
