 第一章 金属及其化合物第四节金属材料与矿物 铜及其化合物.docx
第一章 金属及其化合物第四节金属材料与矿物 铜及其化合物.docx
- 文档编号:9731124
- 上传时间:2023-02-06
- 格式:DOCX
- 页数:40
- 大小:278.16KB
第一章 金属及其化合物第四节金属材料与矿物 铜及其化合物.docx
《第一章 金属及其化合物第四节金属材料与矿物 铜及其化合物.docx》由会员分享,可在线阅读,更多相关《第一章 金属及其化合物第四节金属材料与矿物 铜及其化合物.docx(40页珍藏版)》请在冰豆网上搜索。
第一章金属及其化合物第四节金属材料与矿物铜及其化合物
第一章 金属及其化合物
。
第四节金属材料与矿物 铜及其化合物
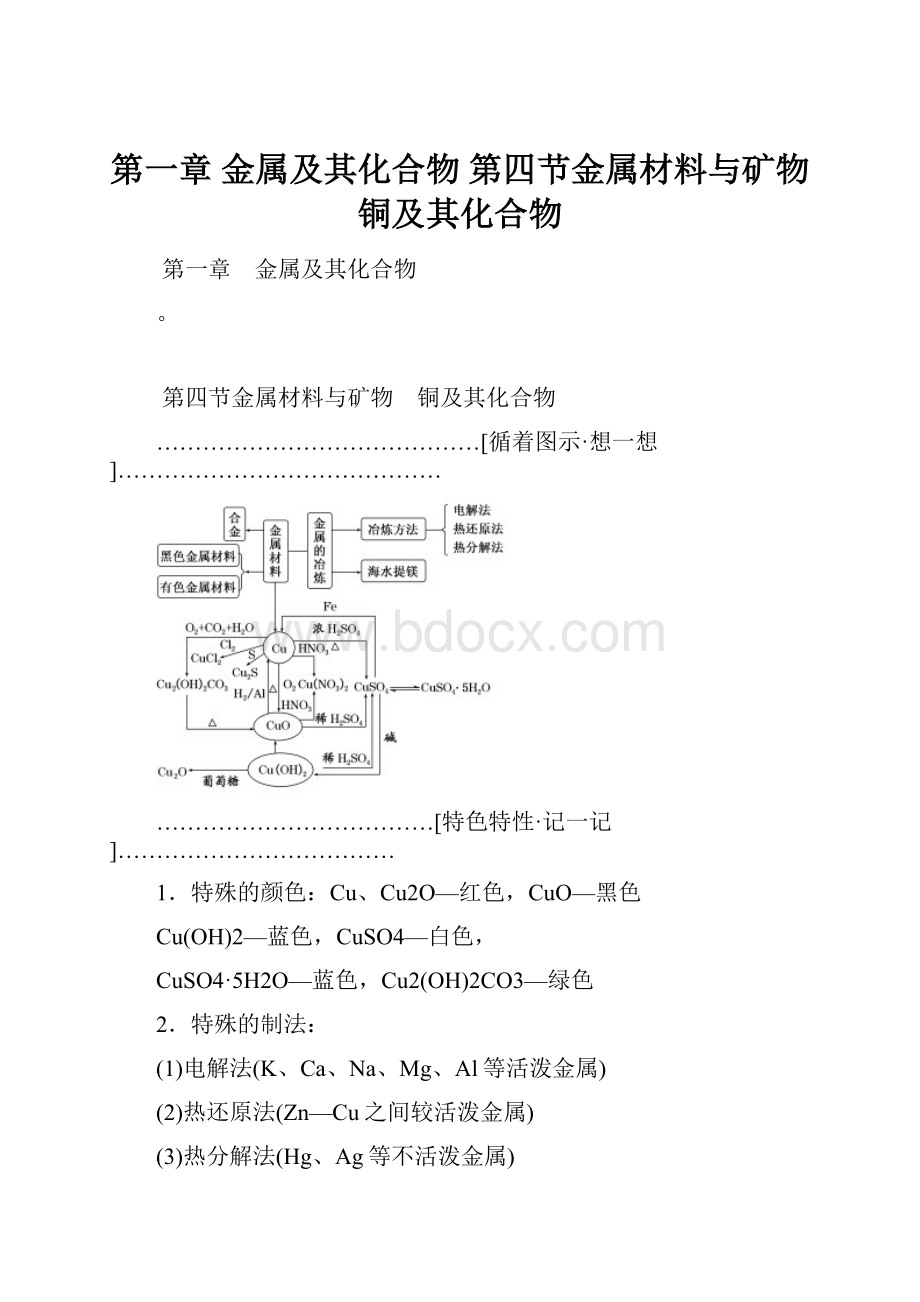
……………………………………[循着图示·想一想]……………………………………
………………………………[特色特性·记一记]………………………………
1.特殊的颜色:
Cu、Cu2O—红色,CuO—黑色
Cu(OH)2—蓝色,CuSO4—白色,
CuSO4·5H2O—蓝色,Cu2(OH)2CO3—绿色
2.特殊的制法:
(1)电解法(K、Ca、Na、Mg、Al等活泼金属)
(2)热还原法(Zn—Cu之间较活泼金属)
(3)热分解法(Hg、Ag等不活泼金属)
3.必记五反应:
(1)工业上冶炼Mg:
MgCl2(熔融)
Mg+Cl2↑
(2)工业上冶炼Al:
2Al2O3(熔融)
4Al+3O2↑
(3)工业上冶炼Fe:
3CO+Fe2O3
2Fe+3CO2
(4)铝热反应:
Fe2O3+2Al
Al2O3+2Fe
(5)铜绿的生成:
2Cu+O2+CO2+H2O===Cu2(OH)2CO3
考点一
合金和常见的金属材料
[教材知识层面]
1.合金
(1)概念:
合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
(2)性能:
①多数合金的熔点比它的各成分金属的熔点低;
②合金的硬度一般比它的各成分金属的硬度大。
2.常见金属材料
(1)黑色金属材料——钢铁。
①钢是用量最大,用途最广的合金。
②
(2)有色金属材料——铜和铝。
①我国使用最早的合金是青铜,常见的铜合金有黄铜和白铜。
②
[高考考查层面]
1.(2013·重庆高考)航母螺旋桨主要由铜-铝合金制造。
80.0gCuAl合金用盐酸完全溶解后,在溶液中加入过量氨水,过滤后得到白色沉淀39.0g,则合金中Cu的质量分数为________。
解析:
反应过程为:
Al(OH)3↓故39.0g为Al(OH)3的质量。
因此合金中m(Al)=
×27g·mol-1=13.5g,合金中铜的质量分数为:
×100%≈83.1%。
答案:
83.1%
2.(2014·北京高考)碳、硫的含量影响钢铁性能。
碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x克钢样中碳、硫转化为CO2、SO2。
①气体a的成分是________。
②若钢样中硫以FeS形式存在,A中反应:
3FeS+5O2
1________+3________。
(2)将气体a通入测硫装置中(如图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式:
_________________________________________
________________________________________________________________________。
②用NaOH溶液滴定生成的H2SO4,消耗zmLNaOH溶液。
若消耗1mLNaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:
________。
(3)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。
①气体a通过B和C的目的是_________________________________________。
②计算钢样中碳的质量分数,应测量的数据是________。
解析:
(1)①根据题给信息可知气体a的成分为CO2、SO2和过量的O2。
②根据原子守恒和得失电子守恒配平方程式得:
3FeS+5O2
Fe3O4+3SO2。
(2)①过氧化氢具有氧化性,二氧化硫具有还原性,二者发生氧化还原反应生成硫酸。
②消耗1mLNaOH溶液相当于硫的质量为yg,则消耗xmLNaOH溶液相当于硫的质量为yzg,所以钢样中硫的质量分数为
。
(3)①整个装置要准确测定CO2的质量,故需要排除干扰气体SO2,由题给装置可知,活性二氧化锰的作用是除去气体a中的SO2,重铬酸钾和浓硫酸的作用是检验SO2是否除尽。
②通过测量二氧化碳吸收瓶吸收CO2前、后的质量计算出钢样中碳的质量分数。
答案:
(1)①O2、SO2、CO2 ②Fe3O4 SO2
(2)①H2O2+SO2===H2SO4 ②
(3)①排除SO2对CO2测定的干扰 ②吸收CO2前、后吸收瓶的质量
[方法技巧]
定量测定合金组成与含量的两种方法
(1)定量集气法:
定量集气法是指收集合金中某种物质溶于酸或碱溶液时所产生的气体的量,应用化学方程式或关系式来判断合金的组
成。
其原理的关键点是根据某组分的特殊性质(特别是与酸或碱反应能产生气体),其操作要点和注意事项有:
保证装置的气密性良好,注意收集气体的读数方法。
(2)沉淀法:
沉淀法测定物质含量是常用的一种方法,采用沉淀法时,涉及的基本实验操作和主要问题有:
称量、溶解(溶解试剂)、沉淀(重点是沉淀试剂的选择)、过滤、沉淀洗涤、沉淀的干燥、称量及数据的处理(包括测定结果的误差分析)。
[考点达标层面]
1.判断下列描述的正误(正确的打“√”,错误的打“×”)。
(1)铝合金的熔点比纯铝的高。
( )
(2)合金材料中不可能含有非金属元素。
( )
(3)云南鲁甸地震灾区重建使用了大量钢材,钢材是合金。
( )
(4)合金中的金属元素以化合物的形式存在。
( )
(5)合金中各元素的含量一定,所以合金是纯净物。
( )
答案:
(1)×
(2)× (3)√ (4)× (5)×
2.将下列合金与其用途连线
①青铜 A.不锈钢
②铬镍合金B.司母戊鼎
③低碳钢C.门窗框架
④铝合金D.钢丝、钢管
答案:
①—B,②—A,③—D,④—C
3.现代建筑的门窗架常用电解加工成的古铜色硬铝制造。
取硬铝样品进行如下实验(每一步试剂均过量),由此可以推知硬铝的组成可能为(提示:
Si+2OH-+H2O===SiO
+2H2↑)( )
A.Al、Mg、Si、ZnB.Al、Fe、Zn、Na
C.Al、Na、Cu、FeD.Al、Cu、Mg、Si、Mn
解析:
选D 硬铝中一定含有Al,样品加入足量稀盐酸后有难溶物存在,说明有金属活动性在H之后的金属或非金属存在,再加入浓NaOH溶液后有气体生成和难溶物存在,根据题目信息可知硬铝样品中含有Si,最终的难溶物为Cu,D项中含有上述三种物质。
考点二
金属的冶炼
[教材知识层面]
1.金属在自然界中的存在形式
金、铂等化学性质不活泼的金属,在自然界以游离态存在;化学性质较活泼的金属在自然界中以化合态存在。
2.金属冶炼的一般步骤
(1)富集:
除去杂质,提高矿石中有用成分的含量。
(2)冶炼:
利用氧化还原反应,用还原剂把金属矿石中的金属离子还原成金属单质。
(3)精炼:
提纯金属。
3.金属的冶炼方法
(1)热分解法:
加热分解HgO和Ag2O的化学方程式分别为:
2HgO△,2Hg+O2↑;2Ag2O△,4Ag+O2↑。
(2)热还原法:
①焦炭还原法:
用C还原CuO的化学方程式:
C+2CuO
2Cu+CO2↑。
②一氧化碳还原法:
工业上炼铁的反应原理:
3CO+Fe2O3
2Fe+3CO2。
③H2还原法:
用H2还原WO3的化学方程式:
3H2+WO3
W+3H2O。
④活泼金属还原法:
用Al还原Cr2O3的化学方程式:
2Al+Cr2O3
2Cr+Al2O3。
(3)电解法:
电解熔融Al2O3、MgCl2冶炼Al、Mg的化学方程式分别为:
2Al2O3(熔融)电解,4Al+3O2↑,
MgCl2(熔融)电解,Mg+Cl2↑。
[高考考查层面]
命题点1 金属冶炼的方法
[典题示例]
1.(2013·山东高考,节选)金属冶炼与处理常涉及氧化还原反应。
由下列物质冶炼相应金属时采用电解法的是________。
A.Fe2O3 B.NaCl
C.Cu2SD.Al2O3
解析:
选BD 非常活泼的金属,如Na、K、Mg、Al等,用电解的方法冶炼。
2.(2014·天津高考,节选)已知:
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
工业制镁时,电解MgCl2而不电解MgO的原因是__________________________
________________________________________________________________________;
制铝时,电解Al2O3而不电解AlCl3的原因是________________________________
________________________________________________________________________;
解析:
MgO和MgCl2均为离子化合物,但MgO的熔点太高,熔融时需要消耗大量能量,故使用熔点较低的MgCl2。
AlCl3属于共价化合物,熔融时不导电,故不能用电解AlCl3的方法冶炼Al。
答案:
MgO的熔点高,熔融时耗费更多能源,增加生产成本 AlCl3是共价化合物,熔融态难导电
[方法技巧]
金属冶炼三方法
1.电解法
在金属活动性顺序中Al之前(含铝)的金属,用电解的方法冶炼。
如电解熔融NaCl制Na,电解熔融MgCl2制镁,电解熔融Al2O3制铝。
2.热还原法
在金属活动性顺序中,Al之后,Cu之前(含Cu)的金属一般用还原法冶炼。
常使用的还原剂有焦炭、CO和H2。
用焦炭作还原剂冶炼的金属会混有一定量的碳,如钢铁。
用CO作还原剂时产物的纯度较高,但CO有毒,污染环境。
用H2作还原剂时产物的纯度高、对环境无污染,但H2不易获得,且难以贮存和运输。
3.加热分解法
在金属活动性顺序中,Cu之后的金属(如Hg、Ag)一般可采用加热分解氧化物的方法冶炼。
如加热HgO、Ag2O制得Hg、Ag。
命题点2 铝热反应及应用
1.铝热反应
(1)原理:
高温下铝将较不活泼的金属从其氧化物中还原出来。
(2)实验装置:
铝粉还原氧化铁的实验装置:
如图所示。
(3)实验现象:
①镁条剧烈燃烧,放出一定的热量,使氧化铁粉末和铝粉在较高温度下发生剧烈的反应。
②反应放出大量的热,并发出耀眼的强光。
③纸漏斗的下部被烧穿,有熔融物落入沙中。
④待熔融物冷却后,除去外层熔渣,仔细观察,可以发现落下的是铁珠。
(4)反应特点:
①高温条件。
②剧烈燃烧,放出大量的热。
③新生成的液态金属单质易与Al2O3(固态)分离。
(5)引燃剂和铝热剂:
①引燃剂:
镁条、氯酸钾。
②铝热剂:
铝粉和金属氧化物(Fe2O3、Cr2O3、V2O5等)组成的混合物。
2.铝热反应的应用
(1)该反应为放热反应,铝在高温下还原出了金属单质。
在冶金工业上也常用这一原理制取熔点较高的金属,如铬、锰等,3MnO2+4Al
2Al2O3+3Mn。
(2)该反应原理可以应用在生产上,如焊接钢轨等。
[典题示例]
1.(2014·山东高考,节选)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有________。
A.KCl B.KClO3
C.MnO2D.Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,________(填“能”或“不能”)说明固体混合物中无Fe2O3,理由是________________________(用离子方程式说明)。
解析:
做铝热反应的实验时,需要KClO3作助燃剂,且用镁条引燃。
固体混合物中若有Fe2O3,因发生反应:
Fe2O3+6H+===2Fe3++3H2O和Fe+2Fe3+===3Fe2+,Fe3+转化为Fe2+,KSCN溶液也不会变红。
答案BD 不能 Fe2O3+6H+===2Fe3++3H2O、Fe+2Fe3+===3Fe2+
2.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。
进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20gA全部溶于0.15L6.0mol/L盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L(标准状况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是_____________________________________,
产物中的单质B是________。
(2)②中所发生的各反应的化学方程式是_________________________________
________________________________________________________________________。
(3)③中所发生的各反应的离子方程式是___________________________________
________________________________________________________________________。
解析:
(2)Fe2O3和MgO都是碱性氧化物,能与酸反应生成盐和水:
Fe2O3+6HCl===2FeCl3+3H2O
MgO+2HCl===MgCl2+H2O。
(3)混合物中只有Fe2O3能和Al发生铝热反应并生成铁单质。
C溶液中有反应生成了FeCl3,还有未反应的HCl,发生的离子反应为Fe+2H+===Fe2++H2↑,Fe+2Fe3+===3Fe2+。
答案:
(1)加少量KClO3,插上镁条并将其点燃 Fe
(2)Fe2O3+6HCl===2FeCl3+3H2O、
MgO+2HCl===MgCl2+H2O
(3)Fe+2H+===Fe2++H2↑、
Fe+2Fe3+===3Fe2+
[考点达标层面]
1.判断下列描述的正误(正确的打“√”,错误的打“×”)。
(1)(2012·重庆高考)钢铁厂用热还原法冶炼铁。
( )
(2)(2012·广东高考)工业上电解熔融状态的Al2O3制备Al涉及氧化还原反应。
( )
(3)电解AlCl3、FeCl3、CuCl2的混合溶液时,阴极上依次析出Cu、Fe、Al。
( )
(4)电解氯化镁溶液制取金属镁。
( )
(5)用金属钠置换四氯化钛(TiCl4)溶液中的钛来制取单质钛。
( )
(6)将MgO与铝粉混合发生铝热反应制备镁。
( )
答案:
(1)√
(2)√ (3)× (4)× (5)× (6)×
2.某同学对“铝热反应”的现象有这样的描述:
“反应放出大量的热,并放出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。
查阅《化学手册》知:
Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下:
物质
Al
Al2O3
Fe
Fe2O3
熔点/℃
660
2054
1535
1462
沸点/℃
2467
2980
2750
(1)该同学推测,铝热反应所得到的熔融物应是铁铝合金。
理由是:
该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。
你认为他的解释是否合理:
________(填“合理”或“不合理”)。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。
该实验所用试剂是________,反应的离子方程式为___________________________________________。
(3)实验室溶解该熔融物,下列试剂中最好的是________(填序号)。
A.浓硫酸 B.稀硫酸
C.稀硝酸D.氢氧化钠溶液
解析:
(1)这种解释是合理的,它体现了铝热反应的特点之一——放热较多,并且结合了表格中提供的熔点数据。
(2)证明某固体是不是含有铝,只要加入足量的NaOH溶液即可,若含有铝,则固体部分溶解,有气泡产生。
相应的离子方程式为2Al+2OH-+2H2O===2AlO
+3H2↑。
(3)铁铝熔融物在一定条件下与浓硫酸或稀硝酸反应,会产生有毒气体,而且消耗的两种酸量又多;熔融物中铁不能与氢氧化钠溶液反应,故最好选用稀硫酸。
答案:
(1)合理
(2)NaOH溶液
2Al+2OH-+2H2O===2AlO
+3H2↑ (3)B
考点三
铜及其化合物
[教材知识层面]
1.铜的性质
(1)物理性质:
紫红色固体,有良好的延展性、导电、导热性,不能被磁铁吸引。
(2)化学性质:
反应物质
化学方程式
非金属
O2
2Cu+O2
2CuO
S
2Cu+S
Cu2S
Cl2
Cu+Cl2
CuCl2
氧化性酸
浓H2SO4
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
浓HNO3
Cu+4HNO3(浓)===
Cu(NO3)2+2NO2↑+2H2O
稀HNO3
3Cu+8HNO3(稀)===
3Cu(NO3)2+2NO↑+4H2O
盐溶液
AgNO3溶液、
FeCl3溶液
Cu+2AgNO3===Cu(NO3)2+2Ag
Cu+2FeCl3===CuCl2+2FeCl2
2.氧化铜
(1)物理性质:
黑色粉末状固体
(2)化学性质:
3.氢氧化铜
(1)物理性质:
蓝色不溶于水的固体。
(2)化学性质及应用:
反应①的化学方程式:
Cu(OH)2
CuO+H2O
反应②的离子方程式:
Cu(OH)2+2H+===Cu2++2H2O
4.铜盐
(1)Cu2(OH)2CO3的名称为碱式碳酸铜,是铜绿的成分,是铜在潮湿的空气中被锈蚀的结果,其受热分解的化学方程式为Cu2(OH)2CO3
2CuO+H2O+CO2↑。
(2)CuSO4·5H2O为蓝色晶体,俗称蓝矾、胆矾,其受热分解的化学方程式为CuSO4·5H2O
CuSO4+5H2O,蓝色晶体受热转化为白色粉末。
无水CuSO4遇水变蓝色(生成CuSO4·5H2O),可作为水的检验依据。
(3)铜盐溶液有毒,主要是因为Cu2+作为一种重金属离子能与蛋白质作用,使蛋白质变性失去生理活性,因此人们利用了它的这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。
[高考考查层面]
命题点1 铜的两种重要氧化物(CuO、Cu2O)
1.氧化铜和氧化亚铜的比较
名称
氧化铜
氧化亚铜
颜色
黑色
砖红色
与酸反应(H+)
CuO+2H+===Cu2++H2O
Cu2O+2H+===Cu2++Cu+H2O
与H2反应
H2+CuO
Cu+H2O
H2+Cu2O
2Cu+H2O
转化关系
4CuO
2Cu2O+O2↑
2.区别红色物质Cu和Cu2O的方法
向红色物质中加入稀硫酸,若溶液由无色变成蓝色,则该红色物质为Cu2O,否则为Cu。
反应的化学方程式为:
Cu2O+H2SO4===CuSO4+Cu+H2O
[典题示例]
1.已知CuO经高温灼烧生成Cu2O,Cu2O与H+发生:
Cu2O+2H+===Cu+Cu2++H2O。
将经高温灼烧后的CuO样品投入足量的热的稀硝酸溶液中,下列有关说法中正确的是( )
A.如果溶液变为蓝色、同时有紫红色固体出现,说明样品全部生成了Cu2O
B.溶液中最终可能有紫红色固体出现
C.这种实验的结果无法说明CuO分解的程度
D.如果溶液中出现蓝色,最终没有紫红色固体出现,说明CuO没有分解
解析:
选C 若误认为Cu不与热的稀硝酸反应会造成错选D。
如果样品部分生成了Cu2O,也会有类似现象发生,即这种实验的结果无法说明CuO分解的程度,A项错误、C项正确;由于Cu能够与热的稀硝酸反应,所以不论CuO是否完全分解,溶液中最终不可能有紫红色固体出现,B项不正确、D项错误。
2.已知酸性条件下有如下反应:
2Cu+===Cu2++Cu↓。
由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。
一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下:
加入试剂
稀硫酸
浓硫酸、加热
稀硝酸
浓硝酸
实验现象
有红色固体剩余和溶液变为蓝色
产生无色气体
产生无色气体和溶液变为蓝色
产生红棕色气体和溶液变为绿色
由此推出本次氢气还原氧化铜实验的产物( )
A.是Cu
B.是Cu2O
C.一定有Cu,一定有Cu2O
D.一定有Cu2O,可能有Cu
解析:
选D 浓H2SO4(加热)、硝酸均能氧化Cu或Cu2O;而稀H2SO4与Cu不反应,与Cu2O反应。
命题点2 铜的冶炼方法
[典题示例]
1.Cu2S是火法炼铜的重要原料之一,下面是由Cu2S冶炼铜及制取CuSO4·5H2O的流程图。
Cu2S
Cu
Cu2O、CuO
A
B
胆矾
Cu2S中铜元素的化合价为________________,火法炼铜的反应原理是________________________________________________________________________
(用化学方程式表示)。
解析:
Cu2S中铜元素的化合价为+1;Cu2S在加热条件下与O2反应生成Cu,依据氧化还原反应的实质判断硫元素对应的产物是SO2。
反应方程式为:
Cu2S+O2
2Cu+SO2。
答案:
+1 Cu2S+O2
2Cu+SO2
2.孔雀石的主要成分为Cu2(OH)2CO3。
某同学设计的从孔雀石中冶炼铜的方案如下(假设孔雀石中杂质不溶于水和稀硫酸):
(1)反应①能观察到的现象是________________________________________,
有关反应的化学方程式为________________________________________________
________________________________________________________________________。
(2)反应②加入的金属可能是________,有关反应的离子方程式为_____________。
解析:
孔雀石中加入稀硫酸可看到孔雀石逐渐溶解,溶液由无色变为蓝色,且有气泡产生;反应的化学方程式为Cu2(OH)2CO3+2H2SO4===2CuSO4+CO2↑+3H2O。
经过滤除去难溶于水和稀硫酸的杂质,则滤液中主要含有CuSO4,加入的金属粉末能将Cu2+从溶液中置换出来即可,故金属可能是Fe或Zn等。
答案:
(1)固体逐渐消失,溶液由无色变成蓝色,有气泡产生 Cu2(OH)2CO3+2H2SO4===2CuSO4+CO2↑+3H2O
(2)铁粉 Fe+Cu2+===Fe2++Cu
[方法技巧]
铜的冶炼“三方法”
(1)湿法炼铜:
Fe+CuSO4===FeSO4+Cu。
(2)高温炼铜:
工业上用高温冶炼黄铜矿的方法获得铜(粗铜):
2CuFeS2+4O2
Cu2S+3SO2+2FeO(炉渣)
2Cu2S+3O2
2Cu2O+2SO2
2Cu2O+Cu2S
6Cu+SO2↑
粗铜中铜的含量为99.5%~99.7%,主要含
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第一章 金属及其化合物 第四节金属材料与矿物 铜及其化合物 金属 及其 化合物 第四 金属材料 矿物
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
