 九年级第一学期第二次月测化学试题.docx
九年级第一学期第二次月测化学试题.docx
- 文档编号:9500601
- 上传时间:2023-02-05
- 格式:DOCX
- 页数:12
- 大小:201.71KB
九年级第一学期第二次月测化学试题.docx
《九年级第一学期第二次月测化学试题.docx》由会员分享,可在线阅读,更多相关《九年级第一学期第二次月测化学试题.docx(12页珍藏版)》请在冰豆网上搜索。
九年级第一学期第二次月测化学试题
九年级第一学期第二次月测化学试题
姓名:
________班级:
________成绩:
________
一、单选题
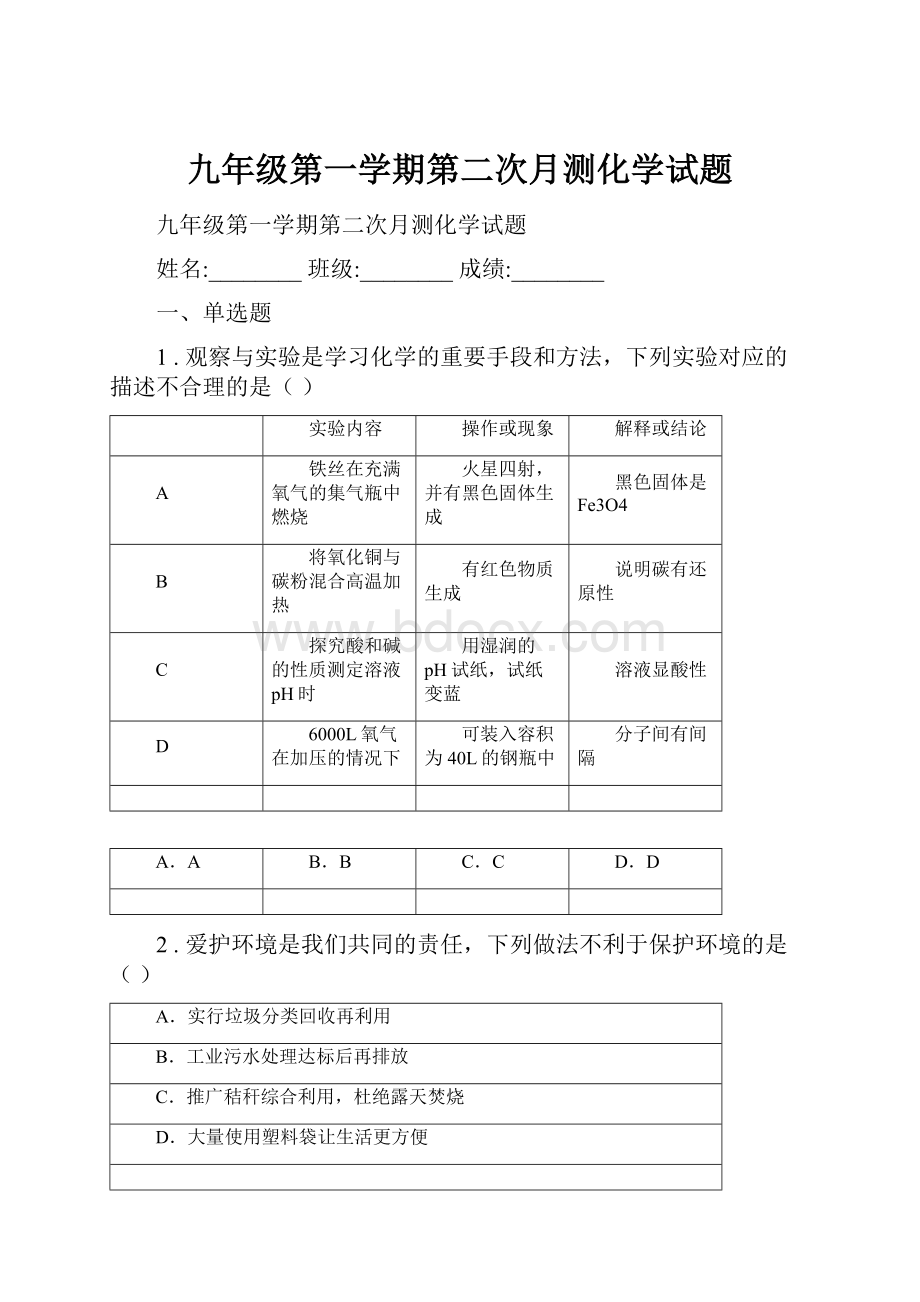
1.观察与实验是学习化学的重要手段和方法,下列实验对应的描述不合理的是()
实验内容
操作或现象
解释或结论
A
铁丝在充满氧气的集气瓶中燃烧
火星四射,并有黑色固体生成
黑色固体是Fe3O4
B
将氧化铜与碳粉混合高温加热
有红色物质生成
说明碳有还原性
C
探究酸和碱的性质测定溶液pH时
用湿润的pH试纸,试纸变蓝
溶液显酸性
D
6000L氧气在加压的情况下
可装入容积为40L的钢瓶中
分子间有间隔
A.A
B.B
C.C
D.D
2.爱护环境是我们共同的责任,下列做法不利于保护环境的是()
A.实行垃圾分类回收再利用
B.工业污水处理达标后再排放
C.推广秸秆综合利用,杜绝露天焚烧
D.大量使用塑料袋让生活更方便
3.下列关于水的说法中,正确的是
A.天然水中硬水属于混合物,软水属于纯净物
B.在自来水厂净水的过程中,包括蒸馏这一步骤
C.活性炭净水器里,活性炭的作用是吸附、并过滤水中的杂质
D.生活中常用肥皂水鉴别硬水和软水,泡沫少的是软水。
4.下列图象分别表示对应的四种操作过程,其中表示正确的图像是
A.①加热氯酸钾和二氧化锰固体至质量不再减轻,固体中二氧化锰的质量
B.②向pH=1的硫酸溶液中逐滴加入pH=13的氢氧化钠溶液
C.③某温度下,向一定量的水中持续加入食盐并不断搅拌,所得溶液的质量分数
D.④等质量的锌、铁与足量的同种稀硫酸反应,产生氢气的质量M与反应时间
5.归纳总结和逻辑推理是化学学习中常用的思维方法。
以下说法正确的是
A.酸碱中和反应生成盐和水,则生成盐和水的反应都是中和反应
B.同种分子构成的物质是纯净物,则纯净物都是由分子构成
C.碳酸盐与盐酸反应放出气体,则与盐酸反应放出气体的物质都是碳酸盐
D.点燃氢气和氧气的混合物可能爆炸,则点燃可燃性气体和氧气的混合物都可能爆炸
6.下列说法中正确的是()
A.化合物中一定含有不同种元素
B.只含有一种元素的物质一定是单质
C.混合物一定由不同种分子构成
D.含氧元素的物质一定是氧化物
7.下列做法可以达到预期目的是()
A.在火炉旁放一盆水,防止煤气中毒
B.向食品袋中充入氮气,延长食品的保质期
C.做测定空气中氧气含量的实验时,用木炭代替红磷
D.实验室制CO2时,用稀硫酸代替稀盐酸和石灰石(大理石)反应
8.下图是表示气体分子的示意图,图中“○”和“●”分别表示两种不同的原子,其中可能表示氧化物的是()
A.
B.
C.
D.
9.下列所示实验操作,错误的是()
A.A
B.B
C.C
D.D
10.根据已配平的反应方程式:
4K2Cr2O7
4R+2Cr2O3+3O2
可推测R的化学式是
A.KOH
B.K2CrO4
C.K2CrO2
D.K2CrO3
11.下列粒子结构示意图中,表示阴离子的是
A.
B.
C.
D.
12.茉莉的香气清新淡雅,檀木的香气持久醇厚。
从微观角度分析,上述语句中隐含的分子性质有()
①分子的质量很小
②分子之间有间隔
③分子在不断运动
④不同分子性质不同
A.③④
B.①②
C.①③
D.②④
13.在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法错误的是()
物质
A
B
C
D
反应前质量(g)
10
10
10
2
反应后质量(g)
待测
2
21
2
A.该反应是化合反应,D可能是催化剂
B.A、B两种物质中元素种类一定与C物质中元素种类相同
C.A物质可能是单质
D.反应后C物质的质量“待测”为3g
14.氮肥硝酸铵在不同条件下分解不可能的产物是()
A.NO2、H2O
B.CO2、H2O
C.N2、H2O
D.NH3、NO
二、填空题
15.化学用语是国际通用语言,是学习化学的重要工具。
用化学用语填空:
(1)两个氮原子:
_________。
(2)氯化钠中的阴离子_________。
(3)红磷在空气中燃烧产物的化学符号:
_________。
(4)3个氧离子:
_________
(5)在水通电分解生成氢气和氧气的化学变化中的最小微粒是__________和_________。
三、实验题
16.如图是实验室制取氧气的两种发生装置。
回答下列问题:
⑴乙图中标号①的仪器的名称是________________;
⑵下列反应都能生成氧气,其中不宜用于实验室制取氧气的是________________(填序号);
A.加热氯酸钾和二氧化锰的混合物
B.常温下过氧化氢溶液和二氧化锰混合反应
C.利用植物光合作用
⑶请写出一种实验室制取氧气的化学反应主程式:
_____________________________;反应类型是________________;用排水法收集一瓶氧气,发现不纯,可能的原因是__________(答出一点即可);
⑷实验室制取下列气体,可以用甲图装置作为发生装置的是________________(填序号)
A.电石(固体)和水在常温下反应制乙炔气体
B.浓盐酸和二氧化锰共热制氯气
C.浓氨水和碱石灰常温下制氨气
四、简答题
17.写出符合要求的化学反应的符号表达式:
(1)有水生成的化合反应:
_____。
(2)有水生参加的分解反应:
_____。
(3)氯酸钾与二氧化锰固体混合加热:
_____。
18.测定空气中氧气体积分数的实验装置如图所示,在烧杯内加入少量的水,集气瓶五等分做上记号,用弹簧夹夹紧乳胶管.
(1)点燃燃烧匙内稍过量的红磷后,立即伸入瓶中并把塞子塞紧,看到的现象是_______;化学方程式为______________________。
(2)待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处,由此可知氧气约占空气总体积的_________。
(3)如果未冷却到室温便打开弹簧夹则实验结果将(填偏大、偏小或不变)_________。
红磷熄灭后,集气瓶内剩下主要气体具有_______(化学性质)、_________(物理性质)的性质。
若将上述实验中的红磷换成木炭,严格按操作步骤进行实验,并未发现倒吸现象,其原因是_____________________;
(4)实验中红磷需稍过量,目的是_________________;
(5)某小组对教材中“测定空气里氧气含量”的实验(见图I)进行了大胆改进,设计图(Ⅱ)(试管容积为45mL)实验方案进行,收到了良好的效果.请你对比分析下面图I、图Ⅱ实验,回答下列有关问题:
①实验室中若用图I装置测定空气中氧气的体积分数,下列说法正确的是_______.
A.红磷一熄灭就可以打开夹子 B.实验中,水的量可以随意
C.红磷的量要足量 D.瓶中消耗掉的气体跟剩下的气体的体积比约为1:
4.
②小军用图Ⅱ装置进行实验:
A.点燃酒精灯; B.撤去酒精灯,待试管冷却后松开弹簧夹;C.将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,按图Ⅱ中所示的连接方式固定好,夹紧橡皮管;D.读取注射器活塞的数据。
正确的实验操作顺序是____(填序号).
③图Ⅱ实验中,注射器活塞将从10mL刻度处慢慢前移到约为______mL刻度处才停止.
④对照图I、图Ⅱ实验,图Ⅱ实验的装置有何优点____(回答一点即可).
19.宏观辨识与微观探析是研究化学的主要方法和手段之一。
(1)构成物质的粒子有分子、原子和___________;
(2)从微观的角度看,氧分子是由氧原子构成,可推断出氧气是由________组成;
(3)“见著知微”是通过对宏观现象的观察、思考、推理,建立起对微观粒子的认识。
①将红墨水滴入水中,迅速扩散,说明分子在_____________;
②将铜丝深入硝酸银溶液中,观察到溶液逐渐变为蓝色,铜丝表面出现银的白色,推断溶液中粒子种类发生了变化,试写出化学反应方程式_______________。
(4)组成H2O和H2O2的元素种类相同,分子结构不同,可以推断二者的化学性质不同,试写出实验室分解H2O2制氧气的化学方程式______________。
20.在研究某大理石样品(杂质不溶于水也不与盐酸反应)的活动中,兴趣小组同学进行了如下实验,过程如图所示:
求
(1)反应中生成二氧化碳的质量。
(2)该大理石样品中碳酸钙的质量分数。
21.化学与生活密切相关。
请回答下列问题。
(1)对自行车的支架进行喷漆处理可以防止其生锈,原因是_________________。
(2)森林火灾时,常砍伐出一条隔离带的目的是___________。
(3)我国在南海成功开采出可燃冰。
可燃冰主要含有甲烷水合物。
请写出甲烷燃烧的化学方程式____________________________。
(4)柚子皮可以吸附室内异味,请写出初中化学中学过的具有同样性质的一种物质名称____________。
五、推断题
22.图中A、B、C、D、E五环分别代表初中化学中常见的五种物质,两环相连表示两种物质之间能发生化学反应;其中A、E常温下都是黑色固体,且E为一种非金属单质;B、C、D常温下均为无色气体,其中B为光合作用的产物之一,C的固体可用于人工降雨;A、D反应可生成一种红色固体和C。
(1)写出物质A、E的化学式为________ 、_______。
(2)实验室常用___________(填化学式)检验C气体,请写出该反应的化学方程式:
_______________。
六、科学探究题
23.工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4,为了测定铁红中铁的质量分数,兴趣小组的同学称取10.0g铁红样品进行如下实验,请你参与过程分析。
(资料)1.草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:
2.浓硫酸具有吸水性,氢氧化钠溶液可以吸收CO2。
3.碱石灰的主要成分是CaO和NaOH,可以吸收水与CO2。
(问题讨论)用下图所示装置实行实验:
(1)实验前应先_____。
(2)C装置的作用是_____。
(3)对E装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前_____;②停止加热后把反应生成的二氧化碳全部排入F装置中。
(4)写出E装置中所发生反应的一个化学方程式_____。
(数据分析与计算)
(5)充分反应后称得F装置增重6.6g,则此铁红中铁的质量分数是_____。
(实验评价)
(6)本实验中如果缺少D装置(不考虑其它因素),则测得样品中铁的质量分数会_____(填“偏小”、“不变”或“偏大”)。
(7)请指出实验装置的一个明显缺陷_____。
24.同学们在实验室发现了三种金属——铝、铁、铜,其中一块铜片生锈了,表面附有部分铜绿[铜绿的主要成分是Cu2(OH)2CO3],他们的实验探究过程如下:
(1)铜绿是铜与空气中的氧气、水和 (填化学式)共同作用的结果。
(2)为探究铝、铁、铜的活动性顺序,某同学设计了一组实验:
①铝片浸入稀硫酸中;②铜片浸入稀硫酸中;③铝片浸入氯化亚铁溶液中,这组实验还不能完全证明三种金属的活动性顺序。
请你补充一个实验来达到实验目的(写出实验步骤、现象) 。
(3)他们还想用加热的方法除去铜绿,加热时却发现铜片表面全部变黑。
经查阅资料知道:
①铜绿受热分解会生成黑色的氧化铜 ②酒精在不完全燃烧时会生成炭黑 ③炭黑与稀硫酸不以应。
a、他们提出猜想:
该黑色物质可能是氧化铜,也可能是氧化铜和 的混合物。
b、设计了下述实验方案,用于检验黑色物质。
实验步骤
实验现象
结论
剪下一片变黑的铜片,放入盛有足量稀硫酸的试管中,微热
铜片表面黑色固体全部消失,露出红色的铜,溶液变 色。
此黑色固体是 (填化学式)
七、计算题
25.为测石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙质量分数,进行如图所示实验,计算:
(1)碳酸钙也可用于人体补钙,缺钙会引起________(列举一条即可)。
(2)样品中碳酸钙的质量分数为多少_______?
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 九年级 第一 学期 第二次 化学试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
