 北京高考化学含答案完整版doc.docx
北京高考化学含答案完整版doc.docx
- 文档编号:9323597
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:14
- 大小:698.50KB
北京高考化学含答案完整版doc.docx
《北京高考化学含答案完整版doc.docx》由会员分享,可在线阅读,更多相关《北京高考化学含答案完整版doc.docx(14页珍藏版)》请在冰豆网上搜索。
北京高考化学含答案完整版doc
2018北京高考化学
6.下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
A.甲醇低温所制氢气用于新能源汽车
B.氘、氚用作“人造太阳”核聚变燃料
C.偏二甲肼用作发射“天宫二号”的火箭燃料
D.开采可燃冰,将其作为能源使用
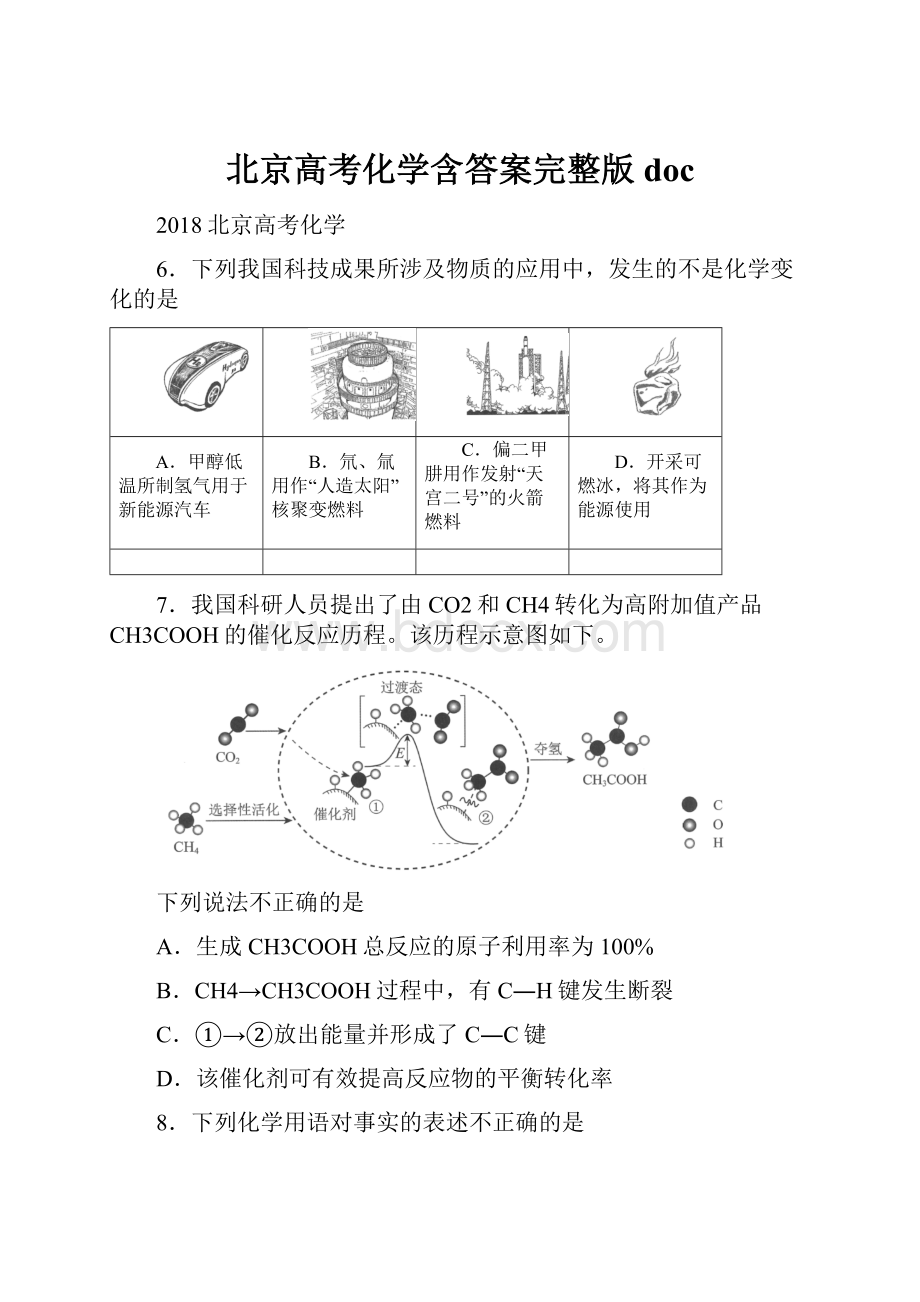
7.我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。
该历程示意图如下。
下列说法不正确的是
A.生成CH3COOH总反应的原子利用率为100%
B.CH4→CH3COOH过程中,有C―H键发生断裂
C.①→②放出能量并形成了C―C键
D.该催化剂可有效提高反应物的平衡转化率
8.下列化学用语对事实的表述不正确的是
A.硬脂酸与乙醇的酯化反应:
C17H35COOH+C2H518OH
C17H35COOC2H5+H218O
B.常温时,0.1mol·L-1氨水的pH=11.1:
NH3·H2O
+OH−
C.由Na和C1形成离子键的过程:
D.电解精炼铜的阴极反应:
Cu2++2e−
Cu
9.下列实验中的颜色变化,与氧化还原反应无关的是
A
B
C
D
实验
NaOH溶液滴入FeSO4溶液中
石蕊溶液滴入氯水中
Na2S溶液滴入AgCl浊液中
热铜丝插入稀硝酸中
现象
产生白色沉淀,随后变为红褐色
溶液变红,随后迅速褪色
沉淀由白色逐渐变为黑色
产生无色气体,随后变为红棕色
10.一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。
其结构片段如下图
下列关于该高分子的说法正确的是
A.完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B.完全水解产物的单个分子中,含有官能团―COOH或―NH2
C.氢键对该高分子的性能没有影响
D.结构简式为:
11.测定0.1mol·L-1Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻
①
②
③
④
温度/℃
25
30
40
25
pH
9.66
9.52
9.37
9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是
A.Na2SO3溶液中存在水解平衡:
+H2O
+OH−
B.④的pH与①不同,是由于
浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的Kw值相等
12.验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
①
②
③
在Fe表面生成蓝色沉淀
试管内无明显变化
试管内生成蓝色沉淀
下列说法不正确的是
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
25.(17分)8−羟基喹啉被广泛用作金属离子的络合剂和萃取剂,也是重要的医药中间体。
下图是8−羟基喹啉的合成路线。
已知:
i.
ii.同一个碳原子上连有2个羟基的分子不稳定。
(1)按官能团分类,A的类别是。
(2)A→B的化学方程式是。
(3)C可能的结构简式是__________。
(4)C→D所需的试剂a是__________。
(5)D→E的化学方程式是__________。
(6)F→G的反应类型是__________。
(7)将下列K→L的流程图补充完整:
(8)合成8−羟基喹啉时,L发生了__________(填“氧化”或“还原”)反应,反应时还生成了水,则L与G物质的量之比为__________。
26.(13分)磷精矿湿法制备磷酸的一种工艺流程如下:
已知:
磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。
溶解度:
Ca5(PO4)3(OH) (1)上述流程中能加快反应速率的措施有__________。 (2)磷精矿粉酸浸时发生反应: 2Ca5(PO4)3(OH)+3H2O+10H2SO4 10CaSO4·0.5H2O+6H3PO4 ①该反应体现出酸性关系: H3PO4__________H2SO4(填“>”或“<”)。 ②结合元素周期律解释 中结论: P和S电子层数相同,__________。 (3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。 写出生成HF的化学方程式: 。 (4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。 相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。 80℃后脱除率变化的原因: ____________________。 (5)脱硫时,CaCO3稍过量,充分反应后仍有SO42−残留,原因是__________;加入BaCO3可进一步提高硫的脱除率,其离子方程式是____________________。 (6)取ag所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用bmol·L−1NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液cmL,精制磷酸中H3PO4的质量分数是________。 (已知: H3PO4摩尔质量为98g·mol−1) 27.(12分)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。 过程如下: (1)反应Ⅰ: 2H2SO4(l) 2SO2(g)+2H2O(g)+O2(g)ΔH1=+551kJ·mol-1 反应Ⅲ: S(s)+O2(g) SO2(g)ΔH3=-297kJ·mol-1 反应Ⅱ的热化学方程式: ________________。 (2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。 p2_______p1(填“>”或“<”),得出该结论的理由是________________。 (3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。 将ii补充完整。 i.SO2+4I-+4H+ S↓+2I2+2H2O ii.I2+2H2O+_________ _________+_______+2I- (4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下: 分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。 (已知: I2易溶解在KI溶液中) 序号 A B C D 试剂组成 0.4mol·L-1KI amol·L-1KI 0.2mol·L-1H2SO4 0.2mol·L-1H2SO4 0.2mol·L-1KI 0.0002molI2 实验现象 溶液变黄,一段时间后出现浑浊 溶液变黄,出现浑浊较A快 无明显现象 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 ①B是A的对比实验,则a=__________。 ②比较A、B、C,可得出的结论是______________________。 ③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因: ________________。 28.(16分)实验小组制备高铁酸钾(K2FeO4)并探究其性质。 资料: K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。 (1)制备K2FeO4(夹持装置略) ①A为氯气发生装置。 A中反应方程式是________________(锰被还原为Mn2+)。 ②将除杂装置B补充完整并标明所用试剂。 ③C中得到紫色固体和溶液。 C中Cl2发生的反应有 3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl+8H2O,另外还有________________。 (2)探究K2FeO4的性质 ①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。 为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案: 方案Ⅰ 取少量a,滴加KSCN溶液至过量,溶液呈红色。 方案Ⅱ 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。 取少量b,滴加盐酸,有Cl2产生。 Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。 Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。 用KOH溶液洗涤的目的是________________。 ②根据K2FeO4的制备实验得出: 氧化性Cl2________ (填“>”或“<”),而方案Ⅱ实验表明,Cl2和 的氧化性强弱关系相反,原因是________________。 ③资料表明,酸性溶液中的氧化性 > ,验证实验如下: 将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 > 。 若能,请说明理由;若不能,进一步设计实验方案。 理由或方案: ________________。 6.B7.D8.A9.C10.B11.C12.D 25.(17分) (1)烯烃 (2)CH2=CHCH3+Cl2 CH2=CHCH2Cl+HCl (3)HOCH2CHClCH2ClClCH2CH(OH)CH2Cl(4)NaOH,H2O (5)HOCH2CH(OH)CH2OH CH2=CHCHO+2H2O (6)取代反应 (7) (8)氧化3∶1 26.(13分) (1)研磨、加热 (2)①< ②核电荷数P<S,原子半径P>S,得电子能力P<S,非金属性P<S (3)2Ca5(PO4)3F+10H2SO4+5H2O 10CaSO4·0.5H2O+6H3PO4+2HF↑ (4)80℃后,H2O2分解速率大,浓度显著降低 (5)CaSO4微溶BaCO3+ +2H3PO4 BaSO4+CO2↑+H2O+2 (6) 27.(12分) (1)3SO2(g)+2H2O(g) 2H2SO4(l)+S(s)ΔH2=−254kJ·mol−1 (2)>反应Ⅱ是气体物质的量减小的反应,温度一定时,增大压强使反应正向移动,H2SO4的物质的量增大,体系总物质的量减小,H2SO4的物质的量分数增大 (3)SO2SO42−4H+(4)①0.4 ②I−是SO2歧化反应的催化剂,H+单独存在时不具有催化作用,但H+可以加快歧化反应速率 ③反应ii比i快;D中由反应ii产生的H+使反应i加快 28.(16分) (1)①2KMnO4+16HCl 2MnCl2+2KCl+5Cl2↑+8H2O ② ③Cl2+2OH− Cl−+ClO−+H2O (2)①i.Fe3+4FeO42−+20H+ 4Fe3++3O2↑+10H2Oii.排除ClO−的干扰 ②>溶液的酸碱性不同 ③理由: FeO42−在过量酸的作用下完全转化为Fe3+和O2,溶液浅紫色一定是MnO4−的颜色 方案: 向紫色溶液b中滴加过量稀H2SO4,观察溶液紫色快速褪去还是显浅紫色高考 赠送以下资料 考试知识点技巧大全 一、考试中途应饮葡萄糖水 大脑是记忆的场所,脑中有数亿个神经细胞在不停地进行着繁重的活动,大脑细胞活动需要大量能量。 科学研究证实,虽然大脑的重量只占人体重量的2%-3%,但大脑消耗的能量却占食物所产生的总能量的20%,它的能量来源靠葡萄糖氧化过程产生。 据医学文献记载,一个健康的青少年学生30分钟用脑,血糖浓度在120毫克/100毫升,大脑反应快,记忆力强;90分钟用脑,血糖浓度降至80毫克/100毫升,大脑功能尚正常;连续120分钟用脑,血糖浓度降至60毫克/100毫升,大脑反应迟钝,思维能力较差。 我们中考、高考每一科考试时间都在2小时或2小时以上且用脑强度大,这样可引起低血糖并造成大脑疲劳,从而影响大脑的正常发挥,对考试成绩产生重大影响。 因此建议考生,在用脑60分钟时,开始补饮25%浓度的葡萄糖水100毫升左右,为一个高效果的考试加油。 二、考场记忆“短路”怎么办呢? 对于考生来说,掌握有效的应试技巧比再做题突击更为有效。 1.草稿纸也要逐题顺序写草稿要整洁,草稿纸使用要便于检查。 不要在一大张纸上乱写乱画,东写一些,西写一些。 打草稿也要像解题一样,一题一题顺着序号往下写。 最好在草稿纸题号前注上符号,以确定检查侧重点。 为了便于做完试卷后的复查,草稿纸一般可以折成4-8块的小方格,标注题号以便核查,保留清晰的分析和计算过程。 2.答题要按先易后难顺序不要考虑考试难度与结果,可以先用5分钟熟悉试卷,合理安排考试进度,先易后难,先熟后生,排除干扰。 考试中很可能遇到一些没有见过或复习过的难题,不要蒙了。 一般中考试卷的题型难度分布基本上是从易到难排列的,或者交替排列。 3.遇到容易试题不能浮躁遇到容易题,审题要细致。 圈点关键字词,边审题边画草图,明确解题思路。 有些考生一旦遇到容易的题目,便觉得心应手、兴奋异常,往往情绪激动,甚至得意忘形。 要避免急于求成、粗枝大叶,防止受熟题答案与解题过程的定式思维影响,避免漏题,错题,丢掉不该丢的分。 4.答题不要犹豫不决选择题做出选择时要慎重,要关注题干中的否定用词,对比筛选四个选项的差异和联系,特别注意保留计算型选择题的解答过程。 当试题出现几种疑惑不决的答案时,考生一定要有主见,有自信心,即使不能确定答案,也不能长时间犹豫,浪费时间,最终也应把认为正确程度最高的答案写到试卷上,不要在答案处留白或开天窗。 5.试卷检查要细心有序应答要准确。 一般答题时,语言表达要尽量简明扼要,填涂答题纸绝不能错位。 答完试题,如果时间允许,一般都要进行试卷答题的复查。 复查要谨慎,可以利用逆向思维,反向推理论证,联系生活实际,评估结果的合理性,选择特殊取值,多次归纳总结。 另外,对不同题型可采用不同的检查方法。 选择题可采用例证法,举出一两例来能分别证明其他选项不对便可安心。 对填空题,则一要检查审题;二要检查思路是否完整;三要检查数据代入是否正确;四要检查计算过程;五要看答案是否合题意;六要检查步骤是否齐全,符号是否规范。 还要复查一些客观题的答案有无遗漏,答案错位填涂,并复核你心存疑虑的项目。 若没有充分的理由,一般不要改变你依据第一感觉做出的选择。 6、万一记忆短路可慢呼吸考试中,有些考生因为怯场,导致无法集中精神,甚至大脑忽然一片空白,发生记忆堵塞。 此时不要紧张,不妨尝试如下方式: 首先是稳定心态,保持镇静,并注意调节自己的呼吸率。 先慢吸气,当对自己说放松时缓慢呼气,再考虑你正在努力回忆的问题,如果你仍不能回想起来,就暂时搁下这道题,开始选做其他会的试题,过段时间再回过头来做这道题。 第二,积极联想。 你不妨回忆老师在讲课时的情景或自己的复习笔记,并努力回忆与发生记忆堵塞问题有关的论据和概念,把回忆起的内容迅速记下来,然后,看能否从中挑出一些有用的材料或线索。 第三,进行一分钟自我暗示。 即根据自己的实际,选择能激励自己,使自己能心情平静和增强信心的话,在心中默念3至5遍。 比如: 我已平静下来,我能够考好、我有信心,一定能考出理想的成绩等等。 第四,分析内容,查找相关要点。 借助试卷上其它试题,也许会给考生提供某些线索。 因此不要轻易放弃,查看试题中的相关要点,看看是否能给考生提供线索或启发。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 北京 高考 化学 答案 完整版 doc
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
 追忆英雄PPTPPT文档格式.pptx
追忆英雄PPTPPT文档格式.pptx
 招聘专员工作饱和度统计表(含公式)表格文件下载.xls
招聘专员工作饱和度统计表(含公式)表格文件下载.xls
