 高三化学中的平衡习题1.docx
高三化学中的平衡习题1.docx
- 文档编号:8923985
- 上传时间:2023-02-02
- 格式:DOCX
- 页数:94
- 大小:1.05MB
高三化学中的平衡习题1.docx
《高三化学中的平衡习题1.docx》由会员分享,可在线阅读,更多相关《高三化学中的平衡习题1.docx(94页珍藏版)》请在冰豆网上搜索。
高三化学中的平衡习题1
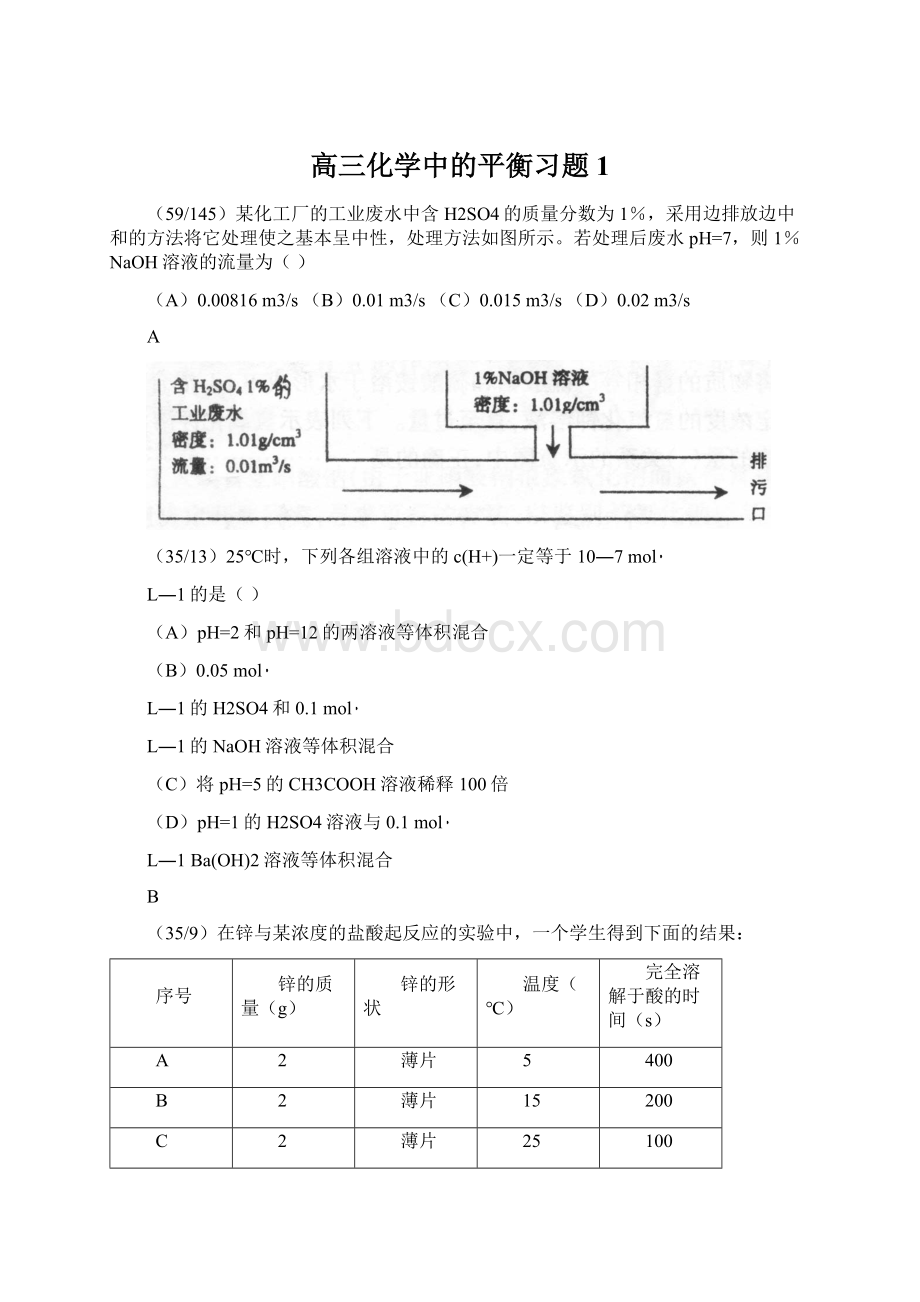
(59/145)某化工厂的工业废水中含H2SO4的质量分数为1%,采用边排放边中和的方法将它处理使之基本呈中性,处理方法如图所示。
若处理后废水pH=7,则1%NaOH溶液的流量为()
(A)0.00816m3/s(B)0.01m3/s(C)0.015m3/s(D)0.02m3/s
A
(35/13)25℃时,下列各组溶液中的c(H+)一定等于10―7mol
L―1的是()
(A)pH=2和pH=12的两溶液等体积混合
(B)0.05mol
L―1的H2SO4和0.1mol
L―1的NaOH溶液等体积混合
(C)将pH=5的CH3COOH溶液稀释100倍
(D)pH=1的H2SO4溶液与0.1mol
L―1Ba(OH)2溶液等体积混合
B
(35/9)在锌与某浓度的盐酸起反应的实验中,一个学生得到下面的结果:
序号
锌的质量(g)
锌的形状
温度(℃)
完全溶解于酸的时间(s)
A
2
薄片
5
400
B
2
薄片
15
200
C
2
薄片
25
100
D
2
薄片
30
t1
E
2
薄片
35
50
F
2
颗粒
15
t2
G
2
粉末
15
t3
则下列说法正确的是()
①t1=75s②t2<200
①①②②全部正确
C
(35/15)在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等质量的氢气。
下列说法正确的是()
(A)甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大
(B)甲烧杯的酸过量
(C)两烧杯中参加反应的锌等量
(D)反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
AC
已知一种c(H+)=1.0×10―3mol
L―1的酸溶液和一种c(OH―)=1.0×10―3mol
L―1的碱溶液等体积混合后呈酸性,其原因可能是()
(A)浓的强酸跟稀的强碱溶液反应(B)浓的弱酸跟稀的强碱溶液反应
(C)等浓度的强酸跟弱碱溶液反应(D)生成了一种强酸弱碱盐
1.将固体NH4I置于密闭容器中,在某温度下发生下列反应:
NH4I(s)
NH3(g)+HI(g),2HI(g)
H2(g)+I2(g),当达到平衡时,c(H2)=0.5mol
L―1,c(HI)=4mol
L―1,则[NH3]为()
(A)3.5mol
L―1(B)4mol
L―1(C)4.5mol
L―1(D)mol
L―1
(35/9)反应A2+B2
2AB+Q,在不同温度和压强改变的条件下,产物AB的质量分数AB%。
生成情况如下图:
a为500℃时的情况;b为300℃时的情况;c为反应在300℃时从时间t3开始向容器中加压的情况。
则下列叙述正确的是()
(A)A2、B2及AB均为气体,Q<0
(B)AB为气体,A2、B2中至少由一种为非气体,Q>0
(C)AB为气体,A2、B2中有一种为非气体,Q>0
(D)AB为固体,A2、B2中有一种为非气体,Q<0
B
(35/13)下列说法正确的是()
(A)相同温度下,1mol
L―1氨水与0.5mol
L―1氨水中,c(OH―)之比为2:
1
(B)0.1mol
L―1NH4Cl溶液中的c(NH4+)=c(Cl―)
(C)向0.1mol
L―1NaNO3溶液中滴加稀盐酸,使溶液pH=5,此时混合液中的c(Na+)=c(NO3―)
(D)向CH3COONa溶液中加入适量CH3COOH,使混合液的pH=7,此时混合液中c(Na+)=c(CH3COO―)
CD
(35/13)0.02mol
L―1的HCN溶液与0.02mol
L―1的NaCN等体积混合,已知混合液中c(CN―) (A)c(HCN)+c(CN―)=0.04mol L―1 (B)c(CN―)>c(HCN) (C)c(Na+)+c(H+)=c(CN―)+c(OH―) (D)c(Na+)>c(CN―)>c(OH―)>c(H+) CD (59/177)在100mLCaCl2和盐酸的混合溶液中加入Na2CO3溶液时,测得生成沉淀和所加入Na2CO3溶液的体积关系曲线如图所示。 若CaCl2溶液的浓度为0.025mol L―1,则原混合溶液的pH为() (A)1.0(B)1.3(C)1.7(D)2.0 B (59/177)地壳内,深度每增加1km,压强大约增加25250~30300kPa,在这样的压强下,对固体物质的转化会发生较大影响,如: CaAl2Si2O8+Mg2SiO4→CaMg2Al2Si3O12 钙长石镁橄榄石钙镁石榴子石 摩尔质量278140.6413.6 密度g/cm32.703.223.50 在地壳区域变质的高压条件下,有利于哪种变化() (A)钙长石的生成(B)镁橄榄石的生成 (C)钙长石和镁橄榄石共存(D)钙镁石榴子石的生成 D (59/155)中学化学教材中有大量数据,下列是某同学对数据的利用情况,其中不正确的是() (A)物质的熔点常可用来判断物质晶体的类型 (B)溶液的密度是溶液的物质的量浓度与溶质质量分数之间换算的必不可少的数据 (C)化学键的键能可用来判断晶体的类型和比较物质的稳定性 (D)电离常数可用来判断某些殿军诶之在溶液中能不能反应,某些场合还可用来判断反应的产物 C (06走向成功3/3)在100mL0.1mol L―1的AgNO3溶液中加入100mL溶有2.08gBaCl2的溶液,再加入 100mL溶有0.01mol L―1CuSO4·5H2O的溶液,充分。 下列说法中正确的是() 最终得到白色沉淀和无色溶液 最终得到的白色沉淀是等物质的量的两种化合物的混合物 在最终得到的溶液中,Cl―的物质的量为0.2mol 在最终得到的溶液中,Cu2+的物质的量浓度为0.01mol L―1 B (06走向成功28/24)在10L固定容积的密闭容器中,A、B、C、D四种气体之间存在着可逆反应。 起始时,A、B的物质的量分别是2mol,C、D为零。 在其它条件不变时各物质的量随反应时间(min)的变化情况如下: 实验序号 I II 温度(℃) 200 250 时间(min) 物质的量(mol) 物质 A B C D A B C D 10 1.70 1.40 0.60 0.30 1.50 1.00 1.00 0.50 20 1.50 1.00 1.00 0.50 1.20 0.40 1.60 0.80 30 1.40 0.80 1.20 0.60 1.20 0.40 1.60 0.80 40 1.40 0.80 1.20 0.60 根据上述数据,回答下列问题: (1)在实验I中,反应0~10min内,A的平均反应速率为_______________________。 (2)该反应的正反应为_________(吸热、放热)反应。 理由为______________________________ _________________________________________________________________________________________。 (3)该反应的平衡常数表达式_________________________________。 (4)若设200℃化学平衡常数为K1,250℃时化学平衡常数为K2,则K1______K2(>、<、=)。 (5)保持实验II的其它条件不变,把A、B混合物放在5L固定容器中反应,则达到平衡的时间一定________(>、<、=)20min,平衡时D的量一定________(>、<、=)0.80min。 3×10―3mol/L·min略略<<= (06走向成功62/26B)某课外兴趣小组对双氧水(H2O2的水溶液)做了如下实验探究。 (1)将质量相同的MnO2分别加入到5mL5%的双氧水中,并用带火星的木条测试。 测定结果如下: 催化剂(MnO2) 操作情况 观察结果 反应完成所需的时间 粉末状 混合不振荡 剧烈反应,带火星的木条复燃 3.5分钟 块状 反应较慢,火星红亮但木条未复燃 30分钟 ①写出H2O2发生的化学反应方程式________________________________________。 ②实验结果说明催化剂作用的大小与______________________________有关。 (2)取三份含有等量的H2O2,但质量分数不同的双氧水,分别向其中加入1gMnO2粉末。 测定结果如下: 双氧水体积 操作情况 反应完成所需的时间 收集到气体体积 反应后液体温度 a1%的150mL 混合不振荡 11分钟 539mL 24℃ a2%的15mL 1分20秒 553mL 56℃ a3%的7.5mL 振荡 9秒 562mL 67℃ 请简要说明: ①反应完成所需的时间不同的原因_______________________________________________________。 ②反应后液体温度不同的原因___________________________________________________________。 ③收集到气体体积不同的原因____________________________________________________________。 2H2O2→2H2O+O2↑(MnO2做催化剂)催化剂的表面积大小(催化剂的颗粒大小) 溶液质量分数不同,液体温度不同,振荡情况不同 反应放热相同,但液体的量不同 液体的量不同,液体温度不同(影响气体在溶液中的溶解量) (66/一)已知NaHSO4在水中的电离方程式为: NaHSO4→Na++H++SO42―。 某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。 下列对该溶液的叙述中,不正确的是() 该温度高于25℃ 由水电离出来的c(H+)=1×10―10 NaHSO4晶体的加入抑止了水的电离 该温度下加入等体积pH为12的NaOH溶液,可使反应后的溶液恰好呈中性 D (66/一)在一恒温、恒容的密闭反应器中发生如下反应: C+H2O CO+H2,为了判定该可逆反应是否达到平衡,没有参考价值的物理量是() 反应器内气体的总压强反应器内气体的总的物质的量 反应器内固体的总质量反应器内物质的总质量 D (66/四)相同温度(25℃)pH=10的水溶液中水的电离度 与纯水的电离度 相比较,下列关系的描述正确的是() 一定是 > 一定是 < 可能是 > ,也可能是 < 一定是 = C (06走向成功虹口/4)700K时,在密闭容器中进行可逆反应SO2(g)+NO2(g) SO3(g)+NO(g),下表表示反应物和生成物的浓度变化情况 时间(s) 0 10 20 30 40 50 SO2(mol L―1) 0.1 0.09 0.07 0.06 0.02 0.02 NO2(mol L―1) 0.2 0.19 0.17 0.16 0.12 0.12 NO(mol L―1) 0 0.01 0.03 0.04 0.08 0.08 SO3(mol L―1) 0 0.01 0.03 0.04 0.08 0.08 (1)该反应的化学平衡常数表达式K=________________________。 (2)根据上表数据,反应开始时,平均反应速率 为_______________________。 (3)若体系的温度升高至900K,该反应的平衡常数值增大,则该反应的逆反应是_________(吸、放)热反应。 (4)若保持温度700K,增大体系的压强至一定数值后,该反应的平衡向正反应方向移动,根据有关知识判断: 此时的平衡常数表达式K与 (1)题中你书写的平衡常数表达式是否相同? ___________。 (5)根据上表数据判断,反应进行至30~40s时,数据发生变化的原因可能是_______________(用文字表达);50s后改变外界条件,在新的条件下,反应至60s达到新的平衡,经测定发现60s时与50s时相比较,SO2、NO的浓度减小。 SO3、NO2的浓度增大,则50s后改变的外界条件可能是______(填写编号)。 A.增加NO2的物质的量B.缩小容器体积 C.通入一定量的O2D.增加SO3的物质的量 0.002放不同加了催化剂C (06走向成功24/30)在100mL的硫酸和硝酸的混合液中,取出10.00mL,加入足量的BaCl2溶液充分反应后,经过滤、洗涤、烘干,可得到4.66g沉淀。 滤液和25.00mL2.00mol L―1NaOH溶液恰好中和。 求: (1)混合液中H2SO4、HNO3的物质的量浓度各是多少? (2)另取10.00mL原混合酸溶液稀释至500mL,该溶液的pH值是多少? H2SO42mol L―1HNO31mol L―11 (06走向成功25/5)下列不具有丁达尔现象的分散系是() (A)云雾(B)生理盐水(C)Fe(OH)3胶体(D)水 B (06走向成功25/7)pH=2的一元弱酸加水稀释,若溶液的体积扩大1000倍,则c(H+)和c(OH―)变化情况是() (A)c(OH―)增大(B)c(H+)与c(OH―)都减小 (C)c(H+)增大(D)c(OH―)减小 A (06走向成功28/24)在10L固定容积的密闭容器中,A、B、C、D四种气体之间存在着可逆反应。 起始时,A、B的物质的量分别是2mol,C、D为零。 在其它条件不变时各物质的量随反应时间(min)的变化情况如下: 实验序号 I II 温度(℃) 200 250 时间(min) 物质的量(mol) 物质 A B C D A B C D 10 1.70 1.40 0.60 0.30 1.50 1.00 1.00 0.50 20 1.50 1.00 1.00 0.50 1.20 0.40 1.60 0.80 30 1.40 0.80 1.20 0.60 1.20 0.40 1.60 0.80 40 1.40 0.80 1.20 0.60 根据上述数据,回答下列问题: (1)在实验I中,反应0~10min内,A的平均反应速率为_______________________。 (2)该反应的正反应为_________(吸热、放热)反应。 理由为______________________________ _________________________________________________________________________________________。 (3)该反应的平衡常数表达式_________________________________。 (4)若设200℃化学平衡常数为K1,250℃时化学平衡常数为K2,则K1______K2(>、<、=)。 (5)保持实验II的其它条件不变,把A、B混合物放在5L固定容器中反应,则达到平衡的时间一定________(>、<、=)20min,平衡时D的量一定________(>、<、=)0.80min。 3×10―3mol/L·min略略<<= (06走向成功34/15)常温下将相同体积的氨水和盐酸混合,发现c(NH4+)=c(Cl―),下列叙述中正确的是() (A)混合溶液的pH>7(B)氨水的电离度减少 (C)混合溶液还能继续中和盐酸(D)氨水和盐酸中溶质的物质的量浓度相等 C (06走向成功35/21)已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。 现有浓度均为0.1mol L―1的NaHSO3溶液和NaHCO3溶液,与两溶液中微粒的物质的量浓度之间的关系均相符合的是(R表示S或C)() (A)c(Na+)>c(HRO3―)>c(H+)>c(RO32―)>c(OH―) (B)c(Na+)+c(H+)=c(HRO3―)+2c(RO32―)+c(OH―) (C)c(H+)+c(H2RO3)=c(RO32―)+c(OH―) (D)两溶液中c(Na+)、c(HRO3―)、c(RO32―)分别相等 BC (06走向成功36/24)在100时,将0.200mol的四氧化二氮气体充入2L抽空的密闭容器中,隔一定的时间对该容器内的物质进行分析,得到数据如下。 仔细阅读表中数据,填写下列空格: 浓度 时间(s) 0 20 40 60 80 100 120 c(N2O4)mol L―1 0.100 c1 0.050 c3 a b 0.08 c(NO2)mol L―1 0.000 0.060 c2 0.120 0.120 0.120 0.240 (1)写出该反应的化学方程式______________________________________。 该反应的平衡常数表达式为___________________________。 (2)20s时四氧化二氮浓度c1=________________mol L―1;0~20s内四氧化二氮的平均反应速率为_________________mol L―1·s―1。 (3)120s时改变了条件,该条件可能是___________________,平衡将朝_____(正、逆)方向移动。 N2O4 2NO20.071.5×10―3缩小容器体积逆 (06走向成功44/25)在一个容积固定的密闭容器中,发生如下反应: aA(g)+bB(g) pC(g)+Q(Q>0)。 反应情况如下表: 时间 c(A)(mol L―1) c(B)(mol L―1) c(C)(mol L―1) 起始 1 3 0 第2min 0.8 2.6 0.4 第4min 0.4 1.8 1.2 第6min 0.4 1.8 1.2 第8min 0.1 2.0 1.8 第9min 0.05 1.9 0.3 根据表中提供的信息,回答: (1)a=______________,b=___________,p=__________(取最小整数)。 (2)写出该反应的平衡常数表达式K=______________。 升高温度,K值将____________。 (3)由表中数据可知在反应第2min到第4min内A的平均速率为_____________mol/L·min。 (4)由表中数据可知反应在第4min到第6min处于平衡状态,若在第2min、第6min、第8min之后分别改变了某一反应条件,改变的条件可能是: 第2min________________或_______________,第6min_________________________,第8min__________________。 122略减小0.2加催化剂升温增加B的浓度减小C浓度 (06走向成功62/26B)某课外兴趣小组对双氧水(H2O2的水溶液)做了如下实验探究。 (1)将质量相同的MnO2分别加入到5mL5%的双氧水中,并用带火星的木条测试。 测定结果如下: 催化剂(MnO2) 操作情况 观察结果 反应完成所需的时间 粉末状 混合不振荡 剧烈反应,带火星的木条复燃 3.5分钟 块状 反应较慢,火星红亮但木条未复燃 30分钟 ①写出H2O2发生的化学反应方程式________________________________________。 ②实验结果说明催化剂作用的大小与______________________________有关。 (2)取三份含有等量的H2O2,但质量分数不同的双氧水,分别向其中加入1gMnO2粉末。 测定结果如下: 双氧水体积 操作情况 反应完成所需的时间 收集到气体体积 反应后液体温度 a1%的150mL 混合不振荡 11分钟 539mL 24℃ a2%的15mL 1分20秒 553mL 56℃ a3%的7.5mL 振荡 9秒 562mL 67℃ 请简要说明: ①反应完成所需的时间不同的原因_______________________________________________________。 ②反应后液体温度不同的原因___________________________________________________________。 ③收集到气体体积不同的原因____________________________________________________________。 2H2O2→2H2O+O2↑(MnO2做催化剂)催化剂的表面积大小(催化剂的颗粒大小) 溶液质量分数不同,液体温度不同,振荡情况不同 反应放热相同,但液体的量不同 液体的量不同,液体温度不同(影响气体在溶液中的溶解量) (66/一)已知NaHSO4在水中的电离方程式为: NaHSO4→Na++H++SO42―。 某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。 下列对该溶液的叙述中,不正确的是() (A)该温度高于25℃ (B)由水电离出来的c(H+)=1×10―10 (C)NaHSO4晶体的加入抑制了水的电离 (D)该温度下加入等体积pH为12的NaOH溶液,可使反应后的溶液恰好呈中性 (66/一)在一恒温、恒容的密闭反应器中发生如下反应: C+H2O CO+H2,为了判定该可逆反应是否达到平衡,没有参考价值的物理量是() (A)反应器内气体的总压强(B)反应器内气体的总的物质的量 (C)反应器内固体的总质量(D)反应器内物质的总质量 (66/四)相同温度(25℃)pH=10的水溶液中水的电离度 与纯水的电离度 相比较,下列关系的描述正确的是() (A)一定是 > (B)一定是 < (C)可能
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 中的 平衡 习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
