 学年人教新版高一化学必修二第二章第二节《化学能与电能》基础题Word版有答案.docx
学年人教新版高一化学必修二第二章第二节《化学能与电能》基础题Word版有答案.docx
- 文档编号:8795893
- 上传时间:2023-02-01
- 格式:DOCX
- 页数:28
- 大小:363.92KB
学年人教新版高一化学必修二第二章第二节《化学能与电能》基础题Word版有答案.docx
《学年人教新版高一化学必修二第二章第二节《化学能与电能》基础题Word版有答案.docx》由会员分享,可在线阅读,更多相关《学年人教新版高一化学必修二第二章第二节《化学能与电能》基础题Word版有答案.docx(28页珍藏版)》请在冰豆网上搜索。
学年人教新版高一化学必修二第二章第二节《化学能与电能》基础题Word版有答案
2017-2018学年人教新版高一化学必修二第二章第二节《化学能
与电能》基础题
一.选择题(共20小题)
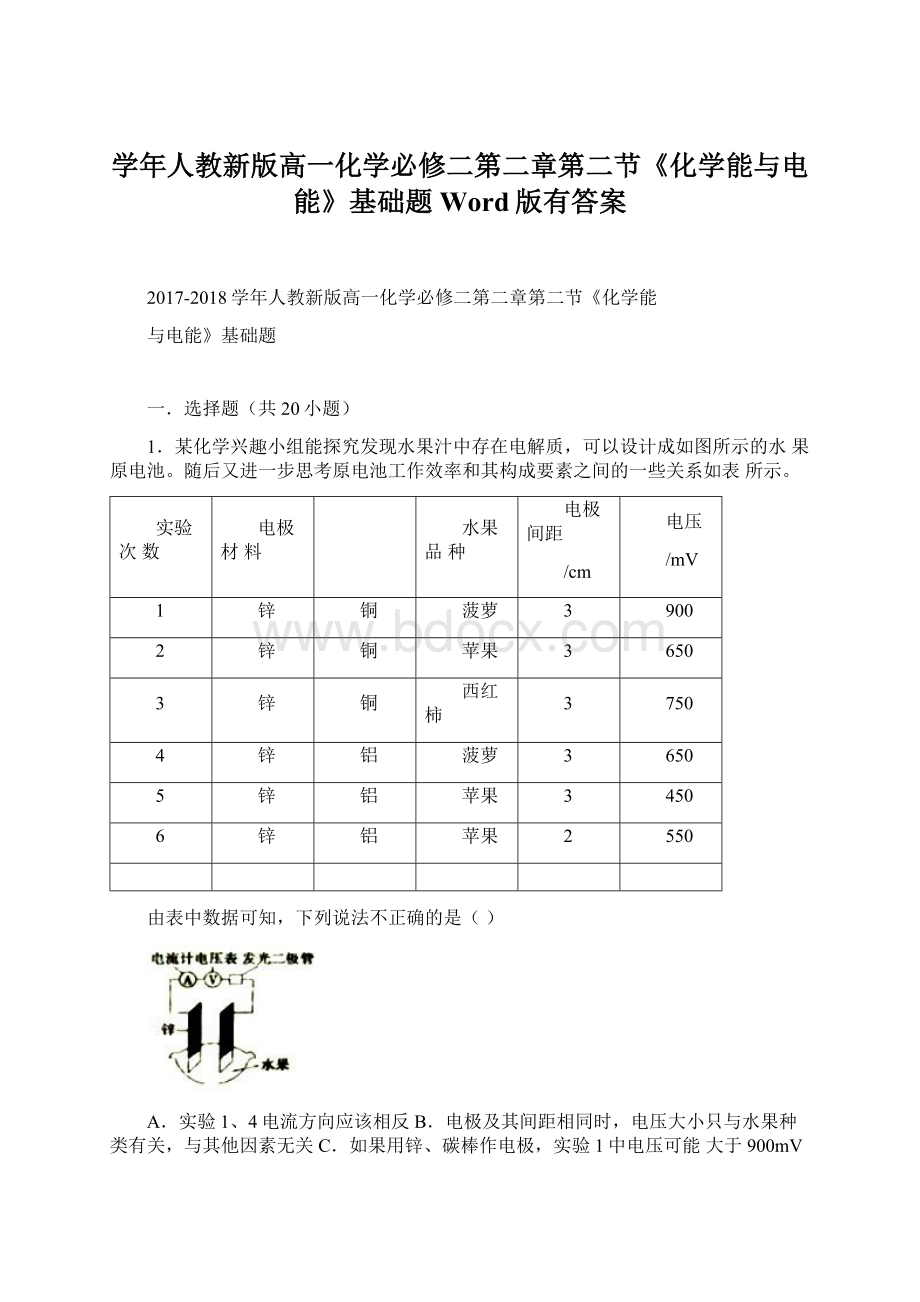
1.某化学兴趣小组能探究发现水果汁中存在电解质,可以设计成如图所示的水果原电池。
随后又进一步思考原电池工作效率和其构成要素之间的一些关系如表所示。
实验次数
电极材料
水果品种
电极间距
/cm
电压
/mV
1
锌
铜
菠萝
3
900
2
锌
铜
苹果
3
650
3
锌
铜
西红柿
3
750
4
锌
铝
菠萝
3
650
5
锌
铝
苹果
3
450
6
锌
铝
苹果
2
550
由表中数据可知,下列说法不正确的是()
A.实验1、4电流方向应该相反B.电极及其间距相同时,电压大小只与水果种类有关,与其他因素无关C.如果用锌、碳棒作电极,实验1中电压可能大于900mVD.实验中发光二极管不太亮,可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来
2.下列有关电池的说法不正确的是()A.手机上用的锂离子电池属于二次电池B.锌锰干电池中,锌电极是负极
C.甲醇燃料电池可把化学能转化为电能
D.铜锌原电池电子沿外电路从铜电极流向锌电极
3.铝表面空气中天然形成的氧化膜耐磨性和抗蚀性不够强,控制一定的条件,用如图所示的电化学氧化法,可在铝表面生成坚硬的氧化膜.下列有关叙述正确的是()
A.阴极上有金属铝生成
B.电极A为石墨,电极
B为金属铝C.OH﹣在电极A上放电,有氧气生成D.阳极的电极反应式为:
2Al﹣6e﹣+3H2O═AL2O3+6H+
4.高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如图所示.下列说法正确的是()
A.铁是阳极,电极反应为Fe﹣2e﹣+2OH﹣═Fe(OH)2
B.电解一段时间后,镍电极附近溶液的pH减小
C.每制得1molNa2FeO4,理论上可以产生67.2L气体
D.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
5.下面有关电化学的图示,完全正确的是()
A.
Cu﹣Zn原电池
B.
粗铜的精炼
C.
铁片镀锌
D.
验证NaCl溶液(含酚酞)电解产物
6.等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是()A.
B.
C.
D.
7.关于下列装置说法正确的是()
A.装置①中,盐桥中的Cl﹣移向CuSO4溶液
B.装置②工作一段时间后,a极表面生成了较多的O2
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,Zn极发生氧化反应
8.关于下列各装置图的叙述中,不正确的是()
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液B.用装置①进行电镀,镀件接在b极上C.装置②的总反应是:
Cu+2Fe3+═Cu2++2Fe2+D.装置③中的铁钉几乎没被腐蚀
9.化学与科技、社会、生产、生活密切相关。
下列有关说法不正确的是()A.铵态氮肥与草木灰混合使用,会损失肥效
B.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质C.绿色化学的核心是应用化学原理对环境污染进行治理
D.天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
10.下列关于铜电极的叙述中不正确的是()A.锌铜原电池中铜是正极
B.在镀件上镀铜时可用金属铜作阳极
C.用电解法精炼粗铜时粗铜作阳极
D.用电解法精炼粗铜时纯铜作阳极
11.我国成功实现持续开采可燃冰。
可燃冰是天然气和水在海底300~3000米的
深度形成的固体,可表示为mCH4•nH2O.下列哪个条件不是形成可燃冰必须具备的()
A.低压B.低温C.高压D.充足的CH4
12.关于下列装置说法正确的是()
4
A.装置①中,盐桥(含有琼胶的KCl饱和溶液)中的K+移向ZnSO溶液
B.装置②工作一段时间后,a极附近溶液的pH减小
C.可以用装置③在铁上镀铜,d极为铜
D.装置④中发生铁的吸氧腐蚀
13.碱性锌锰电池获得了广泛的应用,根据电池的电极反应,下列判断正确()
A.Zn为负极,MnO2为正极
B.Zn为正极,MnO2为负极
C.工作时电子由MnO2经外电路流向Zn极
D.Zn电极发生还原反应,MnO2电极发生氧化反应
14.未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生.下列属于未来新能源标准的是()
①天然气②生物质能③潮汐能④石油⑤太阳能⑥煤⑦风能
⑧氢能.
A.①②③④B.②③⑤⑦⑧C.⑤⑥⑦⑧D.③④⑤⑥⑦⑧
15.根据如图所示的装置,判断下列说法不正确的是()
A.该装置中铜为阳极
B.当铜片的质量变化了12.8g时,a极上消耗的O2在标准状况下的体积为2.24L
C.该装置中b极的电极反应式是:
H2+2OH-﹣2e═2H2O
D.该装置中a极为正极,发生氧化反应
16.下列关于电解池的叙述中不正确的是()
A.与电源正极相连的是电解池的阴极
B.与电源负极相连的是电解池的阴极
C.在电解池的阳极发生氧化反应
D.电子从电源的负极沿导线流入电解池的阴极
17.铅蓄电池充电时,PbSO4()
A.在阳极生成B.在阴极生成
C.在两个电极上生成D.在两个电极上除去
18.在原电池和电解池的电极上所发生的反应,属于氧化反应的是()A.原电池的正极和电解池的阳极所发生的反应
B.原电池的正极和电解池的阴极所发生的反应
C.原电池的负极和电解池的阳极所发生的反应
D.原电池的负极和电解池的阴极所发生的反应
19.对原电池的电极名称,下列叙述中错误的是()A.电子流入的一极为正极B.比较不活泼的一极为正极C.电子流出的一极为负极D.发生氧化反应的一极为正极
20.未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且可以再生.下列最有希望的新能源是()
①天然气②煤③石油④太阳能⑤氢能.
A.①③⑤B.②③④C.①④⑤D.④⑤
二.填空题(共10小题)
21.用铜和硫酸铜溶液、银和硝酸银溶液设计一个原电池,这个原电池的负极是,电极反应式是;正极是,电极反应式是.
22.正确认识和使用电池有利于我们每一个人的日常生活如图所示装置中:
(1)若烧杯中溶液为稀硫酸,正极反应式为.
(2)若烧杯中溶液为氢氧化钠溶液,则负极为,装置中总反应方程式为.
23.按如图装置进行实验,并回答下列问题:
(1)判断装置的名称:
A池为.
(2)锌电极反应式为,石墨棒C1为极,电极反应式为,石墨棒C2附近发生的实验现象为.
(3)当C2极析出2.24L气体(标准状态)时,锌的质量减少了g.CuSO4
溶液的质量增加了g.
24.理论上一个氧化还原反应可以设计成原电池.请将2FeCl3+Cu=CuCl2+2FeCl2
设计为原电池.其负极电极反应为,正极材料可以选.
25.课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图所示连接,C、D、E、F、X、Y都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
(1)电源A极的名称是、电极G的名称是.
(2)甲装置中电解反应相关方程式:
C:
,D:
,总反应方程式:
.
(3)如果收集乙装置中产生的气体,两种气体的体积比是.
(4)欲用丙装置给铜镀银,G应该是(填“铜”或“银”),电镀液的主要成分是(填化学式).
(5)装置丁中的现象是.
26.如图所示,组成一个原电池.当电解质溶液为稀硫酸时:
(1)Fe电极是(填“正”或“负”)极,其电极反应为,该反应是
(填“氧化”或“还原”)反应;
(2)Cu电极是电极,其电极反应为,该反应是反应.
27.如图所示,Zn、Cu与稀硫酸形成的原电池装置中,作负极,发生反应(选填“氧化”或“还原”),负极反应式为;溶液中H+向(选填“正”或“负”)极迁移.
28.在铜锌原电池中,以硫酸铜为电解质溶液,
(1)锌为极,电极反应式为,锌片上观察到的现象为.
(2)铜电极上发生的是反应(填“氧化”或“还原”),电极反应式是,铜片上观察到的现象是.
29.如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图.b电极是极.请写出负极的电极反应方程式:
.
30.已知电池反应Cu+2FeCl3═CuCl2+2FeCl2,则负极材料是,电极反应式为,正极材料是,电极反应式为,电解质为.
2017-2018学年人教新版高一化学必修二第二章第二节
《化学能与电能》基础题
参考答案与试题解析
一.选择题(共20小题)
1.某化学兴趣小组能探究发现水果汁中存在电解质,可以设计成如图所示的水果原电池。
随后又进一步思考原电池工作效率和其构成要素之间的一些关系如表所示。
实验次数
电极材料
水果品种
电极间距
/cm
电压
/mV
1
锌
铜
菠萝
3
900
2
锌
铜
苹果
3
650
3
锌
铜
西红柿
3
750
4
锌
铝
菠萝
3
650
5
锌
铝
苹果
3
450
6
锌
铝
苹果
2
550
由表中数据可知,下列说法不正确的是()
A.实验1、4电流方向应该相反B.电极及其间距相同时,电压大小只与水果种类有关,与其他因素无关C.如果用锌、碳棒作电极,实验1中电压可能大于900mVD.实验中发光二极管不太亮,可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来
【解答】解:
A.实验1中Zn为负极,实验4中Zn为正极,所以实验1、4电流方向应该相反,故A正确;
B.根据图表知,当1、2比较时,电极材料相同,水果不同,导致电压不同,所
以电压与水果有关;比较1、5时,水果相同,电极材料不同,电压不同,所以电压与电极材料有关,故B错误;C.金属性差别越大,电流越强,所以如果用锌、碳棒作电极,实验1中电压可能大于900mV,故C正确;D.原电池中的二极管不亮,说明电压较低,将多个此电池串联起来,增大电压,然后再接发光二极管,故D正确;
故选:
B。
2.下列有关电池的说法不正确的是()A.手机上用的锂离子电池属于二次电池B.锌锰干电池中,锌电极是负极C.甲醇燃料电池可把化学能转化为电能D.铜锌原电池电子沿外电路从铜电极流向锌电极
【解答】解:
A.锂离子电池能充放电,属于二次电池,放电时是将化学能转化为电能,充电时是将电能转化为化学能,故A正确;B.锌锰干电池中,锌易失电子发生氧化反应而作负极、二氧化锰得电子发生还原反应而作正极,故B正确;C.甲醇燃料电池属于原电池,是将化学能转化为电能的装置,故C正确;D.铜锌原电池中,锌作负极、Cu作正极,电子从负极锌沿导线流向正极铜,故D错误;
故选:
D。
3.铝表面空气中天然形成的氧化膜耐磨性和抗蚀性不够强,控制一定的条件,用如图所示的电化学氧化法,可在铝表面生成坚硬的氧化膜.下列有关叙述正确的是()
A.阴极上有金属铝生成
B.电极A为石墨,电极B为金属铝C.OH﹣在电极A上放电,有氧气生成D.阳极的电极反应式为:
2Al﹣6e﹣+3HO═ALO+6H+
223
2
【解答】解:
A、阴极反应为:
2H++2e﹣=H↑,故A错误;
B、电极A为Al,故B错误;
C、电解质为硫酸溶液,氢氧根离子不可能参加反应,阳极反应为:
2Al+3H2O﹣
﹣+
6e=Al2O3+6H,故C错误;
﹣+
D、阳极反应为:
2Al+3H2O﹣6e
故选:
D。
=Al2O3+6H,故D正确;
4.高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶
液制备高铁酸钠(Na2FeO4)的装置如图所示.下列说法正确的是()
2
A.铁是阳极,电极反应为Fe﹣2e﹣+2OH﹣═Fe(OH)
B.电解一段时间后,镍电极附近溶液的pH减小
C.每制得1molNa2FeO4,理论上可以产生67.2L气体
﹣
D.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42
【解答】解:
A.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4),铁失电子生成高铁酸钠,则铁作阳极,镍作阴极,电极反应式为Fe+8OH﹣﹣6e﹣
﹣
=FeO42
+4H2O,故A错误;
B.镍电极上氢离子放电生成氢气,氢离子浓度减小,所以溶液的pH增大,故B
错误;
C.温度和压强未知,所以无法计算生成气体体积,故C错误;
D.若离子交换膜为阴离子交换膜,则电解结束后由于浓度差左侧溶液中会含有
FeO42
﹣,故D正确;
故选:
D。
5.下面有关电化学的图示,完全正确的是()
A.
Cu﹣Zn原电池
B.
粗铜的精炼
C.
铁片镀锌
D.
验证NaCl溶液(含酚酞)电解产物
【解答】解:
A、由图可知,金属性Zn>Cu,则原电池中Zn作负极,故A错误;B、与电源负极相连的为阴极,粗铜的精炼中粗铜作阳极,由图可知,粗铜作阴极,故B错误;C、与电源负极相连的为阴极,铁片镀锌,铁片应作阴极,由图可知,铁片作阳极,故C错误;D、电流由正极流向负极,由图可知,碳棒为阳极,电解食盐水在阳极生成氯气,
氯气与碘化钾淀粉溶液反应使溶液变蓝,在阴极生成氢气,溶液变红,故D正
确;故选:
D。
6.等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是()A.
B.
C.
D.
【解答】解:
锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属锌和硫酸反应的速率,所以反应速率是:
a>b,速率越大,锌完全反应时所用的时间越短,所以a所用的时间小于b的时间;产生氢气的量取决于金属锌的质量,而a中,金属锌一部分用于置换金属铜,导致和硫酸反应生成氢气的量减少,所以氢气的体积是:
a<b。
故选:
A。
7.关于下列装置说法正确的是()
4
A.装置①中,盐桥中的Cl﹣移向CuSO溶液
B.装置②工作一段时间后,a极表面生成了较多的O2
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,Zn极发生氧化反应
【解答】解:
A.原电池中,阴离子向负极移动,题中锌为负极,则盐桥中的Cl
4
﹣移向ZnSO
溶液,故A错误;
B.为电解池,a为阴极,生成氢气和氢氧化钠,a极表面生成了较多的H2,故B
错误;
C.精炼铜时,电解液应为氯化铜,且粗铜为阳极,则c为Cu极,故C错误;D.锌比铁活泼,锌为负极,锌失电子,发生氧化反应,电子从锌流向铁,故D正确。
故选:
D。
8.关于下列各装置图的叙述中,不正确的是()
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液B.用装置①进行电镀,镀件接在b极上C.装置②的总反应是:
Cu+2Fe3+═Cu2++2Fe2+D.装置③中的铁钉几乎没被腐蚀
【解答】解:
A、根据电流的方向可知a为电解池的阳极,则用来精炼铜时,a
极为粗铜,电解质溶液为CuSO4溶液,故A正确;
B、根据电流的方向可知b为电解池的阴极,所以进行电镀时,镀件接在b极上,故B正确;
C、铁比铜活泼,为原电池的负极,发生的反应为Fe+2Fe3+=3Fe2+,故C错误;
D、浓硫酸具有吸水性,在干燥的环境中铁难以腐蚀,故D正确。
故选:
C。
9.化学与科技、社会、生产、生活密切相关。
下列有关说法不正确的是()
A.铵态氮肥与草木灰混合使用,会损失肥效
B.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质C.绿色化学的核心是应用化学原理对环境污染进行治理D.天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
【解答】解:
A、草木灰成分为碳酸钾,溶液中碳酸根离子水解溶液显碱性,氮肥中铵根离子水解溶液显酸性,铵态氮肥能与草木灰碱性物质混合产生氨气,造成肥效降低,故A正确;B.硅胶具有开放的多孔结构,吸附性强,可做食品的吸水剂,铁粉具有强还原性,可作抗氧化剂,故B正确;C.绿色化学的核心是要利用化学原理从源头消除污染,实现零排放,而不是对环境污染进行治理,故C错误;D.沼气是由植物秸秆发酵形成的属于可再生能源;天然气是由古代生物在地下发生复杂的变化形成的,属于化石能源;水煤气是由C与水蒸气在高温条件下反应生成的属于二次能源,故D正确;
故选:
C。
10.下列关于铜电极的叙述中不正确的是()A.锌铜原电池中铜是正极B.在镀件上镀铜时可用金属铜作阳极C.用电解法精炼粗铜时粗铜作阳极D.用电解法精炼粗铜时纯铜作阳极
【解答】解:
A.锌比铜活泼,锌铜原电池中铜是正极,故A正确;B.在镀件上镀铜时可用金属铜作阳极,电解质为铜盐溶液,阴极上析出铜,故B正确;C.用电解法精炼粗铜时粗铜作阳极,粗铜中的锌、铁、银、金等金属可与铜分离,故C正确;
D.用电解法精炼粗铜时纯铜作阴极,可起到提纯铜的目的,故D错误。
故选:
D。
11.我国成功实现持续开采可燃冰。
可燃冰是天然气和水在海底300~3000米的
深度形成的固体,可表示为mCH4•nH2O.下列哪个条件不是形成可燃冰必须具备的()
A.低压B.低温C.高压D.充足的CH4
【解答】解:
可燃冰是天然气和水在海底300~3000米的深度形成的固体,是低温高压条件下许多天然气被包进水分子中,在海底的低温(2~5℃)与压力下结晶,形成“可燃冰”,故不是形成可燃冰必须具备的条件是低压,故选A。
12.关于下列装置说法正确的是()
4
A.装置①中,盐桥(含有琼胶的KCl饱和溶液)中的K+移向ZnSO溶液
B.装置②工作一段时间后,a极附近溶液的pH减小
C.可以用装置③在铁上镀铜,d极为铜
D.装置④中发生铁的吸氧腐蚀
4
【解答】解:
A.原电池中阳离子向正极移动,铜是正极,所以K+移向CuSO溶
液,故A错误;
B.装置②工作一段时间后,a极与电源的负极相连是阴极,电极反应式为:
水中的氢离子放电,产生氢氧根离子,所以溶液的PH值增大,故B错误;C.电镀时,待镀金属作阴极,镀层金属为阳极,则Cu为阳极,即d极为铜,故C正确;D.活泼金属锌是负极,所以锌失电子,则锌为负极,即锌发生吸氧腐蚀,故D错误;
故选:
C。
13.碱性锌锰电池获得了广泛的应用,根据电池的电极反应,下列判断正确()
A.Zn为负极,MnO2为正极
B.Zn为正极,MnO2为负极
C.工作时电子由MnO2经外电路流向Zn极
D.Zn电极发生还原反应,MnO2电极发生氧化反应
【解答】解:
A、碱性锌锰电池中,锌失电子作负极,MnO2得电子作正极,故A
正确;
B、锌失电子作负极,MnO2得电子作正极,故B错误;C、工作时电子从负极经过外电路流向正极,即电子由Zn经外电路流向MnO2,故C错误;
D、锌失电子发生氧化反应,MnO2电极得电子发生还原反应,故D错误;故选:
A。
14.未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生.下列属于未来新能源标准的是()
①天然气②生物质能③潮汐能④石油⑤太阳能⑥煤⑦风能
⑧氢能.
A.①②③④B.②③⑤⑦⑧C.⑤⑥⑦⑧D.③④⑤⑥⑦⑧
【解答】解:
煤、石油、天然气是化石能源是不可再生能源,燃烧时生成的污染物较多,不是新能源;常见新能源有:
太阳能、地热能、潮汐能、风能、氢能、生物质能等,它们都是可再生、无污染的新能源。
故选:
B。
15.根据如图所示的装置,判断下列说法不正确的是()
A.该装置中铜为阳极
B.当铜片的质量变化了12.8g时,a极上消耗的O2在标准状况下的体积为2.24
L
﹣﹣
C.该装置中b极的电极反应式是:
H2+2OH
D.该装置中a极为正极,发生氧化反应
﹣2e
═2H2O
【解答】解:
A、右边装置是电解池,铜电极连接原电池的正极,所以铜电极是
电解池的阳极,故A正确。
B、根据放电过程中,根据得失电子数相等计算消耗氧气的体积,设消耗氧气的体积为v。
根据得失电子数相等得氧气和铜的关系式为:
O2﹣﹣﹣﹣﹣﹣2Cu
22.4L128g
V12.8g
V=
=2.24L,故B正确。
C、左边装置是原电池,负极上氢气失电子和氢氧根离子反应生成水,电极反应
﹣﹣
式为:
H2+2OH
﹣2e
═2H2O,故C正确。
D、左边装置是原电池,正极上氧气得电子发生还原反应,故D错误。
故选:
D。
16.下列关于电解池的叙述中不正确的是()A.与电源正极相连的是电解池的阴极B.与电源负极相连的是电解池的阴极C.在电解池的阳极发生氧化反应D.电子从电源的负极沿导线流入电解池的阴极
【解答】解:
A、电解池中,与外接电源负极相连的为阴极,与正极相连的为阳极,故A错误;
B、电解池中,与外接电源负极相连的为阴极,故B正确;C、与正极相连的为阳极,阳极上得电子发生氧化反应,故C正确;D、与外接电源负极相连的为阴极,电子从负极经导线流入阴极,故D正确;故选:
A。
17.铅蓄电池充电时,PbSO4()
A.在阳极生成B.在阴极生成
C.在两个电极上生成D.在两个电极上除去
42
﹣
【解答】解:
铅蓄电池放电时,负极电解反应:
Pb﹣2e﹣+SO
﹣
=PbSO4
,正极电
+
﹣
﹣
极反应:
PbO2+2e
﹣+4H++SO
=PbSO4+2H2O,充电是放电的逆反应,阳极上发生
42
﹣
反应为:
PbSO4+2H2O﹣2e
=PbO2+4H+2SO42
,阴极发生反应为:
PbSO4=Pb﹣2e
﹣
+SO42,
故选:
D。
18.在原电池和电解池的电极上所发生的反应,属于氧化反应的是()A.原电池的正极和电解池的阳极所发生的反应B.原电池的正极和电解池的阴极所发生的反应C.原电池的负极和电解池的阳极所发生的反应D.原电池的负极和电解池的阴极所发生的反应
【解答】解:
原电池负极上失电子发生氧化反应,正极上得电子发生还原反应;电解池中,阳极上失电子发生氧化反应,阴极上得电子发生还原反应,故选:
C。
19.对原电池的电极名称,下列叙述中错误的是()A.电子流入的一极为正极B.比较不活泼的一极为正极C.电子流出的一极为负极D.发生氧化反应的一极为正极
【解答】解:
A、原电池中,电子从负极沿导线流向正极,所以电子流入的一极为正极,故A正确。
B、原电池中,负极上失电子发生氧化反应,正极上得电子发生还原反应,所以较活泼的金属作负极,较不活泼的电极为正极,故B正确。
C、原
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学能与电能 学年 新版 高一化学 必修 第二 化学能 电能 基础 Word 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
