 高考专题训练工艺流程题二.docx
高考专题训练工艺流程题二.docx
- 文档编号:8640016
- 上传时间:2023-02-01
- 格式:DOCX
- 页数:11
- 大小:271.10KB
高考专题训练工艺流程题二.docx
《高考专题训练工艺流程题二.docx》由会员分享,可在线阅读,更多相关《高考专题训练工艺流程题二.docx(11页珍藏版)》请在冰豆网上搜索。
高考专题训练工艺流程题二
工艺流程练习题
(二)
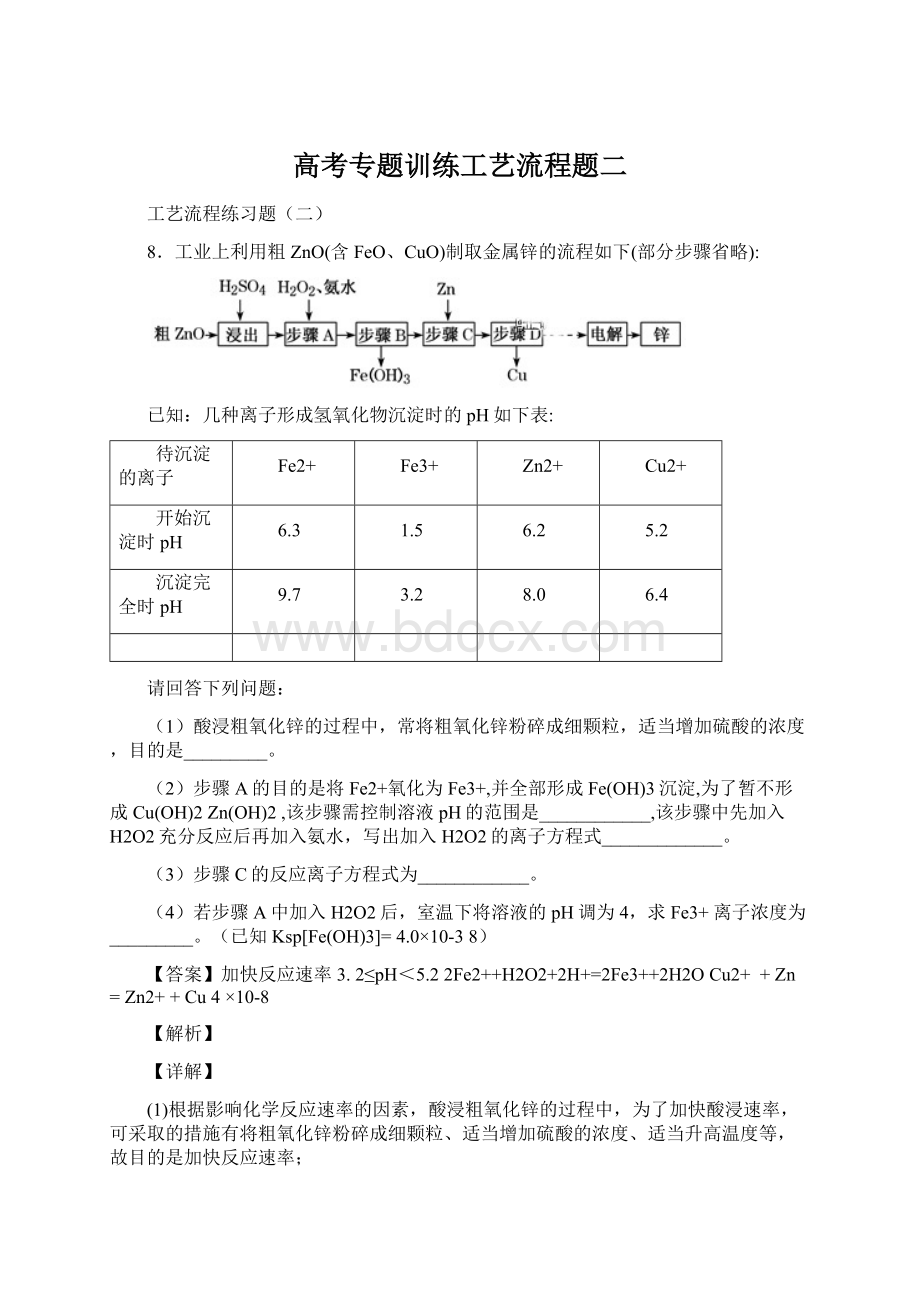
8.工业上利用粗ZnO(含FeO、CuO)制取金属锌的流程如下(部分步骤省略):
已知:
几种离子形成氢氧化物沉淀时的pH如下表:
待沉淀的离子
Fe2+
Fe3+
Zn2+
Cu2+
开始沉淀时pH
6.3
1.5
6.2
5.2
沉淀完全时pH
9.7
3.2
8.0
6.4
请回答下列问题:
(1)酸浸粗氧化锌的过程中,常将粗氧化锌粉碎成细颗粒,适当增加硫酸的浓度,目的是_________。
(2)步骤A的目的是将Fe2+氧化为Fe3+,并全部形成Fe(OH)3沉淀,为了暂不形成Cu(OH)2Zn(OH)2,该步骤需控制溶液pH的范围是____________,该步骤中先加入H2O2充分反应后再加入氨水,写出加入H2O2的离子方程式_____________。
(3)步骤C的反应离子方程式为____________。
(4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,求Fe3+离子浓度为_________。
(已知Ksp[Fe(OH)3]=4.0×10-38)
【答案】加快反应速率3.2≤pH<5.22Fe2++H2O2+2H+=2Fe3++2H2OCu2++Zn=Zn2++Cu4×10-8
【解析】
【详解】
(1)根据影响化学反应速率的因素,酸浸粗氧化锌的过程中,为了加快酸浸速率,可采取的措施有将粗氧化锌粉碎成细颗粒、适当增加硫酸的浓度、适当升高温度等,故目的是加快反应速率;
(2)氢氧化铁沉淀时的pH是1.48~3.2,Zn(OH)2沉淀时的pH为6.2~8.0,和Cu(OH)2沉淀时的pH为5.2~6.4,因此将Fe2+氧化为Fe3+,并全部形成Fe(OH)3沉淀,为了暂不形成Cu(OH)2、Zn(OH)2,该步骤需控制溶液pH的范围为3.2 (3)步骤C中加入锌,发生锌和硫酸铜反应生成铜和硫酸锌,反应离子方程式为Cu2++Zn=Zn2++Cu; (4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,c(H+)=10-4mol/L,c(OH-)=10-10mol/L,Ksp[Fe(OH)3]=c(Fe3+)c3(OH-)=c(Fe3+)×(10-10mol/L)3=4.0×10-38,故c(Fe3+)=4.0×10-8mol/L。 9.某工业废料含SiO2、FeS和CuS等物质,采用如下实验方案进行回收利用。 请回答下列问题: (1)已知步骤①中发生的化学反应为非氧化还原反应,写出产生气体的电子式_______,该气体可用足量的NaOH溶液吸收,该反应的离子方程式是__________________。 (2)步骤②的操作依次为______、_______、过滤、洗涤、干燥。 滤渣2的主要成分是SiO2和S,写出步骤③涉及的化学方程式________________________________。 (3)所得硫酸亚铁晶体中的Fe2+,可以用_________________________(填试剂化学式)检验。 【答案】 H2S+2OH-=S2-+2H2O蒸发浓缩降温结晶CuS+H2O2+H2SO4 CuSO4+S+2H2ONaOH溶液或Cl2、KSCN溶液 【解析】 【详解】 工业废料中含SiO2、FeS和CuS等物质,加入H2SO4溶液酸浸,FeS与硫酸反应产生H2S气体,二氧化硅不溶于硫酸,硫化铜难溶于酸,所以滤渣1为二氧化硅和硫化铜,滤液1为FeSO4溶液,将滤液1蒸发浓缩、冷却结晶、过滤洗涤、干燥得到FeSO4·7H2O,向滤渣1加入H2SO4溶液和H2O2溶液并加热,浸出得到滤渣2为SiO2,高温用C还原SiO2制备Si单质,CuS在酸性溶液中被H2O2氧化生成硫酸铜、硫单质和水,滤液蒸发浓缩、冷却结晶、过滤洗涤、干燥得到硫酸铜晶体。 (1)H2S为共价化合物,硫原子和两个氢原子形成共价键,电子式为: ,H2S和NaOH溶液反应生成Na2S和H2O,反应的离子方程式为: H2S+2OH-=S2-+2H2O; (2)步骤②的操作依次为: 蒸发浓缩降温结晶,过滤、洗涤、干燥。 滤渣2的主要成分是SiO2和S,写出步骤③涉及的化学方程式: CuS+H2O2+H2SO4 CuSO4+S+2H2O; (3)所得硫酸亚铁晶体中的Fe2+,可以向该溶液中加入NaOH溶液,若发生反应: Fe2++2OH-=Fe(OH)2↓,产生白色沉淀;或向该溶液中滴加KSCN溶液,无明显现象,再滴加几滴新制Cl2水,溶液变为血红色,发生反应方程式: 2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-=Fe(SCN)3,使溶液变为血红色。 10.我国是世界上最早制得和使用金属锌的国家。 一种以闪锌矿(主要成份是ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示: 相关金属离子[c(Mn+)=0.10mol·L–1]形成氢氧化物沉淀的pH范围如下: 金属离子 Fe3+ Fe2+ Zn2+ Cd2+ 开始沉淀的pH 1.5 6.3 6.3 7.4 沉淀完全的pH 2.8 8.3 8.2 9.4 回答下列问题: (1)写出ZnS的电子式__________________________; 焙烧过程中主要反应的化学方程式为__________________________。 (2)滤渣1的成分为: ___________________; (3)试剂Y是_________(只要求填写一种),调PH值的范围是___________________。 (4)电解硫酸锌溶液制备单质锌时,电解的总反应离子方程式为: ___________________。 (5)为将溶液中的Fe2+氧化,试剂X可选用的是_______。 (填序号) A.H2O2B.H2SC.HNO3D.O2 【答案】 2ZnS+3O2 2ZnO+2SO2SiO2、PbSO4ZnO(或ZnCO3、Zn(OH)2等)2.8≤PH<6.32Zn2++2H2O 2Zn+4H++O2↑AD 【解析】 【分析】 (1)ZnS为离子化合物,以此写出其电子式;在焙烧过程中产生气体,硫化物高温状态下产生氧化物及SO2,以此写出反应的化学方程式; (2)根据焙烧产生的PbO在H2SO4加入后产生PbSO4固体以及SiO2不溶于硫酸分析滤渣1的成分; (3)加试剂Y是为了调节溶液的pH,不能引入新的杂质,可选用氧化锌等化合物,由Fe3+和Zn2+等沉淀所需的pH分析调pH值的范围; (4)根据阴极得电子,析出单质锌,阳极是水失电子生成氧气,写出电解的总反应离子方程式; (5)为将溶液中的Fe2+氧化,试剂X需选用氧化剂,且不能引入新的杂质,据此分析。 【详解】 (1)ZnS为离子化合物,其电子式为 ; 由流程图可知,在焙烧过程中产生气体,硫化物高温状态下产生氧化物及SO2,化学方程式为: 2ZnS+3O2 2ZnO+2SO2; 故答案为: ;2ZnS+3O2 2ZnO+2SO2; (2)闪锌矿焙烧后的主要成分变为ZnO,还存在少量的SiO2、Fe2O3、CdO、PbO,加稀硫酸后发生一系列反应,其中PbO在H2SO4加入后产生PbSO4固体,PbSO4和SiO2不溶于水,以沉淀的形式沉降下来,所以滤渣1的成分为: SiO2、PbSO4; 故答案为: SiO2、PbSO4; (3)加入ZnO(或ZnCO3、Zn(OH)2等)与过量的H2SO4反应,调节pH,使Fe3+沉淀,所以试剂Y是ZnO(或ZnCO3、Zn(OH)2等);由表可知,使Fe3+沉淀完全,而Zn2+不沉淀,pH范围为: 2.8≤pH<6.3, 故答案为: ZnO(或ZnCO3、Zn(OH)2等);2.8≤PH<6.3; (4)电解硫酸锌溶液制备单质锌时,阴极得电子,因为Zn2+浓度较大,Zn2+得电子析出单质锌,阳极是水失电子生成氧气,所以电解的总反应离子方程式为: 2Zn2++2H2O 2Zn+4H++O2↑, 故答案为: 2Zn2++2H2O 2Zn+4H++O2↑; (5)为将溶液中的Fe2+氧化,试剂X需选用氧化剂,且不能引入新的杂质,选项中H2O2和O2符合题意,即应选AD。 故答案为: AD。 11.孔雀石的主要成分为Cu2(OH)2CO3,还含少量的FeO、Fe2O3、SiO2。 实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下: 为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如表。 请回答: 物质 pH(开始沉淀) pH(完全沉淀) Fe(OH)3 1.9 3.2 Fe(OH)2 7.0 9.0 Cu(OH)2 4.7 6.7 (1)孔雀石首先要粉碎,其目的是_____;溶液A中的金属阳离子有_________;若调pH=9.0将杂质铁元素除去,其后果是: ________________________________。 (2)“除杂”时先加入足量H2O2,目的是________________________;再加入CuO固体调节溶液pH的范围至_________,其中加入CuO作用是____________________。 (3)操作X包括________________、_________________、过滤和洗涤等;在进行该操作时,将溶液B再适当酸化目的是_________________________________________。 (4)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论)________________。 【答案】增大接触面,加快反应速率,使反应更充分Cu2+、Fe2+、Fe3+溶液pH=9.0时Cu2+也会沉淀将Fe2+氧化成Fe3+3.2<pH<4.7H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀蒸发浓缩、冷却结晶抑制Cu2+的水解取待检溶液少许,加入KSCN溶液,若溶液不变红色,说明Fe3+已完全除去若溶液变红色,则说明Fe3+未完全除去 【解析】 【分析】 孔雀石的主要成分为Cu2(OH)2CO3,还含少量FeO、Fe2O3、SiO2,加入稀硫酸反应后生成二氧化碳气体,得到溶液A,溶液A的主要成分为硫酸铜、硫酸亚铁、硫酸铁,过滤得到二氧化硅固体;然后将滤液中的Fe2+氧化成Fe3+,再加入CuO固体调节溶液pH沉淀铁离子,过滤得到硫酸铜溶液,硫酸铜溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到胆矾晶体。 【详解】 (1)孔雀石首先要粉碎,目的是增大孔雀石的表面积,增大与硫酸的接触面积,加快反应速率,使反应更充分;加入稀硫酸反应后,得到溶液A,溶液A的主要成分为硫酸铜、硫酸亚铁、硫酸铁,金属阳离子有Cu2+、Fe2+、Fe3+;调溶液pH的目的是使铁离子沉淀时铜离子不会沉淀,由表中数据可知溶液pH=9.0 时Cu2+也会沉淀,故答案为: 增大接触面,加快反应速率,使反应更充分;Cu2+、Fe2+、Fe3+;溶液pH=9.0时Cu2+也会沉淀; (2)溶液A中的金属阳离子有Cu2+、Fe2+、Fe3+,亚铁离子沉淀时铜离子也会沉淀,而铁离子沉淀时铜离子不会沉淀,故应将亚铁离子氧化为铁离子再除去,则需要加氧化剂,双氧水能氧化亚铁离子且不会引入新杂质,由表中数据可知,铁离子沉淀完全的pH为3.2,而铜离子开始沉淀的pH为4.7,调节溶液pH的范围至3.2~4.7之间,CuO固体能中和溶液中H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀,故答案为: 将Fe2+氧化成Fe3+;3.2<pH<4.7;H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀; (3)硫酸铜溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到胆矾晶体,铜离子在水溶液中会水解,应适当酸化抑制其水解,故答案为: 蒸发浓缩;冷却结晶;抑制Cu2+的水解; (4)检验溶液中Fe3+是否完全除去,就是检验溶液中是否存在Fe3+,检验Fe3+的方法是取待检溶液少许,加入KSCN溶液,若溶液不变红色,说明Fe3+已完全除去,若溶液变红色,则说明Fe3+未完全除去,故答案为: 取待检溶液少许,加入KSCN溶液,若溶液不变红色,说明Fe3+已完全除去,若溶液变红色,则说明Fe3+未完全除去。 【点睛】 本题考查了化学工艺流程,试题知识点较多、综合性较强,充分考查了分析能力及化学实验能力,涉及了物质制备的过程分析判断、杂质离子的分离、离子性质的理解应用、离子的检验等,明确实验目的、实验原理,理解流程为解答关键。 12.海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。 其流程如下图所示: (1)写出镁原子的结构示意图: _________________。 在反应①→⑤中属于氧化还原反应的是___________(填序号); (2)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下: ①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、________溶液;③_________;④滤液中加适量盐酸;⑤__________(请补全缺少的实验步骤或试剂); (3)某同学利用反应①原理制备氯气,将200mL5.0mol·L-1NaCl溶液进行电解,则理论上最多可制得标准状况下氯气的体积为__________L; (4)实验室模拟Mg的制取流程时,用11.3mol·L-1的浓盐酸配置反应③所需要的0.5mol·L―1稀盐酸100mL,需要用量筒量取浓盐酸________mL,接下来的配制过程除了玻璃棒和烧杯外,还需要用到的玻璃仪器有___________________。 【答案】 ①⑤Na2CO3过滤蒸发结晶11.24.4胶头滴管、100mL容量瓶 【解析】 【分析】 (1)镁离子质子数为12,核外电子数为10,有2个电子层,各层电子数为2、8;有元素化合价发生变化的反应属于氧化还原反应,结合具体反应判断; (2)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,据此判断; (3)根据n=cV计算NaCl的物质的量,结合方程式计算生成氯气的体积; (4)根据稀释过程中溶质的物质的量不变计算,结合物质的量浓度溶液的配制原理和步骤判断需要的仪器。 【详解】 (1)镁离子质子数为12,核外电子数为10,有2个电子层,各层电子数为2、8,镁离子结构示意图为 ;反应①是电解食盐水生成氢氧化钠、氯气与氢气,属于氧化还原反应,反应②是溶液中镁离子与石灰乳反应生成氢氧化镁沉淀,属于非氧化还原反应,反应③是氢氧化镁与盐酸反应,属于非氧化还原反应,反应④是氯化镁晶体失去结晶水得到氯化镁,属于非氧化还原反应,反应⑤是分解熔融氯化镁生成镁与氯气,属于氧化还原反应,故答案为①⑤; (2)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后过滤,向滤液加入盐酸酸化。 但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,因此为制得纯净的NaCl晶体,操作如下: ①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③过滤;④滤液中加适量盐酸;⑤蒸发结晶; (3)200mL5mol•L-1NaCl溶液中NaCl的物质的量=0.2L×5mol/L=1mol,由2NaCl+2H2O 2NaOH+Cl2↑+H2↑可知生成氯气为1mol×1/2=0.5mol,标况下,生成氯气的体积=0.5mol×22.4L/mol=11.2L; (4)由于稀释过程中溶质的物质的量不变,则需要用量筒量取浓盐酸的体积为100mL×0.5mol·L-1/11.3mol·L-1≈4.4mL;用浓盐酸配制稀盐酸的一般步骤分别是计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,需要的仪器除了量筒、玻璃棒和烧杯外,还需要用到的玻璃仪器有胶头滴管、100mL容量瓶。 【点睛】 本题以海水资源开发利用为载体,考查核外电子排布、氧化还原反应、离子方程式、化学计算、化学实验基本操作等,需要学生熟练掌握基础知识,明确物质的性质和原理是解答的关键。 13.某铜矿石的主要成分是Cu2O,还含有少量的Al2O3、Fe2O3和SiO2。 某工厂利用此矿石炼制精铜的工艺流程如图所示(已知: Cu2O+2H+=Cu+Cu2++H2O)。 (1)滤液A中铁元素的存在形式为______________(填离子符号),生成该离子的离子方程式为____________________________________________________________________, (2)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为_____________, 在实验室中完成此实验还需要的试剂是________。 a.KClO3b.KClc.Mgd.MnO2 (3)溶液G与固体混合物B反应的离子方程式为__________________________。 【答案】Fe2+2Fe3++Cu=2Fe2++Cu2+2Al+Fe2O3 Al2O3+2FeacSiO2+2OH−=SiO32−+H2O 【解析】 【分析】 某铜矿石的成分中含有Cu2O,还含有少量的Al2O3、Fe2O3和SiO2,加入足量稀硫酸过滤,Cu2O溶于酸反应生成铜和铜盐,所以固体混合物B为Cu、SiO2,滤液A中为亚铁离子、铝离子和铜离子,加入足量氢氧化钠溶液过滤得到固体混合物D为氢氧化铜、氢氧化铁,滤液为C为AlO2-离子,金属E与固体F发生的某一反应可用于焊接钢轨,金属E为Al,固体混合物D空气中加热灼烧得到氧化铁和氧化铜,和铝发生铝热反应得到粗铜,含有铁杂质,粗铜精炼得到精铜;固体混合物B中加足量的G为NaOH溶液,过滤,滤渣为Cu,滤液为硅酸钠溶液;结合物质的性质分析。 【详解】 (1)Cu2O溶于酸反应生成铜和铜盐,铜和铁离子反应生成亚铁离子,所以滤液A中为亚铁离子,生成离子的离子方程式为: Cu+2Fe3+=2Fe2++Cu2+; (2)金属E与固体F发生的某一反应可用于焊接钢轨,是金属Al与氧化铁和氧化铜发生置换反应生成金属单质,该反应的化学方程式为2Al+Fe2O3 Al2O3+2Fe,在实验室中完成此实验还需要的试剂是引发剂氯酸钾和镁条,镁条点燃后引发氯酸钾分解生成氧气促进燃烧反应进行放出大量的热量,选ac; (3)溶液G为氢氧化钠溶液与固体混合物B为Cu、SiO2,其中二氧化硅是酸性氧化物和氢氧化钠溶液反应生成硅酸钠和水,反应的离子反应方程式为: SiO2+2OH-=SiO32-+H2O. 14.一种回收并利用含碘(I-)废液(废液中杂质沉淀后进入滤液中)的工艺流程如下: (1)“沉淀”后滤渣为______________________(填化学式,其中滤渣中Cu元素为+1价) (2)“氧化”反应的离子方程式为______________________。 (3)反应I中只生成化合物FexIy(其中I与Fe的质量比为127︰21),反应中铁屑是___________(填“氧化剂”“还原剂”或“催化剂”,下同),水是___________。 反应消耗的铁与转移电子的物质的量之比为___________。 (4)反应Ⅱ的化学方程式为_________________________________。 (5)操作I除蒸发皿、酒精灯外还需用到的玻璃仪器有______________________。 冰水洗涤的目的是_________________________________。 【答案】CuI2CuI+4NO3-+8H+=2Cu2++I2+4NO2↑+4H2O还原剂催化剂3: 8Fe3I8+4K2CO3=Fe3O4+8KI+4CO2↑玻璃棒、漏斗、烧杯除去KI表面的可溶性杂质,同时减少其溶解损失 【解析】 【分析】 结合流程可以知道回收废液中碘离子的步骤为: 先向废液中加入亚硫酸钠、硫酸铜溶液生成CuI沉淀,过滤得到滤渣CuI,然后加入浓硝酸氧化CuI,向氧化产物碘单质中加入铁屑和水后得到FexIy,FexIy与碳酸钾溶液反应生成Fe3O4、KI和CO2;过滤后将反应Ⅱ的滤液经过加热浓缩、冷却结晶、过滤,初步得到碘化钾;因为碘化钾混有可溶性杂质,需要经过洗涤才能得到较纯净的产品,同时为了减少KI的溶解损失,需要用冰水洗涤,最后得到纯净的碘化钾,据此分析。 【详解】 结合流程可以知道回收废液中碘离子的步骤为: 先向废液中加入亚硫酸钠、硫酸铜溶液生成CuI沉淀,过滤得到滤渣CuI,然后加入浓硝酸氧化CuI,向氧化产物碘单质中加入铁屑和水后得到FexIy,FexIy与碳酸钾溶液反应生成Fe3O4、KI和CO2;过滤后将反应Ⅱ的滤液经过加热浓缩、冷却结晶、过滤,初步得到碘化钾;因为碘化钾混有可溶性杂质,需要经过洗涤才能得到较纯净的产品,同时为了减少KI的溶解损失,需要用冰水洗涤,最后得到纯净的碘化钾。 (1)由于滤渣中Cu为+1价,“沉淀”后滤渣为CuI; (2)“氧化”时是滤渣与浓硝酸反应生成硝酸铜、碘、二氧化氮和水,反应的离子方程式为2CuI+4NO3-+8H+=2Cu2++I2+4NO2↑+4H2O; (3)反应I中铁由单质变为铁的化合物,化合价升高,作为还原剂;加入水可以加快反应速率,水起到了催化剂的作用,水是催化剂;在反应中生成铁与碘的化合物,其中铁元素与碘元素的质量比为21: 127,即Fe与I物质的量之比为: : =3: 8,反应Ⅰ生成物化学式是Fe3I8,根据碘的化合价,碘的化合价由0价变为-1价,则反应消耗的铁与转移电子的物质的量之比为3: 8; (4)根据流程Fe3I8与碳酸钾溶液反应生成Fe3O4、KI和CO2,反应Ⅱ的化学方程式为Fe3I8+4K2CO3=Fe3O4+8KI+4CO2↑; (5)操作I包括蒸发浓缩、冷却结晶、过滤,除蒸发皿、酒精灯外,还需用到的玻璃仪器有玻璃棒、漏斗、烧杯;冰水洗涤的目的是除去KI表面的可溶性杂质,同时减少其溶解损失。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 专题 训练 工艺流程
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
