 HAIC肝动脉灌注化疗.docx
HAIC肝动脉灌注化疗.docx
- 文档编号:8539639
- 上传时间:2023-01-31
- 格式:DOCX
- 页数:8
- 大小:149.34KB
HAIC肝动脉灌注化疗.docx
《HAIC肝动脉灌注化疗.docx》由会员分享,可在线阅读,更多相关《HAIC肝动脉灌注化疗.docx(8页珍藏版)》请在冰豆网上搜索。
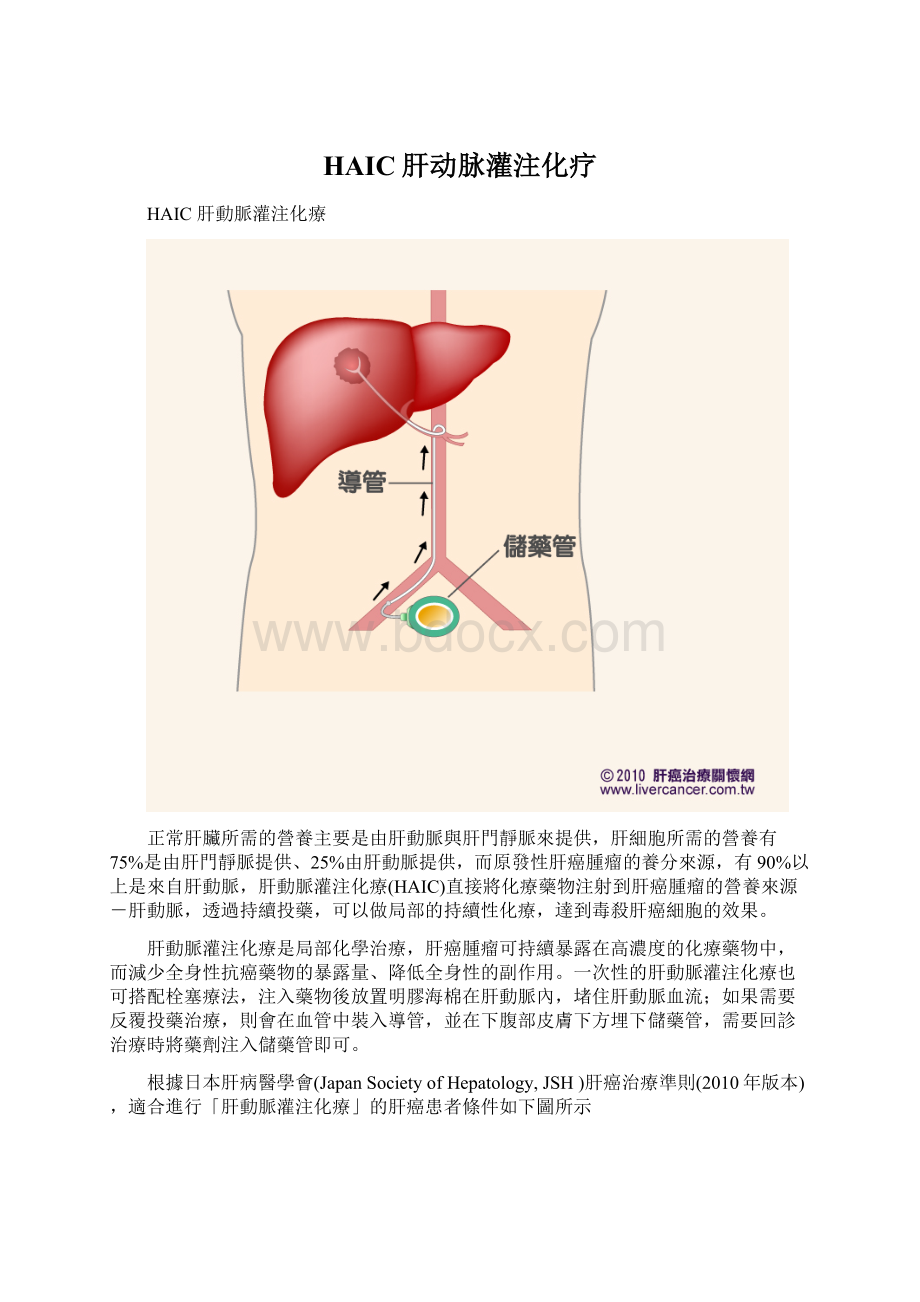
HAIC肝动脉灌注化疗
HAIC肝動脈灌注化療
正常肝臟所需的營養主要是由肝動脈與肝門靜脈來提供,肝細胞所需的營養有75%是由肝門靜脈提供、25%由肝動脈提供,而原發性肝癌腫瘤的養分來源,有90%以上是來自肝動脈,肝動脈灌注化療(HAIC)直接將化療藥物注射到肝癌腫瘤的營養來源-肝動脈,透過持續投藥,可以做局部的持續性化療,達到毒殺肝癌細胞的效果。
肝動脈灌注化療是局部化學治療,肝癌腫瘤可持續暴露在高濃度的化療藥物中,而減少全身性抗癌藥物的暴露量、降低全身性的副作用。
一次性的肝動脈灌注化療也可搭配栓塞療法,注入藥物後放置明膠海棉在肝動脈內,堵住肝動脈血流;如果需要反覆投藥治療,則會在血管中裝入導管,並在下腹部皮膚下方埋下儲藥管,需要回診治療時將藥劑注入儲藥管即可。
根據日本肝病醫學會(JapanSocietyofHepatology,JSH)肝癌治療準則(2010年版本),適合進行「肝動脈灌注化療」的肝癌患者條件如下圖所示
註1:
米蘭治療準則:
肝癌腫瘤小於3公分且數量少於3顆;或是單一顆腫瘤且腫瘤小於5公分。
即使病患肝功能尚佳(Child-Pugh等級A/B),對於肝癌易復發的病患來說,肝臟移植也是醫師會列入考慮的療法。
註2:
目前肝癌標靶藥物在台灣由衛生署核可的適應症為「轉移性或無法手術切除,且不適合局部治療或局部治療失敗之晚期肝細胞癌,且肝功能需為Child-PughAClass患者」
哪些病人適合肝動脈灌注化療(HAIC)
◎肝癌病情惡化,有4顆以上腫瘤、腫瘤開始侵犯血管的病患,且目前不適用其他療法時
本身有下列任何一種狀況的患者,並不適合使用肝動脈灌注化療(HAIC)來治療:
◎患者肝功能太差(肝功能Child-Pugh等級C),黃疸狀況嚴重、腹水無法治癒
◎肝癌腫瘤開始移轉到週邊器官
◎患者心臟、腎臟有問題
肝動脈灌注化療(HAIC)的進行方式
肝動脈灌注化療通常由醫院放射診斷科醫師來進行導管的放入,醫師會在病患大腿處開一個小孔,將導管置入大腿動脈後注射顯影劑確認血管位置,並同時搭配血管攝影,將導管穿過股動脈、副主動脈,達到最靠近肝癌腫瘤的肝動脈分支,然後將抗癌藥劑注入距離肝癌腫瘤最近的位置,將腫瘤毒殺。
肝動脈灌注化療(HAIC)通常會搭配栓塞療法,如果需要反覆進行,肝動脈灌注化療,醫師通常會在病人下腹部皮膚下方置入儲藥管,需要治療時在直接把藥劑注射到儲藥管裡即可。
肝動脈灌注化療(HAIC)的安全性與併發症
肝動脈灌注化療(HAIC)所帶來的主要副作用是抗癌藥劑所致,一般狀況是噁心、嘔吐、腹瀉、掉髮,較嚴重副作用是發生「骨髓抑制」(白血球、紅血球、血小板等血球製造能力低下),可能會導致身體免疫力下降,引起細菌、病毒感染,也可能會有貧血或是凝血功能不全,當骨髓抑制狀況太嚴重時,應先停止注射抗癌藥物。
肝動脈灌注化療(HAIC)的後續追蹤
◎影像檢查(CT電腦斷層掃描、MRI-核磁共振)
◎每個月抽血進行肝功能檢查、腫瘤指標檢查
HAIC+TargetTherapy
Summary
(日本)2009年5月20日首次獲得證實可治療肝細胞癌的全身化學療法sorafenib抗癌藥物之保險給付已獲得許可。
肝癌口服標靶的上市為肝細胞癌全身性治療帶來莫大的變化,尤其是在適合使用肝癌口服標靶的advancedstage(肝癌晚期)階段,對於肝動脈注射化學療法與肝癌口服標靶的使用意見分歧。
本篇概略說明使用於advancedstage的治療方法:
肝動脈注射化療與分子標靶藥物,並進一步說明目前情況下該等治療方法的使用情形,以及其未來的展望。
前言
如「具科學依據之肝癌診療指南2009年版」1)中所述,由於我國(日本)對於病毒性肝炎、肝硬化病患進行定期影像檢查及癌症指數檢測的監測系統(surveillancesystem)普及,可早期發現肝細胞癌,早期給予根治治療並逐漸改善預後情形。
然而,最後幾乎均因反覆復發而難以藉由射頻燒灼療法(radiofrequencyablation;RFA)或經導管肝動脈化學栓塞療法(transcatheterarterialchemoembolization;TACE)等治療方法進行局部控制,因此逐漸發展出動脈注射化學療法作為新的對策療法。
但動脈注射化學療法對遠處轉移無效,因此有效的抗癌藥物十分受到期待。
2009年5月20日首次獲得證實可治療肝細胞癌的分子標靶藥之保險給付已獲得許可,雖為肝細胞癌治療體系帶來莫大的變化,但仍存在該藥物之定位及其與過去治療方法使用上的相異點等種種問題。
Ⅰ動脈注射化學療法
動脈注射化學療法主要係針對已侵襲血管的惡化肝細胞癌所施行的初次治療,對於因為反覆施行TACE所導致的血管侵犯等亦可採用該治療方法。
動脈注射化學療法分為兩種,一種是使用留置導管的蓄液器(reservoir)肝動脈注射化學療法,另一種則是每次以Seldinger法插入導管施行大劑量衝擊(one-shot)動脈注射療法。
如大家所知,肝細胞癌流出的血管為肝門靜脈,因此最初會出現肝內轉移,直到末期前,腫瘤會侷限在肝臟內部,因此一般採用動脈注射化學療法為肝臟局部治療的治療方法。
藉由將抗癌藥劑直接注射於產生癌細胞的肝動脈血管,如此即可提高肝細胞癌組織中的抗癌藥劑濃度。
此外,由於肝臟可代謝藥物,因此可減少藥物轉移至全身器官的情形。
亦即利用少量的抗癌藥劑即可達到最大的效果與最小的副作用,與全身性的化療法相較之下具有不少優點。
動脈注射化學療法常用於肝門靜脈侵犯,尤其是不適用TACE療法的Vp3、4病例,對於肝葉兩葉多發性病例或難以TACE治療的巨大肝細胞癌病例亦採用該治療法。
即使已出現遠處轉移,但原發病灶可決定預後情形時,亦可作為相對適應症的療法。
在肝功能方面,動脈注射化學療法亦適用於Child-Pugh分類A或B的病例,Child-Pugh分類C病例因治療導致發生肝衰竭的危險性較高,故不適用該療法。
有肝硬化病史時可能會導致全血球減少症或肝功能降低,故施行該療法時必須特別留意血球的監測、投藥量及投藥間隔。
施行動脈注射化學療法時必須留置導管。
一般利用經皮放置法留置導管。
導管留置路徑有經由大腿動脈留置法,以及經由左側鎖骨下動脈留置法等,分別為一長一短的路徑,實際上目前各設施係選擇自己擅長的方法留置導管。
固定導管前端亦有複數的方式,一般採用的固定法係將導管前端插入胃十二指腸動脈(gastroduodenalartery;GDA),並將側孔置於總肝動脈的GDA固定法。
採用此法時,導管不會造成肝動脈的負擔,因此頗受歡迎。
其他留置的方法尚有將導管的前端投入肝動脈的末梢,側孔置於固有肝動脈的投擲側孔法。
採用此法時,有時不需要改變血流或固定導管前端等繁雜的過程,極為便利。
原則上應對每個病例進行適當的評估,判斷藥劑是否有效的分布於肝臟內(肝細胞癌),未流至其他器官。
施行蓄液器肝動脈注射化學療法時,必須嚴格執行導管的維護作業。
除了定期的追蹤檢查(followcheck)外,亦須進行頻繁的系統功能檢視等,在上述原則下執行維護作業。
動脈注射療法所使用的主要藥劑為5-FU,5-FU的藥劑特性為時間依存性,與腫瘤細胞接觸的時間愈長效果愈佳。
因為該點特性,採用蓄液器系統時多使用該藥劑。
目前主要施行的療法有兩種,1)?
Low-doseFP療法2)、‚2)併用干擾素(interferon)的5-FU動脈注射化學療法3)。
該兩種療法均以5-FU為主要藥劑,另為增強其效果(biochemicalmodulation)亦使用少量的ciplatin及干擾素(interferon)。
在許多報告中均提到了動脈注射化學療法的效果,客觀的反應率平均約為40%左右,可說是效果較佳的治療法。
此外若治療有可達部份反應,長期預後的效果可期,因此我國(日本)將該療法定位為標準療法。
但對於是否有助於存活率此點則未獲得明確的證實。
「有科學依據的肝癌診療指南2009年版」中對「與全身化學療法相比,動脈注射化學療法是否較有用」的clinicalquestion(臨床上問題)僅有「無充分的科學證據」(gradeC1)之評論,證據等級(evidencelevel)低。
又對於「併用干擾素的化學療法是否有用」的clinicalquestion(臨床上問題)答覆亦同「併用干擾素的化學療法應屬有用,可考慮採用,但無充分的科學證據」(gradeC1)。
此外,歐美的指南及亞洲太平洋肝臟學會會議(APASL)的共識準則(consensusguideline)中並未將動脈注射化學療法定位為標準的治療方法,可說是日本所特有的治療方法。
由於此法在理論上屬於優良的治療方法,因此我們期望能夠予以普及,但仍必須先在良好的前瞻性試驗中證實其survivalbenefit。
Ⅱ分子標靶藥
全身化學療法一直被認為不適用於肝細胞癌。
當然目前有一些可由保險給付的抗癌藥劑(殺細胞性抗癌藥劑)的存在,且有報告根據其反應率指出其有效性,但並無是否有助於存活的positive(正向)數據,因此無論在證據上或是實際臨床上幾乎均未使用該等藥劑,亦不建議使用。
在實際上使用時,應該多是在沒有其他方法的狀況而不得不採用。
相對的,分子標靶藥的上市為肝細胞癌治療體系帶來莫大的變化。
在歐美以肝細胞癌惡化病患為對象實施的隨機比較第III期臨床試驗(SHARP試驗)4)中,分子標靶藥的存活期間及未惡化期間均較安慰劑為長,且具有統計學上的意義。
此外,相同試驗在日本以外的亞洲各國實施時(AsiaPacific試驗5))亦顯示出相同的結果。
據此結果,我們可以將分子標靶藥定位為惡化肝細胞癌的標準治療。
我國(日本)已依據上述SHARP試驗的數據進行國內第I相臨床試驗,並針對此試驗的結果優先接受審查,並於2009年5月20日獲准保險給付。
肝癌分子標靶藥的作用機轉可分為2大類,其一、阻礙腫瘤細胞內細胞增生的重要訊息傳達系統RAF-MEK-ERK路徑(MAP激酶)中的絲胺酸/蘇胺酸激酶(serine/threoninekinase),抑制腫瘤細胞增生的機轉。
其二、係於血管內皮細胞及周邊細胞中阻礙血管內皮細胞生長因子受體(vascularendothelialgrowthfactorreceptor;VEGFR)及血小板衍生生長因子受體(platelet-derivedgrowthfactorreceptor;PDGFR)等受體型酪胺酸酶,進而抑制血管新生的血管新生抑制作用7)。
該等激酶因為阻礙多處的標的,亦被稱為多激酶(multi-kinase)抑制劑。
有關其直接的抗腫瘤效果,如SHARP試驗所示,雖然反應率較低,但病情長期穩定(SD),可說是其主要特徵。
且我國(日本)自2009年5月核准以來,出現許多歐美國家中所沒有的明顯有效案例,因而備受矚目。
將肝癌分子標靶藥使用於下述3種情形時,對於其治療上的定位可達到共識(日本肝臟學會提倡的共識準則下之肝細胞癌循序治療(algorithm))8)。
亦即1)Child-PughA中有遠處轉移的病例,
2)Child-PughA中已侵襲血管(Vp3、Vp4)的病例,
3)Child-PughA中無法使用TACE治療的病例。
目前肝癌口服標靶的使用方式為單獨使用,與TACE或動脈注射化學療法等標準治療的併用、或與其他抗癌藥劑的併用等併用治療均未獲得許可。
關於肝癌口服標靶的耐受性,於SHARP試驗、AsiaPacific試驗中已獲得確認,但實際在臨床上仍存在各種問題,因此須採取各種不同的對策9)。
手足皮膚症候群是最需要留意的副作用之一,雖然該副作用並不會危及生命,但病情轉變為重度後明顯影響病患的生活品質,經常難以繼續投藥。
該副作用發生的機轉雖不詳,但已訂立預防方法並採取充分的對策,目前已可克服此問題。
例如、可利用保濕等肌膚保養或避免刺激等預防皮膚問題,若嚴格執行預防對策,即使出現皮膚症候群多屬輕微。
另一重要的注意事項,即是對病患充分說明無論是誰均可能發生副作用等觀念,使其具有應具備的背景知識。
令病患具有正確的知識及洞悉病情是治療成功的秘訣。
其他具有特徵性的副作用如下痢及高血壓等,一般以藥物治療即可,很少衍生為重大的問題。
保險給付核准後,曾發生過肝癌口服標靶導致肝衰竭的病例,2009年11月厚生勞動省發佈blueletter(雖非緊急安全性資訊般的緊急,但有重要修訂必須迅速提醒醫療人員注意時發佈,緊急性介於緊急安全性通報與一般使用上注意之間),依適當使用諮詢委員會(AdvisoryCommittee)之建議,僅使用於Child-Pugh分類A之病患。
原本肝細胞癌病患的肝功能即可能有許多問題,因此需要頻繁的檢查肝功能。
Ⅲ動脈注射化學療法與分子標靶藥的使用區分
兩者均為惡化性肝細胞癌的治療方法,臨床上常見的問題即是如何區分使用,我們可參考前述的肝癌口服標靶適用條件。
1.有遠處轉移情形的病例
有遠處轉移時,基本上毫無疑問的肝癌口服標靶應是首選治療法。
但肝內病變嚴重影響預後時,以動脈注射化學療法為首選療法亦無不可。
2.伴隨著侵襲血管(Vp3、Vp4)的病例
在此情形下,肝癌口服標靶與動脈注射化學療法的適應症對象完全重疊,因此常有不同的見解。
就方法論而言,有下述兩種方法,
1)首先施行動脈注射化學療法,觀察反應情形,若無效果,再改為投予肝癌口服標靶治療;
2)投予肝癌口服標靶,惡化(PD)時再改為採用動脈注射化學療法。
雖有各種不同的想法,但目前仍未達到共識。
然而,實際上重複施行TACE的結果,對已侵襲血管的病例反應率極低,故在此情形下肝癌口服標靶成為第一首選治療法。
相對的,初次發病且伴隨Vp3、Vp4的病例,首先施行動脈注射化學療法,觀察反應情形後,再改為投予肝癌口服標靶治療亦為選擇之一。
在此情形下,施行動脈注射化學療法大致1個月(1療程)即可清楚觀察到反應情形,因此可在該時間點判斷是否繼續施行動脈注射化學療法、或改為投予肝癌口服標靶治療。
3.無法施行或不適用TACE的病例
在此必須將無法施行TACE及不適用TACE分開進行討論。
無法施行TACE及不適用TACE的定義一直是爭論的焦點,但在「肝癌診療手冊第2版」中已初次明文規定其定義。
【無法施行TACE】
1)治療用的血管損壞時,導管無法通過血管時
此情形下,多數無法放置導管,因此難以施行動脈注射化學療法,適合投予治療。
2)重複治療,在Child-Pugh分類上C肝功能惡化時
在此情形下非常遺憾,兩種治療均不適宜。
3)Vp3、Vp4病例
在此情形下,如前所述,可首先施行動脈注射化學療法,觀察其反應情形後,再決定投予肝癌口服標靶治療亦可,但重複施行TACE的結果,出現侵襲血管的病例時,則採用肝癌口服標靶治療法。
4)巨大A-P分流病例
在此情形下,若藥劑能適當地分布於腫瘤,則可作為動脈注射化學療法的適應症,反之則必須採用肝癌口服標靶療法較為妥當。
【不適用TACE的病例】
1)即使施行TACE腫瘤仍持續長大,並可確認為新病變時
在此情形下,雖然TACE的次數不明確,但重複施行TACE的次數愈多肝功能惡化愈嚴重,因此建議在肝功能尚佳的早期階段改為投予肝癌口服標靶治療,先行確認其效果為佳。
在肝功能低下的階段,已無法適用肝癌口服標靶治療法,結果造成治療的選擇性變少。
若肝癌口服標靶的效果不佳,可再度恢復施行TACE,在此必須轉換不同角度進行思考。
2)出現血管侵犯
如前所述,施行動脈注射化學療法能達到效果的情形較少,故屬sorafenib的適應症。
3)出現遠處轉移
基本上屬sorafenib的適應症,但遠處轉移影響預後較少,亦可優先採用動脈注射化學療法。
4)癌症指數上升
此情形下,施行動脈注射化學療法並觀察其反應情形,再改為投予sorafenib較佳。
投予sorafenib時的癌症指數變化情形較難評估,必須特別留意。
實際運用時,可能逐案而異(casebycase),但上述的使用區分方式應是實務上的方法。
Ⅳ動脈注射化學療法與分子標靶藥的併用療法
從可能提高肝細胞癌治療效果的觀點來看,自然而然地會產生併用動脈注射化學療法與分子標靶藥的想法。
若動脈注射化學療法的局部病灶高控制率能加上sorafenib的存活期間延長效果,良好預後(包含QOL)的相乘效果可期。
由於此一想法,我們提出了併用sorafenib與動脈注射化學療法(Low-doseFP療法)的計畫。
在第I階段臨床試驗中決定建議用量,並已顯示其有效性。
之後、驗證併用療法的有效性的第III階段臨床試驗獲得2010年度厚生勞動省科學研究費補助金,自2010年10月起開始辦理登錄為全國19所設施複數設施共同研究。
計劃書(protocol)的概要公開登錄於UMIN-CTR(UMIN000004315)及Clinicaltrials(NCT01214343)。
本試驗為驗證sorafenib標準治療加上動脈注射化學療法後是否能改善預後的第III階段隨機化比較臨床試驗。
本試驗的意義不僅確立併用sorafenib與動脈注射化學療法的標準治療,並證明至今尚未獲得證實的動脈注射化學療法的survivalbenefit,確立了動脈注射化學療法的意義,同時向全世界發表。
結論
概略說明動脈注射化學療法與分子標靶藥的實際使用方法及其使用上的區分。
該領域尚有許多unmetneeds,因此必須實施設計完善且具有前瞻性的臨床試驗方能解決該等問題。
例如在動脈注射化學療法上,各設施在試行試驗時,草案內容有參差不齊的情形,因此無法獲得高品質的成果。
日本的肝細胞癌治療具有享譽全世界的技術及成果。
由日本將具有高可信度的證據傳達予全世界,對全世界肝細胞癌病患貢獻非凡。
因此,在日本的體制下,取得肝癌治療設施協助,團結一致發展臨床試驗實屬重要。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- HAIC 动脉 灌注 化疗
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
