 届高三化学二轮复习夯基提能作业本 专题六 化学反应速率和化学平衡 Word版含答案.docx
届高三化学二轮复习夯基提能作业本 专题六 化学反应速率和化学平衡 Word版含答案.docx
- 文档编号:848584
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:13
- 大小:265.22KB
届高三化学二轮复习夯基提能作业本 专题六 化学反应速率和化学平衡 Word版含答案.docx
《届高三化学二轮复习夯基提能作业本 专题六 化学反应速率和化学平衡 Word版含答案.docx》由会员分享,可在线阅读,更多相关《届高三化学二轮复习夯基提能作业本 专题六 化学反应速率和化学平衡 Word版含答案.docx(13页珍藏版)》请在冰豆网上搜索。
届高三化学二轮复习夯基提能作业本专题六化学反应速率和化学平衡Word版含答案
专题六 化学反应速率和化学平衡
时间:
45分钟 分值:
100分
一、选择题(本题包括7小题,每小题6分,共42分)
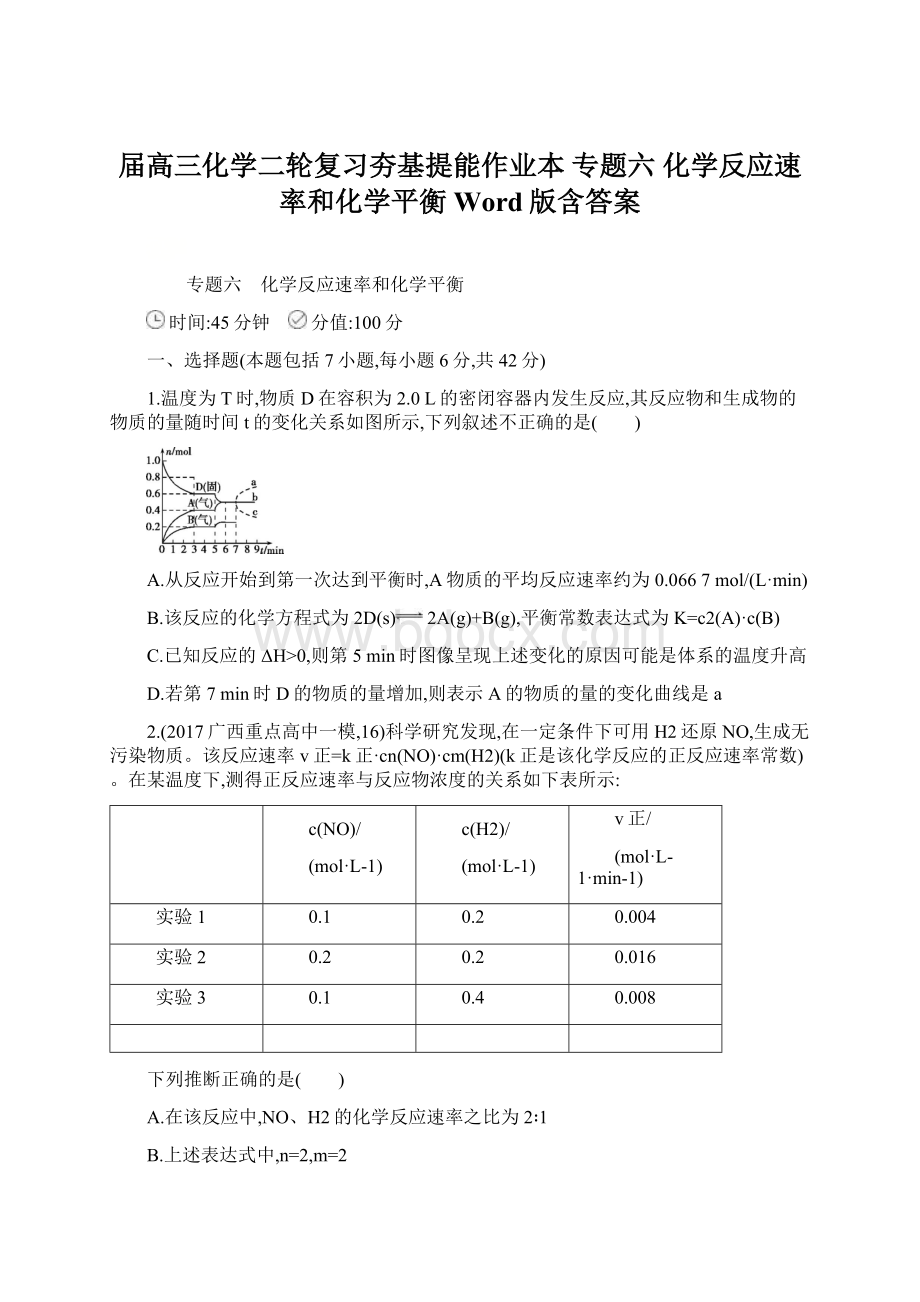
1.温度为T时,物质D在容积为2.0L的密闭容器内发生反应,其反应物和生成物的物质的量随时间t的变化关系如图所示,下列叙述不正确的是( )
A.从反应开始到第一次达到平衡时,A物质的平均反应速率约为0.0667mol/(L·min)
B.该反应的化学方程式为2D(s)2A(g)+B(g),平衡常数表达式为K=c2(A)·c(B)
C.已知反应的ΔH>0,则第5min时图像呈现上述变化的原因可能是体系的温度升高
D.若第7min时D的物质的量增加,则表示A的物质的量的变化曲线是a
2.(2017广西重点高中一模,16)科学研究发现,在一定条件下可用H2还原NO,生成无污染物质。
该反应速率v正=k正·cn(NO)·cm(H2)(k正是该化学反应的正反应速率常数)。
在某温度下,测得正反应速率与反应物浓度的关系如下表所示:
c(NO)/
(mol·L-1)
c(H2)/
(mol·L-1)
v正/
(mol·L-1·min-1)
实验1
0.1
0.2
0.004
实验2
0.2
0.2
0.016
实验3
0.1
0.4
0.008
下列推断正确的是( )
A.在该反应中,NO、H2的化学反应速率之比为2∶1
B.上述表达式中,n=2,m=2
C.上述表达式中,k正=2.0mol-2·L2·min-1
D.其他条件不变,加入催化剂或改变温度,k正不变
3.(2017宁夏银川一模,14)恒温条件下,体积为1L的容器中,P、Q、W三种气体的起始浓度和平衡浓度如下:
物质
P
Q
W
起始浓度/(mol·L-1)
0.1
0.1
0
平衡浓度/(mol·L-1)
0.05
0.05
0.1
下列说法不正确的是( )
A.反应达到平衡时,Q的转化率为50%
B.反应可表示为P(g)+Q(g)2W(g),其平衡常数K=4
C.达到平衡后,再加入0.1molW,达到新的化学平衡时,W的体积百分含量增加
D.达到平衡后,保持其他条件不变,P、W各加入0.05mol,则化学平衡逆向移动
4.(2017湖南六校联考,14)一定温度下,在三个体积均为2.0L的恒容容器中发生反应:
2NO(g)+2CO(g)N2(g)+2CO2(g)。
各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间的变化关系如图所示。
下列说法不正确的是( )
容器
温度/℃
起始物质的量/mol
NO(g)
CO(g)
甲
T1
0.20
0.20
乙
T1
0.30
0.30
丙
T2
0.20
0.20
A.该反应的正反应为放热反应
B.达到平衡时,乙中CO2的体积分数比甲中的大
C.T1℃时,若起始时向甲中充入0.40molNO、0.40molCO、0.40molN2和0.40molCO2,则反应起始时v正>v逆
D.T2℃时,若起始时向丙中充入0.06molN2和0.12molCO2,则达平衡时N2的转化率小于40%
5.在容积为2L的密闭容器中发生反应xA(g)+yB(g)zC(g)。
图甲表示200℃时容器中A、B、C的物质的量随时间的变化关系,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。
则下列结论正确的是( )
A.200℃时,反应从开始到平衡的平均速率v(B)=0.04mol·L-1·min-1
B.200℃时,该反应的平衡常数为25
C.当温度由200℃降到100℃时,原平衡一定被破坏,且正、逆反应速率均增大
D.由图乙可知,反应xA(g)+yB(g)zC(g)的ΔH<0,且a=2
6.(2017天津理综,6)常压下羰基化法精炼镍的原理为:
Ni(s)+4CO(g)Ni(CO)4(g)。
230℃时,该反应的平衡常数K=2×10-5。
已知:
Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:
将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:
将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是( )
A.增加c(CO),平衡向正向移动,反应的平衡常数增大
B.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C.第二阶段,Ni(CO)4分解率较低
D.该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
7.(2017河南豫北质量评估,16)T1℃时,在2L的密闭容器中,反应CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH<0达到平衡,反应过程中部分数据见下表。
下列说法正确的是( )
反应时间
n(CO2)/mol
n(H2)/mol
n(CH3OH)/mol
n(H2O)/mol
反应Ⅰ恒温恒容
0min
2
6
0
0
10min
4.5
20min
1
30min
1
反应Ⅱ绝热恒容
0min
0
0
2
2
A.达到平衡时,反应Ⅰ、Ⅱ对比,平衡常数:
K(Ⅰ)>K(Ⅱ)
B.对于反应Ⅰ,前10min内的平均反应速率v(CH3OH)=0.025mol·L-1·min-1
C.对于反应Ⅰ,若30min时只改变温度为T2℃,再次达到平衡时H2的物质的量为3.2mol,则T1>T2
D.对于反应Ⅰ,若30min时向容器中再充入1molCO2(g)和1molH2O(g),则平衡正向移动
二、非选择题(本题包括4小题,共58分)
8.(14分)应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。
甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
Ⅰ.已知:
①CH3OH(g)+H2O(l)CO2(g)+3H2(g)
ΔH=+93.0kJ·mol-1
②CH3OH(g)+O2(g)CO2(g)+2H2(g)
ΔH=-192.9kJ·mol-1
③CH3OH(g)CH3OH(l) ΔH=-38.19kJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为 。
Ⅱ.一定条件下用CO和H2合成CH3OH:
CO(g)+2H2(g)CH3OH(g)。
在2L恒容密闭容器中充入1molCO和2molH2,在催化剂作用下充分反应,如图表示平衡混合物中CH3OH的体积分数在不同压强下随温度变化的平衡曲线。
回答下列问题:
(1)该反应的反应热ΔH (填“>”或“<”)0,压强的相对大小为p1 (填“>”或“<”)p2。
(2)压强为p2,温度为300℃时,该反应的化学平衡常数K= 。
(3)下列各项中,不能说明该反应已经达到平衡的是 。
A.容器内气体压强不再变化
B.v(CO)∶v(H2)∶v(CH3OH)=1∶2∶1
C.容器内气体的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
(4)某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡 (填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
作出此判断的依据是
。
9.(11分)消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题。
(1)工业上常用活性炭还原一氧化氮,反应的化学方程式为:
2NO(g)+C(s)N2(g)+CO2(g)。
向容积均为1L的甲、乙、丙三个恒容恒温容器中分别加入足量的活性炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min
n(NO)/mol
T
0
40
80
120
160
甲
T℃
2
1.45
1
1
1
乙
400℃
2
1.5
1.1
0.8
0.8
丙
400℃
1
0.8
0.65
0.53
0.45
甲容器反应温度T℃ 400℃(填“>”“<”或“=”);乙容器中,0~40min内平均反应速率v(CO2)= ;丙容器中达平衡后NO的物质的量为 mol。
(2)活性炭还原NO2的反应为2NO2(g)+2C(s)N2(g)+2CO2(g),在恒温条件下,1molNO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压强的关系如下图所示:
①A、B、C三点中NO2的转化率最高的是 点(填“A”或“B”或“C”)。
②计算C点时该反应的平衡常数Kp= (Kp是用平衡分压代替平衡浓度计算得到的,分压=总压×物质的量分数)。
10.(2017江西九校3月联考,27)(15分)目前降低尾气的可行方法是在汽车排气管上安装催化转化器。
NO和CO气体均为汽车尾气的成分,这两种气体在催化转化器中发生反应:
2CO(g)+2NO(g)N2(g)+2CO2(g)
ΔH=-akJ·mol-1。
(1)CO2的结构式为 。
(2)已知2NO(g)+O2(g)2NO2(g)ΔH=-bkJ·mol-1;
CO的燃烧热ΔH=-ckJ·mol-1。
写出在消除汽车尾气中NO2的污染时,NO2与CO的可逆反应的热化学方程式(已知该反应为放热反应):
。
(3)在一定温度下,将2.0molNO、2.4molCO通入容积固定为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:
①有害气体NO的转化率为 。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是 (填序号)。
a.缩小容器体积
b.在恒压条件下再充入2.0molNO、2.4molCO
c.降低温度
d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,反应将 (填“向左”或“向右”)进行,再次达到平衡时的平衡常数为 。
④若保持反应体系的温度不变,20min时再向容器中充入与平衡组分相同的气体,达到平衡后,CO的体积分数将 (填“增大”“减小”或“不变”)。
11.(2017河北保定一模,26)(18分)雾霾天气严重影响人们的生活和健康。
其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。
因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染。
请回答下列问题:
(1)将一定量的某PM2.5样品用蒸馏水溶解制成待测试样(忽略OH-)。
常温下测得该试样的组成及其浓度如下表:
离子
K+
Na+
N
S
N
Cl-
浓度(mol/L)
4×10-6
6×10-6
2×10-5
4×10-5
3×10-5
2×10-5
根据表中数据判断该试样的pH= 。
(2)汽车尾气中NOx和CO的生成:
已知汽缸中生成NO的反应为N2(g)+O2(g)2NO(g) ΔH>0。
恒温、恒容密闭容器中,能说明该反应达到化学平衡状态的是 。
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.N2、O2、NO的物质的量之比为
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 届高三化学二轮复习夯基提能作业本 专题六 化学反应速率和化学平衡 Word版含答案 届高三 化学 二轮 复习 夯基提能 作业本 专题 化学反应 速率 化学平衡 Word 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
