 美国FDA企业产品列示方法.docx
美国FDA企业产品列示方法.docx
- 文档编号:7966343
- 上传时间:2023-01-27
- 格式:DOCX
- 页数:10
- 大小:1.48MB
美国FDA企业产品列示方法.docx
《美国FDA企业产品列示方法.docx》由会员分享,可在线阅读,更多相关《美国FDA企业产品列示方法.docx(10页珍藏版)》请在冰豆网上搜索。
美国FDA企业产品列示方法
FDA产品列示图例
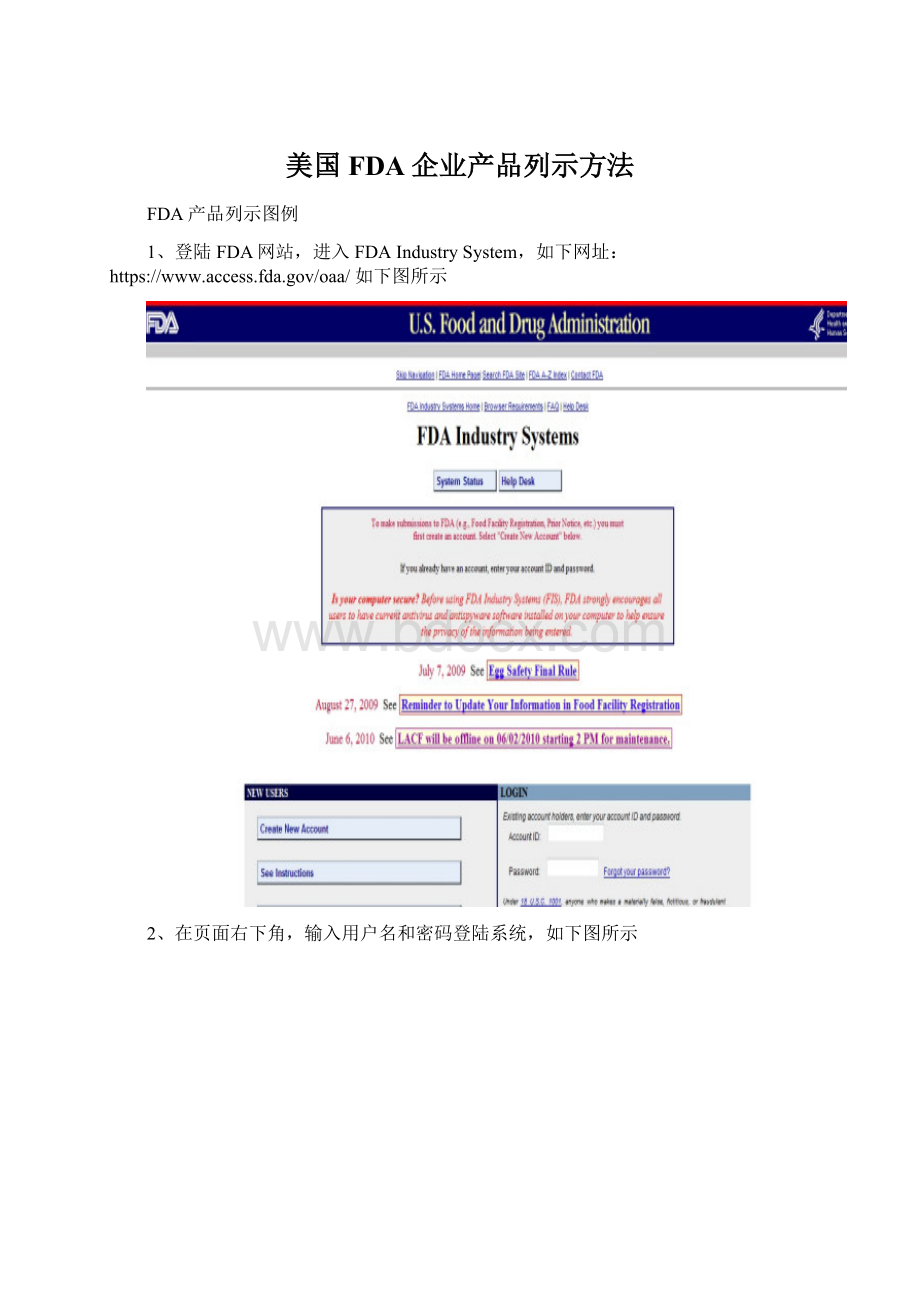
1、登陆FDA网站,进入FDAIndustrySystem,如下网址:
https:
//www.access.fda.gov/oaa/如下图所示
2、在页面右下角,输入用户名和密码登陆系统,如下图所示
3、登陆后的界面如下:
4、选择DeviceRegistration&listing选项,一般情况下在企业注册的时候注册为医疗器械企业的都只有这一个选项,进入如下界面:
5、点击Continue,进入如下界面
6、选择CreatelistingsforMedicalDevices,进入如下界面
7、输入客户代理我公司产品相应的K号,点击Continue,进入如下界面
8、我涂黑的部分会根据不同的K号显示相应的信息,但是只要K号一定了,这些信息都是固定的,不会改变,点击Continue,进入如下界面
9、在方框中打钩,选择公司相应的注册名称地址以及注册号,涂黑的部分会显示客户在FDA的注册信息。
点击Continue,进入如下界面
10、客户选择对应自己的公司性质,一般OEM客户都选择repackorrelabelMedicaldevice(免费的),如果选择Manufacturer会需要每年给FDA交费。
涂黑部分是显示客户的公司名称,网页下拉有Continue按钮,点击继续,进入如下界面
11、确认涂黑部分的信息正确,选择CertificationStatement的方框,点击finish完成,进入如下界面
12、完成列示,即可生成列示号,今后客户在通过美国海关的时候,使用我公司的K号和客户自己的列示号就不会有任何问题。
否则客户的公司没有任何FDA的注册信息,而包装盒上没有任何我公司的信息,客户在过海关的时候会遇到麻烦。
在今后的工作中应该注意,所有OEM的客户,即在产品label和labeling中如果不体现超思的信息,而客户又要以超思的K号报关,那么客户必须在FDA进行企业注册和产品列示。
这些对他们都是免费,并不会对他们有任何影响。
否则一旦海关查到,是必然要扣留货物的。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 美国 FDA 企业 产品 方法
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
