 第40讲 化学与工农业生产2.docx
第40讲 化学与工农业生产2.docx
- 文档编号:785451
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:11
- 大小:162.93KB
第40讲 化学与工农业生产2.docx
《第40讲 化学与工农业生产2.docx》由会员分享,可在线阅读,更多相关《第40讲 化学与工农业生产2.docx(11页珍藏版)》请在冰豆网上搜索。
第40讲化学与工农业生产2
开卷速查 规范特训
课时作业 实效精练
开卷速查(四十) 化学与工农业生产
1.氨在国民经济中占有重要地位。
现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料。
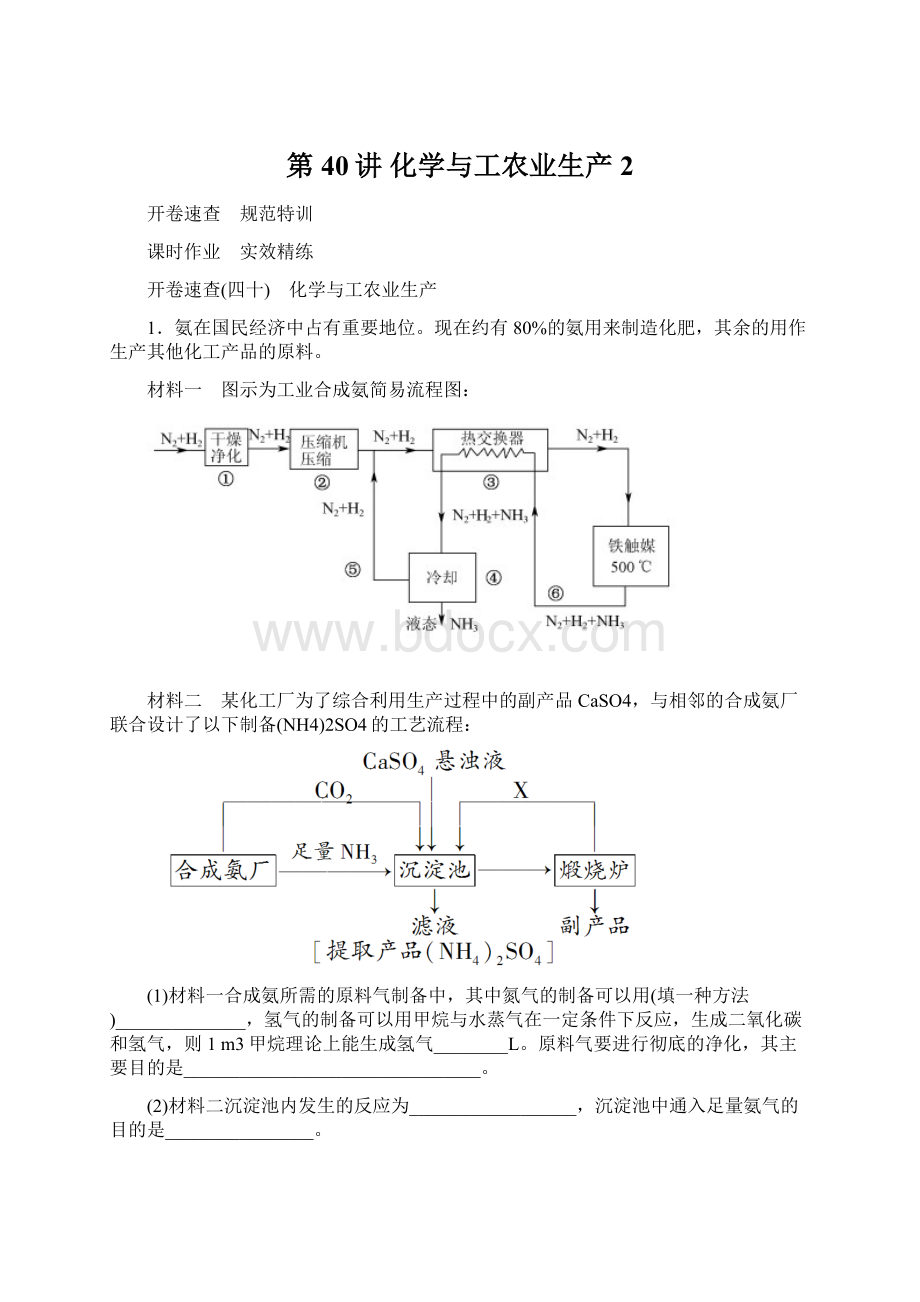
材料一 图示为工业合成氨简易流程图:
材料二 某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程:
(1)材料一合成氨所需的原料气制备中,其中氮气的制备可以用(填一种方法)______________,氢气的制备可以用甲烷与水蒸气在一定条件下反应,生成二氧化碳和氢气,则1m3甲烷理论上能生成氢气________L。
原料气要进行彻底的净化,其主要目的是________________________________。
(2)材料二沉淀池内发生的反应为__________________,沉淀池中通入足量氨气的目的是________________。
(3)材料三沉淀池内发生的反应为__________________,侯德榜主要是设计了上述流程中的循环__________(填“Ⅰ”或“Ⅱ”),使原料氯化钠的利用率从70%提高到90%以上。
从沉淀池中提取出沉淀的操作是__________。
解析:
本题考查合成氨工业、纯碱工业等。
合成氨中氮气可以通过分离空气得到。
无论在材料二还是材料三中,沉淀池通入氨气主要是为了使溶液呈碱性,有利于CO2的吸收。
答案:
(1)液化空气法(合理均可) 4000 防止催化剂中毒
(2)CaSO4+CO2+2NH3+H2O===CaCO3↓+(NH4)2SO4
一方面提供反应物,另一方面使溶液呈碱性有利于CO2的吸收
(3)NH3+CO2+H2O+NaCl===NH4Cl+NaHCO3↓ Ⅰ 过滤
2.[2012·海南卷]污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。
下列物质不能作为沉淀剂的是________。
A.氨水 B.硫化氢气体
C.硫酸钠溶液D.纯碱溶液
解析:
选项A,加氨水会有络合离子生成,不可能全都生成沉淀。
选项B,H2S与重金属离子均能生成沉淀。
选项C,加入Na2SO4溶液,Cu2+不能生成沉淀,不符合要求。
选项D,加入纯碱,可调节溶液的pH,可使重金属离子全部沉淀。
答案:
AC
3.[2014·衡阳联考]工业接触法制硫酸的流程如下图所示:
(1)若沸腾炉中每燃烧120gFeS2放出85.3kJ热量,试写出FeS2燃烧的热化学方程式____________________________________________________
______________________________________________________________。
(2)反应2SO2(g)+O2(g)2SO3(g)是在500℃恒温密闭的接触室中进行的,能充分说明此反应已达到平衡的标志是________(填序号)。
①气体的平均相对分子质量不再改变
②SO2、O2、SO3的浓度相同
③SO2、O2、SO3的物质的量之比为2∶1∶2
④压强不随时间变化而变化
(3)在接触室中,下列措施有利于提高SO2转化率的有________(填字母序号)。
A.升高温度 B.减小压强
C.不断补充空气D.及时分离出SO3
(4)从沸腾炉出来的气体经净化干燥处理后进入接触室,其气体体积组成是:
SO27%,O211%,N282%。
若有100体积这样的混合气体在接触室中反应,一段时间后,气体总体积变为96.7体积,则反应后混合气体中N2和SO3的体积比为________,此时SO2的转化率为________。
(5)接触室采用常压而不采用高压的原因是____________________
_____________________________________________________________。
(6)某硫酸厂每天用含FeS260%的硫铁矿500t生产硫酸,如果在沸腾炉内损失5%的硫,SO2的转化率为90%。
每天能生产98%的硫酸________t。
解析:
(4)100体积混合气体含N282体积,SO27体积,
设反应的SO2的体积为V,则
2SO2+O22SO3 ΔV
221
VV100-96.7
V=6.6
则N2与SO3的体积比为82∶6.6=410∶33
SO2的转化率为
×100%=94.3%
(6)设每天能生产98%的硫酸xt
FeS2 ~ 2H2SO4
1202×98
500×60%×(1-5%)×90%98%x
x=
x=427.5(t).
答案:
(1)4FeS2(s)+11O2(g)===2Fe2O3(s)+8SO2(g) ΔH=-341.2kJ·mol-1
(2)①④ (3)CD (4)410∶33 94.3%
(5)常压时SO2的转化率已经很高,采用高压SO2的转化率提高不大却会大大增加设备成本
(6)427.5
4.[2012·上海卷]碳酸氢铵是一种重要的铵盐。
实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。
完成下列填空:
(1)二氧化碳通入氨水的过程中,先有________晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
(2)含0.800molNH3的水溶液质量为54.0g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为________%。
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。
实验步骤依次为:
①粗盐溶解;②加入试剂至沉淀完全,煮沸;③________;④加入盐酸调pH;⑤加入________;⑥过滤;⑦灼烧,冷却,称重。
(4)上述步骤②中所加入的试剂为________、________。
(5)上述步骤④中加盐酸调pH的目的是___________________________
______________________________________________________________。
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:
含0.1molNH4HCO3的溶液中加入0.1molNaOH,反应完全后,滴加氯化钙稀溶液。
若有沉淀,则NH4HCO3与NaOH的反应可能为______________________________(写离子方程式);
若无沉淀,则NH4HCO3与NaOH的反应可能为______________________________(写离子方程式);
该实验方案有无不妥之处?
若有,提出修正意见。
解析:
(1)CO2气体通入氨水中时,先发生反应CO2+2NH3·H2O===(NH4)2CO3+H2O,当CO2过量时发生反应(NH4)2CO3+CO2+H2O===2NH4HCO3,所以先有(NH4)2CO3晶体析出。
(2)由CO2+NH3·H2O===NH4HCO3知,当0.800molNH3完全反应时,生成NH4HCO3的物质的量为0.800mol,参加反应的CO2的物质的量为0.800mol,则NH4HCO3的产率为
×100%≈92%。
(3)过滤,除去反应产生的CaCO3、Mg(OH)2等沉淀物;加入NH4HCO3的目的是产生NaHCO3沉淀。
(4)题述步骤②中主要除去Ca2+、Mg2+,且不引入其他杂质,因此选用NaOH和Na2CO3。
(6)该实验是探究NH4HCO3与NaOH等物质的量混合时,OH-与NH
反应,还是与HCO
反应,因此在反应后滴加氯化钙是用Ca2+来检验产物中是否有CO
。
假设反应为HCO
+OH-===CO
+H2O,则CO
与Ca2+反应生成CaCO3沉淀;假设反应为NH
+OH-===NH3+H2O,则需加热煮沸使NH3逸出,再滴加CaCl2稀溶液,避免NH3·H2O的影响。
答案:
(1)(NH4)2CO3
(2)92
(3)过滤 碳酸氢铵 (4)氢氧化钠 碳酸钠
(5)中和过量的氢氧化钠和碳酸钠
(6)HCO
+OH-===CO
+H2O NH
+OH-===NH3+H2O
需先煮沸,然后滴加氯化钙稀溶液
5.[2014·西宁模拟](NH4)2SO4是农业生产中的常见化肥之一,某工厂用石膏、NH3、H2O、CO2制备(NH4)2SO4,首先将石膏磨成粉末制成CaSO4悬浊液,然后按如图工艺流程进行生产:
(1)操作1与操作2的顺序能否调换?
________(填“能”或“否”),理由是_____________________________________________________。
(2)若已知常温下CaCO3和CaSO4的溶解度分别为1.5×10-3g和2.1×10-1g,则由此可知CaSO4向CaCO3转化的原因是_______________________
_____________________________________________。
(3)判断操作2通入的是“适量CO2”(非“过量”)的简单实验方法是__________________________。
(4)从绿色化学角度考虑,该工艺流程中应增加一个操作,这个操作是________________________。
(5)豆腐是日常食品之一,它的制作过程中使用了石膏或盐卤,其中包含的化学原理是__________________。
解析:
(1)先通入氨气的目的是使溶液显弱碱性,这样有利于二氧化碳的溶解吸收。
(2)在溶液中溶解度小的沉淀可以转化为溶解度更小的沉淀。
(3)若通入的二氧化碳过量,则溶液中会有Ca(HCO3)2生成,此时加NaOH会析出碳酸钙沉淀。
(4)原料的循环利用是工业节能减排的有效方法之一。
(5)豆腐的制作利用了胶体的聚沉。
答案:
(1)否 中性条件下CO2的溶解度很小,不能把CaSO4完全转化为CaCO3
(2)由CaSO4向CaCO3的转化过程中并存着两个沉淀溶解平衡:
CaSO4(s)Ca2++SO
,Ca2++CO
CaCO3(s),随着CO2的通入,CO
的浓度增大,平衡向CaSO4溶解和CaCO3沉淀生成的方向移动,即溶解度小的沉淀转化成溶解度更小的沉淀
(3)取少量滤液至试管中,加入少量NaOH溶液,若无浑浊出现则证明操作2通入的是“适量CO2”
(4)将提纯(NH4)2SO4后的滤液用于制CaSO4悬浊液
(5)胶体中加入电解质,胶体发生聚沉
6.我国著名化学家侯德傍先生发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉国内外。
“侯氏制碱法”的基本做法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱。
它的反应原理可用下列化学方程式表示:
NaCl(饱和)+NH3+CO2+H2O===NaHCO3↓+NH4Cl,2NaHCO3
Na2CO3+CO2↑+H2O。
某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下一套实验装置:
实验室可供选用的药品有:
浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化铵、氯化钠。
(1)A、D中最合适的试剂为:
A______________;D______________(填名称)。
(2)指出该装置中的错误________________________________________
__________________________________________________(至少两处)。
(3)在改进装置后,该同学进行了实验,实验所用的
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第40讲 化学与工农业生产2 40 化学 工农业生产
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
