 大容量注射液密封性验证.docx
大容量注射液密封性验证.docx
- 文档编号:7235879
- 上传时间:2023-01-22
- 格式:DOCX
- 页数:10
- 大小:56.30KB
大容量注射液密封性验证.docx
《大容量注射液密封性验证.docx》由会员分享,可在线阅读,更多相关《大容量注射液密封性验证.docx(10页珍藏版)》请在冰豆网上搜索。
大容量注射液密封性验证
大容量注射液密封系统
完好性验证方案
1.概述
本次容器密封系统的完好性试验采用灌装大豆胰蛋白胨肉汤培养基,经压塞、扎盖、灭菌、微生物侵入试验,试验分为2组,A组为正常微生物侵入试验,B组为微生物挑战试验,检查产品无菌可靠性是否达到要求,并对试验结果进行分析研究。
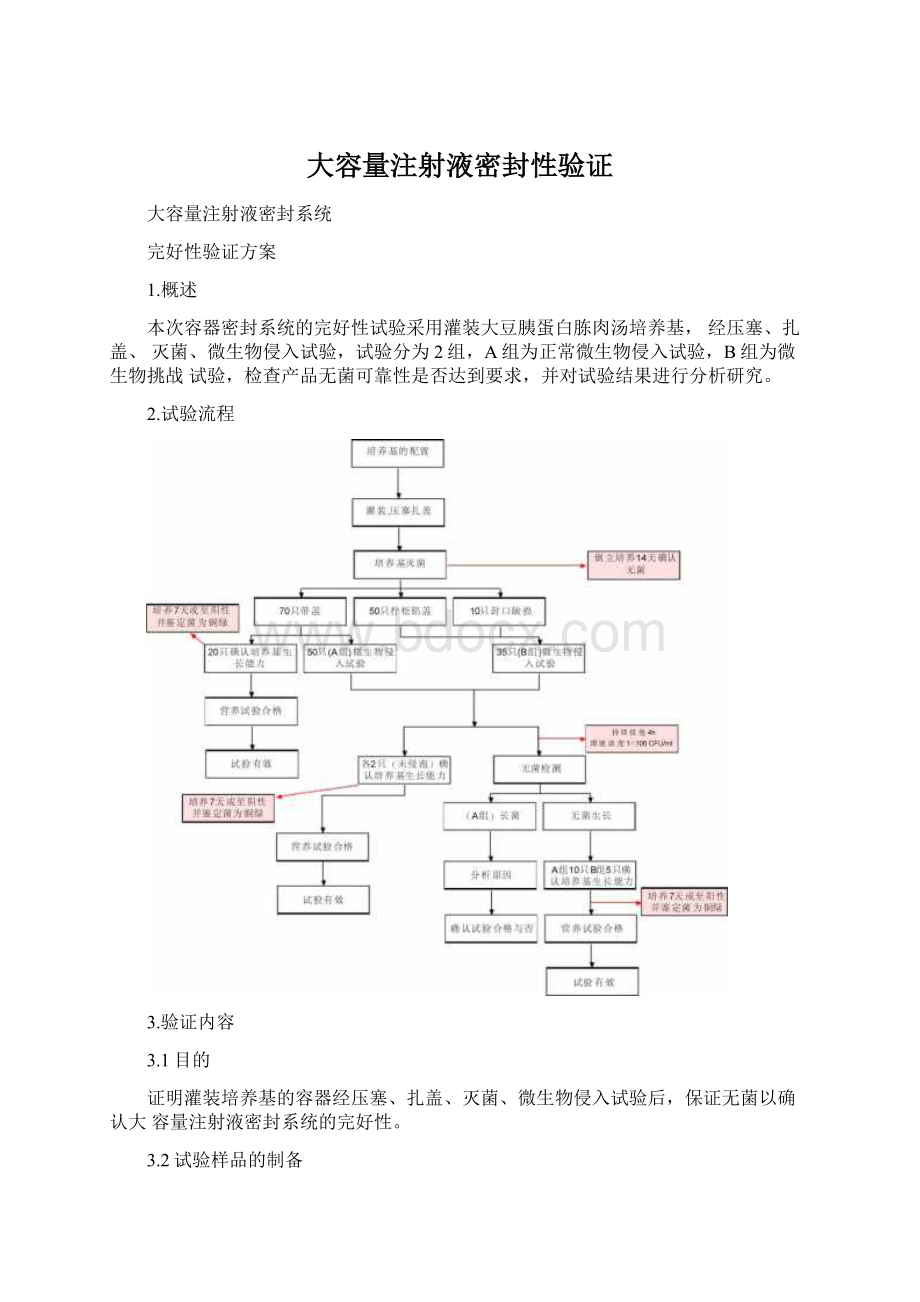
2.试验流程
3.验证内容
3.1目的
证明灌装培养基的容器经压塞、扎盖、灭菌、微生物侵入试验后,保证无菌以确认大容量注射液密封系统的完好性。
3.2试验样品的制备
3.2.1在生产线上取足够量的输液瓶,灌装大豆胰蛋白胨肉汤培养基,使用自动压塞和压盖设备将容器密封。
3.2.2将灌装好的容器经115C、20分钟灭菌。
3.2.3从灭菌柜中取出试样,冷却,将每一试样倒转,使培养基与容器内表面充分接触,在30~35°C下竖放培养14天。
3.2.4小心拧松至少50个试样的铝盖,注意不要破坏其密圭寸口。
将拧松铝盖时不慎损坏容器密封性的所有试样剔除。
按3.2.3培养样品。
3.2.5挑选至少10个封口处缺损的容器,按3.2.3培养样品。
3.3确定培养基促菌生长能力营养性试验
3.3.1所有试样培养14天均不长菌时,随即取20个带盖试样,每个试样内接种1ml的铜绿假单胞菌ATCC9027,菌液浓度:
10~100CFU/1ml。
3.3.230~35C下培养7天,或培养至所有试样都呈阳性结果。
3.3.3若7天内,所有接种铜绿假单胞菌的试样中,微生物生长良好,则容器内培养基的促菌生长能力可判为合格。
3.3.4使用革兰染色和紫外灯下肉汤呈蓝绿色荧光的性质,来签订并确认试样容器内生长的菌为接入的铜绿假单胞菌。
3.4挑战菌悬浮液的制备
3.4.1从铜绿假单胞菌ATCC9027的新鲜斜面上取一整环培养基,分别接入含10ml无
菌培养基的试管中,在30~35C下培养16~18h。
3.4.2将每管的培养物分别转入含1000ml相同培养基(SCDM/2)的容器中,于30~35C下培养22~24h。
在培养结束时,能明显见容器内培养基出现浑浊。
3.4.3培养结束后的菌悬液即可用来作容器/密封系统完好性试验。
3.5微生物侵入试验操作步骤
3.5.1本试验须在生物安全柜或其他不影响生产环境的地方进行。
3.5.2将新鲜的铜绿假单胞菌ATCC9027的菌悬液倒入合适的盆中,用金属丝架固定试样容器,使试验样品倒置在菌悬液中。
3.5.3将50个经最长灭菌程序灭菌的试样倒置,并侵入菌悬液中,该组试样为A组。
试样容器内的无菌培养基应充分接触封口内表面,样品的颈部及封口的外表面应完全泡在菌悬液中,见图:
试样为B组。
3.5.5实验开始时取一份菌悬液,平均计数每毫升所含活菌数。
按334确认试验用
微生物是铜绿假单胞菌。
3.5.6将A组和B组试样容器在菌悬液中持续浸泡约4小时。
3.5.7浸泡结束时,再用平板计数菌悬液的浓度。
3.5.8从菌悬液中取出试样,擦干试样容器外残余的菌悬液,然后用含0.5%过乙酸
的70%异丙醇消毒容器外表面。
3.5.9取装满培养基未拧松铝盖与拧松铝盖的试样各2个,作阳性对照。
阳性对照用样品制备方法同试样,但不经菌悬液浸泡,其外表面用含0.5%过乙酸的70%异丙醇消毒。
此后,接种入10~100CFU铜绿假单胞菌ATCC9027,按步骤3.3进行培养基的营养试验。
3.5.10将消毒后的容器放在塑料袋中,置30~35C培养7天,操作中应特别注意不要损坏B组无铝盖试样胶塞的密封性。
3.5.11挑战试验用菌悬液经灭菌后丢弃。
3.5.12将挑战试验用的试样培养7天,观察检查试样容器内培养基中微生物的生长情况。
3.5.13对每一试样进行观察检查,有生长的记作十,无生长的记作一。
3.5.14如果试样容器长菌,按3.3.4方法确认生长菌是挑战微生物一一铜绿假单胞菌。
3.5.15如果所有容器都不长菌,则从浸过菌悬液的A组取10个试样,B组5个试样,
分别按3.3进行培养基的营养检查。
3.5.16试验注意事项
3.5.16.1步骤3.3、步骤3.5.9、步骤3.5.15中进行的营养试验都合格,试样的挑战试
验才有效。
3.5.16.2在挑战试验开始时,挑战用菌悬液浓度(活菌数)必须达到1X106CFU/ml。
3.5.16.3挑战试验中A组和B组如有长菌,需记录长菌的试样数。
在A组中如出现长菌试验,则需按下述需求进一步调查。
第一,仔细去除微生物生长的容器盖和塞,检查容器封口是否有缺损,造成微生物侵入。
第二,将观察到试样容器封口的缺陷,采用拍照或
及其他适当详细记录。
3.5.16.4如果任何挑战试验中长菌的容器不是由于容器封口明显的物理性缺损所致,即
判定容器/密封系统挑战试验作失败。
3.6检验方法与可接受标准
3.6.1培养基无菌检查
取样方法:
生产线上罐装100mlSCDM/2(大豆胰蛋白胨肉汤)培养基,经过最长灭菌程序灭菌,从灭菌釜中取出试样,冷却,将每一试样倒转,在30~35°C下竖放培养14天。
检测方法:
可接受标准:
3.6.2营养试验
取样方法:
随机抽取经检验过的20个带盖试样。
检测方法:
每个试样内接种0.1ml铜绿假单胞菌ATCC9027,菌液浓度:
10~100CFU/0.1ml。
在30~35°C下培养7天,或者培养到所有试样都呈阳性结果。
可接受标准:
若7天内,所有接种的铜绿试样,微生物都生长良好,则培养基的促进生长能力判断合格。
3.6.3菌种鉴别试验
取样方法:
取接种铜绿的试样,经革兰氏染色实验鉴别待检试样存在铜绿假单胞菌。
检测方法:
革兰氏染色实验
可接受标准:
镜检结果应呈红色,并观察细胞形态结构符合铜绿假单胞菌特征,证明是铜绿假单胞菌。
3.6.4计算菌悬液浓度
铜绿假单胞菌:
【ATCC9024】第5代菌号:
9024-4-5-2
铜绿假单胞菌斜面培养物少许至10ml营养肉汤35°C24小时培养。
铜绿假单胞菌新鲜肉汤培养物1ml9ml0.9%无菌NaCl溶液至10-11含菌量10~100
10倍系列稀释
大容量注射液密封系统
完好性验证报告
1.概述
本次容器密封系统的完好性试验采用灌装大豆胰蛋白胨肉汤培养基,经压塞、扎盖、灭菌、微生物侵入试验,试验分为2组,A组为正常微生物侵入试验,B组为微生物挑战试验,检查产品无菌可靠性是否达到要求,并对试验结果进行分析研究。
2.试验流程
3.验证过程
3.1目的
证明灌装培养基的容器经压塞、扎盖、灭菌、微生物侵入试验后,保证无菌以确认大
容量注射液密封系统的完好性。
3.2验证样品的制备
3.2.1验证样品
培养基
输液瓶规格
胶塞厂家规格
灌封数
火菌条件
大豆胰蛋白胨肉汤
100ml
博生胶塞
130
115C、30分钟
3.2.2无菌检查结果:
培养基没有出现浑浊现象,证明无菌落生长。
3.3确定培养基促菌生长能力营养性试验
3.3.1营养试验检查结果统计:
编号
有菌生长
无菌生长
编号
有菌生长
无菌生长
1
+
/
11
+
/
2
+
/
12
+
/
3
+
/
13
+
/
4
+
/
14
+
/
5
+
/
15
+
/
6
+
/
16
+
/
7
+
/
17
+
/
8
+
/
18
+
/
9
+
/
19
+
/
10
+
/
20
+
/
结论:
从上面统计结果可以看出,培养基的营养实验合格,说明培养基有效,证明试验可以继续。
3.3.2鉴别培养基生长的菌是否为铜绿假单胞菌,检查结果统计:
编号
是否铜绿假单胞菌
编号
是否铜绿假单胞菌
1
是
11
是
2
是
12
是
3
是
13
是
4
是
14
是
5
是
15
是
6
是
16
是
7
是
17
是
8
是
18
是
9
是
19
是
10
是
20
是
结论:
符合规定
3.4挑战菌悬浮液的制备
侵入前菌悬液浓度统计:
取试验菌悬液1ml注入3个平皿,立即倾注琼脂培养基,培养、计数。
菌浓度:
1xiO-11CFU/ml
含菌量10—100cfu/mlo
结论:
菌悬液浓度符合规定,说明菌悬液可用。
3.5微生物侵入试验
3.5.1侵入后菌悬液浓度统计:
取试验菌悬液1ml注入3个平皿,立即倾注琼脂培养基,培养。
菌浓度:
1X106CFU/ml;
结论:
从统计可以看出,侵入试验后菌悬液浓度符合浓菌液要求,说明侵入试验具有有效性。
3.5.2A组2只与B组2只阳性对照营养试验检查结果统计:
A组编号
有菌生长
无菌生长
B组编号
有菌生长
无菌生长
1
+
/
3
+
/
2
+
/
4
+
/
结论:
2组营养试验均阳性,说明培养基符合规定
3.5.3鉴别培养基生长的菌是否为铜绿假单胞菌,检查结果统计:
编号
是否铜绿假单胞菌
编号
是否铜绿假单胞菌
1
是
3
是
2
是
4
是
结论:
符合规定
3.5.4微生物侵入检查结果统计:
编号
有菌生长
无菌生长
编号
有菌生长
无菌生长
1
/
-
26
/
-
2
/
-
27
/
-
3
/
-
28
/
-
4
/
-
29
/
-
5
/
-
30
/
-
6
/
-
31
/
-
7
/
-
32
/
-
8
/
-
33
/
-
9
/
-
34
/
-
10
/
-
35
/
-
11
/
-
36
/
-
12
/
-
37
/
-
13
/
-
38
/
-
14
/
-
39
/
-
15
/
-
40
/
-
16
/
-
41
/
-
17
/
-
42
/
-
18
/
-
43
/
-
19
/
-
44
/
-
20
/
-
45
/
-
21
/
-
46
/
-
22
/
-
47
/
-
23
/
-
48
/
-
24
/
-
49
/
-
25
/
-
50
/
-
结论:
从上面的统计可以看出侵入后样品经过培养7天以后,均无菌生长,说明大容量注射液密封系统在现有的工艺生产条件下符合规定。
3.5.5B组微生物侵入检查结果统计:
编号
有菌生长
无菌生长
编号
有菌生长
无菌生长
1
/
-
6
/
-
2
/
-
7
/
-
3
/
-
8
+
/
4
+
/
9
/
-
5
+
/
10
/
-
结论:
从上面的统计可以看出侵入后样品经过培养7天以后,有3瓶有菌生长,分析其
原因应该是去铝盖过程中破坏容器的密封性所致。
3.5.6A组10只与B组5只营养试验检查结果统计:
A组编号
有菌生长
无菌生长
B组编号
有菌生长
无菌生长
1
+
/
11
+
/
2
+
/
12
+
/
3
+
/
13
+
/
4
+
/
14
+
/
5
+
/
15
+
/
6
+
/
7
+
/
8
+
/
9
+
/
10
+
/
3.5.7鉴别培养基生长的菌是否为铜绿假单胞菌,检查结果统计:
编号
是否铜绿假单胞菌
编号
是否铜绿假单胞菌
1
是
11
是
2
是
12
是
3
是
13
是
4
是
14
是
5
是
15
是
6
是
7
是
8
是
9
是
10
是
结论:
符合规定
验证结论及意见:
此次验证所使用的容器胶塞以及灌封、压塞、扎盖工序完全模拟车间正常生产,从试验的结果统计可以看出,培养基无菌检查、营养试验均符合要求,且微生物侵入试验以及营养试验也符合要求,说明试验有效,证明大容量注射液密封系统具备完好性。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 容量 注射液 密封性 验证
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
 外教外事办理指南PPT文件格式下载.ppt
外教外事办理指南PPT文件格式下载.ppt
