 ok第三章 第3讲 铁及其化合物.docx
ok第三章 第3讲 铁及其化合物.docx
- 文档编号:7063480
- 上传时间:2023-01-16
- 格式:DOCX
- 页数:23
- 大小:293.32KB
ok第三章 第3讲 铁及其化合物.docx
《ok第三章 第3讲 铁及其化合物.docx》由会员分享,可在线阅读,更多相关《ok第三章 第3讲 铁及其化合物.docx(23页珍藏版)》请在冰豆网上搜索。
ok第三章第3讲铁及其化合物
第3讲 铁及其化合物
[考纲要求]
1.了解铁及其重要化合物的主要性质及其应用。
2.以Fe2+、Fe3+的相互转化为例,理解变价金属元素的氧化还原反应。
3.能鉴别溶液中的Fe2+、Fe3+。
【考点分布】
考点一 用物质分类思想认识铁及其重要化合物
考点二 +2、+3价铁的化学性质
考点三 铁及其化合物的综合应用
高考方向与练习
考点一 用物质分类思想认识铁及其重要化合物
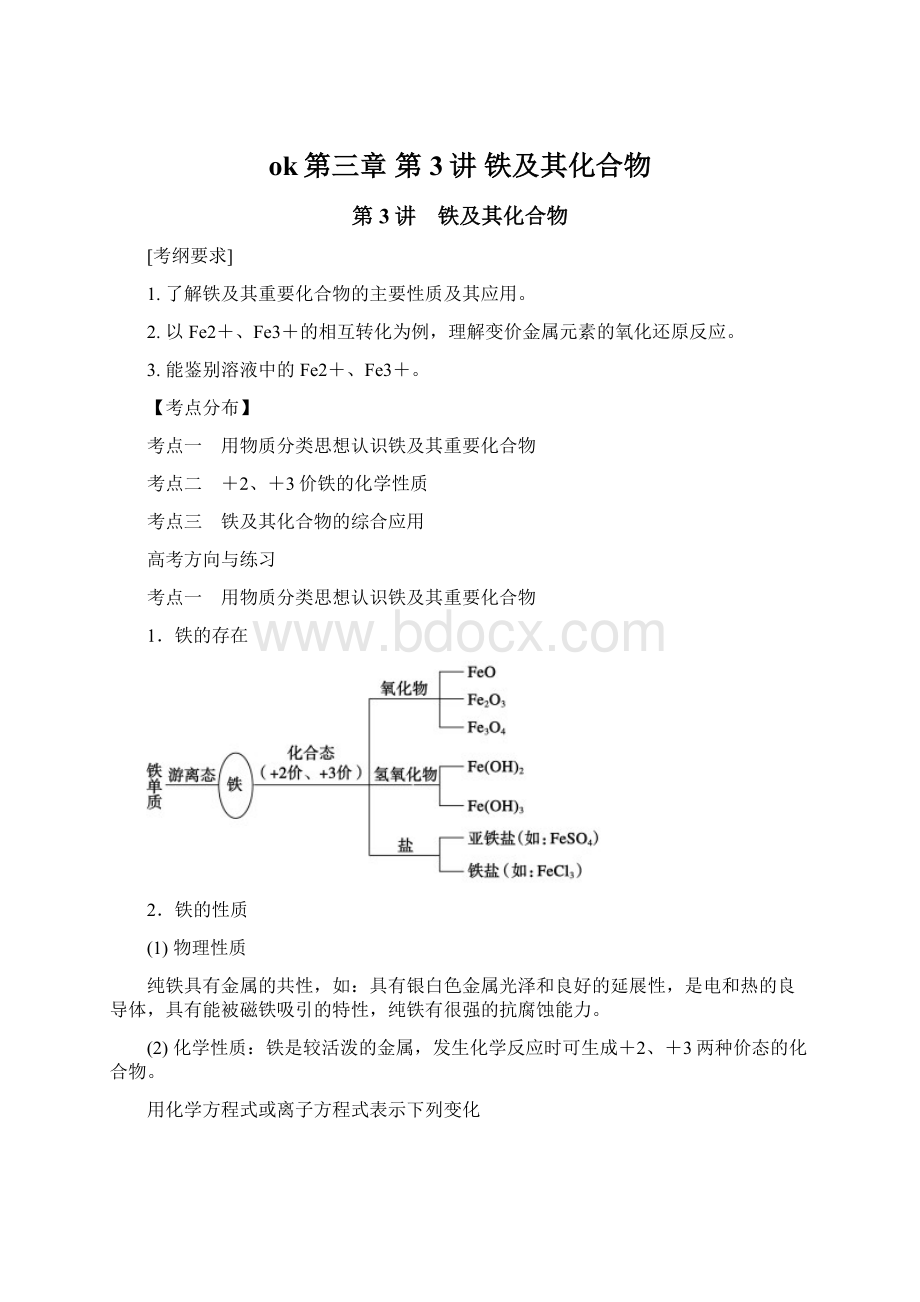
1.铁的存在
2.铁的性质
(1)物理性质
纯铁具有金属的共性,如:
具有银白色金属光泽和良好的延展性,是电和热的良导体,具有能被磁铁吸引的特性,纯铁有很强的抗腐蚀能力。
(2)化学性质:
铁是较活泼的金属,发生化学反应时可生成+2、+3两种价态的化合物。
用化学方程式或离子方程式表示下列变化
Fe+
Fe+H2O(g)
④3Fe+4H2O(g)
Fe3O4+4H2
Fe—
3.铁的氧化物和氢氧化物
(1)铁的氧化物
化学式
FeO
Fe2O3
Fe3O4
俗名
铁红
磁性氧化铁
颜色状态
黑色粉末
红棕色粉末
黑色晶体(有磁性)
溶解性
难溶于水
难溶于水
难溶于水
铁的化合价
+2
+3
+2,+3
稳定性
不稳定
稳定
稳定
与H+反应的离子方程式
FeO+2H+===
Fe2++H2O
Fe2O3+6H+===
2Fe3++3H2O
Fe3O4+8H+===
Fe2++2Fe3++4H2O
(2)铁的氢氧化物
Fe(OH)2
Fe(OH)3
色态
白色固体
红褐色固体
与盐酸反应
Fe(OH)2+2H+===
Fe2++2H2O
Fe(OH)3+3H+===
Fe3++3H2O
受热分解
2Fe(OH)3
Fe2O3+3H2O
制法
可溶性亚铁盐与碱溶液反应Fe2++2OH-===Fe(OH)2↓
可溶性铁盐与碱溶液反应
Fe3++3OH-===Fe(OH)3↓
二者的关系
在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是白色絮状沉淀迅速变成灰绿色,最后变成红褐色,反应方程式为4Fe(OH)2+O2+2H2O===4Fe(OH)3
【深度思考】
1.铁有很强的抗腐蚀能力,为什么日常生活中的铁制品容易生锈?
答案:
主要因为铁不纯,往往含有碳等杂质,当这些铁制品在潮湿的空气中或接触到电解质溶液(如食盐水)时会发生电化学腐蚀。
2.铁、铝遇浓硫酸或浓硝酸发生钝化,是物理变化还是化学变化?
答案:
常温下铁、铝遇冷的浓HNO3、浓H2SO4时表面会生成一层致密的氧化物薄膜,化学上称为钝化,属于化学变化。
3.铁元素是典型的变价金属元素,它在化合物中主要表现为+2价和+3价,请归纳总结:
(1)Fe单质通常与哪些氧化剂反应生成+2价?
写出有关反应的化学方程式或离子方程式。
答案:
Fe→Fe2+:
铁与氧化性比较弱的非金属单质(如S、I2),非氧化性酸(如盐酸、稀硫酸),不活泼金属的盐溶液(如CuSO4溶液)反应,都可实现这种转化。
如:
Fe+S
FeS,2H++Fe===Fe2++H2↑,Cu2++Fe===Fe2++Cu。
(2)Fe单质通常与哪些氧化剂反应生成+3价?
写出有关反应的化学方程式。
答案:
Fe→Fe3+:
铁与强氧化剂(如Cl2、HNO3、浓硫酸)在一定条件下反应都会实现这种转化。
例如:
2Fe+3Cl2
2FeCl3,Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O,
2Fe+6H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O。
4.FeCl3、FeCl2和Fe(OH)3是否都可以通过化合反应制取?
答案 都可以。
2Fe+3Cl2
2FeCl32FeCl3+Fe===3FeCl24Fe(OH)2+O2+2H2O===4Fe(OH)3
题组一 铁及其化合物的性质
1.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( B )
A.Fe(OH)3 Fe2O3B.Fe(OH)2 Fe2O3
C.Fe(OH)2 Fe(OH)3D.Fe(OH)2 Fe3O4
2.铁与水蒸气反应,通常有以下两种装置,请思考以下问题:
装置一
装置二
实验装置
(1)方法一中,装置A的作用______________________________________________。
方法二中,装湿棉花的作用______________________________________________。
(2)实验完毕后,取出装置一的少量固体,溶于足量稀盐酸,再滴加KSCN溶液,溶液颜色无明显变化,试解释原因:
________________________________________。
答案:
(1)提供水蒸气 提供水蒸气
(2)在溶液中Fe3+被未反应的铁粉完全还原为Fe2+
题组二 铁及其化合物的定量计算
3.由FeO、Fe2O3和Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21∶8,则这种混合物中FeO、Fe2O3和Fe3O4的物质的量之比是( D )
A.1∶2∶1B.2∶1∶1C.1∶3∶1D.1∶1∶3
解析:
可用平均组成法来求解:
在混合物中铁原子和氧原子物质的量之比为(21/56)∶(8/16)=3∶4,则混合物的平均组成为Fe3O4,在三种组合中Fe3O4则不必多考虑,应注意FeO和Fe2O3混合后也应符合Fe3O4,所以在混合物中它们的物质的量之比必须是1∶1。
4.含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中加入0.1mol铁粉,充分搅拌后,Fe溶解,溶液中不存在Fe3+,同时析出0.1molAg,下列结论错误的是( B )
A.溶液质量减轻B.溶液中Cu2+与Fe2+的物质的量比为1∶1
C.Fe3+的氧化性大于Cu2+D.1molFe可还原2molFe3+
解析:
由溶液析出0.1molAg,溶解0.1mol铁粉可知溶液质量减轻;依信息可知只有Ag析出,Cu2+没有参加反应,Ag+全部被铁还原,2Ag++Fe===2Ag+Fe2+,消耗Fe为0.05mol,生成0.05molFe2+;溶液中不含Fe3+,余下的0.05molFe恰好完全反应,Fe+2Fe3+===3Fe2+,生成0.15molFe2+;溶液中的Cu2+与Fe2+的物质的量比为1∶2。
5.在一定量的稀HNO3中慢慢加入铁粉,得到的Fe2+的物质
的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图
所示。
请将正确答案的序号填在相应的横线上。
①Fe3+ ②Fe2+ ③Fe、Fe2+④Fe2+、Fe3+
(1)AB段铁元素以__________形式存在。
(2)BC段铁元素以__________形式存在。
(3)CD段铁元素以__________形式存在。
答案:
(1)①
(2)④ (3)③
【归纳总结】
分析铁与稀HNO3反应的关键
一是明确哪种物质过量,二是根据两种物质的量分析讨论判断,根据反应方程式:
HNO3过量:
Fe+4HNO3===Fe(NO3)3+NO↑+2H2O,
Fe过量时:
Fe+2Fe(NO3)3===3Fe(NO3)2,
两者相加得总方程式:
3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O,可以用数轴表示:
解题时需注意量的范围。
即:
①
≤
,产物仅有Fe(NO3)3,HNO3可能有剩余;
②
≥
,产物仅有Fe(NO3)2,Fe可能有剩余;
③
<
<
,产物为Fe(NO3)3和Fe(NO3)2,Fe和HNO3都反应完全。
考点二 +2、+3价铁的化学性质
1.Fe2+的氧化性和还原性
Fe2+处于铁的中间价态,既有氧化性,又有还原性。
在中学阶段接触Fe2+的氧化还原反应中其主要表现还原性,如:
Fe2+遇Br2、Cl2、H2O2、NO
(H+)等均表现还原性。
2.Fe3+的氧化性
Fe3+处于铁的高价态,表现较强的氧化性,如:
它能氧化Fe、Cu、HI、H2S等。
3.Fe2+与Fe3+的相互转化
用离子方程式实现下列转化:
Fe2+
Fe3+
①2Fe2++Cl2===2Fe3++2Cl-;②3Fe2++4H++NO
===3Fe3++2H2O+NO↑;
③2Fe3++Fe===3Fe2+;④Cu+2Fe3+===Cu2++2Fe2+。
题组一 根据试剂判断Fe2+、Fe3+的转化
1.下列试剂中,不能使Fe2+转化为Fe3+的是( D )
①氯气 ②NaCl溶液 ③KMnO4溶液 ④稀硝酸 ⑤盐酸 ⑥NaNO3溶液
A.①②③B.①③④C.②④⑤D.②⑤⑥
2.将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是( D )
①硫酸 ②氯水 ③硝酸锌 ④氯化铜
A.①③B.②④C.③④D.②③
3.在含有Fe3+、Fe2+、Al3+、NH
的稀溶液中加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是( B )
A.Fe3+、Al3+B.Al3+C.Fe2+、NH
D.Fe3+
题组二 实现转化时试剂的选择
4.硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列物质中的
(C)
A.锌粉B.镁粉C.铁粉D.铝粉
5.如何除去括号中的杂质
(1)Fe2+(Fe3+):
加过量铁粉过滤;
(2)FeCl3(FeCl2):
加氯水或H2O2;
(3)FeCl2(CuCl2):
加过量铁粉过滤;(4)Fe(Al):
加过量强碱溶液过滤;
(5)Fe2O3(Al2O3、SiO2):
加过量强碱溶液过滤。
题组三 Fe3+、Fe2+的检验
6.为了验证Fe3+的性质,某化学兴趣小组设计了下图所示的一组实验,其中实验方案设计错误的是
( C )
A.④B.③C.③④D.①②③④⑤
解析:
③不反应,实验方案及现象均错;④检验的是Cl-,与Fe3+的性质无关。
7.要证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时,最佳顺序为( C )
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量NH4SCN溶液
A.①③B.③②C.③①D.①②③
8.下列离子的检验方法合理的是( C )
A.向某溶液中滴入KSCN溶液呈血红色,说明不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变血红色,说明原溶液中含有Fe2+
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
考点三 铁及其化合物的综合应用
“铁三角”的转化关系及应用举例
【归纳总结】
(1)判断离子共存
①Fe2+、Fe3+均水解,与HCO
、AlO
、CO
等因水解相互促进,在溶液中不能大量共存。
②Fe3+与S2-、I-、HS-、SO
,Fe2+与NO
(H+)、ClO-、MnO
(H+)在溶液中因发生氧化还原反应不能大量共存。
(2)盐溶液的配制与保存
①Fe2+的盐溶液:
加少量铁粉,防止Fe2+被氧化;加少量相应的酸,防止Fe2+水解。
②Fe3+的盐溶液:
加少量相应的酸防止Fe3+水解。
【深度思考】
根据铁及其化合物的重要性质思考如下几个问题
(1)请设计由FeSO4制取Fe2O3的最佳方案。
答案:
向FeSO4溶液中加入过量NaOH溶液,过滤、洗涤、加热灼烧即可得到Fe2O3。
(2)加热蒸干FeCl2、FeCl3溶液并灼烧,最终得到的固体是(Fe2O3)。
题组一 实验探究——Fe(OH)2的制备
1.用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入__________________________________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是________________________________________________。
答案:
(1)稀H2SO4、铁屑
(2)煮沸 (3)避免生成的Fe(OH)2沉淀接触O2而被氧化
解析:
Fe2+易水解,要加入稀H2SO4防止其水解;Fe2+易被空气中的O2氧化,要加铁粉,将被氧化生成的Fe3+还原成Fe2+。
气体的溶解度是随温度升高而降低的,所以煮沸后的蒸馏水中溶解的O2减少。
优点:
装置简单。
缺点:
难以控制FeSO4、NaOH中不含氧气。
即使加热煮沸FeSO4、NaOH溶液,在冷却和实验过程中还会有少量氧气溶解。
2.下列各图示中能较长时间看到Fe(OH)2白色沉淀的是①②③⑤(填序号)。
解析:
①、②原理一样,都是先用氢气将装置中的空气排尽,并使生成的Fe(OH)2处在氢气的保护中;③的原理为铁作阳极产生Fe2+,与电解水产生的OH-结合生成Fe(OH)2,且液面用汽油保护,能防止空气进入;⑤中液面加苯阻止了空气进入;④由于带入空气中的氧气,能迅速将Fe(OH)2氧化,因而不能较长时间看到白色沉淀。
题组二 含铁化合物的框图推断
3.A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿色气体,C为无色气体。
D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。
它们之间的转化关系如下图所示(其中某些反应条件和部分反应物已略去)。
请回答下列问题:
(1)写出下列物质的化学式:
A__________、D__________、E__________、X_________。
(2)在反应①~⑦中,不属于氧化还原反应的是__________(填编号)。
(3)反应④的离子方程式是_____________________________________________;
(4)反应⑦的化学方程式是_____________________________________________;
该反应中每消耗0.3mol的A,可转移电子______mol。
(5)写出D的溶液与小苏打溶液反应的离子方程式是_______________________________________。
(6)除去D溶液中混有的少量G的方法是_________________________________________________。
(7)在D溶液中制备无水D固体的方法是_________________________________________________。
答案:
(1)Fe FeCl3 Fe3O4 HCl
(2)③⑥(3)2Fe3++Fe===3Fe2+
(4)3Fe+4H2O(g)
Fe3O4+4H2 0.8
(5)Fe3++3HCO
===Fe(OH)3↓+3CO2↑
(6)向混合液中通入足量的氯气(或加入足量的H2O2)
(7)在HCl气流中加热蒸干FeCl3溶液
4.
请回答下列问题:
(1)B中所含元素位于周期表中第________周期,________族。
(2)A在B中燃烧的现象是____________________________________________。
(3)D+E―→B的反应中,被氧化与被还原的物质的物质的量之比是__________。
(4)G+J―→M的离子方程式是__________________________________________。
(5)Y受热分解的化学方程式是___________________________________________。
答案:
(1)三 ⅦA
(2)产生苍白色火焰 (3)2∶1
(4)3AlO
+Fe3++6H2O===3Al(OH)3↓+Fe(OH)3↓(5)4Fe(NO3)3
2Fe2O3+12NO2↑+3O2↑
题组三 实验探究题
5.某同学为了验证Fe3+是否能将H2SO3氧化成SO
,他用50mL0.1mol·L-1FeCl3溶液吸收制取SO2气体的尾气后,进行以下实验:
(1)检验吸收液中的SO
:
__________________,证明Fe3+能够把H2SO3氧化成SO
。
(2)请配平并完成上述反应中的化学方程式:
2FeCl3+SO2+_______===_______+H2SO4+______,反应中的氧化产物是________(写化学式)。
(3)吸收液中除了含有H+、Cl-、SO
以外,对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。
假设1:
溶液中存在Fe3+、Fe2+;假设2:
溶液中存在______________。
②设计方案,进行实验,验证假设。
请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:
试管、滴管、0.1mol·L-1KMnO4溶液、0.1mol·L-1KSCN溶液、品红稀溶液。
实验步骤
预期现象和结论
步骤1:
用试管取样品溶液2~3mL,并滴入_______________________________________
若出现血红色,则假设1成立;若未出现血红色,则假设1不成立(或假设2成立)
步骤2:
答案:
(1)取少量样品溶液于试管中,先滴入足量的稀盐酸,再滴入氯化钡溶液,如果有白色沉淀生成
(2)2H2O 2FeCl2 2HCl H2SO4(3)①Fe2+、H2SO3
②
实验步骤
预期现象和结论
步骤1:
1~2滴0.1mol·L-1KSCN溶液
步骤2:
另取2~3mL样品溶液于试管中,滴入1~2mL品红稀溶液
若品红溶液红色褪去,则假设2成立;若品红溶液不褪色,则假设2不成立(或假设1成立)
解析:
(3)验证“假设2”不能使用KMnO4溶液,因它可以同时氧化Fe2+和H2SO3。
由于用FeCl3溶液吸收制取SO2气体的尾气,Fe3+可以氧化H2SO3,故Fe3+与H2SO3不能大量共存,溶液中有H2SO3就一定有Fe2+。
所以用品红验证了H2SO3的存在就不必再验证Fe2+。
1.判断正误,正确的划“√”,错误的划“×”
(1)Fe3+有氧化性,所以FeCl3溶液可用于回收废旧电路板中的铜(√)
(2)在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热(×)
解析:
硫酸亚铁铵是通过降温结晶的方法来制备的,其制备过程是先制成高温饱和溶液,然后冷却,而不是用蒸发结晶的方法来获得的。
(3)Fe在足量Cl2中燃烧生成FeCl2和FeCl3(×)
(4)Fe分别与氯气和稀盐酸反应所得氯化物相同(×)
(5)Fe与S混合加热生成FeS2(×)
(6)
实验Ⅲ:
试管中溶液颜色变为红色(√)
(7)Fe2O3
FeCl3(aq)
无水FeCl3(×)
2.(2009·江苏,16)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。
其主要流程如下:
(1)反应Ⅰ前需在FeSO4溶液中加入____(填字母),以除去溶液中的Fe3+。
A.锌粉B.铁屑C.KI溶液D.H2
(2)反应Ⅰ需控制反应温度低于35℃,其目的是__________________________________________。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是_______________________
_________________________________________________________________。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(过二硫酸铵)。
电解时均用惰性电极,阳极发生的电极反应可表示为_______________________________________________________。
答案:
(1)B
(2)防止NH4HCO3分解(或减少Fe2+的水解)
(3)降低K2SO4的溶解度,有利于K2SO4析出(4)2SO
-2e-===S2O
解析:
(3)K2SO4在醇中的溶解度比在水中的还小,加入醇类溶剂的目的是降低K2SO4的溶解度,有利于K2SO4的析出。
(4)由题中主要流程图可知:
反应Ⅱ中主要物质是(NH4)2SO4,电解(NH4)2SO4,发生反应Ⅳ得H2和(NH4)2S2O8,阳极发生氧化反应,即2SO
-2e-===S2O
。
3.[2012·新课标全国卷,26
(1)
(2)]铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。
实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。
交换完成后,流出溶液的OH-用0.40mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0mL。
计算该样品中氯的物质的量,并求出FeClx中x的值:
__________________(列出计算过程)。
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe)∶n(Cl)=1∶2.1,则该样品中FeCl3的物质的量分数为__________。
在实验室中,FeCl2可用铁粉和__________反应制备,FeCl3可用铁粉和__________反应制备。
答案:
(1)n(Cl)=0.0250L×0.40mol·L-1=0.010mol
0.54g-0.010mol×35.5g·mol-1=0.185g
n(Fe)=0.185g/56g·mol-1≈0.0033mol
n(Fe)∶n(Cl)=0.0033∶0.010≈1∶3,x=3
(2)0.10 盐酸 氯气
解析:
解答此题的关键是明确阴离子交换柱交换出的OH-的物质的量等于Cl-的物质的量,从而求出FeClx中x的值。
(2)根据题意可设该混合物的组成为FeCl2.1,利用十字交叉法可得样品中FeCl3的物质的量分数为0.10。
注意制备FeCl2选用弱氧化剂,制备FeCl3选用强氧化剂。
1.铁是人类应用较早,当前应用量最大的金属元素。
下列有
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- ok第三章 第3讲 铁及其化合物 ok 第三 及其 化合物
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
