 电荷守恒物料守恒质子守恒知识doc.docx
电荷守恒物料守恒质子守恒知识doc.docx
- 文档编号:681133
- 上传时间:2022-10-12
- 格式:DOCX
- 页数:20
- 大小:23.29KB
电荷守恒物料守恒质子守恒知识doc.docx
《电荷守恒物料守恒质子守恒知识doc.docx》由会员分享,可在线阅读,更多相关《电荷守恒物料守恒质子守恒知识doc.docx(20页珍藏版)》请在冰豆网上搜索。
电荷守恒物料守恒质子守恒知识doc
电荷守恒、物料守恒、质子守恒知识
电荷守恒、物料守恒、质子守恒知识
一、电荷守恒:
整个溶液不显电性
1.概念:
溶液中阳离子所带的正电总数=阴离子所带的负电总数
2.注意:
离子显几价其浓度前面就要乘上一个几倍的系数
3.指出:
既要考虑溶质的电离,也要考虑水的电离,还要考虑盐的水解
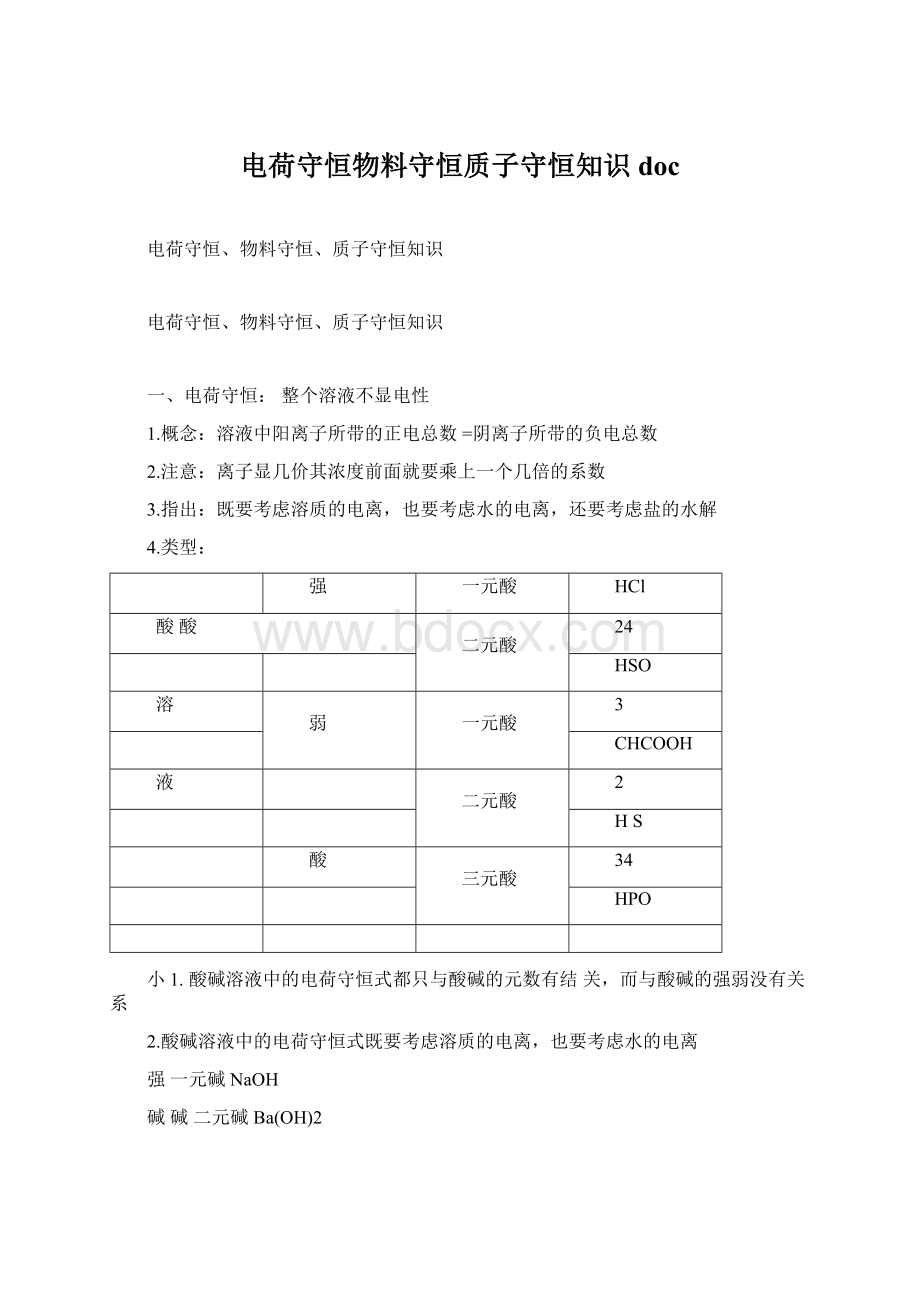
4.类型:
强
一元酸
HCl
酸酸
二元酸
24
HSO
溶
弱
一元酸
3
CHCOOH
液
二元酸
2
HS
酸
三元酸
34
HPO
小1.酸碱溶液中的电荷守恒式都只与酸碱的元数有结关,而与酸碱的强弱没有关系
2.酸碱溶液中的电荷守恒式既要考虑溶质的电离,也要考虑水的电离
强一元碱NaOH
碱碱二元碱Ba(OH)2
溶弱
一元碱NH·HO
3
2
液
二元碱
2
中学化学
碱
Cu(OH)
三元碱
3
对此均不做要求
Fe(OH)
不能
NaCl
水解
2
4
NaSO
的盐
2
BaCl
3
强CHCOONa
盐
碱
NaCN
正弱
2
3
NaCO
能
酸
2
NaS
盐Na3PO4
水强酸NH4Cl
溶
弱碱
424
(NH)SO
解盐
盐
弱酸CHCOONH
3
的
弱碱
4
盐
423
(NH)SO
液盐
(NH4)3PO4
酸强酸强NaHSO4
式碱盐
盐强酸弱NH4HSO
中碱盐
4
强碱弱NaHCO3
酸盐
弱酸弱NH4HS
碱盐
复盐KAl(SO4)2
小结盐电荷守恒既要考虑溶质的电离,也要考虑水的电离,还要考虑盐的水解
二、物料守恒:
也叫原子守恒
在电解质溶液中,某些离子能够发生水解或者电离,变成其它离子或分子等,这虽然可使离子的种类增多,但却不能使离子或分子中某种特定元素的原子的数目发生变化,因此应该始终遵循原子守恒。
1.某一种原子(团)的数目守恒:
若已知以下各电解质的浓度均为0.1mol/L则它电离或水解出的各种粒子的浓度之和就
等于0.1mol/L
弱
一元
CH3COOH
酸
酸
溶
酸
二元
23
HCO
液
酸
中
三元
H3PO
4
酸
强
HCl、HSO
强酸或强碱溶液中
2
4
酸
均不存在物料守恒
碱
强
NaOH、Ba(OH)
2
溶
碱
液
弱NH3·H2O
中
碱
强酸弱
NHCl
4
正
碱盐
盐
3
CHCOON
强碱弱
a
溶盐
酸盐
2
NaS
NaPO
3
4
液
弱酸弱
4
2
C
(NH)
碱盐
O3
中
强酸强
Na2SO4
强酸强碱盐不论是正盐还是
碱盐
酸式盐均
强酸强
4
无物料守恒式可写
NaHSO
酸
碱盐
式
强酸弱
4
4
NHHSO
盐
碱盐
强碱弱
-
2-
)+c(HCO)=0
NaHCOc(HCO)+c(CO
3
3
3
2
3
酸盐
.1
弱酸弱
NHHCO
4
3
碱盐
2.某两种原子(团)的比例守恒:
此比例来自于化学式且与化学式
一致
一
元
CH3COOH
弱酸溶酸
液中
二
元
2
3
HCO
酸
三
元
HPO
3
4
酸
强酸或强碱溶
HCl、H2SO4、NaOH、均不存在物料守
液中
Ba(OH)
恒
2
弱碱溶
NH·HO
3
2
液中
强酸弱
NH
c(NH
+
3
2
4
4
正
碱盐
Cl
c(Cl-)
盐CH3COONa
强碱弱Na2S
溶盐
酸盐
Na3
PO
4
弱酸弱
(NH)
CO
4
2
3
液
碱盐
强酸强
NaSO
强酸强碱盐不论是正盐还
2
4
中
碱盐
是酸式盐均
强酸强
NaHSO4
无物料守恒式可写
酸
碱盐
式
强酸弱
4
4
NHHSO
盐
碱盐
强碱弱
NaHCO
3
酸盐
弱酸弱
NHHCO
4
3
碱盐
(三)质子守恒:
1.概念:
由水电离出的H+总数永远等于由水电离出的
第一种
OH-总数,所以
理解
在强碱弱酸盐溶液中有:
c(OH-)=c(H+)+c(酸式弱酸根离子)+c(弱酸分子)
在强酸弱碱盐溶液中有:
c(H+)=c(OH-)+c(弱
碱分子)
电解质溶液中分子或离子得到或失去质子
第二种(H+)的物质的量应相等
理解得质子所得产物的总浓度=失质子所得产物的
总浓度
若某产物是得两个质子得来的,则该产物的浓
度前应乘个2倍系数
2.范围:
只有可水解的盐溶液中才存在着质子守
恒
3.类型:
(1)强碱弱酸盐的溶液中:
如Na2CO3溶液中
由水电离
出的
H+的存在
形式
由水电离
出的
OH-存在
形式
质子
第一种理解
第二种理解
H
+,酸式弱酸根离子,
2
3O+
HO得质子得
H
弱酸分子
2-
-
CO3
得质子得HCO3、
+
-
、23
23
H
、
3
HCO
HCOHCO
只以OH-本身形式存
H2O失质
在
OH-
规c(OH-)=c(H+)+c(酸式弱酸根离子)+c(弱
律酸分子)
举
-
+
-
CO)
c(OH)=
c(H
3
2
)+c(HCO)+2c(H
3
例
推
-
-
)
+
+
-
CO)
c(OH)
=c(OH
=c(H
)
=c(H
)
+c(HCO
液
水
水
液
3
23
导
(2)强酸弱碱盐的溶液中:
如
NH4
溶液中
Cl
第一种理解
第二种理解
H+的存在
H+
H2O得质子得H3O+
形式
OH
-的存在
OH
-
、
H
2
-
,NH4+失质子
O失质子得OH
形式
NH
3
2
得NH3
2
O
·HO
·H
质子
规
c(H+)=c(OH-)+c(弱碱分子)
律
举
+
)=c(OH
-
3
2
c(H
)+c(NH
·HO)
例
推c(H+)液=c(H+)水=c(OH-)水=c(OH-)液+c(NH3·H2O)
导
(3)弱酸弱碱盐的溶液中:
①正盐:
以(NH)CO
为例
42
3
第一种理解
第二种理解
+
+-
+
2-
-
H、HCO、HCO
H2O得质子得HO,CO得质子得HCO、HCO
H的存在形式
3
2
3
3
3
3
2
3
OH-存在形式
OH-、NH3·H2O
-
H2O失质子得OH,NH4+失质子得NH3·H2O
质子规律c(H+)+c(酸式弱酸根离子)+2c(弱酸分
子)=c(OH-)+c(弱碱)
举例
+
-
CO)=c(OH
-
c(H)+c(HCO
)+
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 电荷 守恒 物料 质子 知识 doc
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
