 研究与创新化学实验方案苯甲酸的制备.docx
研究与创新化学实验方案苯甲酸的制备.docx
- 文档编号:6608198
- 上传时间:2023-01-08
- 格式:DOCX
- 页数:8
- 大小:227.81KB
研究与创新化学实验方案苯甲酸的制备.docx
《研究与创新化学实验方案苯甲酸的制备.docx》由会员分享,可在线阅读,更多相关《研究与创新化学实验方案苯甲酸的制备.docx(8页珍藏版)》请在冰豆网上搜索。
研究与创新化学实验方案苯甲酸的制备
研究与创新化学实训
苯甲酸的制备
一、实验目的
1.学习从甲苯、高锰酸钾和盐酸制备苯甲酸的原理的方法;
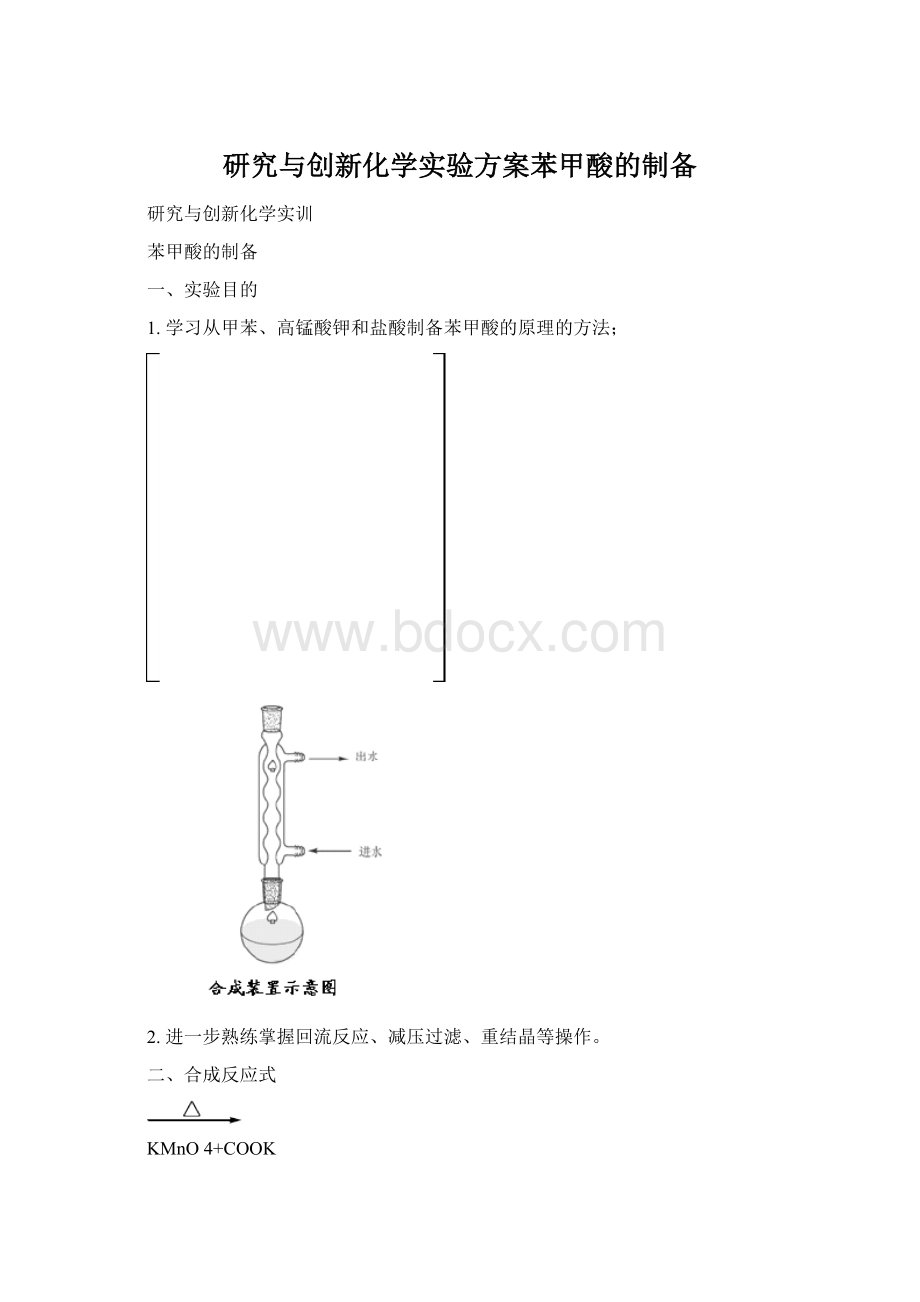
2.进一步熟练掌握回流反应、减压过滤、重结晶等操作。
二、合成反应式
KMnO4+COOK
+MnO2+H2
O+HClCOOH
+KClCH3COOK
三、实验仪器及试剂仪器:
250mL圆底烧瓶、球形冷凝管、表面皿、布氏漏斗、吸滤瓶,量筒(100ml,10ml),烧杯(400ml)。
试剂:
甲苯、浓盐酸(25%)、高锰酸钾、亚硫酸氢钠。
四、实验步骤
在250毫升圆底烧瓶中放入3.45g(4.05ml,0.0375mol)甲苯和150ml水,投入沸石数块,瓶口装上回流冷凝管,打开冷凝水,在石棉网上加热至沸。
从冷凝管上口分数次加入12g(0.075mol)高锰酸钾,并用少量水冲洗冷凝管内壁。
继续回流并时常摇动烧瓶,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
(此过程可能约需两个小时)
将反应混合物趁热用水泵减压过滤,用少量热水洗涤滤渣二氧化锰,洗涤的过程是将抽气暂时停止,在滤渣上加少量水,用玻棒小心搅动(不要使滤纸松动)使用在滤渣润湿,静置一会儿再行抽气。
如果滤液呈紫色,可加入少量的亚硫酸氢钠溶液使紫色褪去,并重新抽滤。
将滤液倒入400mL烧怀中,烧杯放在冷水浴中冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止。
抽滤,压干,若产品不够纯净,可用水重结晶,必要时加少量活性炭脱色。
干燥后称量并计算产率。
五、注意事项
1.高锰酸钾要分批加入,并用少量蒸馏水冲洗管壁上的粉末。
2.控制氧化反应速度;防止发生暴沸冲出现象。
3.酸化要彻底,使苯甲酸充分结晶析出。
5.NaHSO3小心分批加入,温度也不能太高,否则会发生暴沸;而若还原不彻底,会影响产品颜色和纯度。
苯甲酸的重结晶提纯实验原理:
苯甲酸在水中的溶解度随温度的变化较大,
通过重结晶可以使它与杂质分离,
而达到分离提纯的目的。
温度/℃255095
苯甲酸在水中的溶解
度/g0.170.956.8
实验仪器:
烧杯、铁架台(带铁圈)、酒精灯、普通漏斗、布式漏斗、铜漏斗、玻璃棒、抽滤瓶、滤纸、石棉网、
实验步骤:
二、过滤
①将准备好的铜漏斗放在铁架台的铁圈上,漏斗下放一小烧杯,点燃酒精灯加热,在漏斗里放一张折叠好的折叠滤纸,并用少量热水润湿。
这时将上述热溶液尽快地沿玻璃棒倒入漏斗中,每次倒入的溶液不要太满,也不要等溶液滤完后再加。
所有溶液过滤完毕后,用少量热水洗涤锥瓶和滤纸。
②将烧杯中的混合液趁热过滤。
(过滤时可用坩埚钳夹住烧杯,避免烫手),使滤液沿玻璃棒缓缓注入过滤器中。
三、冷却结晶
将滤液静置冷却,观察烧杯中晶体的析出。
待结晶完全析出后,用布氏漏斗抽滤,并用少量冷蒸馏水洗涤结晶,以除去结晶表面的母液。
洗涤时,先从吸滤瓶上拔去橡皮管,然后加入少量冷蒸馏水,使结晶体均匀浸透,再抽滤至干。
如此重复洗涤2次。
四、将得到的苯甲酸晶体交到指定地方,让其慢慢干燥,同时便于老师打分。
注意事项:
1.加热后的烧杯不要直接放在实验台上,以免损坏实验台。
2.进行趁热过滤时,注意使烧杯保持适当的倾斜角度,同时注意安全,防止烫伤。
3.不要用手直接接触刚加热过的烧杯、铁架台。
4.注意活性炭的加入时间和热过滤时的速度。
5.抽滤时注意先接橡皮管,抽滤后先拔橡皮管。
附:
苯甲酸
别名:
安息香酸
分子式C
7H
6
O
2
;C
6
H
5
COOH外观与性状鳞片状或针状结晶,具有苯或甲醛的臭味
分子量:
122.13蒸汽压:
0.13kPa/96℃闪点:
121℃
熔点:
121.7℃沸点:
249.2℃
溶解性:
微溶于水,溶于乙醇、乙醚、氯仿、苯、四氯化碳等有机溶剂。
密度:
相对密度(水=1)1.27;相对密度(空气=1)4.21
稳定性:
稳定
主要用途:
用作制药和染料的中间体,用于制取增塑剂和香料等,也作为钢铁设备的防锈剂
苯甲酸是弱酸,比脂肪酸强。
它们的化学性质相似,都能形成盐、酯、酰卤、酰胺、酸酐等,都不易被氧化。
最初苯甲酸是由安息香胶干馏或碱水水解制得,也可由马尿酸水解制得。
工业上苯甲酸是在钴、锰等催化剂存在下用空气氧化甲苯制得;或由邻苯二甲酸酐水解脱羧制得。
苯甲酸及其钠盐可用作乳胶、牙膏、果酱或其他食品的抑菌剂,也可作染色和印色的媒染剂。
实验室中制备苯甲酸多采用甲苯高锰酸钾氧化法。
采用此法进行制备苯甲酸,高锰酸钾作为氧化剂,在碱性条件下进行反应,产率在68%-74%之间,产生的二氧化锰沉淀过多,反应时间较长。
由于高锰酸钾是水溶性的,通常情况下很难与油溶性的甲苯发生反应。
加入相转移催化剂(PTC),则可加速或使互不相容的两相中的物质发生反应。
在酸性介质中用相转移催化法来强化苯甲酸的制备反应,反应缩短2-3h,产率提高8%以上,二氧化锰沉淀减少15%,以苯作溶剂,产率提高15%以上,二氧化锰沉淀减少25%.采用苄基三一基氯化铵和十六烷基三丁基溴化磷做催化剂,产率分别是50.5%,70.1%,但催化剂昂贵,反应时间长达7h以氧化铁为催化剂、n(甲苯):
n(高锰酸钾)=1:
1,分段加热的新工艺4h(75℃加热1.5h,85℃加热1.5h,95℃加热1h),产率可达74.32%,反应时间4h.在制备过程中,高锰酸钾配成饱和溶液直接加入反应器,不必分次加入den莫,这不仅有利于反应,减少环境污染,还大大方便了操作。
此外,采用苯甲酸苄酯的苯溶液与氢氧化钠水溶液在少量TBAB作相转移催化剂的情况下反应液可得到苯甲酸,反应6h苯甲酸收率超过70%。
相转移催化剂(Phasetransfercatalyst)简称PTC或PT,是20世纪70年代以来在有机合成中应用日趋广泛的一种新的合成技术。
在有机合成中常遇到非均相有机反应,这类反应的通常速度很慢,收率低,反应不完全的缺点。
但如果用水溶性无机盐,用极性小的有机溶剂溶解有机物,并加入少量(0.05mol以下)的季铵盐或季磷盐,反应则很容易进行,这类能促使提高反应速度并在两相间转移负离子的鎓盐,称为相转移催化剂。
一般存在相转移催化的反应,都存在水溶液和有机溶剂两相,离子型反应物往往可溶于水相,不溶于有机相,而有机底物则可溶于有机溶剂之中。
不存在相转移催化剂时,两相相互隔离,几个反应物无法接触,反应进行得很慢。
相转移催化剂的存在,可以与水相中的离子所结合(通常情况),并利用自身对有机溶剂的亲和性,将水相中的反应物转移到有机相中,促使反应发生。
二.苯甲酸乙酯的制备
A.实验目的
a)学习苯甲酸乙酯的合成方法和原理。
b)掌握分水器的原理与使用方法。
c)进一步练习蒸馏、萃取、干燥和折光率的测定等基本操作。
B.实验原理
酸催化直接酯化法是工业和实验室制备羧酸酯最重要的方法,需用的催化剂有硫酸、盐酸和甲苯磺酸等。
酸的作用是使羰基质子化从而提高羰基的反应活性。
反应是可逆的,为了使反应向有利于生成酯的方向移动,通常采用过量的羧酸或醇,或者除去反应中生成的酯或水,或者二者同时采用。
仪器:
50mL圆底烧瓶、冷凝管、温度计(100℃)、移加热套、200mL烧杯、分水器、
分液漏斗
试剂:
苯甲醇,过氧化氢,无水乙醇,15mL环己烷,2mL浓硫酸,15mL乙醚,碳酸钠,无水氯化钙。
实验步骤
1.制备苯甲酸乙酯:
a)在50mL圆底烧瓶中放入4g苯甲酸,10mL无水乙醇,15mL环己烷和2mL浓硫酸摇匀
后加入沸石,再装上分水器,事先从分水器上端小心加水至分水器支管处然后再放去6mL水,分水器上端装上回流冷凝管。
b)将烧瓶放在水浴中加热回流,开始时回流速度不宜过快。
随着回流的进行,分水器中出
现了上、中、下三层液体,且中层越来越多。
约1.5-2h后,分水器中的中层液体已达5-6mL左右,即可停止加热,放出里面液体。
继续用水浴加热,使多余的乙醇和环己烷蒸至水分离器中,充满时可由活塞放出。
c)将烧瓶中的残留液倒入盛有30mL冷水的烧杯中,用数毫升乙醇洗涤烧瓶,并与烧杯中的
水溶液合并。
在此溶液中,分批加入碳酸钠粉末并不断搅拌,直至二氧化碳不再逸出,溶液PH=7为止,约需4g碳酸钠。
d)将溶液转移至分液漏斗中,分出粗产物后用15mL乙醚提取水层,合并粗产物和醚萃取液,
用无水氯化钙干燥。
先蒸去乙醚,再在石棉网上加热,收集210-213C的馏分。
加热回流控制馏出液温度62-65℃,反应约2h,记录分水器中生成水的量。
蒸除溶剂反应完毕,放出分水器中全部液体,然后蒸除体系中过量的乙醇和环己烷到分水器。
3实验步骤
3.1粗产品的制备
(1)加料:
于100ml圆底烧瓶中加入:
4g苯甲酸;10ml乙醇;10ml环己烷,3ml硫酸,摇匀后加入2粒沸石。
装上分水器,小心加水至分水器支管处,然后放出约5ml水,记录体积,分水器上端安装球形冷凝管。
(2)开始小火加热,让其缓慢回流。
反应初期回流速度一定要适当慢一些,随着反应的进行,分水器中逐渐出现上、中、下三层液体。
在反应过程中应控制分水器中液面位置,以中层不流回到反应瓶中为准
(3)加热回流2h,停止加热,放出分水器中的水层。
(4)继续加热回流(水浴加热),蒸出多余的环己烷和乙醇,当回流速度减慢或瓶内有白色烟雾出现,立即停止加热。
3、2粗产品的精制
(1)冷却后将残液倒入盛有20ml冷水的烧杯中。
(2)搅拌下分批加入饱和碳酸钠溶液,中和至无二氧化碳气体产生,pH试纸检验呈溶液中性。
(3)分液:
倒入分液漏斗中,放出下层溶液,倒出有机层(上层),下层溶液再用10ml石油醚萃取,分出萃取液。
(4)干燥:
将有机层和萃取液倒入干燥的锥形瓶中,加入无水CaCl2干燥10分钟。
(5)精馏:
将干燥后的苯甲酸乙酯的醚溶液转入100mL圆底烧瓶中,在常压下先小火蒸出石油醚;再蒸出没有除尽的环已烷和乙醇,然后改用减压蒸馏,收集210℃~213℃的馏分。
(6)量出馏分的体积,计算产率。
制取苯甲酸乙酯反应装置提纯装置
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 研究 创新 化学 实验 方案 苯甲酸 制备
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
