 液基薄层宫颈细胞学3.docx
液基薄层宫颈细胞学3.docx
- 文档编号:6565441
- 上传时间:2023-01-07
- 格式:DOCX
- 页数:16
- 大小:221.86KB
液基薄层宫颈细胞学3.docx
《液基薄层宫颈细胞学3.docx》由会员分享,可在线阅读,更多相关《液基薄层宫颈细胞学3.docx(16页珍藏版)》请在冰豆网上搜索。
液基薄层宫颈细胞学3
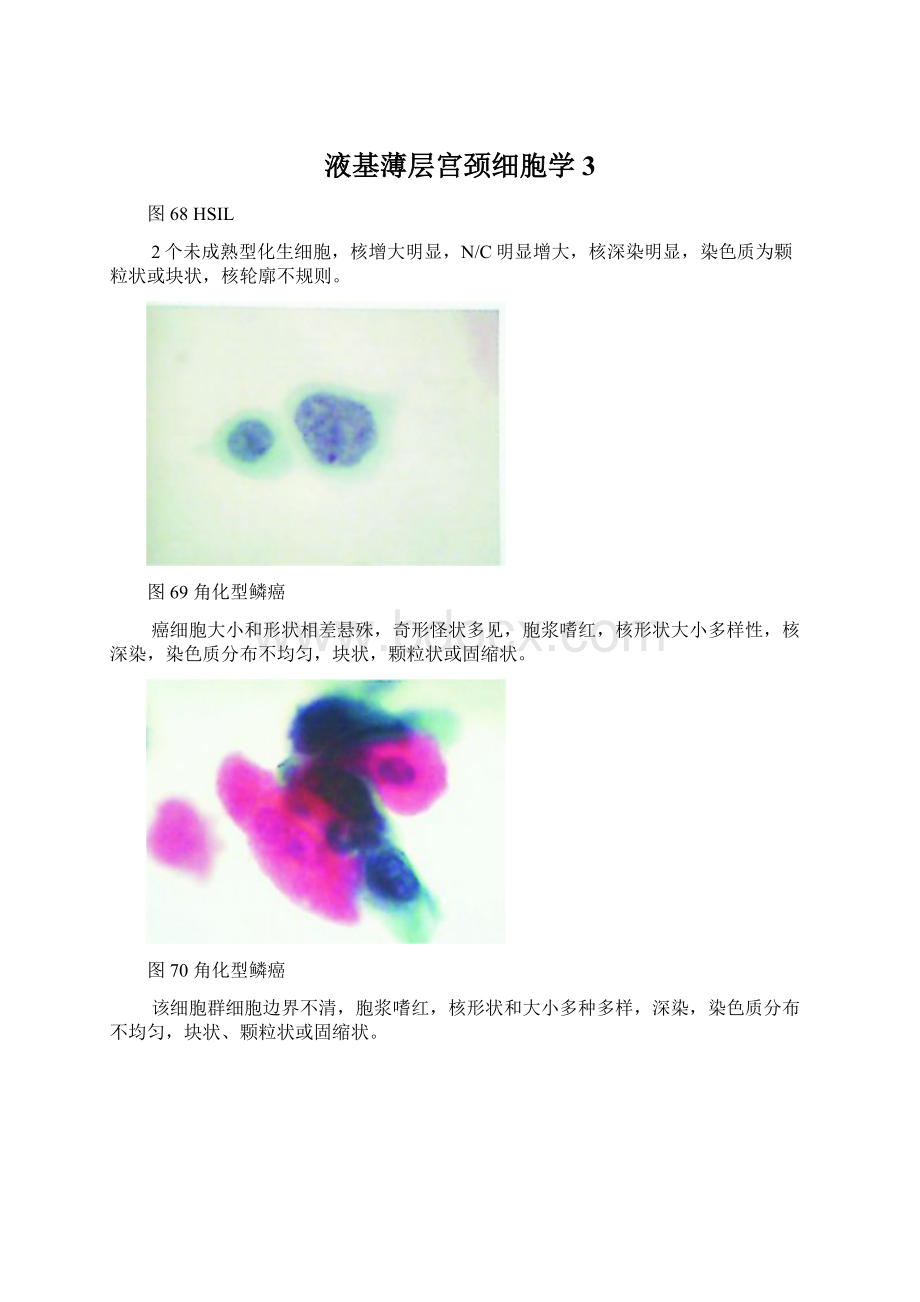
图68HSIL
2个未成熟型化生细胞,核增大明显,N/C明显增大,核深染明显,染色质为颗粒状或块状,核轮廓不规则。
图69角化型鳞癌
癌细胞大小和形状相差悬殊,奇形怪状多见,胞浆嗜红,核形状大小多样性,核深染,染色质分布不均匀,块状,颗粒状或固缩状。
图70角化型鳞癌
该细胞群细胞边界不清,胞浆嗜红,核形状和大小多种多样,深染,染色质分布不均匀,块状、颗粒状或固缩状。
图71角化型鳞癌
细胞片状排列,多形性明显,胞浆多嗜红,核形状大小异型性明显,核深染明显,染色质分布不均匀,块状、颗粒状或固缩状。
图72角化型鳞癌
薄片中3个癌细胞呈纤维状,核畸形,固缩深染,左方细胞核亦增大明显、深染、不规则。
图73角化型鳞癌
细胞松散排列,癌细胞大小和形状相差悬殊,奇形怪状多见,胞浆多嗜红,薄片中癌细胞呈长带状,周围细胞核形状和大小亦多种多样、深染、染色质呈块状。
图74角化型鳞癌
薄片中央为两蝌蚪状癌细胞,细胞核增大,核形长梭状,核深染明显,染色质增粗。
图75非角化型鳞癌
细胞散在排列,细胞大,多数细胞核浆比重失调,胞浆多蓝染,核大明显,不规则,该薄片中癌细胞形状畸形显著,核染色质深染呈黑煤块状。
图76非角化型鳞癌
薄片中癌细胞形状畸形,核浆比重失调,胞浆多蓝染,核增大明显,不规则,染色质增多深染,可见癌性背景如炎细胞等。
图77非角化型鳞癌
薄片中两癌细胞畸形明显,似蝌蚪状,胞浆蓝染,核增大明显,核形不规则,染色质增多深染。
图78非角化型鳞癌
细胞合体细胞样排列,胞浆多蓝染,核大明显,不规则,核深染,染色质增多颗粒状分布不均匀,核仁常见。
腺上皮细胞不正常
1、不典型腺上皮细胞,未明示
2、不典型腺上皮细胞,倾向瘤变
3、宫颈内膜原位腺癌。
4、腺癌(子宫颈管内膜腺癌,子宫内膜腺癌,其他)
不典型腺上皮细胞
图79不典型腺上皮细胞(子宫颈管内膜),未明示
细胞片状排列,核无明显重叠,核增大,大小形态轻度不一致,轻度深染,染色质轻度增多细颗粒状,核膜光滑,胞浆丰富,在炎症或修复时,常常可见核仁。
图80不典型腺上皮细胞(子宫颈管内膜),未明示
细胞片状排列,核无明显重叠,核增大,大小形态轻度不一致,轻度深染,染色质轻度增多细颗粒状,核膜光滑或轻度不规则,胞浆丰富,细胞界限清楚,可见核仁。
图81不典型腺上皮细胞(子宫内膜细胞),未明示
细胞成群出现,胞浆缺乏,细胞边界不清,核增大,大小不一,核拥挤重叠,轻度深染,可见核仁。
图82不典型腺上皮细胞,未明示
细胞成群出现,胞浆缺乏,核轻度深染,核大小,形状不一,可见核仁。
图83不典型腺上皮细胞(子宫颈管内膜),倾向瘤变
细胞排列成片状,正常的蜂窝状结构消失,核拥挤重叠,核浆比增加,胞浆少,胞界不清,核大小形状不同,增大增长,染色质增多,核仁小或不明显。
图84不典型腺上皮细胞(子宫颈管内
膜),倾向瘤变
细胞排列成片状,正常的蜂窝状结构消失,核拥挤重叠,核浆比增加,胞浆少,胞界不清,核大小形状不同,增大增长,染色质增多,核仁小。
图85不典型腺上皮细胞(子宫颈管内
膜),倾向瘤变
异常细胞排列条索状,正常的蜂窝状结构消失,核浆比增加,胞界不清,核大小形状不同,增大增长,染色质增多,核仁小或不明显。
图86不典型腺上皮细胞(子宫颈管内
膜),倾向瘤变
异常细胞排列成片状,正常的蜂窝状结构消失,核拥挤重叠,核浆比增加,胞浆少,胞界不清,核大小形状不同,增大增长,假复层排列,染色质增多。
宫颈内膜原位腺癌
图87宫颈内膜原位腺癌
异常宫颈腺上皮细胞拉长呈高柱状、细胞呈羽毛状排列、细胞核朝向细胞群周边,细胞浆朝向向中心,核增大程度不一,核深染,染色质中颗粒状,核仁不明显或仅一个小核仁。
图88宫颈内膜原位腺癌
宫颈腺上皮细胞拉长呈高柱状,细胞核过度拥挤排列成假复层,细胞核朝向细胞群周边,细胞浆朝向中心,胞核增大,拉长形成层状结构,染色质颗粒状,核仁不明显或仅一个小核仁。
图89宫颈内膜原位腺癌
宫颈腺上皮细胞拉长呈高柱状,细胞核过度拥挤排列成假复层,细胞核朝向细胞群周边,细胞浆朝向中心,胞核增大,拉长形成层状结构,染色质颗粒状,核仁不明显或仅一个小核仁。
图90宫颈内膜原位腺癌
宫颈腺上皮细胞片状排列,细胞界限不清,细胞核过度拥挤,胞核增大,拉长形成层状结构,核中度深染,染色质颗粒状,核仁不明显或仅一个小核仁。
腺癌
图91腺癌(宫颈内膜)
腺细胞呈玫瑰花样排列,可见单个散在细胞,核增大,直径为正常细胞的2倍以上,核大小不一致,核多形性更明显,核边增厚而不规则,核仁明显,胞浆蓝染,大小不等或囊状空泡出现。
图92腺癌(子宫内膜)
一群细胞中排列疏密不一致,核增大,核大小不一致,核多形性更明显,染色质可分布不均匀,核间距甚窄,可能见到拥挤重叠,核边不规则性增厚,染色质粗颗粒状,核仁明显增大,过度拥挤的细胞中出现非常小的细胞,其核非常致密,极难看清核结构,胞浆蓝染,大小不等或囊状空泡出现。
图93腺癌(子宫内膜)
细胞呈团状出现,细胞胞界不清楚,胞浆蓝染,大小不等或囊状空泡出现,核增大,大小不一致,核边增厚而不规则,核仁明显,染色质粗颗粒状,分布不均。
图94腺癌(子宫内膜)
一群细胞中排列疏密不一致,核增大为正常细胞的2倍以上,核大小不一致,核间距甚窄,可能见到拥挤重叠,核边不规则性增厚,染色质粗颗粒状,分布不均匀,核仁小,核多形性更明显,细胞排列呈团块三维结构,胞浆蓝染,有空泡出现。
第八章
TBS系统中异常上皮细胞的诊断与处理
不典型鳞状细胞ASC
细胞学结果为ASC,包括ASC-US和ASC-H;对ASC-H的病人进行阴道镜检查,病理报告CINⅡ、CINⅢ,来自ASC-H比例较大(24%—94%);但ASC妇女患浸润性宫颈癌的危险性很低(0.1%0.2%)。
ASC-US的诊断与处理
1、ASC-US伴高危型HPV-DNA阴性妇女采用重复宫颈细胞学检查,间隔4-6个月一次,直至连续2次阴性为止,然后转回常规细胞学筛查方案,如果随访中发现第2次涂片结果为ASC-US,应做阴道镜下活检。
2、ASC-US伴高危型HPV-DNA阳性妇女应做阴道镜下活检。
3、ASC-US伴高危型HPV-DNA经活检未证实有CIN者,可随访6-12个月,做细胞学检查,若又出现ASC-US,则做阴道镜下活检,或于12个月后检测高危型HPV-DNA,阳性者做阴道镜下活检。
4、ASC-US妇女直接做阴道镜时,若未发现CIN,可随访至12个月重复细胞学检查,若活检证实为CIN,则按宫颈组织学异常的常规处理。
5、为了防止过度治疗,ASC妇女活检未证实CIN,不常规采用子
宫颈环形电切术(LEEP)。
6、ASC-US的特殊情况
(1)绝经后妇女:
对临床或细胞学证实有宫颈阴道萎缩,且无阴
道内应用雌激素禁忌者,可用1疗程的阴道内雌激素,停药
一周后再做宫颈细胞学检查,如果再次检查结果阴性,则4-
6个月复查,仍为阴性者转回常规细胞学筛查,其中任何一
次细胞学出现ASC-US或更高级别,应做阴道镜下活检。
(2)免疫抑制妇女:
所有免疫抑制妇女,包括HPV感染,出现
ASC-US者,建议做阴道镜下活检。
(3)妊娠妇女:
出现ASC-US时的处理同非妊娠妇女。
ASC-H的诊断与处理
1、ASC-H妇女应做阴道镜下活检。
2、经阴道镜活检无病变,建议复习细胞学、阴道镜和组织病理
学结果。
3、若复习后结果有修正,则按修正结果常规处理。
4、若复习后仍确定为ASC-H,则随访6-12个月做细胞学复查,或
12个月后检测HPV-DNA,两者之一出现阳性应行阴道镜下活
检。
低度鳞状上皮内病变LSIL
在美国LSIL的中位数发生率为1.6%,但高危人群为7.7%,多
数妇女将自然逆转为正常,10%-30%的细胞学诊断为LSIL的妇
女通过宫颈活检证实为CINⅡ、CINⅢ。
LSIL包括CINⅠ和HPV
感染,两者细胞病理形态难以区别。
LSIL的诊断与处理
1、推荐做HPV-DNA检测和阴道镜下活检。
2、宫颈管搔刮取材活检。
3、LSIL患者经活检不能证实为CIN者,随访6-12个月做细胞
学复查,结果为ASC-US或更高级别者做阴道镜活检,或
随访12个月,高危型HPV-DNA阳性做阴道镜活检。
4、LSIL患者经活检证实为CIN者,则根据宫颈组织学异常的
常规处理(CINI可用药物或物理治疗)。
5、LSIL的特殊情况
(1)绝经后妇女:
开始不做阴道镜检,而是随访6-12个月细
胞学检查,若又出现≥ASC-US或于12个月后高危型HPV-
DNA阳性者,做阴道镜下活检,临床或细胞学证实有宫颈
阴道萎缩,且无阴道内应用雌性激素禁忌者,先用1疗程
的阴道内雌性激素,停药一周后再做宫颈细胞学检查,
若细胞学出现ASC-US或更高级别,应做阴道镜下活检,
若组织病理学结果排除上皮内瘤变或更高度病变,可间
隔4-6个月重复细胞学检查,两次结果阴性者转回常规筛
查。
(2)青春期少女:
可随访,不立即做阴道镜检,6-12个月复
查细胞学,或12个月检测HPV-DNA,如果出现ASC或高危
型HPV-DNA阳性,应立即行阴道镜检。
(3)妊娠妇女:
同HSIL处理。
高度鳞状上皮内病变HSIL
HSIL包括CINⅡ、CINⅢ,发展为癌的危险性分别为30%、45%
HSIL的诊断与处理
1、行HPV-DNA检测和阴道镜下活检及宫颈管搔刮取材,此后
处理按所确定的病变决定。
2、若活检证实无病变,或仅为CINI,建议复习细胞学、阴
道镜和组织学结果,若复习后结果有修正,则按修正结
果常规处理,若复习后仍确定为HSIL,则做诊断性宫颈
锥切或LEEP术。
3、若计划行诊断性宫颈锥切,则可免除宫颈管内搔刮取
材。
4、妊娠妇女,HSIL孕妇应由经验丰富的医生进行阴道镜检
查,对怀疑为高度病变或癌的部位可做活检,但不做宫
颈管内搔刮术。
不典型腺细胞AGC和宫颈内膜原位腺癌AIS
2001年TBS系统将腺上皮细胞异常(严重程度低于腺癌者)分为三类:
AGC:
不典型的子宫颈管内膜细胞、子宫内膜细胞和腺细胞,
未明示(NOS,AGC-NOS);
AGC:
不典型的子宫颈管内膜细胞和腺细胞,倾向瘤变(AGC-
favorneoplasia);
宫颈内膜原位腺癌(AIS)
AGC-favorneoplasia与AGC-NOS为两种不同危险程度
的病变,AGC-NOS妇女活检证实为CINⅡ、CINⅢ或浸润
癌者占9%-41%,而AGC-favorneoplasia中为27%-
96%,细胞学AIS者活检证实为原位癌者48%-69%,浸润
癌38%。
AGC和AIS的处理
1、对所有AGC妇女均建议行阴道镜活检和宫颈管搔刮取材
(ECC);但在不典型子宫内膜细胞(未明示,NOS)妇
女,首先应做子宫内膜取材检查,对细胞学结果AIS者,
同样建议行阴道镜活检和宫颈管搔刮取材。
2、若阴道镜活检为原位腺癌或怀疑浸润腺癌,则建议AGC-
favorneoplasia或AIS患者行诊断性宫颈锥切,宜用冷
刀锥形切除。
3、若AGC-NOS妇女活检无癌或癌前病变,则建议4-6个月做细
胞学复查,直至连续四次阴性为止,然后转回常规筛查。
宫颈癌筛查流程图
近年来,许多研究证明液基薄层细胞学和HPV-DNA检测(HC
2)结合起来,对宫颈癌的筛查效果是最理想的,欧美国家多
主张医生取材HPV-DNA(HC2)检测和液基薄层细胞学同时进
行,但中国从经济的角度出发,多数专家认为先进行细胞学
筛查,异常者再行HPV-DNA的筛查。
宫颈癌筛查流程图如下图(转下页):
宫颈癌前病变的治疗
对CIN的治疗包括药物、物理和手术治疗。
依据CIN诊断级
别,参照HPV检测,明确诊疗原则,使治疗规范化,对病人年
龄、婚育情况以及症状、随诊及技术条件、病人意愿等综合
考虑,做到治疗个体化。
宫颈癌筛查流程图
HPV阳性的处理
1、HPV疫苗是最有前途的。
从主动特异性免疫治疗方面,研究
了HPV16和HPV18的病毒疫苗,人工合成的多肽疫苗,病毒
颗粒样疫苗和DNA疫苗。
2、对于35岁以上持续性高危型HPV感染者,同时又合并CIN
的,应以治疗CIN为主,通过治疗CIN,也就是通过治疗HPV
感染造成的病变,达到在一定时间内使HPV转阴的目的。
CIN治疗注意点
1、CINI、CINⅡ主要应用物理治疗,包括冷冻、激光、微波
和LEEP。
2、LEEP主要应用于面积较大的CINⅡ、CINⅢ。
对于原位癌,
除非可足够切除一定的宽度(病灶外0.5cm)和高度
(2.5cm),否则应选择冷刀锥切(CKC)。
CKC能根据病变程度和范围,做出可靠的锥形活检和适宜的治疗。
宫颈癌的诊断与处理
细胞学结果为鳞状细胞癌或腺癌的病例,一旦组织病理学诊断
后,则按浸润癌常规处理,宫颈癌治疗的新进展概括如下:
1、选择个体化、人性化的治疗原则
对于宫颈癌Ia和个别Ib1期要求保留生育功能的宫颈癌病例,可
行广泛性子宫颈切除术加淋巴清扫术。
广泛性子宫切除手术包
括:
切除部分阴道,子宫内口以下的子宫颈,骶韧带和主韧带
的处理同次广泛性子宫切除术。
切除宫颈后,将内口以上子宫
体与阴道残端吻合缝合。
2、局部晚期和大病灶病人,最好先行新辅助化疗(指病人在手术
或放疗有先期化疗),然后手术或放疗。
3、首选新辅助化疗,然后手术,已成为中、青年宫颈癌病人治疗
方案的发展趋势。
4、Ⅱ期、Ⅲ期宫颈癌病人新辅助化疗后,行广泛性子宫切除术并
不增加手术危险性;相反,手术时间缩短,出血减少,术后合
并症发生率降低,生存率提高。
因此,新辅助化疗后选择合适
的方案行广泛性子宫切除术是有前途的。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 薄层 宫颈 细胞学
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
