 精编版初中四大基本反应类型练习含答案.docx
精编版初中四大基本反应类型练习含答案.docx
- 文档编号:654836
- 上传时间:2022-10-11
- 格式:DOCX
- 页数:12
- 大小:31.41KB
精编版初中四大基本反应类型练习含答案.docx
《精编版初中四大基本反应类型练习含答案.docx》由会员分享,可在线阅读,更多相关《精编版初中四大基本反应类型练习含答案.docx(12页珍藏版)》请在冰豆网上搜索。
精编版初中四大基本反应类型练习含答案
初中化学四大基本反应类型
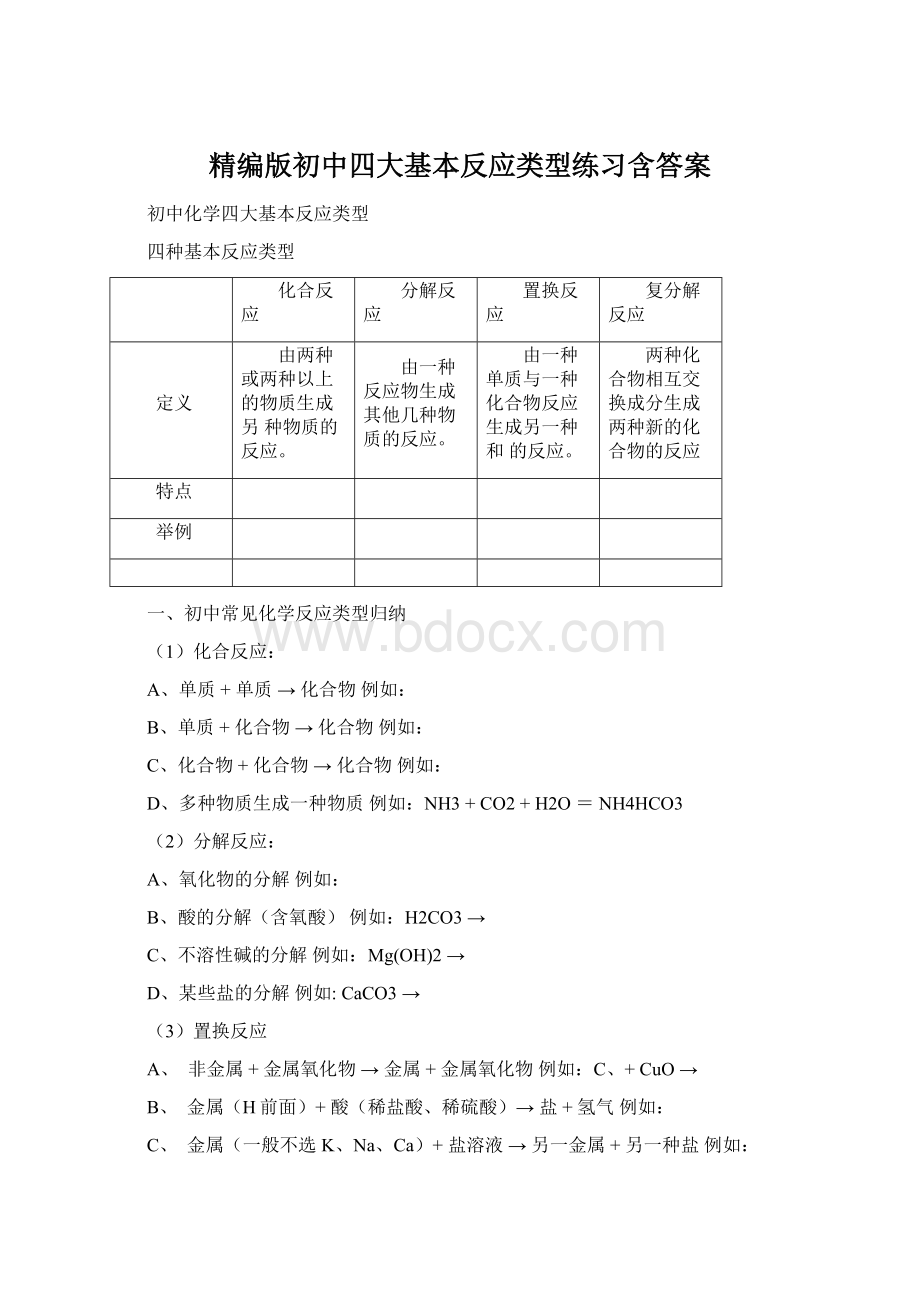
四种基本反应类型
化合反应
分解反应
置换反应
复分解反应
定义
由两种或两种以上的物质生成另种物质的反应。
由一种反应物生成其他几种物质的反应。
由一种单质与一种化合物反应生成另一种和的反应。
两种化合物相互交换成分生成两种新的化合物的反应
特点
举例
一、初中常见化学反应类型归纳
(1)化合反应:
A、单质+单质→化合物例如:
B、单质+化合物→化合物例如:
C、化合物+化合物→化合物例如:
D、多种物质生成一种物质例如:
NH3+CO2+H2O=NH4HCO3
(2)分解反应:
A、氧化物的分解例如:
B、酸的分解(含氧酸)例如:
H2CO3→
C、不溶性碱的分解例如:
Mg(OH)2→
D、某些盐的分解例如:
CaCO3→
(3)置换反应
A、 非金属+金属氧化物→金属+金属氧化物例如:
C、+CuO→
B、 金属(H前面)+酸(稀盐酸、稀硫酸)→盐+氢气例如:
C、 金属(一般不选K、Na、Ca)+盐溶液→另一金属+另一种盐例如:
D、 水与其它单质的反应例如:
2Na+2H2O=2NaOH+H2↑,C+H2O=CO+H2
(4)复分解反应
A、 金属氧化物+酸→盐+水例如:
B、 碱+酸→盐+水例如:
C、 碱+盐→另一种碱+另一种盐例如:
D、 盐+盐→两种新盐例如:
E、 盐+酸→另一种盐+另一种酸例如:
二、化学反应发生的条件
化学反应能否发生与反应物质本身的性质(内因)和外界条件(外因)有关。
(1)外界条件
例如,燃烧需要点燃,氢气还原氧化铜需要加热,水分解需要通电,碳酸钙分解需要高温,氯酸钾分解制氧气需要加热和催化剂,像点燃、加热、高温、通电、催化剂都是外界条件。
(2)金属活动性顺序表(注重基础)
A按金属活动性由强到弱的顺序写出14种常见金属的活动性顺序表。
KCa(H)
B、排在氢前面的金属置换酸中的氢生成氢气。
C、排在前面的金属能把排在后面的金属从它的盐溶液中置换出来。
(一般不使用K、Ca、Na)
D、Fe与排在其后的金属的盐溶液反应也只能生成亚铁盐。
(3)复分解反应发生的条件
A、反应物:
在上面的复分解反应类型中C、D两类的反应物一般要求均可溶;
B、生成物:
一般要有或或水生成。
一、化合反应
(一)、金属+氧气--------金属氧化物
1、镁在空气中燃烧:
2、铁在氧气中燃烧:
3、铝在空气中燃烧:
4、铜在空气中受热:
5、汞在空气中受热:
(二)、非金属+氧气--------非金属氧化物
6、氢气在空气中燃烧:
7、红磷在空气中燃烧:
8、硫粉在空气中燃烧:
9、碳在氧气中充分燃烧:
10、碳在氧气中不充分燃烧:
(三)、金属氧化物+水--------碱(可溶性)
11、生石灰溶于水:
12、氧化钠溶于水:
(四)、非金属+水--------非金属氧化物
13、二氧化碳和水反应:
14、二氧化硫溶于水:
15、三氧化硫溶于水:
(五)、其他
16、二氧化碳通过灼热碳层:
17、一氧化碳在氧气中燃烧(煤气燃烧):
18、钠在氯气中燃烧:
19、氯气在氢气中点燃(共价化合物的形成、制备盐酸):
20、无水硫酸铜作干燥剂:
二、分解反应
21、氧化汞受热分解:
22、双氧水制氧气(实验室制备氧气):
23、加热高锰酸钾(实验室制备氧气):
24、加热氯酸钾(有少量的二氧化锰)(实验室制备氧气):
25、水在直流电的作用下分解:
26、碳酸不稳定而分解:
27、高温煅烧石灰石(二氧化碳工业制法):
28、硫酸铜晶体受热分解:
29、碱式碳酸铜(铜绿)受热分解:
30、碳酸氢铵受热分解(碳酸氢铵长期暴露空气中会消失):
三、置换反应(一定属于氧化还原反应)
(一)、金属单质+酸--------盐+氢气
31、锌和稀硫酸反应(实验室制氢气):
32、铁和稀硫酸反应:
33、铝和稀硫酸反应:
34、镁和稀硫酸反应:
35、锌和稀盐酸:
36、铁和稀盐酸:
37、铝和稀盐酸:
38、镁和稀盐酸:
(二)、非金属单质+金属氧化物--------金属单质+水
39、氢气还原氧化铜:
40、氢气还原氧化铁:
41、氢气还原四氧化三铁:
42、木炭还原氧化铜:
43、焦炭还原氧化铁:
44、水蒸气通过灼热碳层:
(三)、金属单质+盐(溶液)-------另一种金属+另一种盐
45、铁和硫酸铜溶液反应(湿法炼铜、镀铜原理):
46、锌和硫酸亚铁溶液反应:
47、锌和硫酸铜溶液反应(镀铜):
48、铜和硝酸汞溶液反应:
49、铜和硝酸银溶液反应(镀银):
四、复分解反应
(一)、碱性氧化物(金属氧化物)+酸--------盐+水
50、氧化铁和稀盐酸反应:
51、氧化铁和稀硫酸反应:
52、氧化铜和稀盐酸反应:
53、氧化铜和稀硫酸反应:
54、氧化镁和稀硫酸反应:
55、氧化钙和稀盐酸反应:
56、氧化钠和稀盐酸反应:
(二)、酸+碱--------盐+水【中和反应】
57、盐酸和烧碱起反应:
58、盐酸和氢氧化钾反应:
59、盐酸和氢氧化铜反应:
60、盐酸和氢氧化钙反应:
61、盐酸和氢氧化铁反应:
62、氢氧化铝药物治疗胃酸过多:
63、硫酸和烧碱反应:
64、硫酸和氢氧化钾反应:
65、硫酸和氢氧化铜反应:
66、硫酸和氢氧化铁反应:
67、硫酸和氢氧化钡反应:
68、硝酸和烧碱反应:
(三)、酸+盐--------另一种酸+另一种盐
69、石灰石(或大理石)与稀盐酸反应:
70、碳酸钠与稀盐酸反应(泡沫灭火器的原理):
71、碳酸镁与稀盐酸反应:
72、盐酸和硝酸银溶液反应:
73、硫酸和碳酸钠反应:
74、硫酸和氯化钡溶液反应:
(四)、碱+盐--------另一种碱+另一种盐
75、氢氧化钠与硫酸铜:
76、氢氧化钠与氯化铁:
77、氢氧化钠与氯化镁:
78、氢氧化钠与氯化铜:
79、氢氧化钙与碳酸钠:
80、氢氧化钠与硝酸铵:
(五)、盐+盐-----两种新盐
81、氯化钠溶液和硝酸银溶液:
82、硫酸钠和氯化钡:
其他(不属于四种基本反应类型)
(一)有机物的燃烧
83、甲烷在空气中燃烧(甲烷和天然气的燃烧):
84、酒精(乙醇)在空气中燃烧(氧炔焰、焊接切割金属):
(二)还原剂和氧化物反应
85、一氧化碳还原氧化铜:
86、一氧化碳还原氧化铁:
(三)酸性氧化物+碱--------盐+水
87、氢氧化钠和二氧化碳反应(苛性钠暴露在空气中变质)(除去二氧化碳):
88、氢氧化钠吸收二氧化硫气体(处理硫酸工厂的尾气SO2):
89、氢氧化钠吸收三氧化硫气体:
90、二氧化碳通过澄清石灰水(消石灰放在空气中变质)(检验二氧化碳):
91、氢氧化钙(熟石灰,消石灰)吸收二氧化硫:
一、化合反应
(一)、金属+氧气--------金属氧化物
1、镁在空气中燃烧:
2Mg+O22MgO(剧烈燃烧,耀眼白光,放热,生成白色固体)
2、铁在氧气中燃烧:
3Fe+2O2 Fe3O4(剧烈燃烧,火星四射,放热,生成黑色固体)
3、铝在空气中燃烧:
4Al+3O2 2Al2O3(银白金属变为白色固体)
4、铜在空气中受热:
2Cu+O22Cu(红色金属变为黑色固体)
5、汞在空气中受热:
2Hg+O22HgO(由银白液体,生成红色固体)
(二)、非金属+氧气--------非金属氧化物
6、氢气在空气中燃烧:
2H2+O2 2H2O(淡蓝火焰,放热,生成使无水CuSO4变蓝的液体)
7、红磷在空气中燃烧:
4P+5O2 2P2O5(剧烈燃烧,放热,放出大量白烟)
8、硫粉在空气中燃烧:
S+O2SO2(剧烈燃烧,放热,生成有刺激味气体;在空气中淡蓝色火焰,在氧气中蓝紫色火焰)
9、碳在氧气中充分燃烧:
C+O2 CO2(剧烈燃烧,发出白光,放热,生成使澄清石灰水变浑浊的气体)
10、碳在氧气中不充分燃烧:
2C+O22CO
(三)、金属氧化物+水--------碱(可溶性)
11、生石灰溶于水:
CaO+H2O==Ca(OH)2(放热)
12、氧化钠溶于水:
Na2O+H2O==2NaOH(放热)
(四)、非金属+水--------非金属氧化物
13、二氧化碳和水反应:
CO2+H2O==H2CO3(二氧化碳通入紫色石蕊试液,溶液变红,说明二氧化碳溶于水显酸性)
14、二氧化硫溶于水:
SO2+H2O==H2SO3
15、三氧化硫溶于水:
SO3+H2O==H2SO4
(五)、其他
16、二氧化碳通过灼热碳层:
C+CO2 2CO
17、一氧化碳在氧气中燃烧(煤气燃烧):
2CO+O2 2CO2(蓝色火焰)
18、钠在氯气中燃烧:
2Na+Cl22NaCl(剧烈燃烧,黄色火焰)
19、氯气在氢气中点燃(共价化合物的形成、制备盐酸):
H2+Cl22HCl(苍白色火焰,瓶口白雾)
20、无水硫酸铜作干燥剂:
CuSO4+5H2O==CuSO4·5H2O(白色固体变蓝)
二、分解反应
21、氧化汞受热分解:
2HgO2Hg+O2↑(红色固体变为银白液体,生成使带火星木条复燃的气体)
22、双氧水制氧气(实验室制备氧气):
2H2O22H2O+O2↑
23、加热高锰酸钾(实验室制备氧气):
2KMnO4K2MnO4+MnO2+O2↑
24、加热氯酸钾(有少量的二氧化锰)(实验室制备氧气):
2KClO32KCl+3O2↑
25、水在直流电的作用下分解:
2H2O2H2↑+O2↑
26、碳酸不稳定而分解:
H2CO3==H2O+CO2↑
27、高温煅烧石灰石(二氧化碳工业制法):
CaCO3CaO+CO2↑
28、硫酸铜晶体受热分解:
CuSO4·5H2OCuSO4+5H2O(蓝色晶体变为白色粉末)
29、碱式碳酸铜(铜绿)受热分解:
Cu2(OH)2CO32CuO+H2O+CO2↑(绿色固体变黑色固体,生成使澄清石灰水变浑浊气体和使无水CuSO4变蓝的液体)
30、碳酸氢铵受热分解(碳酸氢铵长期暴露空气中会消失):
NH4HCO3NH3↑+H2O+CO2↑(白色固体消失,有刺激性气味的气体生成,且能使湿润的PH试纸变蓝,生成使澄清石灰水变浑浊气体)
三、置换反应(一定属于氧化还原反应)
(一)、金属单质+酸--------盐+氢气
31、锌和稀硫酸反应(实验室制氢气):
Zn+H2SO4==ZnSO4+H2↑
32、铁和稀硫酸反应:
Fe+H2SO4==FeSO4+H2↑(溶液由无色变为浅绿色)
33、铝和稀硫酸反应:
2Al+3H2SO4==Al2(SO4)3+3H2↑
34、镁和稀硫酸反应:
Mg+H2SO4==MgSO4+H2↑
35、锌和稀盐酸:
Zn+2HCl==ZnCl2+H2↑
36、铁和稀盐酸:
Fe+2HCl==FeCl2+H2↑(溶液由无色变为浅绿色)
37、铝和稀盐酸:
2Al+6HCl==2AlCl3+3H2↑
38、镁和稀盐酸:
Mg+2HCl==MgCl2+H2↑
(二)、非金属单质+金属氧化物--------金属单质+水
39、
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 精编 初中 四大 基本 反应 类型 练习 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
