 人教版初中化学第十十一单元.docx
人教版初中化学第十十一单元.docx
- 文档编号:6419851
- 上传时间:2023-01-06
- 格式:DOCX
- 页数:11
- 大小:144.79KB
人教版初中化学第十十一单元.docx
《人教版初中化学第十十一单元.docx》由会员分享,可在线阅读,更多相关《人教版初中化学第十十一单元.docx(11页珍藏版)》请在冰豆网上搜索。
人教版初中化学第十十一单元
第十单元 常见的酸和碱
✧常见的酸
Ø酸在水溶液中离解产生的阳离子都是 H+ ,即不同的酸溶液中都含有相同的 H+ ,所
以酸溶液的化学性质 相似 ,我们称之为酸的 通性 ,简称 酸性 ,实际上是 H+ 的性质。
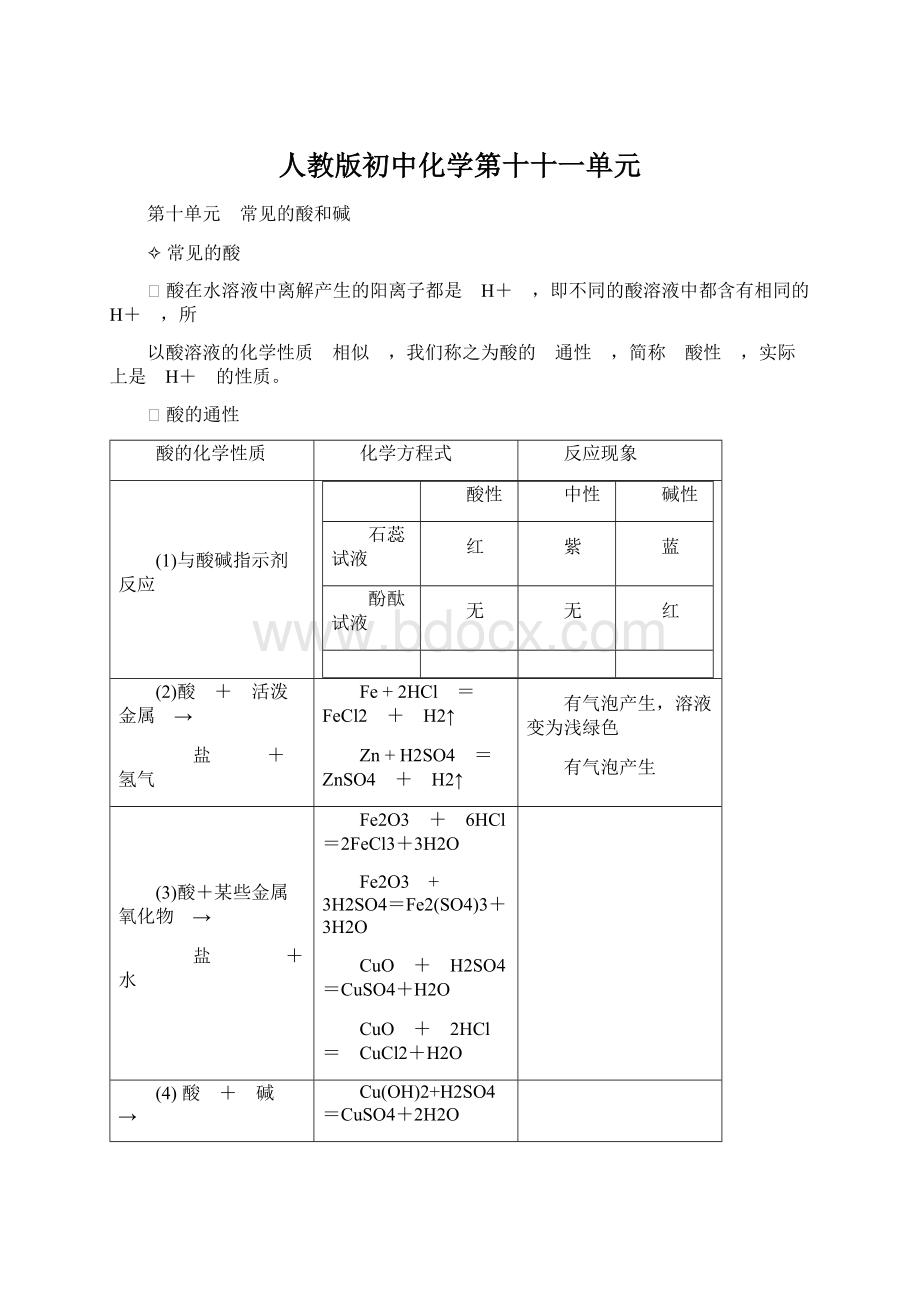
Ø酸的通性
酸的化学性质
化学方程式
反应现象
(1)与酸碱指示剂反应
酸性
中性
碱性
石蕊试液
红
紫
蓝
酚酞试液
无
无
红
(2)酸 + 活泼金属 →
盐 + 氢气
Fe+2HCl = FeCl2 + H2↑
Zn+H2SO4 = ZnSO4 + H2↑
有气泡产生,溶液变为浅绿色
有气泡产生
(3)酸+某些金属氧化物 →
盐 + 水
Fe2O3 + 6HCl =2FeCl3+3H2O
Fe2O3 + 3H2SO4=Fe2(SO4)3+3H2O
CuO + H2SO4 =CuSO4+H2O
CuO + 2HCl= CuCl2+H2O
(4)酸 + 碱 →
盐 + 水
Cu(OH)2+H2SO4=CuSO4+2H2O
2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O
Fe(OH)3+3HCl=FeCl3+3H2O
Cu(OH)2 +2HCl= CuCl2+2H2O
(5)酸 + 盐 →
新酸 + 新盐
条件:
有水、沉淀、气体生成。
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
AgNO3+HCl=AgCl↓+HNO3
Ba(NO3)2+H2SO4=BaSO4↓+2HNO3
Ø浓盐酸具有 挥发 性,打开盛有浓盐酸的瓶盖后,在瓶口会看到 白雾 ,这是因为浓盐酸
挥发 出的 HCl气体 与空气中的 水蒸气 相结合形成 盐酸的小液滴 。
Ø浓硫酸有 吸水 性,在实验室中常用它做干燥剂;浓硫酸有强烈的 脱水 性,能夺取纸张、
木材、皮肤里的水分,生成黑色的 炭 ,而产生 碳化 现象。
因为浓硫酸还具有 强腐蚀 性如果不慎将浓硫酸沾到皮肤或衣服上,应立即用 大量的水冲洗 ,然后 再涂上3%~5%的NaHCO3溶液 。
在稀释浓硫酸时,一定要把 浓硫酸 沿器壁慢慢注入 水 里,并不断 搅拌 。
切不可将 水 倒进
浓H2SO4 里。
这是因为浓硫酸的密度比水 大 ,如将 水 倒入 浓H2SO4 中,则
水 会浮在 浓H2SO4 的上面,而浓硫酸溶解时 放 出的大量热,无法 散失 ,而使液体 沸腾 而溅出伤人。
✧中和反应
Ø中和反应特指 酸 和碱生成 盐 和水的反应。
中和反应仍然属于 复分解
反应
Ø中和反应的实质是:
酸溶液中的 H+ 和碱溶液中的 OH- 生成 H2O 的过程。
中和反应一定有 盐 和 H2O 生成。
但有 盐 和 H2O 生成的反应 不一定 是中和反应。
✧常见的碱
✧碱在水溶液中都能离解出金属离子和 OH- ,不同的碱溶液中都含有相同的 OH-
所以碱溶液的化学性质 相似 ,我们称之为碱的 通性 ,简称 碱性 ,实际上是 OH- 的性质。
Ø常见的碱
氢氧化钠
氢氧化钙
化学式
NaOH
Ca(OH)2
俗 名
火碱、烧碱、苛性钠
熟石灰、消石灰
腐蚀性
强
有
物理性质
NaOH是一种 白 色 易溶于水的 固 体,在空气中易 潮解 。
同时 放出 大量的热。
Ca(OH)2是一种 白 色 固 体,
微溶于水。
保 存
制 备
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
CaO+H2O=Ca(OH)2
用 途
(1)用于 造纸;
(2)用于 纺织;
(3)用于 印染;
(4)用于 石油;
(6)制 肥皂;
(7)能与 油脂反应,所以在生活
和生产中用于去除 油污(炉具)。
(1)建筑业:
制 三合土 ,(主要成分:
沙子 、 粘土 、 熟石灰 )
(2)工业上:
制 NaOH
(3)农业:
改良酸性土壤、制农药 波尔多液 ,(主要成分:
CuSO4 、 Ca(OH)2 )和石硫合剂。
Ø碱的通性
碱的化学性质
化学方程式
反应现象
(1)与酸碱指示剂反应
只有 可溶性 的碱才能使酸碱指示剂变色。
(2)碱+某些非金属氧化物 → 盐 + 水
条件:
碱必须可溶
2NaOH+CO2=Na2CO3+H2O
Ca(OH)2+CO2 =CaCO3↓+H2O
Ca(OH)2+SO2=CaSO3↓+H2O
2NaOH+SiO2=Na2SiO3+H2O
(3)碱 + 酸反应生成 → 盐 + 水
Cu(OH)2+H2SO4=CuSO4+H2O
2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O
(4)碱 + 盐 →
新碱 + 新盐
条件:
碱盐必须都可溶
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
3NaOH+FeCl3=Fe(OH)3↓+3NaCl
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
NaOH+NH4Cl=NH3↑+H2O+NaCl
✧pH
Ø溶液的酸碱性可用 酸碱指示剂 来检测。
Ø溶液酸碱性的强弱与 H+ 或 OH- 的浓度有关。
Ø酸碱度表示溶液 酸碱性的强弱 。
其大小可用 pH 表示。
ØpH可通过 pH试纸 和 pH计 获得
ØpH试纸的使用方法:
先将pH试纸放在 表面皿 中,再用 洗净擦干的玻璃棒
沾取少量待测液滴在 pH试纸 上,30秒后与 标准比色卡 对比读出读数。
通过pH试纸获得的pH值只能为 整数 。
且pH试纸的取值范围是 1~14 。
✧pH与酸碱性
Ø酸性溶液的pH都 < 7,且酸性越强其pH越 小 。
所以溶液的酸性与pH反 比
Ø碱性溶液的pH都 > 7,且碱性越强其pH越 大 。
所以溶液的碱性与pH正 比
Ø向酸性溶液中不断加水其pH将如何变化 pH值不断增大且无限接近于7但不会超过7 。
Ø向碱性溶液中不断加水其pH将如何变化 pH值不断减小且无限接近于7但不会超过7 。
Ø用一带水的玻璃棒测得溶液的pH=5则其pH的真实值 < 5(填“>”“=”或“<”=)
Ø欲将pH=4的溶液变为pH=9,所加入溶液的pH必须 >9 。
第十一单元 盐 化肥
✧氯化钠
Ø化学式:
NaCl
Ø物理性质:
氯化钠是一种 白 色 立方 体形有 咸 味的 固 体, 易 溶于水。
Ø自然存在:
氯化钠主要存在于 海 水,盐 湖 ,盐 井 ,盐 矿 中。
工业:
用于制 Na2CO3 , NaOH , Cl2 和 HCl 。
Ø用途:
农业:
用氯化钠的 饱和 液进行 选种 。
医疗:
用氯化钠制 生理盐水 ,其浓度为 0.9% 。
生活:
用于 腌渍 蔬菜、鱼、肉、蛋等,以 延长 食物的 保存期 ,且使食物有 特殊味道 。
用于消除 冰雪 。
Ø工业盐:
NaNO2
Ø粗盐提纯:
✧碳酸盐
Ø常见的碳酸盐
碳酸钠
碳酸氢钠
碳酸钙
化学式
Na2CO3
NaHCO3
CaCO3
俗 名
纯碱、苏打
小苏打
自然存在
盐湖
大理石、石灰石
物理性质
白色固体易溶于水
白色固体易溶于水
白色固体难溶于水
用 途
用于 制玻璃
用于 造纸
用于 纺织
用于 洗涤剂
是 发酵粉 的主要成分之一。
在医疗上,是治疗胃酸过多 的一种药剂。
但有
胃溃疡的病人不能使用
是 石灰石 、
大理石的主要成分,大量用于 建筑业。
是常用的补钙剂。
Ø碳酸盐的特性:
(1)难溶性的碳酸盐在高温条件下可以分解成金属氧化物和二氧化碳
CaCO3
CaO + CO2↑
(2)所有的碳酸盐都可以和二氧化碳、水反应生成碳酸氢盐
CaCO3 + CO2 + H2O = Ca(HCO3)2
Na2CO3 + CO2 + H2O = 2NaHCO3
(3)所有的碳酸氢盐都可溶
(4)所有的碳酸氢盐固体受热都能分解成碳酸盐、水和二氧化碳
2NaHCO3
Na2CO3 + CO2↑ + H2O
Ca(HCO3)2
CaCO3 + CO2↑ + H2O
(5)所有的碳酸盐和碳酸氢盐都能和酸反应
盐的性质
⏹酸 + 盐
新酸 + 新盐 ( 复分解反应 )
注:
不能 弱酸 制 强酸 。
⏹碱 + 盐
新碱 + 新盐 ( 复分解反应 )
注:
碱和盐必须都 可溶 ;新碱和新盐中至少有一种 难溶 。
⏹盐 + 盐
新盐 + 新盐 ( 复分解反应 )
注:
盐必须都 可溶 ;新盐至少有一种 难溶 。
⏹金属 + 盐
新金属 + 新盐 ( 置换反应 )
注:
金属必须在新金属的 前面 。
K 、 Ca 、 Na 、因为 活泼性 太强,直接与 H2O 反应所以不能置换出任何金属。
盐必须是 可溶 的。
✧八大成盐法
条件:
碱必须 可溶 。
✧化肥
Ø复合肥
(1)判断方法:
N、P、K三种元素中至少含有两种的化合物
(2)复合肥的优点:
能 同时 、 均匀 供给作物几种养分。
充分发挥营养元素间的 相互作用 , 有效成分 高。
Ø常见的化肥
氮 肥
功 能
是植物 蛋白质 、 核酸 和 叶绿素 的组成元素
缺少时症状
植物的生长发育会 迟缓 或 停滞 ,影响 光合作用 的速率及其产物的形成而使作物 品质 降低。
叶片 发黄 。
常见的氮肥
尿素 CO(NH2)2 ( 46.7% ),氨水 NH3·H2O ,
碳酸氢铵 NH4HCO3 ( 17.7% ),氯化铵 NH4Cl ,
硝酸铵 NH4NO3 ( 35% ),硝酸钠 NaNO3 。
磷 肥
功 能
是植物 蛋白质 、 核酸 和 酶 等的组成元素,参与各种重要的 代谢 活动。
促进作物的 根系 发达。
增强作物的抗寒 、 抗旱 能力。
缺少时症状
生长 迟缓 ,植株 矮小 ,产量 降低 。
过多时症状
引起 贪青晚熟 , 结实率 下降。
常见的磷肥
磷矿粉Ca3(PO4)2,钙镁磷肥 Mg3(PO4)2 和 Ca3(PO4)2 ,
过磷酸钙 Ca(H2PO4)2 和 CaSO4 的混合物。
钾 肥
功 能
保证植物各种 代谢 过程的顺利进行、促进植物 生长 ,增强 抗病虫害 和 抗倒伏 的能力。
缺少时症状
易 倒伏 ,易受 病虫害 。
常见的钾肥
硫酸钾 K2SO4 ,氯化钾 KCl 。
✧常见化肥的鉴别
鉴别化肥的常用方法:
氮肥
钾肥
磷肥
看(外观)
白色
灰白色
加水溶解
易溶
难溶
与熟石灰研磨或加热
有刺激性气味
(只适合于铵态氮肥)
无现象
✧两种特殊的化肥
碳酸氢铵(NH4NO3)硝酸铵(NH4NO3)
✧农药、化肥的利与弊
(1)利:
提高农作物产量
二、
铵根离子的鉴定:
(NH4++OH-=NH3+H2O)
取样,加入熟石灰研磨,若有刺激性气味的气体产生,则含NH4+离子。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版 初中化学 第十 十一 单元
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
