 套卷河北省石家庄市无极中学届高三上学期第二次月考化学试题.docx
套卷河北省石家庄市无极中学届高三上学期第二次月考化学试题.docx
- 文档编号:6398298
- 上传时间:2023-01-06
- 格式:DOCX
- 页数:12
- 大小:224.35KB
套卷河北省石家庄市无极中学届高三上学期第二次月考化学试题.docx
《套卷河北省石家庄市无极中学届高三上学期第二次月考化学试题.docx》由会员分享,可在线阅读,更多相关《套卷河北省石家庄市无极中学届高三上学期第二次月考化学试题.docx(12页珍藏版)》请在冰豆网上搜索。
套卷河北省石家庄市无极中学届高三上学期第二次月考化学试题
河北省石家庄市无极中学2014届高三上学期第二次月考化学试题
一.选择题:
(只有一个选项符合题意)共40分
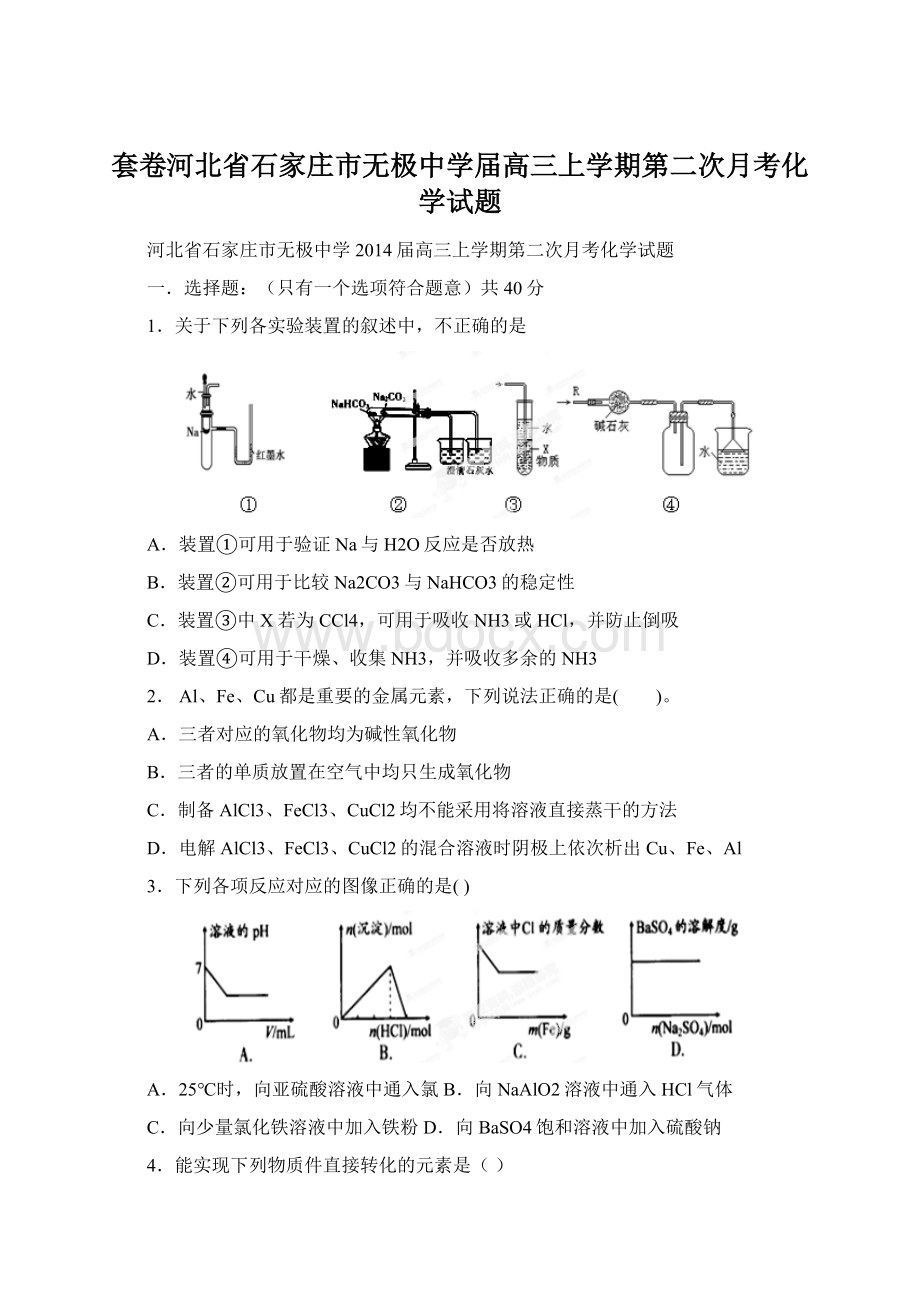
1.关于下列各实验装置的叙述中,不正确的是
A.装置①可用于验证Na与H2O反应是否放热
B.装置②可用于比较Na2CO3与NaHCO3的稳定性
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
2.Al、Fe、Cu都是重要的金属元素,下列说法正确的是( )。
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中均只生成氧化物
C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al
3.下列各项反应对应的图像正确的是()
A.25℃时,向亚硫酸溶液中通入氯B.向NaAlO2溶液中通入HCl气体
C.向少量氯化铁溶液中加入铁粉D.向BaSO4饱和溶液中加入硫酸钠
4.能实现下列物质件直接转化的元素是()
单质
氧化物
酸或碱
盐
A.硅B.氮C.钠D.铁
5.下列关于卤素的叙述中正确的是()
①卤素的钾盐中,最易被氧化的氟化钾;②溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯;③溴化银具有感光性,碘化银不具感光性;④某溶液与淀粉碘化钾溶液反应出现蓝色,则证明该溶液是氯水或溴水;⑤氟气跟氯化钠水溶液反应,一定有HF和O2生成;⑥氯气跟水反应时,水既不是氧化剂也不是还原剂。
A.①③⑤B.②④⑥C.②⑤⑥D.①③④
6.下列实验不能达到预期目的的是()
序号
实验操作
实验目的
A
Cl2、Br2分别与H2反应
比较氯、溴的非金属性强弱
B
MgCl2、AlCl3溶液中分别通入NH3
比较镁、铝的金属性强弱
C
测定Na2CO3、Na2SO4两溶液的pH
比较碳、硫的非金属性强弱
D
用同一电路测定等浓度的盐酸、醋酸两溶液的导电性
比较盐酸、醋酸的酸性强弱
7.一定量的Cu粉与浓硫酸共热产生二氧化硫气体的体积为2.24L(标准状况),则下列情况不可能的是()
A.加入铜的质量为6.4gB.加入浓硫酸中溶质0.2mol
C.加入铜的质量大于6.4gD.加入浓硫酸中含溶质多于0.2mol
8.用向下排气法在容积为VmL的集气瓶中收集氨气。
由于空气未排完,最后瓶内气体的平均相对分子质量为19。
将此盛满气体的集气瓶倒置于水中,瓶内水面上升到一定高度后即停止上升。
则在同温同压下,瓶内剩余气体的体积为()
A.V/4mLB.1/5mLC.V/6mLD.无法判断
9.把3体积的NO2气体,依次通过下列3个分别装有①NaHCO3饱和溶液,②浓H2SO4,③Na2O2的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内气体应是(同温同压下测定)()
A.1体积NOB.2体积NO2和0.5体积O2
C.2体积O2D.0.25体积O2
0.下列各项中的两个量,其比值一定为2∶1的是()
A.在反应2FeCl3+Fe====3FeCl2中还原产物与氧化产物的质量
B.相同温度下,0.2mol·L-1CH3COOH溶液与0.1mol·L-1CH3COOH溶液中c(H+)
C.在密闭容器中,N2+3H2
2NH3已达平衡时c(NH3)与c(N2)
D.液面均在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛溶液的体积
11.某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO—与ClO3—的浓度之比为1:
3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为()
A.21:
5B.11:
3C.3:
1D.4:
1
12.下列有关化学用语表示正确的是()
A.丙烯的结构简式:
C3H6B.氢氧根离子的电子式:
C.氯原子的结构示意图:
D.中子数为146、质子数为92的铀(U)原子14692U
13.四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。
下列说法不正确的是()
A.原子半径Z B.Y的最离价氧化物对应水化物的酸性比X的弱 C.X的最简单气态氢化物的热稳定性比Z的小 D.Z位于元索周期表中第2周期、第ⅥA族 14.常温下,下列各组离子在指定溶液中一定能大量共存的是() A.使甲基橙变红色的溶液: Mg2+、K+、SO42-、NO3- B.使酚酞变红色的溶液: Na+、Cu2+、HCO3-、NO3- C.0.1mol·L-1AgNO3溶液: H+、K+、SO42-、I- D.0.1mol·L-1NaAlO2溶液: H+、Na+、Cl-、SO42- 15下列有质的关物性质与应用不相对应的是()) A.明矾能水解生成Al(OH)3胶体,可用作净水剂 B.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 C.SO2具有氧化性,可用于漂白纸浆 D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 16.海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是 A.海水蒸发制海盐的过程只发生了化学变化 B.海水中含有钾元素,只需要经过物理变化就可以得到钾单质 C.利用潮汐发电是将化学能转化为电能 D.从海水中提取溴单质的过程涉及氧化还原反应 17.下列与碳、氮、氧、硫、硅等非金属元素及其化合物有关的说法不正确的是 A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 B.氮的氧化物是形成光化学烟雾的主要物质,硫的氧化物是形成酸雨的主要物质 C.NO2、CO2和SO2溶于水均可导电,它们都是电解质 D.将SO2通入酸化的Ba(NO3)2溶液中会出现白色沉淀 18.某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色,则下列叙述正确的是( ) A.原溶液中的I-一定被氧化 B.溶液中一定不存在Fe2+ C.通入氯气之后原溶液中的Fe2+一定全部被氧化 D.若取少量所得溶液,再加入CCl4溶液,静置、分液,向上层溶液中加入足量的AgNO3溶液,能产生黄色沉淀 19.“物质的量”是联系宏观世界和微观世界的桥梁。 下列说法正确的是( ) A.“摩尔”是“物质的量”的单位 B.1molO2的质量是32g/mol C.任何气体的“气体摩尔体积”均为22.4L/mol D.10mL2mol/LH2SO4溶液中取出的5mL溶液,其浓度为1mol/L 20.已知33As、35Br位于同一周期。 下列关系正确的是( ) A.原子半径: As>Cl>P B.热稳定性: HCl>AsH3>HBr C.还原性: As3->S2->Cl- D.酸性: H3AsO4>H2SO4>H3PO4 二.填空题: 共63分 1.(共8分)用Cl2消毒会使饮用水中的有机物发生氯化,生成有机氯化合物,于人体有害。 世界环保联盟即将全面禁止用氯气对饮用水消毒。 建议推广采用广谱性高效消毒剂ClO2。 (1)使用ClO2作饮用水消毒剂的优点是: (2)目前,欧洲一些国家用NaClO3氧化浓盐酸制取ClO2,同时有Cl2生成,且Cl2体积为ClO2的一半,该反应的化学方程式是: (3)我国最近研究成功ClO2氧化亚氯酸钠(N2保护下)制ClO2,其反应的化学方程式为: 这一反应的优点是: (4)在H2SO4存在的条件下,用Na2SO3还原NaClO3也可制ClO2,其反应的化学方程式为 2.(共10分)草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色。 某课题组为探究草酸业铁晶体的化学性质,进行了一系列实验探究。 (1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到二氧化碳气体生成。 这说明草酸亚铁晶体具有(填“氧化性”、“还原性”或“碱性”)。 若反应中消耗1molFeC2O4·2H2O,则参加反应的KMnO4为mol。 (2)资料表明: 在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。 课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三: 假设一: 全部是FeO 假设二: 假设三: (3)为验证上述假设一是否成立,课题组进行如下研究。 【定性研究】请你完成下表中内容。 实验步骤(不要求写出具体操作过程) 预期实验现象和结论 取少量黑色固体, 3(共10分) X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最处层电子数相同。 回答下列问题: (1)X、Y和Z的元素符号分别为、、。 (2)由上述元素组成的化合物中,既含有共价键又含有离子键的有、。 (3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是。 此化合物在酸性条件下与高锰酸钾反应的离子方程式为;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为。 4.(共12分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。 根据题意完成下列填空: (1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。 若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为。 (2)上述反应中的氧化剂是,反应产生的气体可用吸收。 (3)As2S3和HNO3有如下反应: As2S3+10H++10NO3—=2H3AsO4+3S+10NO2↑+2H2O 若生成2molH3AsO4,则反应中转移电子的物质的量为。 若将该反应设计成一原电池,则NO2应该在(填“正极”或“负极”)附近逸出。 (4)若反应产物NO2与11.2LO2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量(选填编号)。 5.(共12分)氢化钙固体是登山运动员常用的能源提供剂。 某兴趣小组拟选用如下装置制备氢化钙。 请回答下列问题: (1)请选择必要的装置,按气流方向连接顺序为________(填仪器接口的字母编号)。 (2)根据完整的实验装置进行实验,实验步骤如下: 检查装置气密性后,装入药品;打开分液漏斗活塞;________(请按正确的顺序填入下列步骤的标号)。 A.加热反应一段时间 B.收集气体并检验其纯度 C.关闭分液漏斗活塞 D.停止加热,充分冷却 (3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色。 该同学据此判断,上述实验确有CaH2生成。 ①写出CaH2与水反应的化学方程式__________________________________________; ②该同学的判断不准确,原因是________________________________。 (4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象____________________________________________________________________________。 (5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是___________________。 6(共11分).下图为细菌冶铜和火法冶铜的主要流程。 (1)硫酸铜溶液一般呈________(填“酸”、“碱”或“中”)性,原因是________(用离子方程式表示)。 写出电解硫酸铜溶液的化学方程式: ______________(电解过程中,始终无氢气产生)。 (2)细菌冶金又称微生物浸矿,是近代湿法冶金工业上的一种新工艺。 细菌冶铜与火法冶铜相比,优点为________________(写出一点即可)。 (3)用惰性电极分别电解浓的氯化铜溶液和硫酸铜溶液。 电解浓的氯化铜溶液时发现阴极有金属铜生成,同时阴极附近会出现棕褐色溶液。 而电解硫酸铜溶液时,没有棕褐色溶液生成。 下面是关于棕褐色溶液成分的探究: ①有同学认为,阴极附近出现的棕褐色溶液是氯气反应的结果,你认为他的猜测是否正确? ________(填“正确”或“不正确"),原因是__________ 资料1: 一般具有混合价态(指化合物中同一元素存在两种不同的化合价,如Fe3O4中的Fe元索)的物质的颜色比单一价态的物质的颜色要深。 资料2: CuCl微溶于水,能溶于浓盐酸。 ②猜想: 棕褐色溶液中可能含有的离子是________(填3种主要离子符号)。 ③验证猜想: 完成实验方案(配制棕褐色溶液)。 取少量________固体于试管中,加入________使其溶解,再加入________溶液,观察现象。 ④已知电解前,U形管中加入100mL0.5mol.L-1CuCl2溶液,电解结朿时电路中一共转移了0.03mol电子,且阴极生成0.64g铜,则形成的低价阳离子的物质的量为________mol。 高三化学答题纸 姓名班级考号座位号 ……………………密……………………………………封……………………………………线…………………… 二.填空题: 共63分 1.(共8分) (1)优点是: (2)化学方程式是: (3)化学方程式为: 反应的优点是: (4)反应的化学方程式为 2.(共10分) (1)参加反应的KMnO4为mol。 (2)假设二: 假设三: 实验步骤(不要求写出具体操作过程) 预期实验现象和结论 取少量黑色固体, (3)【定性研究】请你完成下表中内容。 3(共10分) (1)X、Y和Z的元素符号分别为、、。 (2)既含有共价键又含有离子键的有、。 (3)既含有极性共价键又含有非极性共价键的是。 离子方程式为; 离子方程式为。 4.(共12分) (1)As2S3和SnCl2的物质的量之比为。 (2)的氧化剂是,反应产生的气体可用吸收。 (3)转移电子的物质的量为。 NO2应该在附近逸出。 (4)所产生的CO2的量(选填编号)。 5.(共12分) (1)按气流方向连接顺序为。 (2) (3)①化学方程式__________________________________________; ②原因是。 (4)___________________________________________________________________。 (5)其优点是 6(共11分). (1)硫酸铜溶液一般呈_______性, 原因是。 化学方程式: (2)优点为。 (3)①________, 原因是 ②棕褐色溶液中可能含有的离子是。 ③取少量________固体于试管中,加入________使其溶解,再加入________溶液,观察现象。 ④形成的低价阳离子的物质的量为________mol。 5.【答案】 (1)i→e,f→d,c→j,k(或k,j)→a (2)BADC (3)①CaH2+2H2O===Ca(OH)2+2H2↑ ②金属钙与水反应也有类似现象 (4)取适量固体,在加热条件下与干燥氧气反应,将反应气体产物通过装有无水硫酸铜的干燥管,若观察到固体由白色变为蓝色,说明该固体为氢化钙;若观察不到固体由白色变为蓝色,则说明所取固体为钙 (5)氢化钙是固体,便于携带
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 河北省 石家庄市 无极 中学 届高三 上学 第二次 月考 化学试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
