 孙悟空72变万变不离其宗全国化学中考考点扫描适合教师和学生考点54实验型推断题.docx
孙悟空72变万变不离其宗全国化学中考考点扫描适合教师和学生考点54实验型推断题.docx
- 文档编号:6234190
- 上传时间:2023-01-04
- 格式:DOCX
- 页数:22
- 大小:642.21KB
孙悟空72变万变不离其宗全国化学中考考点扫描适合教师和学生考点54实验型推断题.docx
《孙悟空72变万变不离其宗全国化学中考考点扫描适合教师和学生考点54实验型推断题.docx》由会员分享,可在线阅读,更多相关《孙悟空72变万变不离其宗全国化学中考考点扫描适合教师和学生考点54实验型推断题.docx(22页珍藏版)》请在冰豆网上搜索。
孙悟空72变万变不离其宗全国化学中考考点扫描适合教师和学生考点54实验型推断题
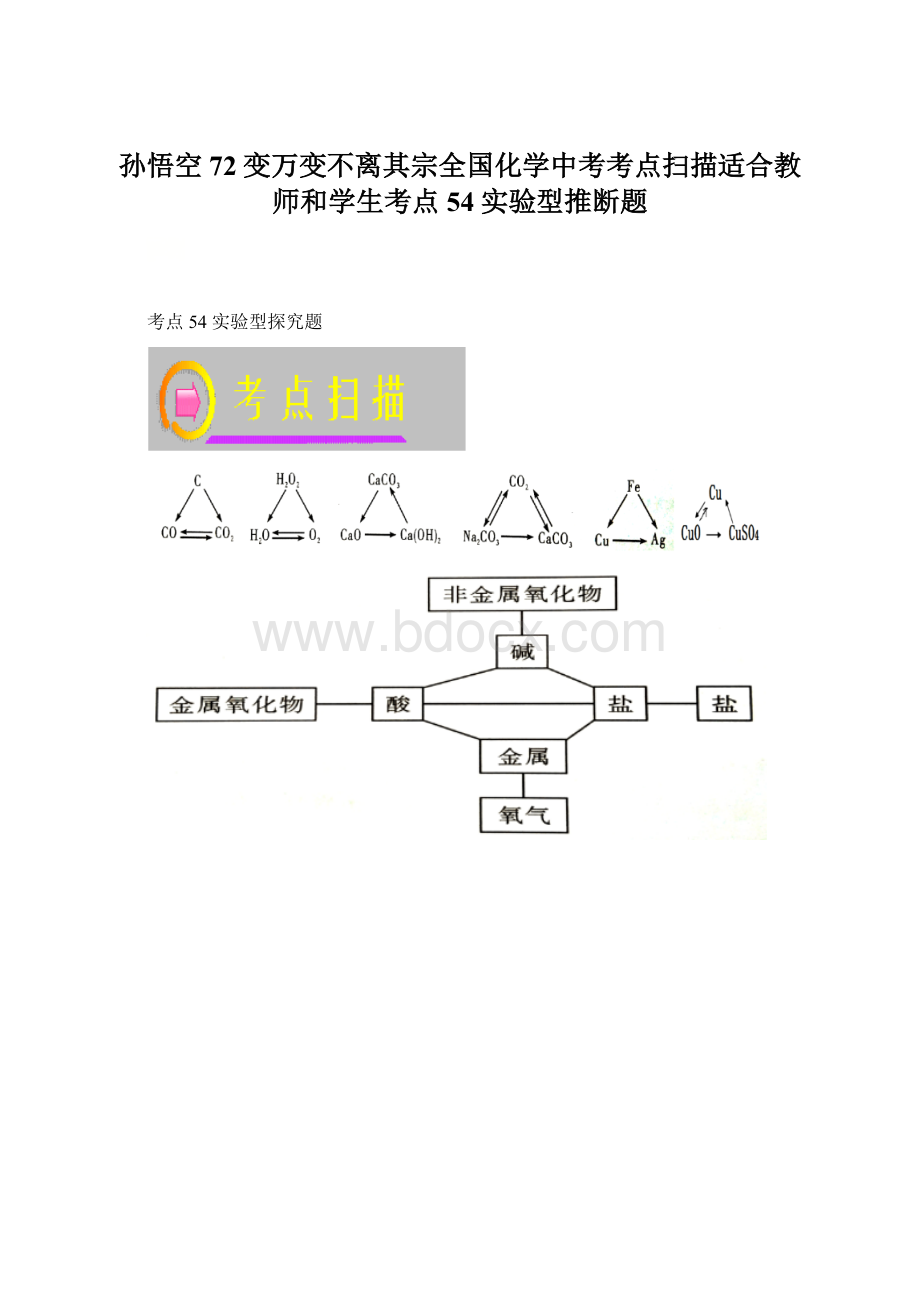
考点54实验型探究题
例(2018•柳州)一瓶不纯的Na2CO3粉末,所含杂质可能是KNO3、Ca(NO3)2、NaCl、CuSO4、K2CO3中的一种或几种。
为确定其成分,进行了如下实验:
(1)取少量该粉末置于烧杯中,加入适量蒸馏水,充分搅拌,得到无色溶液;
(2)取少许上述无色溶液置于两支试管中,分别加入AgNO3溶液和BaCl2溶液,再分别滴加稀硝酸。
现象如下表:
试管编号
现象
1
滴加AgNO3溶液,生成白色沉淀,再滴加稀硝酸,白色沉淀部分溶解
2
滴加BaCl2溶液,生成白色沉淀,再滴加稀硝酸,白色沉淀全部溶解
下列关于该粉末组成的说法中,不正确的是( )
A.杂质可能含KNO3、K2CO3
B.杂质一定含NaCl,可能含Ca(NO3)2
C.杂质一定不含Ca(NO3)2,可能含KNO3
D.杂质一定含NaCl,一定不含CuSO4
【解答】硫酸铜在溶液中显蓝色,碳酸根离子和钡离子反应生成溶于酸的碳酸钡沉淀,氯离子和银离子反应生成不溶于酸的氯化银沉淀,碳酸根离子就饿钙离子反应生成溶于酸的碳酸钙沉淀,所以
取少量该粉末置于烧杯中,加入适量蒸馏水,充分搅拌,得到无色溶液,所以样品中一定不含硫酸铜、硝酸钙;
取少许上述无色溶液置于两支试管中,滴加AgNO3溶液,生成白色沉淀,再滴加稀硝酸,白色沉淀部分溶解,所以样品中一定含氯化钠;
滴加BaCl2溶液,生成白色沉淀,再滴加稀硝酸,白色沉淀全部溶解,所以样品中可能含有碳酸钾、硝酸钾,所以
样品中一定含有氯化钠,一定不含硝酸钙、硫酸铜,可能含有碳酸钾、硝酸钾,【答案】B
1.(2018•湘西)为了给三瓶失去标签的无色溶液Na2CO3、CaCl2、稀HCl贴上正确的标签,某同学首先给三瓶失去标签的无色溶液编号为A、B、C,然后用滴管分别取少量A、B、C两两混合后产生如下现象:
(1)A与B混合无明显现象;
(2)A与C混合后产生白色沉淀(3)B与C混合后,产生气泡。
由此某同学推断出A、B、C正确的顺序是( )
A.Na2CO3、CaCl2、稀HClB.CaCl2、Na2CO3、稀HCl
C.CaCl2、稀HCl、Na2CO3D.稀HCl、CaCl2、Na2CO3
【解答】由题意,
(1)A与B混合无明显现象;
(2)A与C混合后产生白色沉淀(3)B与C混合后,产生气泡,稀盐酸与碳酸钠溶液反应生成二氧化碳气体,碳酸钠与氯化钙溶液反应生成碳酸钙白色沉淀,氯化钙溶液与稀盐酸不反应,则C为碳酸钠溶液,B为稀盐酸,A为氯化钙溶液。
故选:
B。
2.(2018·齐齐哈尔)有一包不纯的碳酸钾粉末,所含杂质可能是硝酸钾、硝酸钙、氯化钾、氯化亚铁、碳酸钠中的一种或几种。
为确定其成分,进行如下实验:
(1)取少量该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。
向该溶液中加入适量的硝酸银溶液,有白色沉淀产生,再加入足量的稀硝酸,充分反应后,部分白色沉淀消失。
(2)另取13.8g该粉末于烧杯中,加水使其完全溶解,再加入200g一定溶质质量分数的氯化钡溶液,恰好完全反应,生成19.7g白色沉淀。
(资料:
稀硝酸与碳酸盐能发生复分解反应,稀硝酸与氯化银不反应)
下列说法正确的是
A.杂质中一定不含有氯化亚铁
B.杂质中一定含有氯化钾,可能含有硝酸钾、碳酸钠
C.该包粉末的组成只有两种情况
D.所用氯化钡溶液中溶质的质量分数为20.8%
【答案】AC
【解析】
(1)取少量该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。
说明不含氯化亚铁和硝酸钙;向该溶液中加入适量的硝酸银溶液,有白色沉淀产生,再加入足量的稀硝酸,充分反应后,部分白色沉淀消失。
说明溶液中含有氯化钾;
(2)
K2CO3+BaCl2=BaCO3↓+2KClNa2CO3+BaCl2=BaCO3↓+2NaCl
138197106197
13.8g19.7g10.6g19.7g
由上面的对应关系可知,纯净的碳酸钠13.8g与氯化钡溶液反应生成19.7g的碳酸钡沉淀,而该粉末中含有氯化钾,故碳酸钠的质量小于13.8g;等质量的碳酸钾、碳酸钠与足量的氯化钡溶液反应,碳酸钠生成碳酸钡的质量多。
另取13.8g该粉末于烧杯中,加水使其完全溶解,再加入200g一定溶质质量分数的氯化钡溶液,恰好完全反应,生成19.7g白色沉淀。
说明粉末中一定含有碳酸钠。
A、由分析可知,杂质中一定不含有氯化亚铁,正确;B、杂质中一定含有氯化钾、碳酸钠,可能含有硝酸钾,错误;C、该包粉末的组成可能是碳酸钾、氯化钾、碳酸钠及碳酸钾、氯化钾、碳酸钠、硝酸钾,共两种情况,正确;D、设所用氯化钡溶液中溶质的质量为x。
K2CO3+BaCl2=BaCO3↓+2KCl
208197
x19.7g
x=20.8g
所用氯化钡溶液中溶质的质量分数为
×100%=10.4%,错误。
故选AC。
3.(2018•青岛)一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、硝酸钙、氯化铜、碳酸钠中的一种或几种。
为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取14.9g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是( )
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钙、氯化铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
【解析】A、氯化钾、氯化钠和硝酸银反应的化学方程式及其质量关系为:
KCl+AgNO3═AgCl↓+KNO3,
74.5143.5
14.9g28.7g
NaCl+AgNO3═AgCl↓+NaNO3,
58.5143.5
11.7g28.7g
取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成,是因为碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠,因此杂质中含有碳酸钠,由计算可知,14.9g氯化钾和硝酸银反应生成28.7g氯化银,11.7g氯化钠和硝酸银反应生成28.7g氯化银,杂质中含有碳酸钠,氯化钾质量小于14.9g,和硝酸银反应生成氯化银质量小于28.7g,因此杂质中一定含有氯化钠,该选项说法不正确;
B、取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成,是因为碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠,因此杂质中含有碳酸钠,则杂质中不含有硝酸钙,加蒸馏水,充分搅拌,得无色澄清溶液,说明杂质中不含有氯化铜,该选项说法不正确;
C、杂质中肯定含有碳酸钠,不含有氯化钠,该选项说法不正确;
D、杂质中肯定含有氯化钠、碳酸钠,由于硝酸钾是否存在不影响实验结果,因此可能含有硝酸钾,也可能不含有硝酸钾,该选项说法正确。
【答案】D
4.(2018·荆州)实验室有四瓶失去标签的无色溶液,分别是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐酸中的一种。
为了鉴别它们,将上述溶液分别标记为甲、乙、丙、丁,做如下实验:
各取少许,将甲分别滴加到另外三种溶液中,观察到乙和丁中产生白色沉淀,丙中无明显现象。
据此可判断甲是( )
A.碳酸钠溶液B.氯化钡溶液C.硫酸钠溶液D.稀盐酸
【解析】根据题意,各取少许,将甲分别滴加到另外三种溶液中,观察到乙和丁中产生白色沉淀,丙中无明显现象。
A、碳酸钠只能与氯化钡溶液反应生成碳酸钡白色沉淀,故选项错误。
B、氯化钡溶液与碳酸钠溶液、硫酸钠溶液反应,分别生成碳酸钡、硫酸钡白色沉淀,与稀盐酸不反应,无明显变化,则甲是氯化钡,故选项正确。
C、硫酸钠溶液只能与氯化钡溶液反应生成硫酸钡白色沉淀,故选项错误。
D、稀盐酸与另外三种溶液混合,均没有沉淀生成,故选项错误。
故选:
B。
5.(2018·天津)某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及到的反应均为初中化学常见的反应,且各步均恰好完全反应)。
下列说法中正确的是
A.溶液N中只含一种溶质
B.原固体粉末中可能含有碳酸钙
C.白色沉淀Y一定是碳酸钙,气体W一定是氢气
D.原固体粉末中一定没有氧化铜,一定含有碳酸钙
【答案】BC
【解析】能使澄清石灰水变浑浊的气体是二氧化碳,所以X是CO2,二氧化碳与澄清石灰水反应生成碳酸钙,Y是CaCO3,则固体粉末中含有碳酸钙;N是浅绿色溶液,N中含有Fe2+,固体粉末中含有氧化铁、木炭粉,3C+2Fe2O3
4Fe+3CO2↑,Fe+2HCl==FeCl2+H2↑,涉及到的反应还有CaO++2HCl==CaCl2+H2O。
A.溶液N中含FeCl2、CaCl2两种溶质,错误;B.原固体粉末中一定含有碳酸钙,错误;C.白色沉淀Y一定是碳酸钙,气体W一定是氢气,正确;D.CuO+2HCl==CuCl2+H2O,含铜离子的溶液是蓝色,所以原固体粉末中一定没有氧化铜,一定含有碳酸钙,正确。
故选BC。
6.(2018•贵阳)实验室有一包白色固体,其中除了碳酸钠以外,还可能含有硝酸钡、硫酸钠、氢氧化钠中的一种或几种。
步骤①:
取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解。
步骤②:
接着向烧杯中加入足量稀硝酸并不断搅拌,此时固体质量变化如图。
下列说法正确的是( )
A.A→B段对应的实验现象是固体部分溶解,无气泡冒出
B.B→C段对应溶液pH逐渐变大
C.C点对应溶液中一定含有的溶质是硝酸、硝酸钠、硝酸钡
D.原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡、氢氧化钠
【解析】碳酸钠和硝酸钡反应生成溶于酸的碳酸钡沉淀,硫酸钠和硝酸钡反应生成不溶于酸的硫酸钡沉淀,所以
步骤①:
取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解,
步骤②:
接着向烧杯中加入足量稀硝酸并不断搅拌,所以固体中含有碳酸钠、硫酸钠、硝酸钠
A、A→B段对应的反应是碳酸钡和硝酸反应生成硝酸钠、水和二氧化碳,实验现象是固体部分溶解,有气泡冒出,故A错误;
B、B→C段对应溶液pH逐渐变小,故B错误;
C、C点对应溶液中一定含有的溶质是硝酸、硝酸钠、硝酸钡,故C正确;
D、原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡,可能含有氢氧化钠,故D错误。
故选:
C。
7.(2018•曲靖)某溶液中可能含有碳酸钾、硫酸钾中的一种或两种溶质,为测定其成分,进行如下实验:
取一定量溶液于烧杯中,先加入过量氯化钡溶液,再加入稀硝酸,反应过程及产生沉淀的质量与所加溶液质量的关系如图所示。
下列说法中正确的个数有( )
①该溶液中一定含有碳酸钾和硫酸钾
②反应进行到a点时,溶液中只含有一种溶质
③bc段上的任意一点(c点除外)都存在两种沉淀
④反应进行到c点时,溶液中只含有两种溶质
A.1个B.2个C.3个D.4个
【解析】①由图中信息可知,加入稀硝酸后沉淀部分溶解,说明沉淀是碳酸钡和硫酸钡的混合物,因此该溶液中一定含有碳酸钾和硫酸钾,该选项说法正确;
②反应进行到a点时,碳酸钾、硫酸钾恰好和氯化钡完全反应,溶液中只含有一种溶质﹣﹣氯化钾,该选项说法正确;
③bc段上的任意一点(c点除外)都存在两种沉淀,即碳酸钡和硫酸钡,该选项说法正确;
④反应进行到c点时,溶液中只含有一种溶质﹣﹣氯化钡,该选项说法不正确。
故选:
C。
8.(2018•南充)实验室有一包白色固体由K2CO3、K2SO4、KCl和CuSO4中的一种或几种组成,实验记录如下:
①取该样品溶于水,得到无色溶液;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀过滤;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并产生气泡。
下列分析中正确的是( )
A.原固体中一定含有K2CO3,可能含有CuSO4和KCl
B.原固体中一定不含K2SO4和CuSO4、可能含有KCl
C.原固体中一定含有K2CO3和K2SO4,一定不含CuSO4
D.若在步骤②所得滤液中滴入AgNO3溶液,出现白色沉淀,则原固体中一定含有KCl
【解析】①取该样品溶于水,得到无色溶液;由于硫酸铜溶液是蓝色的,故一定不会含有硫酸铜;
②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀过滤;碳酸钾和硫酸钾都能与氯化钡反应产生白色沉淀;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并产生气泡,说明一定含有碳酸钡沉淀,则一定含有碳酸钾;一定不含有硫酸钡沉淀,则一定不含有硫酸钾;氯化钾可能存在;
A、原固体中一定含有K2CO3,可能含有CuSO4和KCl,一定不含有硫酸铜,错误;
B、原固体中一定不含K2SO4和CuSO4、可能含有KCl,正确;
C、原固体中一定含有碳酸钾,一定不含有硫酸钾和硫酸铜,错误;
D、由于步骤②加入的是氯化钡,故加入硝酸银产生白色沉淀不能说明含有氯化钾,错误;
【答案】B
9.(2018·随州)有一包固体,可能是Cu(NO3)2、K2SO4、KCl、K2CO3、KOH中的一种或几种组成。
为了探究该固体的组成,某化学小组设计并开展以下实验:
已知,步骤I中固体全部消失,溶液呈蓝色,无气泡产生,步骤II、III中均可观察到有白色沉淀生成。
请回答下列问题:
(1)经推论,原固体中一定不含K2CO3,理由是___________________
(2)原固体中一定含有的物质是________________。
(3)步骤II中产生白色沉淀的化学方程式是_______________。
(4)步骤III所得蓝色滤液中一定含有的阳离子是____________。
【答案】
(1).向固体中加入过量的稀盐酸时,无气泡产生
(2).Cu(NO3)2、K2SO4 (3).Ba(NO3)2+ K2SO4=BaSO4↓+2KNO3(4). Cu2+、K+、H+
【解析】本题是推断题。
首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可。
解题时注意加入试剂的量对反应后溶液成分的影响。
(1)碳酸钾与盐酸反应生成氯化钾、水和二氧化碳。
原固体中一定不含K2CO3,理由是向固体中加入过量的稀盐酸时,无气泡产生;
(2)固体加过量稀盐酸,固体完全溶解且溶液呈蓝色,说明固体中一定有硝酸铜,硝酸铜与氢氧化钾能发生反应不能共存,则说明一定不存在氢氧化钾,根据题
(1)的分析固体中一定不含K2CO3,在步骤Ⅰ得到的蓝色溶液中加入硝酸钡溶液有白色沉淀生成,硫酸钾与硝酸钡反应生成硫酸钡沉淀和硝酸钾,说明固体中一定有硫酸钾,在步骤Ⅱ得到的蓝色溶液中加入硝酸银溶液产生白色沉淀,含氯离子的溶液与硝酸银反应生成氯化银的沉淀,由于在步骤Ⅰ中加入了盐酸,不能说明固体中一定有氯化钾,所以原固体中一定含有的物质是Cu(NO3)2、K2SO4 ;
(3)步骤II中产生白色沉淀的反应是硫酸钾与硝酸钡反应生成硫酸钡沉淀和硝酸钾,化学方程式是Ba(NO3)2+ K2SO4=BaSO4↓+2KNO3;
(4)根据题
(2)中的分析可知,步骤III所得蓝色滤液中一定含有的阳离子是 Cu2+、K+、H+ 。
10.(2018•仙桃)有一种纳米材料添加剂,由铝粉、氧化铝粉末、铜粉中的一种或几种组成,为探究该添加剂的成分,化学学习小组进行了下列实验,请回答实验中的相关问题:
(1)取适量添加剂于试管中,加入足量稀盐酸,有红色固体残留并产生大量气泡,该现象说明添加剂中一定含有 铝粉、铜粉 。
(2)另取适量添加剂于另一试管中,加入一定量的硝酸银溶液,充分反应,过滤,得到滤渣和蓝色溶液。
则生成蓝色溶液的化学方程式为 Cu+2AgNO3=Cu(NO3)2+2Ag 。
蓝色溶液中一定含有的两种溶质是 硝酸铜、硝酸铝 。
(3)取
(2)中的滤渣于试管中, 加入足量稀盐酸,滤渣溶解 ,说明该添加剂中含有氧化铝粉末。
【解析】
(1)取适量添加剂于试管中,加入足量稀盐酸,有红色固体残留,说明添加剂中含有铜,并产生大量气泡,说明添加剂中含有铝,因此添加剂中一定含有铝粉、铜粉。
故填:
铝粉、铜粉。
(2)另取适量添加剂于另一试管中,加入一定量的硝酸银溶液,充分反应,过滤,得到蓝色溶液,说明铝完全反应后,铜和硝酸银反应生成了硝酸铜和银,则生成蓝色溶液的化学方程式为:
Cu+2AgNO3=Cu(NO3)2+2Ag;
蓝色溶液中一定含有的两种溶质是硝酸银和铜反应生成的硝酸铜与铝和硝酸银反应生成的硝酸铝。
故填:
Cu+2AgNO3=Cu(NO3)2+2Ag;硝酸铜、硝酸铝。
(3)取
(2)中的滤渣于试管中,加入足量稀盐酸,滤渣溶解,是因为氧化铝和稀盐酸反应生成了氯化铝和水,说明该添加剂中含有氧化铝粉末。
故填:
加入足量稀盐酸,滤渣溶解。
11.(2018·长沙)我市教育主管部门为了让同学们过好传统佳节——端午节,特意将中考提前一天。
化学兴趣小组的同学们为庆祝端午佳节,决定自己动手制作传统食品一一皮蛋。
制作皮蛋料泥的原料主要有:
生石灰、纯碱、草木灰(含K2CO3)等,将他们按一定比例混合加入适量水得到皮蛋料泥。
料泥的主要成分是什么呢?
同学们进行了如图所示的探究:
(1)步骤②的操作所需的玻璃仪器有:
烧杯、玻璃棒、____________________;
(2)步骤③的现象说明滤渣中一定含有的物质为:
____________________;
(3)由上述实验现象推断,滤液中的溶质一定含有:
____________________;
【答案】
(1)漏斗
(2)碳酸钙(或CaCO3)(3)NaOH、Ca(OH)2、KOH(或氢氧化钠、氢氧化钙、氢氧化钾)
【解析】本题考查了实验探究物质的组成成分;过滤所用的仪器,生石灰的性质,碳酸盐的检验等。
根据问题情景,找到实验的反应原理;再根据实验的反应原理,分析推断出该物质的组成成分。
(1)步骤②的主要操作是过滤,过滤所需的玻璃仪器有:
烧杯、玻璃棒、漏斗;
(2)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾。
步骤③滴加盐酸观察到有气泡产生,滤渣中含碳酸盐,可判断滤渣中一定含有物质是碳酸钙(或CaCO3);
(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾。
步骤④向滤液中加入酚酞,溶液变红色,说明滤液中存在氢氧根离子;步骤⑤向滤液中滴加盐酸无气体产生,说明滤液中没有碳酸盐;步骤⑥向滤液中通入二氧化碳出现白色沉淀,说明滤液中含有氢氧化钙,滤液中的溶质一定含有NaOH、Ca(OH)2、KOH(或氢氧化钠、氢氧化钙、氢氧化钾)。
12.(2018•绥化)某溶液中可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,取一定质量的该溶液,向其中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。
请回答下列问题。
(1)该溶液中一定含有的溶质是 HCl、CuCl2 ,可能含有的溶质是 NaNO3 。
(均填化学式)
(2)请写出上述过程中发生中和反应的化学方程式 2HCl+Ba(OH)2═BaCl2+2H2O 。
(3)当滴加氢氧化钡溶液至图中b点时,溶液中一定含有的溶质是 BaCl2 。
(填化学式)
(4)所取溶液中含有氯化铜的质量为 13.5g 。
【解析】沉淀开始时没有产生,说明原溶液中有酸,因为硫酸与氢氧化钡反应生成硫酸钡白色沉淀,硫酸钡不溶于三大强酸,因此有盐酸,没有硫酸;氯化铜与氢氧化钡能产生氢氧化铜蓝色沉淀,并且符合题意,因此一定有氯化铜,而硝酸钠不能确定;
(1)该溶液中一定含有的溶质是盐酸和氯化铜,可能含有的溶质是硝酸钠,故填:
HCl、CuCl2;NaNO3;
(2)盐酸和氢氧化钡反应生成氯化钡和水,故填:
2HCl+Ba(OH)2═BaCl2+2H2O;
(3)到达b点,则盐酸和氯化铜全部反应完,生成的是氯化钡,故填:
BaCl2;
(4)生成氢氧化铜沉淀的质量为9.8g,设氯化铜的质量为x
Ba(OH)2+CuCl2═Cu(OH)2↓+BaCl2
13598
x9.8g
x=13.5g
故填:
13.5g。
13.(2018•武汉)有一包固体粉末,可能含碳、铝、铜、氧化铝、氧化铜中的一种或几种。
为探究该固体粉末的组成,某化学兴趣小组进行了如图所示实验:
(1)向样品中加入过量稀盐酸产生的气体是 氢气 。
(2)向固体A中加入硝酸银溶液,发生反应的化学方程式为 Cu+2AgNO3=2Ag+Cu(NO3)2 。
(3)固体B中含有的物质是 碳、银 。
(4)原固体样品中一定含有的物质是 碳、铝 。
(5)蓝色溶液丙中一定含有的溶质是 硝酸铝、硝酸铜和硝酸 。
【解析】
(1)向样品中加入过量稀盐酸产生的气体是氢气,故答案为:
氢气;
(2)铜和硝酸银反应生成银和硝酸铜,配平即可;故答案为:
Cu+2AgNO3=2Ag+Cu(NO3)2;
(3)固液混合物过滤后,固体A中加入硝酸银溶液,生成蓝色溶液乙,铜和硝酸银反应生成银和硝酸铜,得到固体B,B在氧气中灼烧生成二氧化碳,说明固体A中一定有铜、碳,B中一定有碳和银;故答案为:
碳、银;
(4)样品中加入过量的盐酸,有气体产生,说明样品中一定有铝;固液混合物过滤后,固体A中加入硝酸银溶液,生成蓝色溶液乙,铜和硝酸银反应生成银和硝酸铜,得到固体B,B在氧气中灼烧生成二氧化碳,说明固体A中一定有铜、碳,B中一定有碳和银;因此原固体样品中一定含有的物质是碳和铝;故答案为:
碳、铝;
(5)蓝色溶液丙中一定含有的溶质是:
硝酸铝、硝酸铜和硝酸,因为盐酸和硝酸银反应生成氯化银白色沉淀和硝酸;故答案为:
硝酸铝、硝酸铜和硝酸;
14.(2018•滨州)某固体物质可能含有氯化钾、硫酸铜、氢氧化钠、硝酸镁,硫酸钠中的一种或几种,为鉴定它们,做如下实验:
(1)将该固体物质全部溶解于水中,得到无色溶液a。
(2)取少量a溶液于试管中,向其中滴加少量硫酸铁溶液,产生红褐色沉淀。
(3)另取少量a溶液于试管中,向其中滴加少量的硝酸钡溶液,产生白色沉淀。
据此推断,该固体物质中一定含有(以下写化学式,下同) ,一定不含有 ,可能含有 。
请写出步骤
(2)中发生反应的化学方程式 ,步骤(3)中发生反应的化学方程式 。
【解析】
(1)将该固体物质全部溶解于水中,得到无色溶液a,由于硫酸铜溶液是蓝色的,一定不会含有硫酸铜;氢氧化钠能与硝酸镁反应产生白色沉淀,氢氧化钠和硝酸镁不会同时存在;
(2)取少量a溶液于试管中,向其中滴加少量硫酸铁溶液,产生红褐色沉淀,说明含有氢氧化钠,一定不会含有硝酸镁;(3)另取少量a溶液于试管中,向其中滴加少量的硝酸钡溶液,产生白色沉淀,说明含有硫酸钠,氯化钾不能确定是否存在;该固体中一定存在氢氧化钠和硫酸钠,一定不存在硫酸铜和硝酸镁,可能含有氯化钾,步骤
(2)中氢氧化钠和硫酸铁反应生成氢氧化铁沉淀和硫酸钠,步骤(3)中硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠。
【答案】NaOH、Na2SO4;CuSO4、Mg(NO3)2;KCl;6NaOH+Fe2(SO4)3═2Fe(OH)3↓+3Na2SO4;Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3
15.(2018·巴中)某固体粉末可能含有碳酸钙,硫酸钠,氧化钡,硫酸铜中的一种或几种。
为确定该固体粉末的成分,进行如下实验:
回答下列问题:
(1)反应I的化学方程式
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 悟空 72 万变不离其宗 全国 化学 中考 考点 扫描 适合 教师 学生 54 实验 推断
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
