 备战中考化学科普阅读题综合题汇编附答案.docx
备战中考化学科普阅读题综合题汇编附答案.docx
- 文档编号:5919358
- 上传时间:2023-01-02
- 格式:DOCX
- 页数:13
- 大小:201.65KB
备战中考化学科普阅读题综合题汇编附答案.docx
《备战中考化学科普阅读题综合题汇编附答案.docx》由会员分享,可在线阅读,更多相关《备战中考化学科普阅读题综合题汇编附答案.docx(13页珍藏版)》请在冰豆网上搜索。
备战中考化学科普阅读题综合题汇编附答案
一、中考初中化学科普阅读题
1.阅读下面科普短文。
鸡蛋营养价值很高,一个重约50g的鸡蛋,约含7g蛋白质。
蛋黄中富含卵磷脂,卵磷脂可以阻止胆固醇和脂肪在血管壁上沉积,被称为“血管清道夫”。
一般人群每天吃1~2个鸡蛋不会造成血管硬化,但多吃会增加肝、肾负担。
鸡蛋不宜生食,也不建议吃溏心鸡蛋。
因为生鸡蛋中含有抗营养因素,会影响营养素的利用,还可能被沙门氏菌污染。
烹调鸡蛋达到70~80℃才能杀灭沙门氏菌,当蛋黄凝固时说明温度已接近。
所以最好是蛋黄刚凝固时起锅,烹调时间过长会降低鸡蛋的营养价值。
市售鸡蛋常采用三种涂膜保鲜技术,分别是:
A-聚乙烯醇溶液涂膜、B-聚乙烯醇和双乙酸钠溶液涂膜、C-聚乙烯醇和氢氧化钙溶液涂膜。
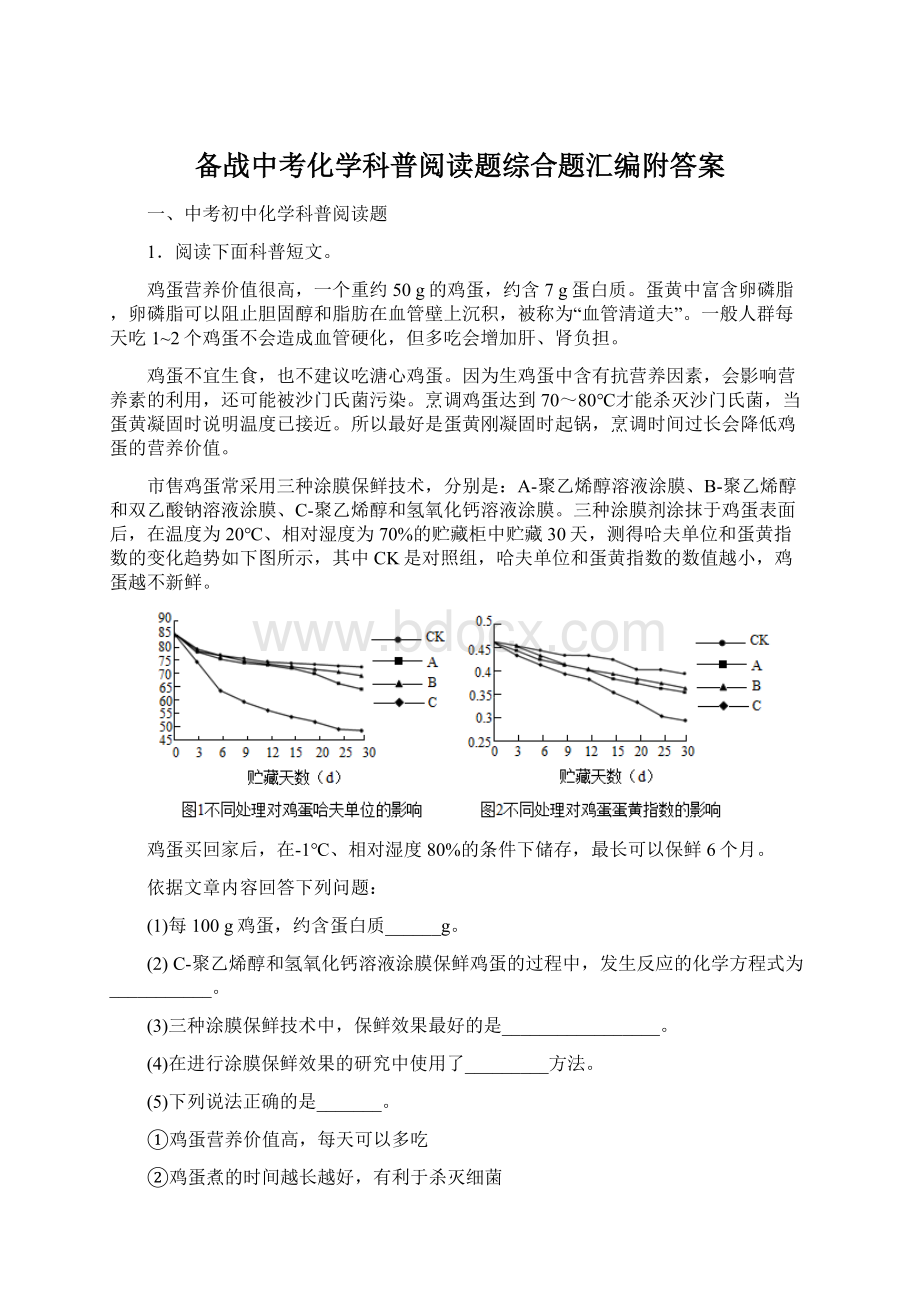
三种涂膜剂涂抹于鸡蛋表面后,在温度为20℃、相对湿度为70%的贮藏柜中贮藏30天,测得哈夫单位和蛋黄指数的变化趋势如下图所示,其中CK是对照组,哈夫单位和蛋黄指数的数值越小,鸡蛋越不新鲜。
鸡蛋买回家后,在-1℃、相对湿度80%的条件下储存,最长可以保鲜6个月。
依据文章内容回答下列问题:
(1)每100g鸡蛋,约含蛋白质______g。
(2)C-聚乙烯醇和氢氧化钙溶液涂膜保鲜鸡蛋的过程中,发生反应的化学方程式为___________。
(3)三种涂膜保鲜技术中,保鲜效果最好的是_________________。
(4)在进行涂膜保鲜效果的研究中使用了_________方法。
(5)下列说法正确的是_______。
①鸡蛋营养价值高,每天可以多吃
②鸡蛋煮的时间越长越好,有利于杀灭细菌
③生吃鸡蛋、吃溏心蛋和不吃蛋黄,是不科学的做法
【答案】14Ca(OH)2+CO2=CaCO3↓+H2OC—聚乙烯醇和氢氧化钙溶液涂膜对比实验③
【解析】
(1)每100g鸡蛋,约含蛋白质=
7=14g;
(2)用C-聚乙烯醇和氢氧化钙溶液涂膜保鲜鸡蛋的过程中,二氧化碳和氢氧化钙反应生成碳酸钙和水,反应的化学方程式为:
Ca(OH)2+CO2=CaCO3↓+H2O;(3)哈夫单位和蛋黄指数的数值越小,鸡蛋越不新鲜,分析两幅图可知,三种涂膜保鲜技术中,保鲜效果最好的是:
C—聚乙烯醇和氢氧化钙溶液涂膜;(4)在进行涂膜保鲜效果的研究中使用了三种方法,利用了对比实验法;(5)①鸡蛋营养价值高,一般人群每天吃1~2个鸡蛋不会造成血管硬化,但多吃会增加肝、肾负担,故错误,②鸡蛋煮的时间越长越好,有利于杀灭细菌,烹调时间过长会降低鸡蛋的营养价值,故错误,③鸡蛋不宜生食,也不建议吃溏心鸡蛋;因为生鸡蛋中含有抗营养因素,会影响营养素的利用,还可能被沙门氏菌污染,故正确。
2.阅读短文并回答问题。
白炽灯泡
白炽灯泡的灯丝是由金属钨制作的,其灯丝发光时温度可达2000℃左右,为防止灯丝在高温下氧化,在制作灯泡时要抽真空,在制作大功率灯泡时,还要把灯泡内充入稀有气体氩等,主要是为了防止灯丝在高温下升华。
白炽灯泡工作时,电能转化为光能的效率较低,因此逐渐被节能灯和LED灯所替代。
(1)由于钨的_____较高,所以用钨制作灯丝;
(2)灯泡内充入稀有气体氦等,主要是为了_____;
(3)白炽灯泡逐渐退出市场,是由于_____。
【答案】熔点做保护气,使灯泡耐用白炽灯泡工作时,电能转化为光能的效率较低,浪费能源
【解析】
【详解】
(1)金属钨的熔点高,所以可以用来制灯丝;故填:
熔点;
(2)稀有气体化学性质稳定,可以用作保护气,使灯泡耐用,题干信息中把灯泡内充入稀有气体氩等,主要是为了防止灯丝在高温下升华故填:
做保护气,使灯泡耐用;
(3)白炽灯泡工作时,电能转化为光能的效率较低,浪费能源,因此逐渐被节能灯和LED灯所替代;故填:
白炽灯泡工作时,电能转化为光能的效率较低,浪费能源。
故答案为
(1)熔点;
(2)做保护气,使灯泡耐用;(3)白炽灯泡工作时,电能转化为光能的效率较低,浪费能源。
3.可燃冰是在低温和高压条件下形成。
可燃冰外观像冰,主要含有甲烷水合物,其组成可表示为CH4·nH2O,还含少量二氧化碳等气体。
可燃冰具有能量高、燃烧值大等优点。
2017年5月,中国首次海域天然气水合物(可燃冰)试采成功,成为全球第一个稳定开采可燃冰的国家。
可燃冰开采困难重重,原因之一是可然冰极不稳定易爆炸,当甲烷气体涌入大气层,会产生比二氧化碳更为严重的温室效应。
置换法是开采方法之一,将CO2液化后进入1500米以下的洋面,就会生成二氧化碳水合物沉入海底,因CO2较甲烷易于形成水合物,因而就可能将甲烷水合物中的甲烷分子置换出来。
(1)一个甲烷分子中含有____个原子。
32g甲烷完全燃烧后可以生成___g二氧化碳。
(2)下列有关说法正确的是__。
A可燃冰的开采不存在任何困难
B可燃冰是一种前景广阔的燃料
C能产生温室效应的气体除二氧化碳外,还有甲烷等气体
(3)某种可燃冰的组成为CH4·nH2O,其中CH4与H2O的质量比是1:
9,则该可燃冰中n=__。
(4)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,其产物是一种单质和一种氧化物,都有可燃性,请写出该反应的化学方程式____。
【答案】588BC8CH4+CO2
2CO+2H2
【解析】
【分析】
可燃冰外观像冰,主要含有甲烷水合物,还含少量二氧化碳等气体,甲烷完全燃烧后可以生成二氧化碳和水,甲烷为清洁燃料,可然冰极不稳定易爆炸,当甲烷气体涌入大气层,会产生比二氧化碳更为严重的温室效应。
【详解】
(1)甲烷的化学式为
一个甲烷分子中含有5个原子,
设32g甲烷完全燃烧后可以生成二氧化碳质量为x.
x=88g
故32g甲烷完全燃烧后可以生成88g二氧化碳。
(2)可燃冰是一种前景广阔的燃料,燃烧产生二氧化碳和水,是清洁燃料,甲烷燃烧产生二氧化碳,过多的燃烧会引起温室效应,能产生温室效应的气体除二氧化碳外,还有甲烷等气体,故选B。
(3)某种可燃冰的组成为CH4·nH2O,其中CH4与H2O的质量比是1:
9,则16:
18n=1:
9,所以n=8。
(4)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,其产物是一种单质和一种氧化物,都有可燃性,根据元素守恒推测生成物是一氧化碳和氢气,反应的化学方程式为CH4+CO2
2CO+2H2。
【点睛】
甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,其产物是一种单质和一种氧化物,都有可燃性,会正确书写化学方程式,根据化学方程式进行计算。
4.阅读下面科普短文。
水果不仅带给我们味觉上的享受,更能提供丰富的营养。
但是水果的保存也会给我们带来小小的烦恼,保存不当,水果会失水或腐烂变质。
在水果的冰点温度下储藏,能较长时间保持鲜果固有的品质和营养,这项技术叫冰温储藏。
为了探究荔枝的冰温储藏(荔枝的冰点温度为﹣1.2℃)是否优于普通冷藏(温度通常为0~10℃)。
科研人员设计了一组实验,实验条件如表1所示。
以荔枝的还原糖含量作为衡量荔枝品质变化的指标(还原糖含量越高,品质越好),每隔七天进行一次水果品质检测,实验结果见图1。
如表实验条件
组号
储藏温度
湿度
备注
1
﹣1.2℃
87%
荔枝的品种、大小、成熟度、数量以及其他条件均相同且适宜
2
3℃
87%
氧气的浓度也影响着水果的保鲜。
在储存水果时为了抑制呼吸作用,一般要降低氧气的浓度,当二氧化碳释放量最小时,呼吸作用最弱,此时对应的氧气浓度适宜水果的储存。
如果降得太低,植物组织就进行无氧呼吸,无氧呼吸的产物往往对细胞有一定的毒害作用,影响水果的保鲜。
此外,储存时还要注意有些水果不能和其他蔬果一起存放,如苹果、木瓜、香蕉等。
这类水果在成熟过程中会释放“乙烯”气体,可加速水果的成熟和老化。
腐烂的水果也会释放乙烯,因此在一堆水果中,如果有一颗是腐烂的,要尽快挑出去。
依据文章内容,回答下列问题。
(1)乙烯_____(填“能”或“不能”)催熟水果。
(2)在文中的荔枝实验中,研究的影响水果储藏的因素是_____。
(3)通过如图可得到的信息是_____(写出1条即可)。
(4)下列说法不正确的是_____。
A普通冷藏温度指的是3℃
B氧气浓度越低越有利于水果的保鲜
C荔枝的还原糖含量在冰温储藏时始终高于普通储藏
(5)请举出日常生活中水果保鲜的方法_____(写出1种即可)。
【答案】能储藏温度超过一定天数后,荔枝冰温储藏比普通冷藏保鲜效果要好ABC装入保鲜袋
【解析】
【详解】
(1)这类水果在成熟过程中会释放“乙烯”气体,可加速水果的成熟和老化,所以乙烯能催熟水果。
(2)探究荔枝的冰温储藏(荔枝的冰点温度为﹣1.2℃)是否优于普通冷藏(温度通常为0~10℃)可知研究的影响水果储藏的因素是储藏温度;
(3)由表中数据可知在一定天数后,在冰温储藏还原糖含量高于普通冷藏还原糖含量,所以得到的信息是超过一定天数后,荔枝冰温储藏比普通冷藏保鲜效果要好;
(4)普通冷藏(温度通常为0~10℃),故A说法错误;
氧气浓度降得太低,植物组织就进行无氧呼吸,无氧呼吸的产物往往对细胞有一定的毒害作用,影响蔬菜水果的保鲜,故B说法错误;
由表中数据可知一开始时,冰温储藏还原糖含量低于普通冷藏还原糖含量,在一定天数后,在冰温储藏还原糖含量高于普通冷藏还原糖含量,故C说法错误;
(5)平常水果保鲜用的是装入保鲜袋。
5.阅读下面科普短文。
随着环境意识的提高,人们对室内空气质量越来越关心。
下表列举了室内空气的主要污染物及来源。
污染源
污染物
建筑材料
NH3、甲醛(CH2O)、苯(C6H6)、甲苯(C7H8)、石棉纤维等
家具
甲醛(CH2O)、甲苯(C7H8)等
办公用品
O3、电磁辐射等
烹饪
CO、NO2、SO3、PM10等
室内微生物
结核杆菌、霉菌等
从上表看出室内污染物种类繁多,其中室内甲醛污染已被列入对公众健康影响最大的环境因素之一。
室内空气中的甲醛主要来自于人造板材料制作的家具、地板以及胶黏剂等。
这些材料用的越多,甲醛在室内空气中的浓度越高。
甲醛的释放期非常长,人们打开人造板家具柜门时,闻到的刺激性气味主要是甲醛的气味。
改善室内空气质量的方法有很多。
通常情况下,开窗通风是改善室内空气质量最有效的方法。
运用功能性装饰材料也可以改善室内空气质量。
研究表明硅藻泥也可以净化空气。
硅藻泥的主要成分是硅藻土,是由水生浮游类生物沉积而成。
电子显微镜显示,硅藻土粒子表面具有无数微小的孔穴,功能与活性炭相似。
正是这种多孔的结构,使硅藻泥成为具有净化空气功能的内墙装饰材料。
“光触媒技术”是20世纪70年代发展起来的一门新兴技术。
“光触媒”是一种纳米级材料,具有强烈的催化分解功能。
图一就是“光触媒”技术应用于分解甲醛、氨气、甲苯等有害物质的原理图。
空气净化器是净化室内空气的重要设备。
图二是某品牌空气净化器的净化效果图,其中a、b、c是甲醛随开机时间浓度变化的三条曲线。
为满足人们对健康住宅的需求,提高人们的生活质量,使生活由舒适型向健康型方向发展,人们正在不断优化新的技术。
依据短文内容,回答下列问题:
(1)甲醛(CH2O)属于________(填“无机物”或“有机物”)。
(2)一氧化碳的污染源是________。
(3)下列说法正确的是________(填序号)。
A.甲醛易挥发
b.硅藻泥通过吸附污染物净化了空气
c.吸收、转化、降低室内污染物的浓度都可以改善室内空气质量
(4)“光触媒技术”可将污染物转化为水和二氧化碳,依据图一写出该反应的条件:
________。
(5)依据图二提出一条使用空气净化器的建议:
________。
【答案】有机物烹饪abc光、TiO2工作时间在1~2小时,降低甲醛的浓度效果显著
【解析】
【分析】
本题在“空气净化方法”的情境下考查物质的分类及其获得信息,处理信息的能力。
认真阅读,结合已有的知识进行分析。
【详解】
(1)含碳元素的化合物叫有机物。
甲醛是由碳、氢、氧组成的化合物,甲醛属于有机物;
(2)由表格列举的室内空气的主要污染物及来源可知,一氧化碳的污染源是烹饪;
(3)a、根据题中“室内空气中的甲醛主要来自于人造板材料制作的家具、地板以及胶黏剂等。
这些材料用的越多,甲醛在室内空气中的浓度越高”,可知甲醛易挥发,故a正确;
b、根据题中“研究表明硅藻泥也可以净化空气”和“硅藻土粒子表面具有无数微小的孔穴,功能与活性炭相似”,可知硅藻泥是具有净化空气功能的内墙装饰材料,具有透气、调湿、净化室内空气的功能,故b正确;
c、根据题中通过硅藻泥吸收甲醛能改善室内空气质量,“光触媒技术”可将污染物转化为水和二氧化碳可知吸收、转化、降低室内污染物的浓度都可以改善室内空气质量,故c正确。
故选abc;
(4)根据图一提供的信息可知,“光触媒”技术即用TiO2在光催化剂作用下将甲醛等有害物质转化为二氧化碳和水,降低室内空气污染。
依据图一可知该反应的条件是:
光、TiO2;
(5)从图二中可以看出,室内的甲醛含量在空气净化器工作两小时左右时下降幅度最大,两小时后变化不再明显,所以工作时间在1~2小时,降低甲醛的浓度效果显著。
【点睛】
认真阅读短文,从中找出有用的信息是解题的基础。
6.阅读下面科普短文。
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C等多种营养物质,是餐桌上的美味食材。
表1鲜土豆中主要营养物质的含量(每100g)
蛋白质/g
脂肪/g
淀粉/g
钙/mg
磷/mg
维生素C/mg
1.5-2.3
0.4-0.94
17.5-28.0
11-60
15-68
20-40
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。
用土豆片进行实验,测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:
土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。
除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。
依据文章内容回答下列问题。
(1)表1中的“钙”指的是______________(填“元素”或“原子”)。
(2)由图1可知:
60min内,_________(填序号,下同)。
A浸泡30min比10min脆性分值高
B浸泡10min,硬度、咬碎感均无明显变化
C随着浸泡时间的增加,粘结性、弹性分值均降低
(3)由图2可知:
土豆片的淀粉含量与浸泡时间的关系是_______________________。
(4)変绿、发芽的土豆不宜食用,其原因是___________________________________。
(5)下列说法正确的是_____________。
A土豆是四大粮食作物之一B土豆中维生素C含量最高
C用水泡可防止土豆片褐変D土豆开发应用的前景广阔
【答案】元素ABC在其他条件相同时,在研究范围内,土豆片的淀粉含量随浸泡时间的延长而降低土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒ACD
【解析】
【分析】
【详解】
(1)一般情况下,没有特别说明,表1中“钙”、“磷”是指元素,故此空填写:
元素;
(2)A、由图1可知:
60min内,浸泡30min比10min脆性分值高,故符合题意;
B、浸泡10min,硬度、咬碎感跟0min比,均无明显变化,故符合题意;
C、由图1可知:
60min内,随着浸泡时间的增加,粘结性、弹性分值均降低,故符合题意。
(3)由图2可知,随横坐标数值的增加,曲线的纵坐标在逐渐减少,故填写:
在其他条件相同时,在研究范围内,土豆片的淀粉含量随浸泡时间的延长而降低;
(4)由题干文字可知,変绿、发芽的土豆不宜食用,其原因是土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒;
(5)A、由题干文字可知,土豆是四大粮食作物之一,故符合题意;
B、由表1可知,土豆中维生素C含量不是最高,“磷”和“钙”的含量有可能比它高,故不符合题意;
C、由题干文字可知,用水泡可防止土豆片褐変,故符合题意;
D、由题干文字可知,土豆开发应用的前景广阔,故符合题意。
7.阅读下面科普短文(原文作者:
段翰英等)。
我国制作泡菜的历史悠久。
制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。
泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。
硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。
亚硝酸盐[如亚硝酸钠(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)和氯化物(如
)。
亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?
含量有多少?
含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。
下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。
用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。
泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。
这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。
但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。
另外,泡制过程也会造成某些营养素的流失。
(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由转化成生的。
(2)亚硝酸钠能与盐酸反应,该反应属于基本反应类型中的反应。
(3)室温下,用芹菜制作的泡菜,最佳食用时间是(填字母序号,下同)。
A.泡制2-3天B.泡制5-6天C.泡制12天后
(4)下列关于制作泡菜的说法中,合理的是。
A.最好加入一些姜汁
B.最好在较低温度下泡制
C.最好加入一些富含维生素C的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(5)请你为喜欢吃泡菜的人提一条食用泡菜的建议:
。
【答案】
(1)硝酸盐
(2)复分解(3)C(4)A、C、D
(5)食用超过12天的泡菜或合理食用泡菜的量
【解析】
【分析】
【详解】
(1)根据质量守恒定律,泡菜中的亚硝酸盐是由硝酸盐转化成生的
(2)亚硝酸钠能与盐酸反应,产生亚硝酸(HNO3)和氯化物(NaCl),是由两种化合物相互交换成分生成另两种化合物的反应,故该反应属于基本反应类型中的复分解反应;
(3)根据室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系图,室温下,用芹菜制作的泡菜,最佳食用时间是泡制12天后,故选C;
(4)实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成,说明制作泡菜时最好加入一些姜汁和一些富含维生素C的水果,故A、C正确,泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。
这与温度较高有利于乳酸菌的繁殖有关,说明最好在较高温度下泡制,说明B错误,根据食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系图可知:
最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关,都是泡制12天后,说明D正确,故选A、C、D;
(5)喜欢吃泡菜的人提一条食用泡菜的建议:
食用超过12天的泡菜或合理食用泡菜的量。
8.阅读下面科普短文(有刪改)
火炸药的绿色制造技术发展
以硝基化合物为代表的含能材料是火炸药技术的基础,其传统的制造工艺过程会产生含有大量有机物的废酸和废水,环境污染严重,治理费用高,因此火炸药原材料组分传统制造工艺需要进行绿色化和低成本改进,以及积极开发含能材料的绿色合成工艺。
硝基含能化合物的生物合成是火炸药原材料制造技术中最新颖的前沿研究领域,是一种真正绿色合成路线。
最具代表性的新型硝化技术是用N2O5作为绿色硝化剂,这一技术的关键是如何制备N2O5和怎样实现N2O5硝化工艺。
研究的N2O5制备方法主要有半渗透膜电解法和臭氧氧化法:
1)半渗透膜电解法是在电解池内用特制的半渗透膜隔开两个电极,电解无水硝酸而生成N2O5;2)臭氧氧化法是将浓度5%~10%的臭氧与氧气的混合物和N2O4进行气相反应生成N2O5。
试验的N2O5硝化工艺主要有2种:
1)用N2O5-HNO3-N2O4作硝化剂进行硝化;2)用N2O5和无水HNO3于液态二氧化碳中进行硝化。
南京理工大学研究了用DADN原料在N2O5-HNO3体系中绿色硝解制备HMX。
以DADN为原料,不同硝解方法的优缺点比较见下表:
硝化体系
收率/%
优点
缺点
HNO3
40
步骤简单
得率低
H2SO4、NH4NO3、HNO3
80-85
工艺成熟
废酸量大,难处理
P2O3-HNO3
99
得率高,纯度好
P2O3和HNO3需大大过量,腐蚀性大
N2O5-有机溶剂
65
无需废酸处理
得率低,溶剂易挥发
N2O5-HNO3
94
得率高,废酸少,硝化剂的过量比小
无
火炸药的安全使用知识有:
防止炸药受热、火焰引起的爆炸;按炸药使用温度使用,不 要超过温度条件;禁止长时间阳光照射;禁止电焊、气焊、气割作业等。
依据文章内容,回答下列问题:
(1)文中涉及到的下列物质:
P2O5、HNO3、O3、NH4NO3、N2O4中,不包括的物质类别是______________ (填序号)。
A.单质 B.氧化物 C.酸 D.碱 E.盐
(2)最具代表性的新型硝化技术是用_____________作为绿色硝化剂。
(3)上表中,以DADN为原料,不同硝解方法比较中,P2O3和HNO3需大大过量,腐蚀性大的硝化体系是__________________。
(4)火炸药的安全使用还有哪些注意事项___________________。
(原文已有方法不能重复,任答一点)
【答案】DN2O5P2O3-HNO3远离烟火等
【解析】
(1)根据物质所属类别解答;
(2)根据题中信息解答;(3)根据题中信息解答;(4)根据已有知识解答。
(1)文中涉及到的下列物质:
P2O5(氧化物)、HNO3(酸)、O3(单质)、NH4NO3(盐)、N2O4(氧化物)中,不包括的物质类别是碱,故选D;
(2)由题中信息可知,最具代表性的新型硝化技术是用N2O5作为绿色硝化剂;(3)由表中可知,以DADN为原料,不同硝解方法比较中,P2O3和HNO3需大大过量,腐蚀性大的硝化体系是P2O3-HNO3;(4)火炸药的安全使用要注意事远离烟火等。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 备战 中考 化学 科普 阅读 综合 汇编 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
