 贵州省学年九年级上学期期末零模化学试题2B卷.docx
贵州省学年九年级上学期期末零模化学试题2B卷.docx
- 文档编号:5886802
- 上传时间:2023-01-01
- 格式:DOCX
- 页数:13
- 大小:330.53KB
贵州省学年九年级上学期期末零模化学试题2B卷.docx
《贵州省学年九年级上学期期末零模化学试题2B卷.docx》由会员分享,可在线阅读,更多相关《贵州省学年九年级上学期期末零模化学试题2B卷.docx(13页珍藏版)》请在冰豆网上搜索。
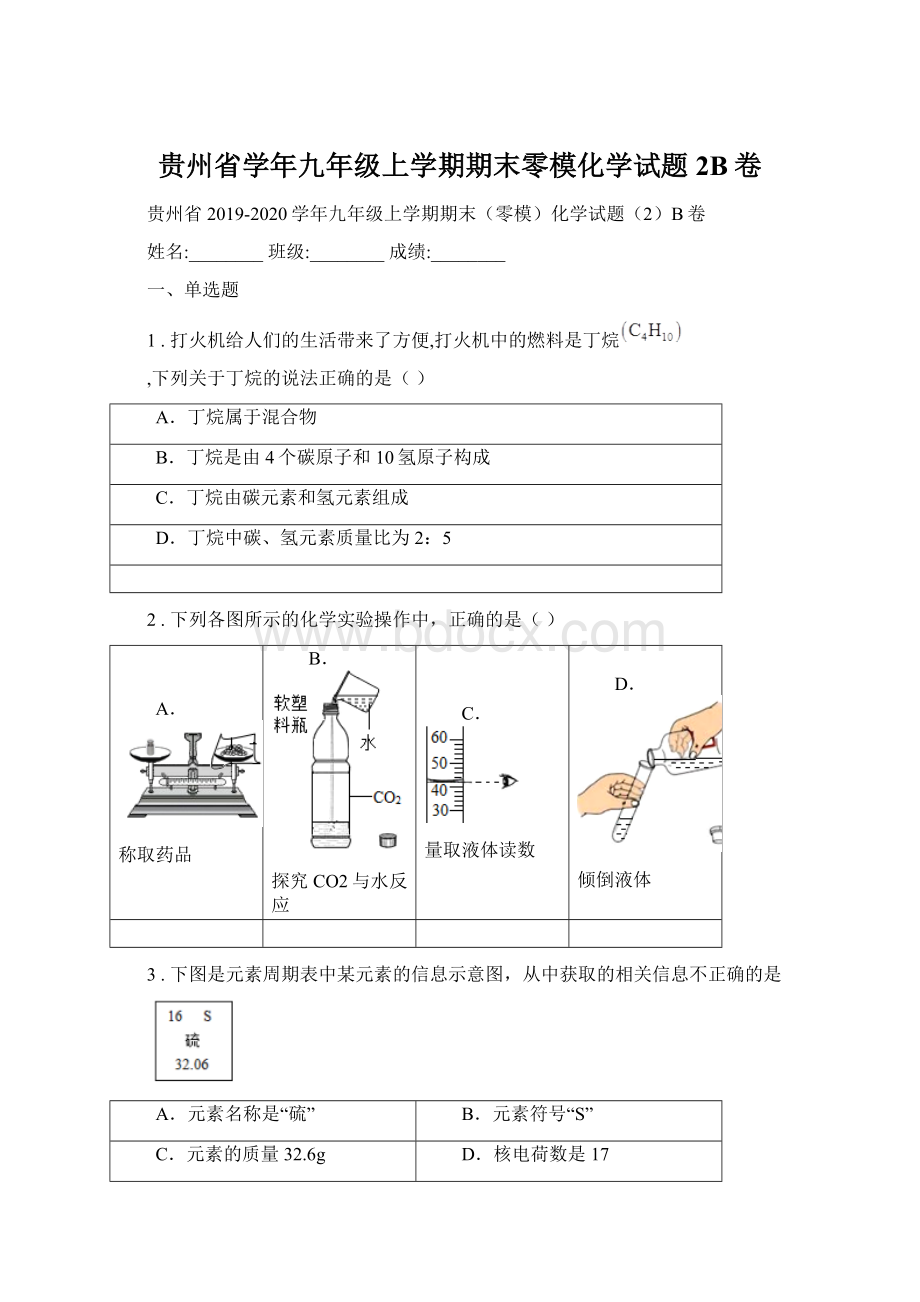
贵州省学年九年级上学期期末零模化学试题2B卷
贵州省2019-2020学年九年级上学期期末(零模)化学试题
(2)B卷
姓名:
________班级:
________成绩:
________
一、单选题
1.打火机给人们的生活带来了方便,打火机中的燃料是丁烷
下列关于丁烷的说法正确的是()
A.丁烷属于混合物
B.丁烷是由4个碳原子和10氢原子构成
C.丁烷由碳元素和氢元素组成
D.丁烷中碳、氢元素质量比为2:
5
2.下列各图所示的化学实验操作中,正确的是()
A.
称取药品
B.
探究CO2与水反应
C.
量取液体读数
D.
倾倒液体
3.下图是元素周期表中某元素的信息示意图,从中获取的相关信息不正确的是
A.元素名称是“硫”
B.元素符号“S”
C.元素的质量32.6g
D.核电荷数是17
4.下列化学方程式书写正确的是()
A.Mg+O2
MgO
B.4Fe+3O2
2Fe2O3
C.
D.
5.下列关于金属材料的叙述错误的是()
A.回收利用废旧金属可减少对环境的污染
B.在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀
C.铝块能制成铝箔是利用了铝的延展性
D.铝比铁更容易跟氧气和其他物质反应,因而铝的抗腐蚀性能比铁差
6.化学用语表达中,正确的是()
A.2个氧分子:
2O
B.一氧化碳:
Co
C.3个氦分子:
3He
D.氧化钠:
NaO
7.地壳中含量最多的前四种元素依次是()
A.碳、氢、氧、硫
B.氮、氧、铝、铁
C.氧、硅、铝、铁
D.铁、铜、锌、铝
8.同种元素的原子都具有相同的()
A.电子数
B.中子数
C.质子数和中子数
D.核电荷数
9.下列物质的用途主要利用其化学性质的是()
A.铜丝作导线
B.干冰用于人工降雨
C.氢气可用作燃料
D.纯净水可用于饮用
10.下列各组物质,前者属于混合物,后者属于化合物的是()
A.酒精,铝合金
B.石灰水,冰水
C.碘酒,液氧
D.氮气,煤
11.下列描述正确的是()
A.“H”既可以表示宏观的氢元素,也可以表示微观的一个氢原子
B.烧碱、熟石灰、纯碱按物质分类均属于碱
C.金刚石、
均为碳单质,所以物理性质、化学性质完全相同
D.泡沫灭火器灭火的原理是提高了可燃物质的着火点
12.下列物质属于氧化物的是()
A.液氧
B.生石灰
C.双氧水
D.火碱
13.某同学梳理了以下知识:
①把少量泥土放入水中搅拌,形成的液体是悬浊液;②稀有气体在通电时能发出不同颜色的光,可制成多种用途的电光源;③最外层电子数为8的粒子都是稀有气体的原子;④原子序数与元素原子核电荷数在数值上相同;⑤化学反应中只有燃烧反应才能放出热量;⑥农药的不合理施用对空气、水、土壤都有污染。
其中正确的个数是
A.1个
B.2个
C.3个
D.4个
14.将面粉、味精、食盐、酒精分别放入水中,不能形成溶液的是
A.面粉
B.味精
C.食盐
D.酒精
15.下列图示的“错误操作”,与对应选项“可能产生的后果”不一致的是()
A.
试管破裂
B.
量取的液体偏少
C.
橡皮塞弹出
D.
灯内酒精燃烧
16.下列有关溶液的说法中,正确的是()
A.植物油加入水中,形成无色溶液
B.无色透明的液体一定是溶液
C.硝酸铵溶于水,使溶液的温度降低
D.不饱和溶液降低温度一定会变成饱和溶液
17.元素观是化学的重要观念之一。
下列有关元素的说法错误的()
A.元素是具有相同核电荷数的一类原子的总称.
B.物质都由元素组成
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素的种类也不会改变
18.下列说法中,正确的是()
A.空气中氮气的质量分数为78%,氧气的质量分数为21%
B.因为氧气能支持燃烧,所以可用作燃料
C.工业上常采用分离液态空气的方法制氧气,该变化属于化学变化
D.实验室制氧气的催化剂除二氧化锰之外,还有其他物质
19.下列有关碳和碳的氧化物的说法中,正确的是()
A.金刚石和石墨均属于碳的单质,所以二者性质完全相同
B.一氧化碳、二氧化碳、碳都能还原氧化铜
C.二氧化碳能使干燥的石蕊纸花变红
D.二氧化碳可用于灭火,既利用了它的物理性质也利用了它的化学性质
20.下列图像与对应叙述相符合的是()
A.
向pH=3的溶液中加水
B.
向一定量质量氯化钙溶液中加入碳酸钾溶液
C.
加热一定质量的氯酸钾固体
D.
向一定质量的过氧化氢溶液中加入二氧化锰
二、填空题
21.《2019年世界与中国能源展望》中提到,世界能源发展趋势是加快向多元化清洁化、低碳化转型。
下列是我国能源结构变化的调整图,请回答相关问题:
(1)煤、石油、天然气属于__________能源(填“可再生”或“不可再生”)。
(2)从2015、2030、2050年能源结构变化看,所占比例增加最多的是_____________。
(3)在新能源开发中,化学发挥着不可替代的作用。
近年,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过下图1的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油(图中c、d是最终制得的汽油中所含物质的分子结构模型)。
①图2是图1中环节Ⅰ在一定的条件下发生的反应,则反应的化学方程式为____________。
②观察图1中c和d两种物质的分子结构模型,发现c和d的分子组成完全相同,但其分子结构不同,化学上将其称为同分异构体。
你认为c和d的化学性质__________(填“是”或“否”)完全相同。
22.写出下列有关金属反应的化学方程式。
(1)常温下,铝在空气中能生成一层致密的氧化铝膜:
___________________。
(2)实验室制取氢气:
____________,氢气点燃前一定要_________________。
(3)铁钉浸入稀盐酸:
______________,液体最终变成___________色。
(4)镁与稀硫酸反应:
______________,反应的基本类型是____________。
(5)钛(Ti)被称作“未来的金属”,钛制的坦克、潜水艇、军舰没有磁性,不会被磁性水雷发现,在氢气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛和另一种化合物,则该反应的化学方程式是__________________,猜想该反应在氩气气氛中进行的原因是____________________________。
23.随着生产的发展,家庭日用品的种类也日益增多。
以下是几种常见的清洁剂。
(1)彩漂液的有效成分为过氧化氢,长期存放会因分解而失效。
用化学方程式解释失效的原因________。
(2)“洁厕灵”的有效成分是稀盐酸,不小心滴到大理石地面上,发现有气泡产生,发生反应的方程式为__________。
(3)“管道通”中的有效成分是氢氧化钠,它不能与“洁厕灵”混合使用,其原因是________(用化学方程式表示)。
24.根据下列图示的实验基本操作,回答下列问题:
(1)若要完成“粗盐中难溶性杂质的去除”的实验,需要进行的操作步骤依次是________(填数字序号),操作③中玻璃棒的作用是________。
(2)若要配制200Kg溶质的质量分数为7%的KNO3溶液作无土栽培的营养液,需KNO3的质量为_______Kg,主要进行的操作步骤依次是_______(填数字序号)。
25.根据如图所示实验回答问题。
(1)甲实验,反应结束后,若先熄灭酒精灯可能导致的后果是_______。
(2)乙实验,干燥的紫色石蕊小花喷水后放入集气瓶中,观察到的现象是________,产生该实验现象的原因是_______(用化学方程式表示)。
(3)丙是探究燃烧条件的实验,热水的作用是隔绝空气和_______,对比①和②处的观象说明燃烧需要______。
三、实验题
26.实验室制取气体的装置如图所示,请回答下列问题:
(1)仪器①的名称是_____。
(2)氢气是种无色、无味、难溶于水的气体密度比空气小、在实验室中常用锌粒和稀硫酸反应制取,则制取氢气的发生装置应选择_____(填字母);氢气与氧气混合点燃可能会发生爆炸,因此点燃氢气之前必须先_______。
(3)实验室若用B装置制取CO2,反应的化学方程式为_____,制取的二氧化碳气体中常混有少量氯化氢气体,需用饱和碳酸氢钠溶液将杂质气体除去,则气体应从_____(填·“a”或"b”)端进入。
四、简答题
27.铜、铁是人类使用最早、应用广泛的金属材料。
(1)下列金属材料不属于合金的是_____;
A磁铁矿 B青铜 C铜 D硬铝
(2)扬州博物馆的馆藏中有不少国宝级的青铜器,如:
铜釭灯、铜镜、铜熏等。
出土时表面有大量的“铜绿”。
古时候人们大量使用青铜而不是纯铜,是因为青铜相较纯铜性能优良,例如青铜硬度比纯铜硬度_____(填“大”或“小”)。
(3)兴趣小组进行了“铜绿”产生原因的实验探究,将四小块铜片分别按下图所示放置一段时间,观察现象如下:
(氢氧化钠溶液能吸收二氧化碳)
实验装置
实验现象
铜片不生锈
铜片不生锈
铜片不生锈
铜片生锈且水面附近锈蚀最严重
说明铜生锈需要水的一组实验是_____(填实验序号),写出铜产生“铜绿”的化学方程式_____。
(4)铁、铜矿石及主要成分有赤铁矿(________)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等。
(5)工业炼铁大多采用赤铁矿、磁铁矿。
以磁铁矿为原料炼铁的化学方程式为_____。
炼铁不采用黄铁矿、黄铜矿,可能的原因是:
黄铁矿、黄铜矿含铁量相对低;_____。
(6)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:
4CuFeS2+17O2+2H2SO4
4CuSO4+2Fe2(SO4)3+2H2O。
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu,所得FeSO4溶液颜色为_____。
主要发生反应的化学方程式:
Fe+Fe2(SO4)3=3FeSO4,_____。
FeSO4溶液经蒸发浓缩、_____、过滤、洗涤、低温干燥等操作得到纯净的FeSO4·7H2O晶体。
洗涤晶体宜用冷水,如果用热水洗涤,可能产生的后果是_____。
28.水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任。
(1)用如图甲装置进行电解水的实验,a中收集到的气体是____。
(2)贵州水资源丰富,但分布不均,有些村民用地下水作为生活用水,人们常用_____________检验地下水是硬水还是软水;某同学自制如图乙所示简易净水器,图中活性炭的主要作用是_____________国家规定的自来水pH范围为6.5~8.5。
为了测定家用自来水是否达到这一标准,可用_____________来进行检测。
五、流程题
29.海洋中蕴含着丰富的资源,人们可以从海水中获取很多物质。
(1)海水淡化是解决淡水资源不足的重要方法。
下列方法中,可以使海水淡化的是_____ (填字母序号)。
A 过滤法 B 沉淀法 C 多级闪急蒸馏法D 分解法
(2)海水蒸发结晶可制得粗盐。
晒制粗盐的主要成分为NaCl,还含有少量的MgCl2;、CaCl2、MgSO4、泥沙等杂质。
下面是由粗盐获取较纯净精盐的一种方法:
①为除去MgCl2、CaCl2、MgSO4可溶性杂质,操作I中依次加入的物质(过量)和顺序,合理的是_____;
a NaOH、BaCl2、Na2CO3; b Ba(NO3)2、Na2CO3、NaOH
c Na2CO3、BaCl2、NaOH d BaCl2、NaOH、Na2CO3
②操作I过量加入各物质的目的是_____;
③操作Ⅱ加入适量的盐酸,作用是_____。
④假设除杂过程中氯化钠没有损失,则理论上除杂后获得食盐的质量_____除杂前食盐的质量(填“>”“<”或“=”)
(3)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:
①在步骤Ⅱ中通入氨气的作用是_____,请写出步骤ⅲ中发生反应的化学方程式_____。
②提取氯化镁经历ⅳ、ⅴ两步转换的目的是_____。
写出步骤ⅳ中发生反应的化学方程式_____。
六、科学探究题
30.科学探究是重要的学习方法,假设和验证是探究过程中的重要环节。
为了探究“铁丝可以在纯净的氧气中燃烧”,同学们将一根火柴梗塞入一段螺旋状“铁丝”(可能是纯铁丝或含碳铁丝)末端,将它固定,用镊子夹住“铁丝”,然后将火柴在酒精灯上点燃,将“铁丝”由集气瓶口向下慢慢伸入,观察现象:
(1)甲同学只发现“铁丝”红热,没有观察到其他现象,请你分析“铁丝”没有燃烧的可能原因:
_________。
(只答一条)
(2)乙同学发现“铁丝”在纯净的氧气中燃烧起来,观察到火星四射,并有黑色固体生成,请写出该反应的文字表达式:
_______________。
(3)为了找出“铁丝”在纯氧中燃烧“火星四射”的原因,根据现有实验用品:
细纯铁丝、细含碳铁丝、镁条、用集气瓶装的几瓶纯氧气、酒精灯、火柴和镊子等,请你提出假设和验证方法。
a.假设1:
___________,验证方法是____________。
b.假设2:
__________,验证方法是____________。
只要假设合理,验证方法准确,根据实验现象,进行分析判断,就能得出结论。
七、计算题
31.实验室有一瓶硫酸溶液,老师请小刚同学设计方案测定该溶液的溶质的质量分数。
小刚先取一只洁净的小烧杯,称其质量为16.4g,然后往其中倒入少量硫酸溶液后称量,总质量为30.2g,之后,将一枚质量为11.8g的铁钉(已用砂纸打磨去铁锈)放入该小烧杯中,待铁钉表面不再有气泡产生后,再次称量,总质量为41.9g。
请回答下列问题:
(1)反应后产生的气体的质量是______g。
(2)计算该硫酸溶液的溶质的质量分数。
(写出计算过程,结果精确到0.1%)______。
八、科普阅读题
32.阅读下面科普短文。
味精,是国内外广泛使用的增鲜调味品之一,为白色柱状结晶体,其主要成分为谷氨酸钠(C5H8NO4Na)和食盐。
味精被摄入人体中,谷氨酸钠与胃酸作用生成谷氨酸和氯化钠,很快被消化吸收为蛋白质,并参与人体中的多种新陈代谢。
最初的味精是水解蛋白质然后纯化得到的。
现代工业生产采用某种擅长分泌谷氨酸的细菌发酵得到,发酵的原料可以用淀粉、甜菜、甘蔗等,使得生产成本大为降低。
这个过程跟酒、醋、酱油的生产是类似的。
味精的使用浓度占食品重量的0.2%~0.8%能最大程度增进食品的天然风味。
味精的鲜味受什么因素影响呢?
经实验测定发现,当加热至100℃以上时,会引起部分失水,生成焦谷氨酸钠,失去鲜味,且有轻微毒性。
下表是焦谷氨酸钠含量与加热温度、加热时间的关系。
加热时间
(小时)
焦谷氨酸钠含量(%)
100℃
107℃
115℃
0.5
0.3
0.4
0.7
1.0
0.6
0.9
1.4
2.0
1.1
1.9
2.8
4.0
2.1
3.6
5.7
实验表明,味精的鲜味与水溶液的酸碱度有关,当pH值在5.5-8.0时,鲜味最强;当pH值小于4.0时鲜味较弱;当pH值大于8.0时由于形成二钠盐而鲜味消失。
实验研究还表明,味精对婴幼儿,特别是几周以内的婴儿生长发育有严重影响。
它能使婴幼儿血中的锌转变为谷氨酸锌随尿排出,造成体内缺锌,影响宝宝生长发育,并产生智力减退和厌食等不良后果。
因此产后3个月内乳母和婴幼儿的菜肴不要加入味精。
依据文章内容,回答下列问题
(1)谷氨酸钠的物理性质有 。
(2)谷氨酸钠进入人体后会转化为 。
(3)谷氨酸钠中碳、氢元素的质量比为 。
(4)下列关于味精的说法中,合理的是 。
A.炒菜时加入味精后生成焦谷氨酸钠的含量只与加热时间有关
B.烹饪时加入味精的最佳时间是大火翻炒时
C.婴幼儿的食品中不应该加入味精
D.味精应避免在酸性或碱性较强的条件下使用
(5)请你为饭店的厨师们提一条使用味精的建议:
。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 贵州省 学年 九年级 学期 期末 化学试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
