 高中化学氧化还原反应.docx
高中化学氧化还原反应.docx
- 文档编号:5542667
- 上传时间:2022-12-19
- 格式:DOCX
- 页数:13
- 大小:112.59KB
高中化学氧化还原反应.docx
《高中化学氧化还原反应.docx》由会员分享,可在线阅读,更多相关《高中化学氧化还原反应.docx(13页珍藏版)》请在冰豆网上搜索。
高中化学氧化还原反应
氧化还原反应是专题
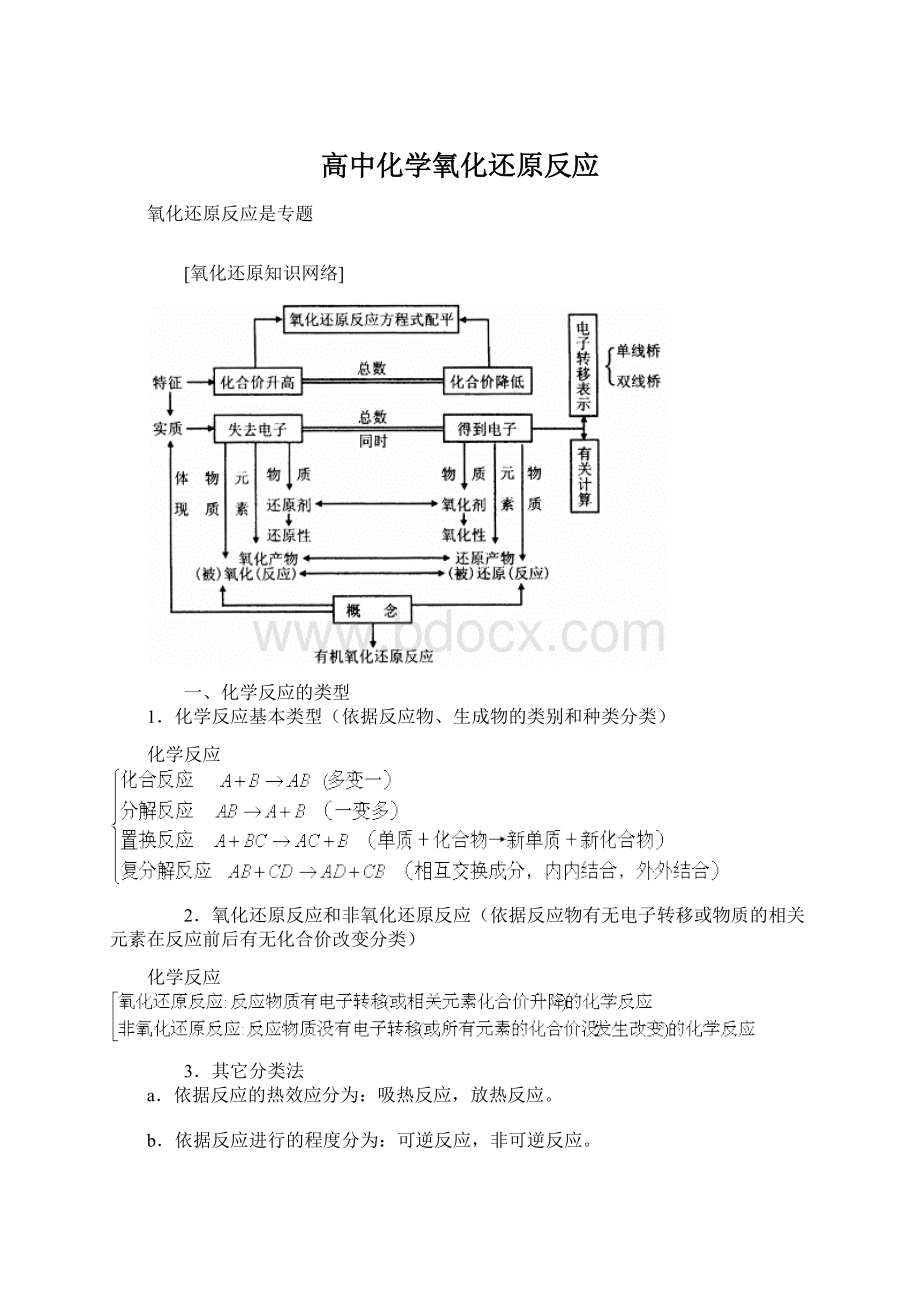
[氧化还原知识网络]
一、化学反应的类型
1.化学反应基本类型(依据反应物、生成物的类别和种类分类)
化学反应
2.氧化还原反应和非氧化还原反应(依据反应物有无电子转移或物质的相关元素在反应前后有无化合价改变分类)
化学反应
3.其它分类法
a.依据反应的热效应分为:
吸热反应,放热反应。
b.依据反应进行的程度分为:
可逆反应,非可逆反应。
c.依据反应中有无离子参与分为:
离子反应,分子反应。
4.氧化还原反应与基本反应类型的关系
⑴置换反应都是氧化还原反应;
⑵复分解反应都是非氧化还原反应;
⑶化合反应和分解反应可能为氧化还原反应;
它们的关系可用下图表示:
说明:
⑴有单质参与的化合反应或分解反应多数为氧化还原反应,但不一定是氧化还原。
如:
①4P(红)=P4为化合反应,但为非氧化还原反应;
②2O3=3O2有单质生成但为非氧化还原;
⑵没有单质参与的化合反应或分解反应也可能是氧化还原反应。
如:
①NH4NO3的分解,随条件不同,产物也不同,可能生成NO2、H2O等为氧化还原反应,但没有单质参与;
②Na2O2与MnO2化合可以生成Na2MnO4也是氧化还原反应,但没有单质参与。
二、氧化还原反应
1、特征:
反应前后元素的化合价发生改变。
2、实质:
有电子转移(电子的得失或共用电子对的偏移)。
3、氧化还原反应概念
①氧化与还原(指反应过程)
②氧化剂与原还剂(指反应物质)
③氧化性与还原性(指物质能获得电子或能失去电子的性质)
注:
物质的氧化性(或还原性)的强弱,指的是得(或失)电子的难易,不是指得(失)电子的多少。
④氧化产物与还原产物(指生成物)
4、氧化还原反应概念间的关系。
5、氧化还原反应中电子转移的表示方法
⑴双线桥法――表明了反应前后某种元素化合价的变化情况
①用两条带箭头的线由反应物指向生成物,且对准同种元素。
②要标明“得”“失”电子,且得失电子总数相等。
③箭头不代表电子转移的方向,而是指某元素从反应到产物时价态的变化。
例如:
⑵单线桥法――表明了一个氧化还原反应中电子的转移方向和数目
①用一条箭线在反应物间表示电子得失。
②箭线从失电子元素到得电子元素。
③在箭线上标明电子转移总数,但不写“得”或“失”。
例:
6、常见的氧化剂和还原剂
①常见的氧化剂有:
a.高价或较高价的含氧化合物:
MnO2 KMnO4 K2Cr2O7 HNO3 H2SO4(浓)
b.高价金属阳离子:
Cu2+、Fe3+、Ag+等。
c.非金属单质:
Cl2、Br2、I2、O2、S等。
注:
具有最高价元素的物质,在氧化还原反应中该元素只能得到电子。
②常见的还原剂有:
a.活泼或较活泼的金属:
K、Ca、Na、Mg、Al、Zn、Fe等。
b.非金属阴离子:
Cl-、Br-、I-、S2-等。
c.较低价的化合物:
CO、H2S、NH3等。
注:
具有最低价元素的物质,在氧化还原反应中该元素只能失去电子。
③具有中间价态的化合物,在氧化还原反应中既能得到电子,又能失去电子,既可作氧化剂,又可作还原剂,它们既有氧化性,又有还原性,如Fe2+等。
三、物质氧化性和还原性相对强弱的判断方法
1.根据金属活动性顺序进行判断
K、Ca、Na、……、Zn、Fe、……、Cu、Hg、Ag
在金属活动性顺序表中,金属的位置越靠前,其还原性就越强;金属的位置越靠后,其阳离子的氧化性就越强。
(注意:
上面说的阳离子中Fe有+2、+3两种价态,其中+2价按正常位置排列,但+3铁的氧化性在Cu2+、Hg2+之间,即:
氧化性Cu2+ 2.根据非金属活动性顺序判断 氧化剂的氧化性越强,则其对应的还原产物的还原性就越弱;还原剂的还原性越强,则其对应的氧化产物的氧化性就越弱。 对单质而言,非金属单质的氧化性越强,对应阴离子的还原性越弱,非金属单质的氧化性越弱,对于阴离子的还原性越强;金属单质的还原性越强,对于阳离子的氧化性越弱,金属单质的还原性越弱,对于阳离子的氧化性越强。 3.根据化学方程式进行判断 氧化性: 氧化剂>氧化产物; 还原性: 还原剂>还原产物。 4.根据氧化还原反应进行的难易程度(反应条件或剧烈程度)的不同进行判断。 氧化还原反应越容易进行(表现为反应所需条件越简单),则氧化剂的氧化性和还原剂的还原性就越强。 例如: 2Na+2H2O=2NaOH+H2↑,Mg+2H2O Mg(OH)2+H2↑ 前者比后者容易发生,可判断还原性: Na>Mg。 5.根据使其它物质被氧化或被还原价态的不同进行判断 例如: Cu+Cl2 CuCl2,2Cu+S Cu2S,根据Cl2、S分别与Cu反应,使Cu氧化的程度不同(Cu2+,Cu+)可判断出单质的氧化性: Cl2>S 6.物质中元素具有最高价,则该元素只有氧化性;物质中元素具有最低价时,该元素只有还原性;物质中元素具有中间价时,该元素既有氧化性又有还原性。 一般,对于同一种元素,价态越高,其氧化性就越强;价态越低,其还原性就越强(正价的卤素相反)。 例如氧化性: Fe3+>Fe2+,H2SO4(浓)>H2SO3,HClO>HClO3>HClO4 7.可根据元素周期表判断 同周期元素,随着核电荷数的递增,单质的氧化性逐渐增强,还原性逐渐减弱;最高价阳离子氧化性逐渐增强,最低价阴离子还原性逐渐减弱。 同主族元素,随着核电荷数的递增,单质的氧化性逐渐减弱,还原性逐渐增强;同价态阳离子氧化性逐渐减弱,同价态阴离子还原性逐渐增强。 8.其它条件 一般溶液的酸性越强或温度越高,则氧化剂的氧化性和还原剂的还原性就越强,反之则越弱。 如: ①温度: 如热的浓H2SO4的氧化性比冷的浓H2SO4的氧化性强。 ②浓度: 氧化性 浓HNO3>稀HNO3;还原性 浓盐酸>稀盐酸。 ③酸碱性: 如KMnO4溶液的氧化性随溶液的酸性的增强而增强。 一般来讲,在酸性条件下KMnO4被还原为Mn2+,在中性条件下被还原为MnO2,碱性条件下被还原为MnO42-。 注意: ①氧化还原性的强弱与该原子得失电子的难易程度有关,而与得失电子数目的多少无关。 得电子能力越强,其氧化性就越强;而失电子能力越强,其还原性就越强。 ②同一元素相邻价态间不发生氧化还原反应。 四、氧化还原类型与配平方法――化合价升降法 理论依据: 氧化还原反应中,氧化剂获得电子总数与还原剂失去电子总数相等,表现为: 化合价升高与化合价降低总数相等。 此外,属于离子反应的氧化还原反应,还遵循电荷守恒。 1、普通氧化还原方程式的配平 ①要标对所有变化了的化合价,单质中元素化合价为零;化合物中,一般情况下H总是+1价,O总是-2价(在个别物质中有例外,如过氧化物)然后推算其它元素的化合价。 ②对于有变价的金属元素在化合物中,常先看阴离子的价态,再定金属的化合价,如: 、 ,Fe3O4可看成是: Fe2O3·FeO,即其中有2个 ,一个 ③先配平发生氧化还原的物质,倍数乘到氧化产物与还原产物中,最后通过质量守恒,完成配平 2、变化的元素带下角标情况――把下角标数的该元素的原子数做为一个整体看待,倍数乘到含该角标元素的物质前(不论该物质是反应物还是生成物) 3、岐化反应和归中反应――一般不必考虑单质的角标,把倍数乘到两端价态元素的物质前;若结果出现化学计量数为分数情况,则乘最小公倍数变为整数(如练习⑺⑻);若归中反应的元素在同一化合物中且所需两原子个数不同时,要满足倍数大者的需要(见练习⑶)。 4、氧化数(化合价)为分数的情况──直接按分数进行配平,兼顾前面的3条原则(把倍数乘到有角码的物质前面等) 5、同一化合物的所有组成元素的价态均升高(或均降低)──把此化合物看成一个整体[保持元素原子个数比且求出化合价升高(或降低)之代数和],并结合其他规则配平。 6、某元素发生岐化或归中反应且还有其它元素得失电子的类型――先求出化合价升高总数与化合价降低总数,再求最水公倍数;同时注意角码。 7、带未知数的氧化还原方程式的配平――把未知数看成一个常数进行配平 例12、Na2Sx+NaClO+NaOH──Na2SO4+NaCl+H2O xS: ↑(6x+2)×1 Cl: +1→-1 ↓2×(3x+1) 填写化学计量数和结论如下: 1Na2Sx+(3x+1)NaClO+(2x-2)NaOH=xNa2SO4+(3x+1)NaCl+(x-1)H2O ① ② ③ ② ① ④ 8、有机方程式的配平――计算有机物中C元素的平均氧化数或根据有机物的结构确定价态变化的元素 例13、H2C2O4+KMnO4+H2SO4──CO2+K2SO4+MnSO4+H2O 把H显+1价、O显+2价代入H2C2O4中求得C显+3价 2C: +3→+4 ↑2×5 Mn: +7→+2 ↓5×2 化学计量数的填写步骤和结论如下: 5H2C2O4+2KMnO4+3H2SO4=10CO2+1K2SO4+2MnSO4+8H2O ① ② ④ ② ③ ① ⑤ 练习: 配平下面的化学方程式 ⑴CrO3(红色)+C2H5OH+H2SO4──Cr2(SO4)3(绿色)+CH3CHO+H2O ⑵K2Cr2O7+H2C2O4+H2SO4-K2SO4+Cr2(SO4)3+CO2+H2O 9、离子反应方程式的配平――除化合升降外,还要充分运用电荷平衡 例14、Fe2++Cl2=2Cl-+Fe3+是错误的。 正确的如下: 2Fe2++Cl2=2Cl-+2Fe3+ 练习: 配平下列离子方程式 ①S2-+SO32-+H+──S↓+H2O ②S2O32-+H+──S↓+SO2↑+H2O ③ClO3-+Cl-+H+──Cl2↑+H2O ④MnO2+H++Cl-──Mn2++Cl2↑+H2O ⑤Cu2++I-──CuI↓+I3- ⑥Cu+H++NO3-──Cu2++NO↑+H2O ⑦Cu+Fe3+──Fe2++Cu2+ ⑧Na+H2O──Na++H2↑+OH- ⑨Al+OH-+H2O──AlO2-+H2↑ ⑩Si+OH-+H2O──SiO32-+H2↑ NO3—+Zn+OH—+H2O──NH3+Zn(OH)42— 10、缺项配平 缺项配平的一般规律: a、缺项一般不可能是氧化剂、还原剂、氧化产物、还原产物。 b、缺项一般是介质,如H2O、KOH、H2SO4,对于离子方程式的缺项通常是H+、OH-、H2O 配平的步骤是: (1)先确定氧化剂、还原剂、氧化产物、还原产物各项化学计量数; (2)根据两边氢、氧原子数或某一原子团确定缺项物质; (3)用观察法确定其它各项化学计量数。 例15、2KMnO4+5KNO2+囗____──2MnSO4+K2SO4+5KNO3+3H2O缺项为H2SO4化学计量数为3 练: 3Pt+4HNO3+18HCl——3H2PtCl6+4NO↑+囗____ 缺项为H2O化学计量数为8 练: 3ClO-+2Fe(OH)3+囗____──3Cl-+2FeO42-+5H2O 缺项为OH-化学计量数为4 注意: 如果是化学反应方程式,其缺项一般为: 水、酸、碱。 如果是离子反应方程式其缺项一般为: 水、H+、OH-。 在离子反应方程式配平其缺项时如有两种可能如(H2O、H+)或(H2O、OH-),还应考虑离子共存的问题如: Cu2++FeS2+囗____──Cu2S+SO42-+Fe2++囗____ 可有两种选择: (14、5、12H2O、7、3、5、24H+)或(14、5、24OH-、7、3、5、12H2O)后一种配平由于OH-与Cu2+不能共存所以不正确。 11、整体把握变化的原子数 练习: 配平下面的化学方程式 ⑴K4[Fe(CN)6]-KCN+Fe+C+N2↑ 提示: 此题中由于C、N原子均部分参加反应,且原子个数比为1∶1,配平时要注意保持二者的比例关系。 如下: 结论与步骤如下: K4[Fe(CN)6]=4KCN+1Fe+2C+1N2↑ ⑵PbO2+MnSO4+H2SO4──Pb(MnO4)2+PbSO4+H2O 分析: 此反应的特点是+4价Pb的还原产物+2价Pb分别在两种生成物中,配平时要从变化的Pb原子总数把握配平。 如下: Pb: +4→+2 ↓2×5 2Mn: +2→+7 ↑10×1 此题把倍数1乘到带角码的物质Pb(MnO4)2前,但倍数5不直接乘到Pb(MnO4)2或PbSO4前,因为5是变化的Pb原子总数,结合反应中+4价Pb变化数也为4,而+4价Pb只有一种存在形式PbO2,所以,应把倍数5乘到只有一种存在形式的PbO2前。 如下: 5PbO2+2MnSO4+2H2SO4=1Pb(MnO4)2+4PbSO4+2H2O 五、氧化还原反应的基本规律及应用 1.氧化还原反应中的守恒 (1)原子守恒: 从宏观上阐述即指质量守恒,从微观上讲就是指原子守恒。 (2)电荷守恒: 方程式左边的净电荷数等于方程式右边的净电荷数。 (3)电子守恒: 氧化还原反应中得失电子总数相等。 2.强弱规律: 较强氧化性的氧化剂和较强还原性的还原剂反应,生成弱还原性的还原产物和弱氧化性的氧化产物。 应用: 在适宜的条件下,用氧化性较强的物质制备氧化性较弱的物质,或用还原性较强的物质制备还原性较弱的物质,亦可用于比较物质间氧化性或还原性的强弱。 3.归中规律: 同一元素不同价态原子间发生氧化还原反应时: 高价态 中间价态 低价态,也可归纳为: 两相靠,不相交。 若中间有多种价态,则原高价物质对应的还原产物价态仍高,原低价态的物质对应的氧化产物的价态仍低,或说成: 同种元素不同价态间反应向中间靠近时,价态: 还原产物≥氧化产物,也可说成: 高对高,低对低。 例如: 此反应中H2S不可能变为SO2,同样,H2SO4也不可能变为生成物中S。 4.歧化反应: 反应物自身氧化还原反应,同种元素一部分化合价升高,一部分化合价降低的反应。 高价态 中间价态 低价态 例如: +2NaOH=Na +Na O+H2O 5.先后规律: 一种氧化剂(或还原剂)与多种还原剂(或氧化剂)相遇时,总是依还原性(或氧化性)强弱顺序先后去氧化还原剂(或去还原氧化剂) 应用: 判断物质的稳定性及反应顺序。 例如: 把Cl2通入FeBr2溶液中,Cl2的强氧化性可将Fe2+、Br-氧化。 由于还原性Fe2+>Br-,所以,当通入少量的Cl2时,根据先后规律,Cl2首先将Fe2+氧化。 当Cl2足量时,方可把Fe2+、Br-一并氧化。 2Fe2++Cl2=2Fe3++2Cl-(Cl2不足量),2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-(Cl2足量) 6.性质规律 ①某元素处于最高价态时,则含有该元素的物质就具有氧化性。 (在化学反应中,该元素化合价只能降低,不可升高)例: K nO4、H2 O4、H O3、 Cl3、 2等。 ②某元素处于最低价态时,则含有该元素的物质具有还原性。 (在化学反应中,该元素的化合价只能升高,不能降低)例: H 、 、Na2 等。 ③某元素处于中间价态时,则含有该元素的物质既有氧化性,又有还原性。 (该元素的化合价可能升高或者降低)例: 、 、 、 等。 ④金属单质只有还原性,非金属单质多数既具有氧化性,又具有还原性,少数只具有氧化性(如O2、F2)。 ⑤含同种元素相邻价态的两种物质之间不发生氧化还原反应。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 氧化 还原 反应
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
