 四川新课标Ⅲ四川省成都市届高三第一次诊断性检测理综化学试题附答案精品.docx
四川新课标Ⅲ四川省成都市届高三第一次诊断性检测理综化学试题附答案精品.docx
- 文档编号:5436571
- 上传时间:2022-12-16
- 格式:DOCX
- 页数:19
- 大小:575.91KB
四川新课标Ⅲ四川省成都市届高三第一次诊断性检测理综化学试题附答案精品.docx
《四川新课标Ⅲ四川省成都市届高三第一次诊断性检测理综化学试题附答案精品.docx》由会员分享,可在线阅读,更多相关《四川新课标Ⅲ四川省成都市届高三第一次诊断性检测理综化学试题附答案精品.docx(19页珍藏版)》请在冰豆网上搜索。
四川新课标Ⅲ四川省成都市届高三第一次诊断性检测理综化学试题附答案精品
四川省成都市2018届高三第一次诊断性检测理综
化学试题
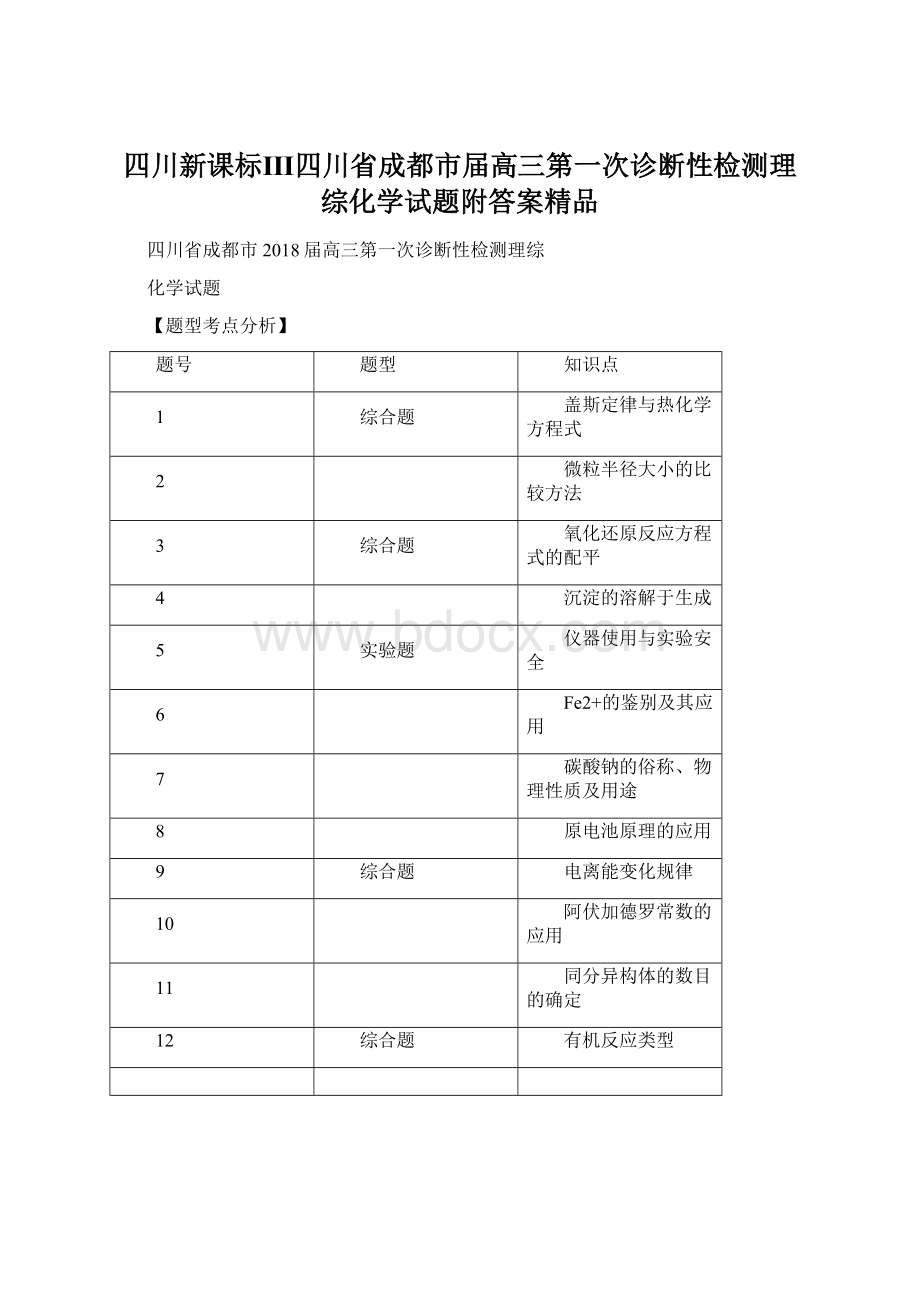
【题型考点分析】
题号
题型
知识点
1
综合题
盖斯定律与热化学方程式
2
微粒半径大小的比较方法
3
综合题
氧化还原反应方程式的配平
4
沉淀的溶解于生成
5
实验题
仪器使用与实验安全
6
Fe2+的鉴别及其应用
7
碳酸钠的俗称、物理性质及用途
8
原电池原理的应用
9
综合题
电离能变化规律
10
阿伏加德罗常数的应用
11
同分异构体的数目的确定
12
综合题
有机反应类型
第I卷(选择题)
1.下列物质的化学性质及在生活中的相关应用均正确的是
A.液氯具有强氧化性,常用作环境消毒剂
B.苏打具有碱性,常用于中和人体过多胃酸
C.铝箔具有还原性,可作为脱氧剂用于药品包装材料
D.烹鱼时加入料酒发生氧化反应,可去腥提香
【答案】C
【解析】A项,液氯具有强氧化性,可作消毒剂,但液氯有毒,易造成环境污染,不能用作环境消毒剂,故A错误;B项,中和人体过多胃酸应使用小苏打而不是苏打,因为小苏打酸性弱、腐蚀性小,苏打碱性强、腐蚀性大,故B错误;C项,铝箔以其无毒、高遮光性、阻氧性和防潮性等优点,在药品包装中得到了广泛的应用,其中“阻氧性”就是指铝箔具有还原性,可作为脱氧剂用于药品包装材料,故C正确;D项,料酒主要成分中含有乙醇、乙酸、小分子酯类、可溶性蛋白质等,鱼体中的腥味物质主要是三甲胺等,能溶解在乙醇中,在加入烹饪料酒时,其腥味随着酒精挥发而被带走,料酒中含有的小分子酯本身具有香味,烹饪过程中乙醇和乙酸可能发生酯化反应生成乙酸乙酯具有香味,所以烹鱼时加入料酒可去腥提香,并不是发生氧化反应的原因,故D错误。
2.下列分析正确的是
A.异丁烷的二氯代物有4种
B.区别蛋白质和淀粉可用浓硝酸做颜色反应
C.石蜡油分解产物均能使酸性KMnO4溶液褪色
D.甲苯的硝化反应方程式为:
【答案】B
【解析】A项,异丁烷为CH3CH(CH3)CH3,其二氯代物中,取代同一碳原子上的2个H原子有:
CH3CH(CH3)CHCl2;取代不同碳原子上的2个H原子有:
ClCH2CH(CH3)CH2Cl,ClCH2CCl(CH3)CH3,所以共有3种,故A错误;B项,浓硝酸可与蛋白质发生颜色反应,显黄色,而淀粉不具有这样的性质,所以可用浓硝酸做颜色反应来区别蛋白质和淀粉,故B正确;C项,石蜡油分解的产物主要是乙烯和烷烃的混合物,乙烯能使酸性KMnO4溶液褪色,而烷烃不能使酸性KMnO4溶液褪色,故C错误;D项,甲苯的硝化反应为:
甲苯、浓硝酸与浓硫酸共热至55℃~60℃,生成硝基苯和水,所以甲苯的硝化反应需要浓硫酸而不是稀硫酸,故D错误。
3.设NA为阿伏加德罗常数的值,下列叙述一定正确的是
A.2.0gH218O和D2O的混合物中含有质子数为NA
B.1.0L2.0mol/LNaOH溶液中含有氧原子数为2NA
C.3.4gH2O2参加氧化还原反应时转移电子数为0.1NA
D.标准状况下2.24L的CCl4含有共价键数目为0.4NA
【答案】A
【解析】A项,H218O与D2O的相对分子质量均为20,且一个分子所含质子数均为10个,所以2.0gH218O和D2O的混合物为0.1mol,含有0.1NA个分子,则含有质子数为NA,故A正确;B项,NaOH和水中都含有氧原子,所以1.0L2.0mol/LNaOH溶液中含有氧原子数应大于2NA,故B错误;C项,3.4gH2O2的物质的量是0.1mol,参加氧化还原反应时,-1价O可能发生自身氧化还原反应(如2H2O2
2H2O+O2),也可能作氧化剂全部被还原(如2Fe2++H2O2+2H+=2Fe3++2H2O),还可以作还原剂被氧化(如2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O),上述三种情况中,只有-1价O的自身氧化还原反应时,3.4g(0.1mol)H2O2反应转移电子数为0.1NA,而另外两种情况,3.4g(0.1mol)H2O2反应转移电子数为0.2NA,故C错误;D项,1molCCl4含有共价键数目为0.4NA,而标准状况下CCl4不是气体,所以标准状况下2.24LCCl4物质的量应大于1mol,含有共价键数目肯定大于0.4NA,故D错误。
点睛:
本题考查阿伏伽德罗常数的应用,该类试题知识覆盖面广,能较好的考查学生对知识的掌握情况,所以几乎是高考必考题。
本题的解题要点为阿伏伽德罗常数有关计算,该部分内容要求学生掌握微粒的构成关系(原子、分子、离子、电子、质子,化学键等数目)、气体体积换算、化学反应中电子的转移等内容,要注意特殊物质的摩尔质量、气体摩尔体积的使用条件、歧化反应中的电子转移等。
如A项,H218O与D2O的相对分子质量都是20;B项,注意溶剂水中的氧原子;C项,H2O2中的-1价O可能发生歧化反应,也可能都被氧化或都被还原;D项,注意标准状况下CCl4是液体,不符合气体摩尔体积的使用条件。
4.W、X、Y、Z是原子序数依次增大的四种短周期主族元素。
其中X、Y为金属元素,W和Z同主族。
Z的核外电子数是W的2倍,W和Z的质子数之和等于X和Y的质子数之和。
下列说法不一定正确的是
A.原子半径:
X>Y>Z>W
B.Y位于第三周期第ⅢA族
C.W和X组成的化合物为碱性氧化物
D.向W、X、Y组成的化合物水溶液中滴入稀盐酸至过量,溶液先变浑浊后澄清
5.下列实验过程中的相关步骤正确的是
选项
实验
操作
A
检验Fe(NO3)2晶体是否变质
将样品溶于稀硫酸,滴入几滴KSCN溶液
B
验证Mg(OH)2和Fe(OH)3的Ksp大小
取2mL1.0mol/LNaOH溶液,先滴3滴1.0mol/LMgCl2溶液,再滴3滴1.0mol/LFeCl3溶液
C
比较醋酸和碳酸酸性强弱
pH计分别伸入0.1mol/LCH3COONa溶液和0.1mol/LNa2CO3溶液中,读取pH
D
测定中和反应反应热
混合前分别用冲洗干净的温度计测量50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液的温度
【答案】D
【解析】A项,将Fe(NO3)2样品溶于稀硫酸后,H+和NO3-同时存在的溶液具有强氧化性,亚铁离子被氧化成铁离子,干扰了检验,故A错误;B项,向2mL1.0mol/LNaOH溶液中先滴3滴1.0mol/LMgCl2溶液,会生成Mg(OH)2白色沉淀;但由于NaOH过量,再滴3滴1.0mol/LFeCl3溶液时,FeCl3直接与NaOH反应生成Fe(OH)3红褐色沉淀,而不会与沉淀Mg(OH)2反应,所以不存在沉淀的转化问题,故B错误;C项,用测盐溶液pH的方法比较比较醋酸和碳酸酸性强弱,应测定等浓度的CH3COONa溶液和NaHCO3溶液的pH,若测Na2CO3溶液的pH,比较的是醋酸和HCO3-的酸性强弱,故C错误;D项,测定中和反应的反应热,需要测量反应前的初始温度,为保证测量结果准确,温度计应该洁净,所以混合前分别用冲洗干净的温度计测量50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液的温度,故D正确。
6.摩拜单车利用车篮处的太阳能电池板向智能锁中的锂离子电池充电,电池反应原理为:
LiCoO2 + 6C
Li1-xCoO2+LixC6。
示意图如右。
下列说法正确的是
A.充电时,阳极的电极反应式为Li1-xCoO2 +xLi++xe-=LiCoO2
B.该装置工作时涉及到的能量形式有3 种
C.充电时锂离子由右向左移动
D.放电时,正极质量增加
【答案】D
【解析】A项,该锂离子电池反应原理为:
LiCoO2+6C
Li1-xCoO2+LixC6,则充电时,阳极发生失电子的氧化反应,电极反应式为:
LiCoO2-xe-=Li1-xCoO2+xLi+,故A错误;B项,锂离子电池工作时,化学能转化为电能,涉及到2种能量形式之间的转化,故B错误;C项,充电时,阳极生成Li+,Li+向阴极(C极)移动,如图所示右边为C极,所以充电时锂离子由左向右移动,故C错误;D项,放电时,正极发生得电子还原反应,电极反应式为:
Li1-xCoO2+xLi++xe-=LiCoO2,所以正极质量增加,故D正确。
7.常温时,若Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线如图所示(已知
=0.58)。
下列分析不正确的是
A.a点表示Ca(OH)2与CaWO4均未达到溶解平衡状态
B.饱和Ca(OH)2溶液和饱和CaWO4溶液等体积混合:
c(OH-)>c(H+)>c(Ca2+)>c(WO42-)
C.饱和Ca(OH)2溶液中加入少量Na2O,溶液变浑浊
D.石灰乳与0.1mol/LNa2WO4溶液混合后发生反应:
Ca(OH)2+WO42-=CaWO4 +2OH-
【答案】B
【解析】A项,如图,为Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线,曲线上的点都代表平衡状态,则Ksp[Ca(OH)2]=c(Ca2+)•c2(OH-)=10-7,Ksp(CaWO4)=c(Ca2+)•c(WO42-)=10-10,a点的浓度商Q[Ca(OH)2]=c(Ca2+)•c2(OH-)=10-18小于Ksp[Ca(OH)2],Q(CaWO4)=c(Ca2+)•c(WO42-)=10-12小于与Ksp(CaWO4),所以a点表示Ca(OH)2与CaWO4均未达到溶解平衡状态,故A正确。
B项,设饱和Ca(OH)2溶液中,c(Ca2+)=x,则c(OH-)=2x,根据Ksp[Ca(OH)2]=c(Ca2+)•c2(OH-)=10-7,则x•(2x)2=10-7,解得x=
;设饱和CaWO4溶液中,c(Ca2+)=y,则c(WO42-)=y,根据Ksp(CaWO4)=c(Ca2+)•c(WO42-)=10-10,则y2=10-10,解得y=10-5;混合时:
c(Ca2+)=
(
)≈
=
=
,c(OH-)=
,c(H+)=
=0.29×10-12,c(WO42-)=
×10-5,Q(CaWO4)=c(Ca2+)•c(WO42-)=
×
×10-5大于Ksp(CaWO4),所以混合后会析出CaWO4,但是溶液中减小的c(Ca2+)=c(WO42-)肯定会小于
×10-5,所以沉淀后溶液中c(Ca2+)还是10-2级别,根据Ksp(CaWO4)=10-10可推出c(WO42-)是10-8级别,而前面已求得c(H+)=0.29×10-12。
综上分析,c(OH-)>c(Ca2+)>c(WO42-)>c(H+),故B错误。
C项,Na2O和水反应使水减少,饱和Ca(OH)2溶液中,Q[Ca(OH)2]>Ksp[Ca(OH)2],析出Ca(OH)2固体,所以溶液变浑浊,故C正确。
D项,由前面的分析可知CaWO4比Ca(OH)2更难溶,所以石灰乳与0.1mol/LNa2WO4溶液混合后,会发生反应Ca(OH)2+WO42-=CaWO4+2OH-,实现沉淀的转化,故D正确。
点睛:
本题考查沉淀溶解平衡曲线,解题思路为:
①明确横纵坐标的含义;②理解曲线上的点、线外的点的含义;③抓住Ksp的特点,结合选项分析判断。
注意本题中横纵坐标不是直接用离子浓度表示的,而是用离子浓度的负对数表示的,所以横纵坐标数值越大,表示的离子浓度越小;B项,因为含Ca(OH)2的溶液显碱性,c(H+)不可能大于c(Ca2+),所以比较容易就能判断该项是错误的,但是要确定c(H+)与c(WO42-)的大小关系,最好通过计算来判断,因为两饱和溶液等体积混合后可能析出CaWO4,溶液中c(WO42-)会很小。
第II卷(非选择题)
8.某化学小组欲进行如下实验探究金属与浓硫酸反应。
试回答下列问题。
(1)利用上图装置研究铜与浓硫酸反应,反应化学方程式为_________;B装置的目的是______;x溶液为___________。
(2)将上述实验中的铜改为黄铜(铜锌合金),实验后阶段可观察到倒立漏斗边缘有气体冒出,且越来越快。
该气体可能为____,气体产生越来越快的原因可能是_____(至少两点)。
验证该气体的实验方案如下:
①装置连接顺序:
x→_________;
②能证明上述假设成立的实验现象是__________。
(3)取少量镁粉加入盛浓硫酸的烧杯,在通风橱中实验。
充分反应后溶液中有灰白色悬浮物,设计方案研究该悬浮物的组成,请帮助完善。
(假设镁的化合物都溶于稀酸)
_____
写出产生该灰白色悬浮物主要反应的化学方程式_____。
【答案】Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O检验产物SO2NaOH溶液(其他合理答案均可得分)H2反应后期,c(H+)增大,与Zn反应生成H2 速率加快;黄铜为铜锌合金,与硫酸形成原电池产生H2 速率加快;反应放热c→d→e→f→a→b→gE中(硬质玻璃管)黑色粉末变红,H中(球形干燥管)固体由白色变为蓝色
3Mg+4H2SO4(浓)==3MgSO4+S+4H2O
【解析】
(1)浓硫酸具有强氧化性,在加热条件下与Cu反应生成CuSO4、SO2和H2O,故化学方程式为:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;二氧化硫具有漂白性,可以使品红溶液褪色,常用品红溶液来检验二氧化硫气体;二氧化硫是有毒气体且为酸性气体,C为尾气吸收装置,故x溶液可以是NaOH溶液。
(2)若将上述实验中的铜改为黄铜(铜锌合金),实验后阶段浓硫酸变稀,与锌反应会产生氢气,所以实验后阶段可观察到倒立漏斗边缘有气体冒出,且越来越快,该气体可能为H2;根据影响化学反应速率的因素,结合该实验原理及条件,气体产生越来越快的原因可能是:
反应后期,浓硫酸变为稀硫酸,电离程度增大,c(H+)增大,与Zn反应生成H2速率加快;黄铜为铜锌合金,与硫酸形成原电池产生H2速率加快;反应放热等。
①若要验证该气体是氢气,根据可供选择的装置及药品,先除去二氧化硫,再吸水干燥,然后通入灼热的氧化铜,最后检验产物是水,所以装置连接顺序:
x→c→d→e→f→a→b→g。
②若E中(硬质玻璃管)黑色粉末变红,说明生成了铜单质,同时H中(球形干燥管)固体由白色变为蓝色,说明生成了水,由此可证明上述假设成立。
(3)镁与浓硫酸反应,硫酸可能表现酸性和强氧化性,固体生成物可能是含有镁元素、S元素的物质,烧杯中的混合物加水部分溶解,则不溶物可能为含S物质,过滤后可加入有机溶剂(如二硫化碳)溶解,故方案未完成部分可以为:
;产生该灰白色悬浮物主要反应的化学方程式为:
3Mg+4H2SO4(浓)=3MgSO4+S+4H2O。
9.氨为重要化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
A.CH4(g)+H2O(g)
CO(g)+3H2(g)△H=+216.4kJ/mol
B.CO(g)+H2O(g)
CO2(g)+H2(g)△H=-41.2kJ/mol
则反应CH4(g)+2H2O(g)
CO2(g)+4H2(g)△H=_________。
(2)起始时投入氮气和氢气分别为1mol、3mol,在不同温度和压强下合成氨。
平衡时混合物中氨的体积分数与温度关系如下图。
①恒压时,反应一定达到平衡状态的标志是______(填序号);
A.N2和H2的转化率相等B.反应体系密度保持不变
C.
比值保持不变D.
=2
②P1_____P2 (填“>”、“<”、“=”、“不确定”,下同);反应平衡常数:
B点____D点;
③C点H2的转化率____;在A、B两点条件下,该反应从开始到平衡时生成氨气平均速率:
v(A)______ v(B)。
(3)N2H4可作火箭推进剂,NH3和NaClO在一定条件下反应可生成N2H4。
①写出NH3和NaClO 反应生成N2H4的化学方程式__________;
②已知25℃时N2H4水溶液呈弱碱性:
N2H4+H2O
N2H5++OH-K1= 1×10-a;
N2H5++H2O
N2H62++OH-K2=1×10-b。
25℃时,向N2H4水溶液中加入H2SO4,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),应控制溶液pH范围_________(用含a、b式子表示)。
【答案】+175.2kJ/molBC<>66.7%<2NH3+NaClO
N2H4+NaCl+H2O(14-b,14-a)
【解析】
(1)a+b可得反应CH4(g)+2H2O(g)
CO2(g)+4H2(g),根据盖斯定律,△H=+216.4kJ/mol+(-41.2kJ/mol)=+175.2kJ/mol。
(2)①A项,氮气和氢气初始物质的量之比为1:
3,由反应方程式N2+3H2
2NH3可得,氮气和氢气按物质的量之比为1:
3反应,所以N2和H2的转化率是相等的,与是否达到平衡状态无关,故A错误;B项,该反应是一个气体分子数变化的反应,恒压时只要不平衡,气体体积就会发生变化,因为气体总质量不变,所以密度就会不断变化,当密度不变时,说明正逆反应速率相等,平衡不再发生移动,故B正确;C项,氢气是反应物,氨气是生成物,只要不平衡,若氢气减少,则氨气必增多,其比值
就会变化,当比值不变时说明已经处于平衡状态,故C正确;D项,氮气是反应物,氨气是生成物,只要不平衡,若氮气减少,则氨气必增多,其比值
就会变化,当比值不变时说明已经处于平衡状态,但当比值=2时,却不一定不再变化,所以不一定是平衡状态,故D错误。
②合成氨反应是一个气体分子数减小的反应,增大压强有利于平衡正向移动,由图可知,温度相同时,压强为P1时平衡混合物中氨的体积分数小于压强为P2时,所以P1 B点>D点。 ③设c点H2的转化率为α(H2),列三段式得: 因为平衡混合物中氨的体积分数为50%,同温同压下气体体积分数=物质的量分数,所以 ×100%=50%,解得α(H2)≈66.7%。 由图可得,A、B两点平衡混合物中氨的体积分数相同,B点温度和压强均高于A点温度和压强,则在A、B两点条件下,该反应从开始到平衡时生成氨气平均速率: v(A) 溶液pH范围为: (14-b,14-a)。 点睛: 本题综合考查化学反应原理知识,主要涉及盖斯定律的应用、化学平衡图像、平衡状态的判断、转化率有关计算、水溶液中有关离子浓度关系的比较等知识。 注意化学平衡图像的分析方法,通过“定一议二”来控制变量,如定温时分析压强与平衡混合物中氨的体积分数的关系、定压时分析温度与平衡混合物中氨的体积分数的关系;注意列三段式解决转化率有关计算;注意最后小题的解题思路: 控制pH使溶液中离子浓度符合某确定关系,要通过K1和K2的表达式找到c(N2H5+)、c(N2H4)、c(N2H62+)与c(OH-)的关系,再根据Kw表达式进一步求得结果。 10.高锰酸钾常用作消毒杀菌、水质净化剂等。 某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。 试回答下列问题。 (1)配平焙烧时化学反应: □MnO2+□_____+□O2 □K2MnO4+□H2O;工业生产中采用对空气加压的方法提高MnO2利用率,试用碰撞理论解释其原因__________。 (2)滤渣II的成分有_______(化学式);第一次通CO2不能用稀盐酸代替的原因是_________。 (3)第二次通入过量CO2生成MnO2的离子方程式为_________。 (4)将滤液Ⅲ进行一系列操作得KMnO4。 由下图可知,从滤液Ⅲ得到KMnO4需经过_____、______、洗涤等操作。 (5)工业上按上述流程连续生产。 含MnO2a%的软锰矿1吨,理论上最多可制KMnO4___吨。 (6)利用电解法可得到更纯的KMnO4。 用惰性电极电解滤液II。 ①电解槽阳极反应式为____________; ②阳极还可能有气体产生,该气体是__________。 【答案】24 KOH122加压增大了氧气浓度,使单位体积内的活化分子数增加,有效碰撞次数增多,反应速率加快,使MnO2反应更充分Al(OH)3、H2SiO3稀盐酸可溶解Al(OH)3,不易控制稀盐酸的用量3MnO42-+4CO2+2H2O=MnO2↓+2MnO4-+4HCO3-蒸发结晶趁热过滤0.018aMnO42--e-= MnO4-O2 【解析】 (1)MnO2中Mn的化合价为+4价,K2MnO4中Mn的化合价为+6价,O2中O的化合价为0价,生成物中都变成了-2价,根据得失电子守恒(化合价升降总数相等)得: MnO2前面系数为2,O2前面系数为1,K2MnO4前面系数为2;结合流程中焙烧时有KOH参与,所以未知的反应物应为KOH,根据原子守恒,KOH前面系数为4,水前面系数为2,故答案为: 24KOH122。 根据有效碰撞理论,加压可增大氧气浓度,使单位体积内的活化分子数增加,有效碰撞次数增多,反应速率加快,使MnO2反应更充分,所以工业生产中采用对空气加压的方法提高MnO2利用率。 (2)根据流程滤液I主要是K2MnO4溶液,还含有SiO32-和AlO2-等杂质离子,通入CO2发生反应: CO2+H2O+SiO32-=H2SiO3↓+CO32-、CO2+H2O+AlO2-=Al(OH)3↓+CO32-,所以滤渣II的成分有Al(OH)3和H2SiO3;因为第一次通入CO2目之一是生成Al(OH)3,而稀盐酸可溶解Al(OH)3,不易控制稀盐酸的用量,所以第一次通CO2不能用稀盐酸代替。 (3)第二次通入过量CO2生成MnO2,则MnO42-发生自身氧化还原反应,生成MnO2和MnO4-,因为CO2过量,所以还会生成HCO3-,故离子方程式为: 3MnO42-+4CO2+2H2O=MnO2↓+2MnO4-+4HCO3-。 (4)滤液Ⅲ溶质主要是KMnO4与KHCO3,由图可看出,KMnO4溶解度受温度影响变化不大,而KHCO3溶解度,受温度影响变化较大,所以从滤液Ⅲ得到KMnO4需经过蒸发结晶、趁热过滤、洗涤、干燥等操作。 (5)根据Mn元素守恒,含MnO2a%的软锰矿1吨,理论上最多可制KMnO4: 1×a%× ≈0.018a(吨)。 (6)①滤液II主要为K2MnO4溶液,用惰性电极电解得到KMnO4,MnO42-在阳极上失电子发生氧化反应,生成MnO4-,故阳极电极反应式为: MnO42--e-=MnO4-;②溶液中的OH-也可能失电子发生氧化反应,生成氧气,故阳极还可能有O2产生。 11.[化学一选修3: 物质结构与性质]我国具有悠久的历史,在西汉就有湿法炼铜(Fe+CuSO4=Cu+FeSO4),试回答下列问题。 (1)Cu2+的未成对电子数有______个,H、O、S 电负性由大到小的顺序为_______。 (2)在硫酸铜溶液中滴加过量氨水可形成[Cu(NH3)4]SO4蓝色溶液。 ①[Cu(NH3)4]SO4中化学键类型有_______,[Cu(NH3)4]2+ 的结构简式为_______,阴离子中心原子杂化类型为______。 ②氨的沸点远高于膦(PH3),原因是______________。 (3)铁铜合金晶体类型为_____;铁的第三(I3)和第四(I4)电离能分别为2957kJ/mol、5290kJ/mol,比较数据并分析原因________
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 四川 新课 四川省 成都市 届高三 第一次 诊断 检测 化学试题 答案 精品
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
