 云南省食品药品监督管理局关于实施云南省医疗器械经营企业检查.docx
云南省食品药品监督管理局关于实施云南省医疗器械经营企业检查.docx
- 文档编号:5399903
- 上传时间:2022-12-15
- 格式:DOCX
- 页数:13
- 大小:19.96KB
云南省食品药品监督管理局关于实施云南省医疗器械经营企业检查.docx
《云南省食品药品监督管理局关于实施云南省医疗器械经营企业检查.docx》由会员分享,可在线阅读,更多相关《云南省食品药品监督管理局关于实施云南省医疗器械经营企业检查.docx(13页珍藏版)》请在冰豆网上搜索。
云南省食品药品监督管理局关于实施云南省医疗器械经营企业检查
附件1:
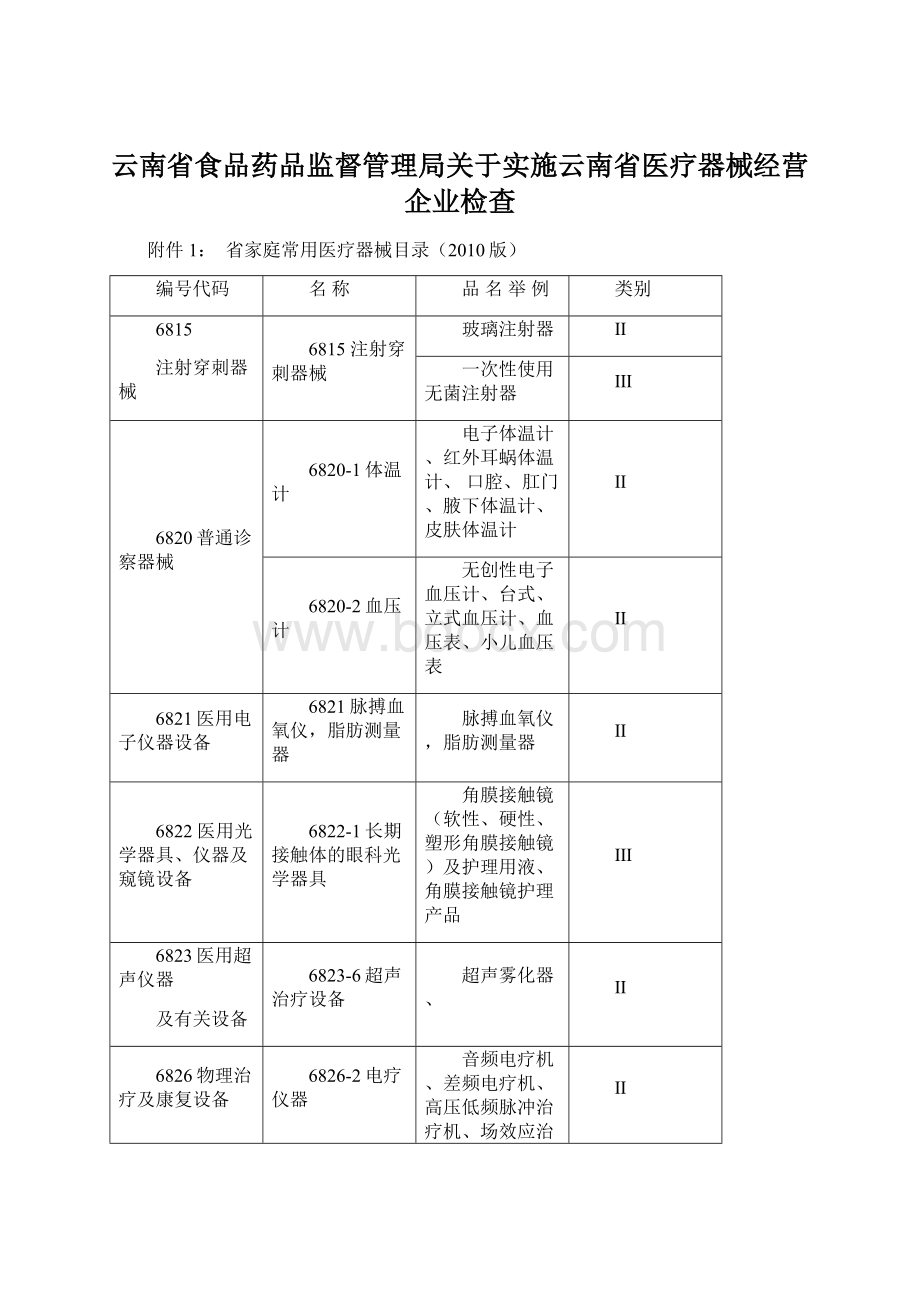
省家庭常用医疗器械目录(2010版)
编号代码
名称
品名举例
类别
6815
注射穿刺器械
6815注射穿刺器械
玻璃注射器
Ⅱ
一次性使用无菌注射器
Ⅲ
6820普通诊察器械
6820-1体温计
电子体温计、红外耳蜗体温计、口腔、肛门、腋下体温计、皮肤体温计
Ⅱ
6820-2血压计
无创性电子血压计、台式、立式血压计、血压表、小儿血压表
Ⅱ
6821医用电子仪器设备
6821脉搏血氧仪,脂肪测量器
脉搏血氧仪,脂肪测量器
Ⅱ
6822医用光学器具、仪器及窥镜设备
6822-1长期接触体的眼科光学器具
角膜接触镜(软性、硬性、塑形角膜接触镜)及护理用液、角膜接触镜护理产品
Ⅲ
6823医用超声仪器
及有关设备
6823-6超声治疗设备
超声雾化器、
Ⅱ
6826物理治疗及康复设备
6826-2电疗仪器
音频电疗机、差频电疗机、高压低频脉冲治疗机、场效应治疗仪(热垫式治疗仪)
Ⅱ
6826-3光谱辐射治疗设备
红外线治疗机、远红外辐射治疗机、光谱治疗仪
Ⅱ
6826-5理疗康复仪器
腰部保健带、非植入式止鼾器、医疗压力带、颈椎固定带、疗疝绷带
Ⅱ
6826-8眼科康复治疗仪器
视力训练仪、弱视治疗仪
Ⅱ
6826-4高压电位治疗设备
高压电位治疗仪
Ⅲ
6827中医器械
6827-1诊断仪器
电麻仪、定量针麻仪、气血循环机
Ⅱ
6827-3中医器具
针灸针、小针刀、三棱针、梅花针
Ⅱ
6840临床检验分析仪器及诊断试剂
诊断试纸条
早早孕检测试剂,排卵检测试条,血糖仪,血糖试纸,尿糖试纸,人绒毛膜促性腺激素诊断试剂
Ⅱ
6841医用化验和基础设备器具
6841-4血液化验设备和器具
采血针
Ⅱ
6846植入材料
和人工器官
6846-5器官辅助装置
助听器
Ⅱ
植入式助听器
Ⅲ
6854
手术室、急救室、
诊疗室设备及器具
6854-8医用制气设备
医用制氧机、手提式氧气发生器
(注:
以上为小型家用)、制氧器耗材,氧气吸入器
Ⅱ
6856病房护理设备及器具
6856-2病床
电动轮椅车、手动轮椅车
Ⅱ
6864医用卫生材料
及敷料
6864-2敷料、护创材料
止血海绵、医用脱脂棉、医用脱脂纱布、脱脂纱布块
Ⅱ
防护产品
防护服、防护口罩、手术口罩、隔离衣、防护帽及防护鞋套、医用口罩、急救包、痤疮治疗笔、疤痕敌
Ⅱ
6863口腔科材料
6863-8齿科预防保健材料
氟防龋材料
Ⅱ
6866
医用高分子材料
及制品
6866-1输液、输血器具及管路
一次性使用输液器、输液针
Ⅲ
6866-3避孕器械
避孕套、避孕帽
Ⅱ
6866-2妇科检查器械
人体润滑剂
Ⅱ
手术手套
无菌医用手套
Ⅱ
附件2:
《医疗器械经营企业许可证》(开办)申请表
企业名称
注册地址
标注使用面积
邮政编码
经营围
二类□三类□
(一)器械类:
□6801、□6802、□6803、□6804、□6805、□6806、□6807、□6808、□6809、□6810、□6812、□6813、□6816、□6820、□6827。
(二)设备、器具类:
□6821(Ⅱ类)、□6822(Ⅱ类)、□6823、□6824、□6825、□6826、□6831、□6834、□6840、□6841、□6845、□6854、□6855、□6856、□6857、□6858。
(三)大型医用设备类:
□6824、□6825、□6828、□6830、□6832、□6833。
(四)植入、介入及人工器官类:
□6821(Ⅲ类)、□6822(Ⅲ类)□6846、□6877。
(五)医用材料类:
□6863、□6864、□6865、□6866(6866-1除外)。
(六)体外诊断试剂类:
□6840。
(七)一次性无菌类:
□6815、□6866。
(八)软件类:
□6870。
(九)验配类:
□角膜接触镜、□助听器、□角膜接触镜及护理液。
(在□打√)
仓库地址标注使用面积
法定代表人
职称
学历
专业
企业负责人
职称
学历
专业
质量管理人
职称
学历
专业
质量管理机构负责人
职称
学历
专业
联系人
手机
座机
传真
电子
职工总数
质量管理人数
技术人员数
设施设备
仓储设施设备
验收养护仪器设备
进销存管理软件名称
计算机配备总量:
台
购进记录用
销售记录用
入库验收用
出库复核用
法定代表人签字(公章):
联系:
日期:
年月日
被委托人签字:
联系:
日期:
年月日
附件3:
《医疗器械经营企业许可证》(换证)申请表
企业名称
注册地址
标注使用面积
邮政编码
经营围
二类□三类□
(一)器械类:
□6801、□6802、□6803、□6804、□6805、□6806、□6807、□6808、□6809、□6810、□6812、□6813、□6816、□6820、□6827。
(二)设备、器具类:
□6821(Ⅱ类)、□6822(Ⅱ类)、□6823、□6824、□6825、□6826、□6831、□6834、□6840、□6841、□6845、□6854、□6855、□6856、□6857、□6858。
(三)大型医用设备类:
□6824、□6825、□6828、□6830、□6832、□6833。
(四)植入、介入及人工器官类:
□6821(Ⅲ类)、□6822(Ⅲ类)□6846、□6877。
(五)医用材料类:
□6863、□6864、□6865、□6866(6866-1除外)。
(六)体外诊断试剂类:
□6840。
(七)一次性无菌类:
□6815、□6866。
(八)软件类:
□6870。
(九)验配类:
□角膜接触镜、□助听器、□角膜接触镜及护理液。
(在□打√)
仓库地址标注使用面积
法定代表人
职称
学历
专业
企业负责人
职称
学历
专业
质量管理人
职称
学历
专业
质量管理机构负责人
职称
学历
专业
联系人
手机
座机
传真
电子
职工总数
质量管理人数
技术人员数
设施设备
仓储设施设备
验收养护仪器设备
计算机(台)
配备总量:
台
购进记录用
销售记录用
入库验收用
出库复核用
涉及变更
事项填写
原核准事项:
申请变更事项:
法定代表人签字(公章):
联系:
日期:
年月日
被委托人签字:
联系:
日期:
年月日
附件4:
《医疗器械经营企业许可证》(变更)申请表
项目
原核准事项
申请变更事项
企业名称
注册地址
标注使用面积
经营围
仓库地址标注使用面积
法定代表人
(号)
企业负责人
(号)
质量管理人
(号)
许可证编号
流水号
发证日期
有效期
联系人
邮政编码
联系
电子
法定代表人签字(公章):
联系:
日期:
年月日
被委托人签字:
联系:
日期:
年月日
附件5:
《医疗器械经营企业许可证》(补证)申请表
企业名称
原经营企业
许可证编号
批准时间
注册地址
标注使用面积
邮政编码
联系人
仓库地址
标注使用面积
电话
传真
补证理由:
企业意见
法定代表人签字
企业盖章
(食品)药品监督管理部门意见
年月日
补证编号
备注
注:
补发的《医疗器械经营企业许可证》不重新编号,并在编号后加“补”字。
附件6:
《医疗器械经营企业许可证》(注销)申请表
企业名称
注册地址
仓库地址
法定代表人
邮编
企业负责人
质量管理人
传真
许可证号
注销原因说明:
企
业
声
明
本企业提交的所有变更资料真实有效,不存在弄虚作假行为,原公司已无任何债权债务,如有弄虚作假行为,由法定代表人承担所引起的法律责任。
法定代表人:
(签名)
日期:
(公章)
食品药品监督管理部门
审查意见:
年月日(公章)
备注
注:
申请表一式二份;
附件7:
省医疗器械经营企业检查验收工作程序
一、受理形式审查要求
1.申报材料应完整、清晰,有签字或盖章,并使用A4纸打印,按照申报材料目录顺序装订成册并标注页码;
2.企业提交的复印件申请人须注明日期,标注“原件与复印件相符”字样并由负责人签字或加盖公章;
3.核对经营企业提交的《医疗器械经营企业许可证》申请表是否有法定代表人或申请人签字或加盖公章,所填写项目是否填写齐全、准确,“经营企业名称”、“注册地址”是否与《工商营业执照》或企业名称核准通知书、房屋产权证相同;
4.核对法定代表人、企业负责人的、学历/职称证明、健康证明、任命文件的有效性;
5.核对工商行政管理部门出具的企业名称核准通知书或《工商营业执照》的有效性。
复印件确认留存,原件退回;
6.核对房屋产权证明、有限期的房屋租赁证明(出租方要提供产权证明)的有效性;
7.核对质量管理人、质量管理机构人员及相关验收、技术培训、售后服务、仓库保管、销售等人员的简历、学历/职称证书、健康证明、《劳动用工合同》、交纳相关社会保障情况的凭证的有效性;复印件确认留存,原件退回;质量管理人三年以上工作经验;
8.核对经营质量管理规文件目录,主要包括管理制度、岗位职责、工作程序等文件;
9.核对申请材料真实性的自我保证声明是否签字或盖章。
二、申请事项处理
药品监督管理部门收到申请后,应当根据下列情况分别作出处理:
1.申请事项依法不属于本部门职权围的,应当即时作出不予受理的决定,并告知申请人向有关行政机关申请;
2.申请事项尚不能确定是否属于本部门职权围的或管理类别尚不确定的,可先接收企业申报材料,并开具《接收申报材料凭证》。
经请示批复后作出是否受理的决定,并通知申请人;
3.申请材料存在可以当场更正的错误的,应当允许申请人当场更正;
4.申请材料不齐全或者不符合形式审查要求的,应当当场或者在5日发给申请人《补正材料通知书》,一次性告知申请人需要补正的全部容,逾期不告知的,自收到申请材料之日起即为受理;
5.申请材料齐全、符合形式审查要求的,或者申请人按照要求提交全部补正申请材料的,予以受理。
受理或者不予受理医疗器械经营企业开办申请的,应当出具加盖本部门受理专用印章并注明日期的《受理通知书》或者《不予受理通知书》。
对出具《受理通知书》的申报材料转入审查环节;
6.医疗器械经营企业申请换证应至少具备开办企业的条件,并在原证有效期届满前6个月,但不少于45个工作日前提出申请。
三、资料审查、现场检查
(一)资料审查要求
1.审查企业质量管理人员是否与所经营产品的要求相适应;
2.审查企业是否具有与所经营产品及经营规模相适应的经营设施设备,经营、仓储场地和环境;
3.审查企业是否设立质量管理机构,并具备与所经营品种和经营规模相适应的质量管理制度。
(二)现场检查
检查容和方法,见《省医疗器械经营企业检查验收记录表》、《省零售药店兼营医疗器械企业检查验收记录表》。
被评定为不合格的项目应有简要的文字说明。
四、处室(科室)领导复审
(一)审核受理和审查工作是否在规定时限完成;
(二)审核受理和审查程序是否符合规定要求;
(三)确认资料审查和现场检查结果。
五、局领导审定
(一)确认复审意见;
(二)签发审定意见。
六、告知
(一)符合《医疗器械经营监督管理办法》和相关规定要求的,予以发证,并公告。
(二)不符合《医疗器械经营监督管理办法》和相关规定要求的,不予发证,并书面说明理由。
(三)作出不予发证决定的,应同时告知申请人享有依法申请行政复议或者提起行政诉讼的权利。
(四)需要听证的,应当向社会公告并举行听证。
七、其他说明
工作程序中受理、审查、现场检查、复审、审定各环节应分段操作,各负职责,互相监督。
现场检查人员由2-3人组成。
检查组组长必须由省局检查员库中人员担任(参加过省局《标准》培训并考核合格的人员)。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 云南省 食品药品 监督 管理局 关于 实施 医疗器械 经营 企业 检查
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
