 与量有关的离子方程式总结.docx
与量有关的离子方程式总结.docx
- 文档编号:5250525
- 上传时间:2022-12-14
- 格式:DOCX
- 页数:6
- 大小:17.32KB
与量有关的离子方程式总结.docx
《与量有关的离子方程式总结.docx》由会员分享,可在线阅读,更多相关《与量有关的离子方程式总结.docx(6页珍藏版)》请在冰豆网上搜索。
与量有关的离子方程式总结
与量有关的离子方程式总结
与量有关的离子方程式的书写技巧:
a.生成物与过量的反应物继续反应的情况:
例:
AlCl3与NaOH(由少到多):
Al3++3OH-→Al(OH)3↓ Al(OH)3+OH-→AlO2-+2H2O
b.滴加顺序不同,离子反应不同:
例:
Na2CO3中逐滴加入HCl:
CO32-+H+→HCO3- HCO3-+H+→H2O+CO2↑
NaOH中逐滴加入AlCl3:
Al3++4OH-→AlO2-+2H2O 3AlO2-+Al3++6H2O→4Al(OH)3↓
c.一种物质中有两种离子参加反应时,反应物用量不同,反应不同。
书写原则:
不足量物质参加反应的离子按组成比参加反应,而过量物质则按需要确定其离子的物质的量。
反应物I
反应物II
滴加顺序
离子方程式
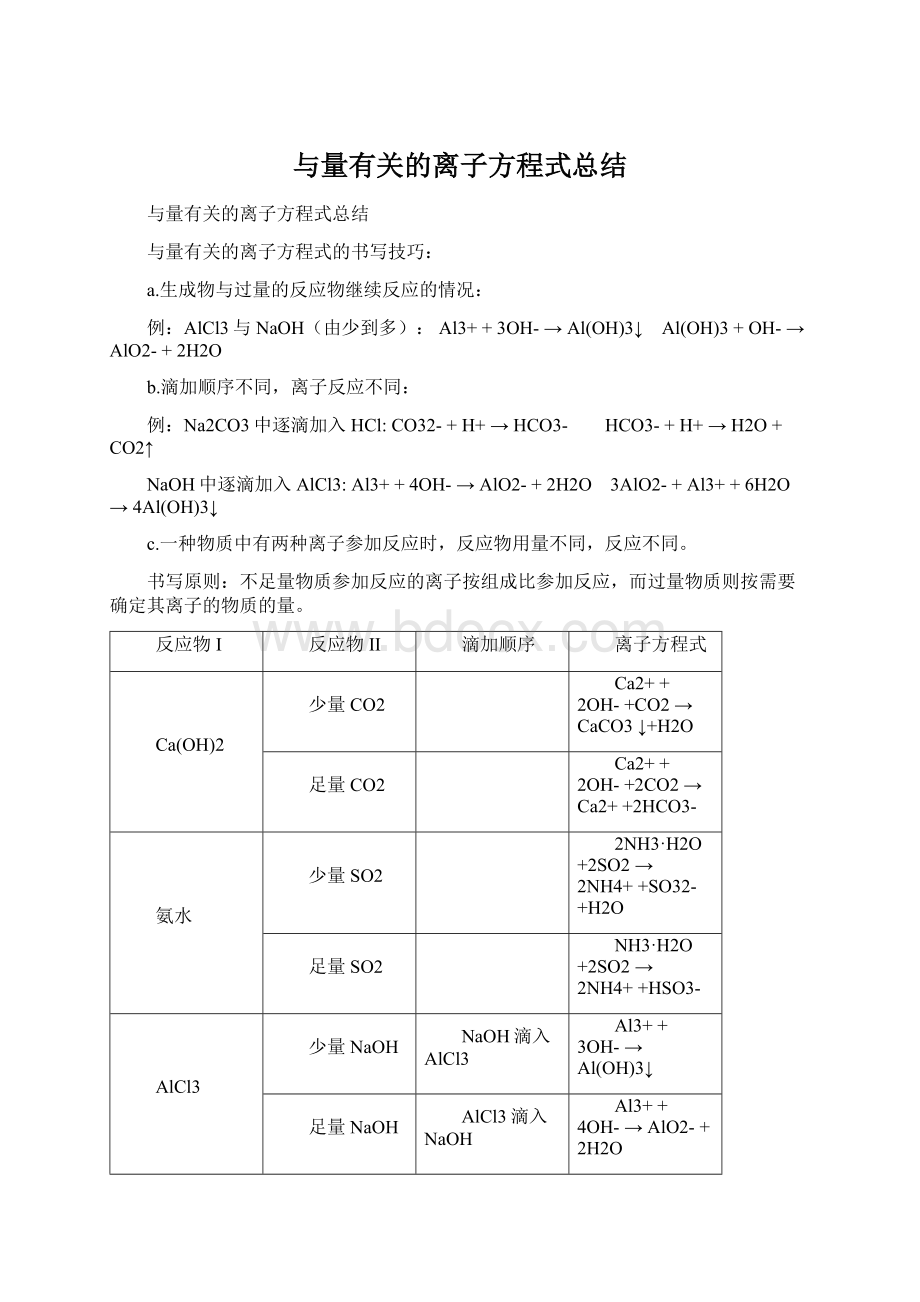
Ca(OH)2
少量CO2
Ca2++2OH-+CO2 →CaCO3↓+H2O
足量CO2
Ca2++2OH-+2CO2 →Ca2+ +2HCO3-
氨水
少量SO2
2NH3·H2O+2SO2→2NH4++SO32-+H2O
足量SO2
NH3·H2O+2SO2→2NH4++HSO3-
AlCl3
少量NaOH
NaOH滴入AlCl3
Al3++3OH-→Al(OH)3↓
足量NaOH
AlCl3滴入NaOH
Al3++4OH-→AlO2-+2H2O
NaAlO2
少量HCl
盐酸滴入NaAlO2
H++AlO2-+H2O →Al(OH)3↓
足量HCl
NaAlO2滴入盐酸
AlO2-+4H+→2H2O+Al3+
FeBr2
少量Cl2
氯水滴入FeBr2
2Fe2++Cl2→2Fe3++2Cl-
足量Cl2
FeBr2滴入氯水
2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl-
Ca(OH)2
少量NaHCO3
NaHCO3滴入石灰水
Ca2++OH-+HCO3-→CaCO3↓+H2O
足量NaHCO3
石灰水滴入NaHCO3
Ca2++2OH-+2HCO3-→CaCO3↓+2H2O+CO32-
Ca(HCO3)2
少量NaOH
NaOH滴入Ca(HCO3)2
Ca2++OH-+HCO3-→CaCO3↓+H2O
足量NaOH
Ca(HCO3)2滴入NaOH
Ca2++2OH-+2HCO3-→CaCO3↓+2H2O+CO32-
AgNO3
少量NH3·H2O
NH3·H2O滴入AgNO3
Ag++NH3·H2O→AgOH↓+NH4+
足量NH3·H2O
AgNO3滴入NH3·H2O
Ag++2NH3·H2O→[Ag(NH3)2]++2H2O
一、生成的产物可与过量的物质继续反应的离子反应
1、向AlCl3溶液中滴入NaOH溶液至过量,其离子反应分步写
(1)Al3++3OH-==Al(OH)3↓
(2)Al(OH)3+OH-==AlO2-+2H2O
2、若向NaOH溶液中滴入AlCl3溶液至过量,其离子反应分步写
(1)Al3++4OH-==AlO2-+2H2O
(2)3AlO2-+Al3++6H2O==4Al(OH)3↓
3、若向AlCl3溶液中加入过量NaOH溶液,其离子反应一步完成
Al3++4OH-==AlO2-+2H2O
4、若向足量Al2(SO4)3溶液中加入少量的NaOH溶液,其离子方程式为
Al3++3OH-==Al(OH)3↓
5、向NaAlO2溶液中滴入盐酸溶液至过量,其离子反应分步写
(1)AlO2-+H++H2O==Al(OH)3↓
(2)Al(OH)3+3H+==Al3++3H2O
6、若向盐酸溶液中滴入NaAlO2溶液至过量,其离子反应分步写
(1)AlO2-+4H+==Al3++2H2O
(2)3AlO2-+Al3++6H2O==4Al(OH)3↓
7、若向NaAlO2溶液中加入过量盐酸溶液,其离子反应一步完成
AlO2-+4H+==Al3++2H2O
8、若向足量NaAlO2溶液中加入少量的盐酸溶液,其离子方程式为
AlO2-+H++H2O==Al(OH)3↓
9、向NaAlO2溶液中通人CO2气体至过量,其离子反应分步写
(1)2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32-
(2)CO32-+CO2+H2O==2HCO3-
10、若向NaAlO2溶液中通人过量CO2气体,其离子反应一步完成
AlO2-+CO2+2H2O==Al(OH)3↓+HCO3-
11、若向足量NaAlO2溶液中通人少量CO2气体,其离子方程式为
2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32-
12、向Na2CO3溶液中滴入盐酸溶液至过量,其离子反应分步写
(1)CO32-+H+==HCO3-
(2)HCO3-+H+==CO2↑+H2O
13、若向盐酸溶液中滴入Na2CO3溶液至不再产生气体,其离子反应一步完成
CO32-+2H+==CO2↑+H2O
14、若向足量Na2CO3溶液中加入少量的盐酸溶液,其离子方程式为
CO32-+H+==HCO3-
15、向NaOH溶液中通人CO2气体至过量,其离子反应分步写
(1)2OH-+CO2==CO32-+H2O
(2)CO32-+CO2+H2O==2HCO3-
16、若向NaOH溶液中通人过量CO2气体,其离子反应一步完成
OH-+CO2==HCO3-
17、若向足量NaOH溶液中通人少量CO2气体,其离子方程式为
2OH-+CO2==CO32-+H2O
二、酸式盐与”量”有关的离子反应
1、向足量的NaHCO3溶液中逐渐滴入澄清石灰水
化学方程式:
Ca(OH)2+2NaHCO3==2H2O+CaCO3↓+Na2CO3
离子方程式:
Ca2++2OH-+2HCO3-==2H2O+CaCO3↓+CO32-
2、向足量的澄清石灰水中逐渐滴入NaHCO3溶液
化学方程式:
NaHCO3+Ca(OH)2==H2O+CaCO3↓+NaOH
离子方程式:
HCO3-+Ca2++2OH-==H2O+CaCO3↓+OH-
或HCO3-+Ca2++OH-==H2O+CaCO3↓
3、向足量的NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液
化学方程式:
Ba(HCO3)2+2NaHSO4==2H2O+2CO2↑+BaSO4↓+Na2SO4
离子方程式:
2HCO3-+Ba2++2H++SO42-==2H2O+2CO2↑+BaSO4↓
4、向足量的Ba(HCO3)2溶液中逐渐滴入NaHSO4溶液
化学方程式:
NaHSO4+Ba(HCO3)2==H2O+CO2↑+BaSO4↓+NaHCO3
离子方程式:
H++SO42-+HCO3-+Ba2+==H2O+CO2↑+BaSO4↓
5、向足量的Ca(HCO3)2溶液中逐渐滴入NaOH溶液
化学方程式:
NaOH+Ca(HCO3)2==H2O+CaCO3↓+NaHCO3
离子方程式:
OH-+Ca2++HCO3-==H2O+CaCO3↓
6、向足量的NaOH溶液中逐渐滴入Ca(HCO3)2溶液
化学方程式:
Ca(HCO3)2+2NaOH==2H2O+CaCO3↓+Na2CO3
离子方程式:
Ca2++2HCO3-+2OH-==2H2O+CaCO3↓+CO32-
7、向NaHSO4溶液中逐渐滴入Ba(OH)2溶液至沉淀完全
化学方程式:
NaHSO4+Ba(OH)2==H2O+BaSO4↓+NaOH
离子方程式:
H++SO42-+Ba2++OH-==BaSO4↓+H2O
8、向NaHSO4溶液中逐渐滴入Ba(OH)2溶液至中性
化学方程式:
2NaHSO4+Ba(OH)2==2H2O+BaSO4↓+Na2SO4
离子方程式:
2H++2SO42-+Ba2++2OH-==2H2O+BaSO4↓+SO42-
或2H++SO42-+Ba2++2OH-==2H2O+BaSO4↓
若在例8的中性溶液中继续滴加Ba(OH)2溶液,将看到白色沉淀生成,
其离子方程式SO42-+Ba2+==BaSO4↓
9、向足量的NH4HCO3溶液中逐渐滴入NaOH溶液
化学方程式:
NH4HCO3+2NaOH==NH3·H2O+H2O+Na2CO3
离子方程式:
NH4++HCO3-+2OH-==NH3·H2O+H2O+CO32-
10、向NH4HCO3溶液中加入过量NaOH溶液并加热
化学方程式:
NH4HCO3+2NaOH==NH3↑+2H2O+Na2CO3
离子方程式:
NH4++HCO3-+2OH-==NH3↑+2H2O+CO32-
三、发生氧化还原反应而且与“量”和“反应顺序”有关的离子反应
(涉及达人精品课,略过)
四、混合顺序不同,即引起“量”不同,则离子反应也不同
1、向NaOH溶液中逐渐滴入Mg(HCO3)2溶液至沉淀完全
化学方程式:
Mg(HCO3)2+4NaOH==2H2O+Mg(OH)2↓+2Na2CO3
离子方程式:
Mg2++2HCO3-+4OH-==2H2O+Mg(OH)2↓+2CO32-
2、向Mg(HCO3)2溶液中逐渐滴入NaOH溶液至沉淀完全
化学方程式:
2NaOH+Mg(HCO3)2==Mg(OH)2↓+2NaHCO3
离子方程式:
2OH-+Mg2+==Mg(OH)2↓
3、向AgNO3溶液中逐滴加入氨水至沉淀恰好溶解为止
离子方程式:
Ag++NH3·H2O==AgOH↓+NH4+
AgOH+2NH3·H2O==[Ag(NH3)2]++OH-+2H2O
4、向氨水中逐滴加入AgNO3溶液,则发生下列反应
离子方程式:
Ag++2NH3·H2O==[Ag(NH3)2]++2H2O
除生成[Ag(NH3)2]+外,还可生成其它物质。
5、向明矾溶液中逐渐滴入Ba(OH)2溶液使SO42-恰好完全沉淀。
化学方程式:
KAl(SO4)2+2Ba(OH)2==2H2O+2BaSO4↓+KAlO2
离子方程式:
Al3++2SO42-+2Ba2++4OH-==2BaSO4↓+AlO2-+2H2O
6、向Ba(OH)2溶液中逐渐滴入明矾溶液时,当生成的沉淀的物质的量为最大值时,发生下列反应。
化学方程式:
2KAl(SO4)2+3Ba(OH)2==3BaSO4↓+2Al(OH)3↓+K2SO4
离子方程式:
2Al3++3SO42-+3Ba2++6OH-==3BaSO44↓+2Al(OH)3↓
总之,书写与“量”有关的离子方程式时,要具体问题具体分析。
特别是要判断不足的物质是什么,以不足的物质完全反应为根据写出对应的化学反应方程式,再改写成离子方程式,防止出差错。
对有离子参加的氧化还原反应,要注意发生反应的离子的顺序问题。
对有具体要求的反应如“中和”或“沉淀量最大”的离子反应,要根据具体的要求去写离子方程式。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 有关 离子 方程式 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
