 关于化学平衡中转化率的求解问题.docx
关于化学平衡中转化率的求解问题.docx
- 文档编号:4981236
- 上传时间:2022-12-12
- 格式:DOCX
- 页数:5
- 大小:21.91KB
关于化学平衡中转化率的求解问题.docx
《关于化学平衡中转化率的求解问题.docx》由会员分享,可在线阅读,更多相关《关于化学平衡中转化率的求解问题.docx(5页珍藏版)》请在冰豆网上搜索。
关于化学平衡中转化率的求解问题
关于化学平衡中转化率的求解问题
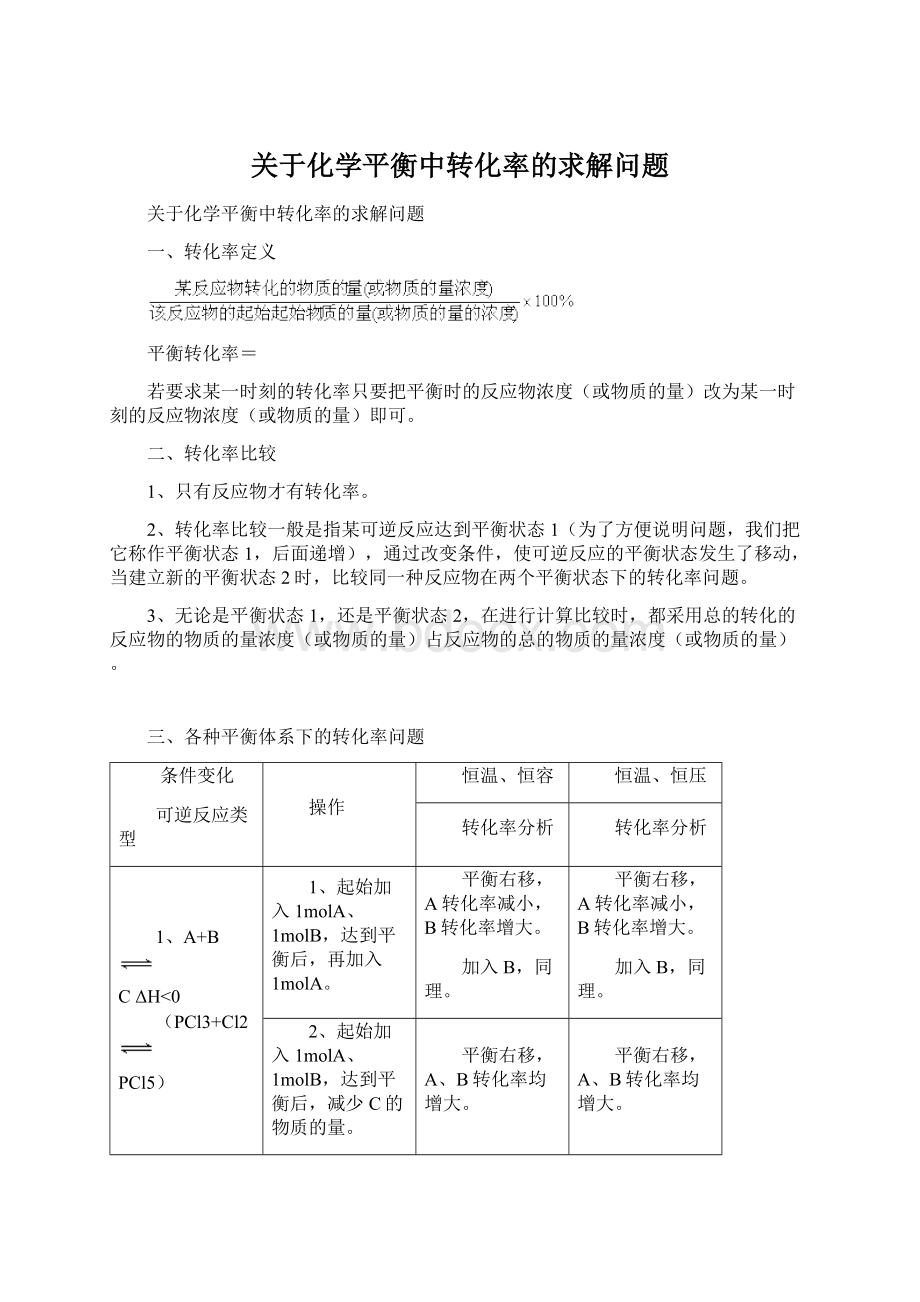
一、转化率定义
平衡转化率=
若要求某一时刻的转化率只要把平衡时的反应物浓度(或物质的量)改为某一时刻的反应物浓度(或物质的量)即可。
二、转化率比较
1、只有反应物才有转化率。
2、转化率比较一般是指某可逆反应达到平衡状态1(为了方便说明问题,我们把它称作平衡状态1,后面递增),通过改变条件,使可逆反应的平衡状态发生了移动,当建立新的平衡状态2时,比较同一种反应物在两个平衡状态下的转化率问题。
3、无论是平衡状态1,还是平衡状态2,在进行计算比较时,都采用总的转化的反应物的物质的量浓度(或物质的量)占反应物的总的物质的量浓度(或物质的量)。
三、各种平衡体系下的转化率问题
条件变化
可逆反应类型
操作
恒温、恒容
恒温、恒压
转化率分析
转化率分析
1、A+B
CΔH<0
(PCl3+Cl2
PCl5)
1、起始加入1molA、1molB,达到平衡后,再加入1molA。
平衡右移,A转化率减小,B转化率增大。
加入B,同理。
平衡右移,A转化率减小,B转化率增大。
加入B,同理。
2、起始加入1molA、1molB,达到平衡后,减少C的物质的量。
平衡右移,A、B转化率均增大。
平衡右移,A、B转化率均增大。
3、起始加入1molA、1molB,达到平衡后,再加入1molA、1molB。
相当于容积可变容器增大压强,平衡右移,A、B转化率均增大。
相当于在容积相同的容器里又建立同一个平衡,平衡右移,A、B转化率均不变。
4、起始加入1molA、1molB,达到平衡后,再加入1molC。
平衡左移,A、B转化率均减小。
A、B浓度增大,体积分数减小。
C的浓度增大,体积分数增大。
加入C的瞬间,C的浓度瞬间增大,A、B浓度不变,平衡左移。
达到新平衡时,A、B、C百分含量不变。
注意:
此种情况下,C无论加多少,都等效于1molA和1molB。
5、起始加入1molA、1molB,达到平衡后,再加入2molA、1molB。
可看成先加入1molA、1molB,然后再加入1molA。
平衡右移,但A的转化率无法确定,B转化率增大。
可看成先加入1molA、1molB(同3),A、B转化率均不变。
然后再加入1molA(同1),A转化率减小,B转化率增大。
6、起始加入2molA、1molB,达到平衡后,再加入3molA、1molB。
同上,先拆成2molA、1molB,然后再加入1molA。
注意:
投入量和起始投入量有关,和化学计量数无关。
同上,先拆成2molA、1molB,然后再加入1molA。
7、起始加入1molA、1molB,达到平衡后,使体系降温。
平衡右移,A、B转化率均增大
平衡右移,A、B转化率均增大
8、起始加入1molA、1molB,达到平衡后,充入不反应气体。
体系内压强增大,但各物质的浓度没有改变,平衡不移动,A、B转化率不变。
体系体积增大,相当于减压,平衡左移。
A、B转化率均减小。
以下可逆反应同上面反应分析方法基本相同,有特殊情况才说明。
2、A+B
2C
3、C
A+B
起始时加入1molC,达到平衡后,再加入1molC。
平衡右移,C的转化率减小,但A、B、C浓度均增大,C体积分数增大,A、B体积分数减小。
平衡右移,但C的转化率不变。
4、2C
A+B
起始时加入2molC,达到平衡后,再加入2,molC。
相当于又有一个4molC的反应和2molC的反应比较,两个平衡等效。
转化率不变。
5、2A+B
C+D
6、A+B
C+D
7、A+B
2C+D
注:
反应中的A、B、C、D均为气体
总结:
(1)对于化学计量数减小的反应,按原物质的量投入反应物,转化率增大;
(2)对于化学计量数不变的反应,按原物质的量投入反应物,转化率不变;
(3)对于化学计量数增大的反应,按原物质的量投入反应物,转化率减小。
四、例题
例1.2NO2
N2O4,反应达到平衡后,再向密闭容器中加入NO2,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,NO2转化率增大。
分析:
该反应可认为后加入NO2与原反应进行叠加,叠加后气体总体积增加,为了使体积维持不变,只能向体系加压从而引起叠加后的平衡向生成N2O4的方向移动。
例2.2NO2
N2O4,反应达到平衡后,再向密闭容器中加入N2O4,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,N2O4向NO2转化的转化率减小。
分析:
该反应可认为后加入NO2与原反应进行叠加,叠加后气体总体积增加(此时,NO2的量会比原来的多,)为了使体积维持不变,只能向体系加压从而引起叠加后的平衡向生成N2O4的方向移动。
【变式练习1】.PCl5
PCl3+Cl2反应达到平衡后,再向密闭容器中加入PCl5,达到平衡后,PCl3的物质的量会,(填“增加”还是“减少”)但是反应达到新的平衡时PCl5物质的量会,(填“增加”还是“减少”)PCl5的转化率(填增大还是减小),PCl5在平衡混合物中的百分含量较原平衡时,(填“增加”还是“减少”)答案:
增加、增加、减小,增加
【变式练习2】.2HI
H2+I2反应达到平衡后,再向密闭容器中加入HI,HI的平衡转化率。
H2的物质的量,I2的物质的量。
答案:
不变,增加,增加
五、练习题
1、在一容积可变的密闭容器中,通入1molX和3molY,在一定条件下发生如下反应:
X(g)+3Y(g)
2Z(g),到达平衡后,Y的转化率为a%,然后再向容器中通入2molZ,保持在恒温恒压下反应,当达到新的平衡时,Y的转化率为b%。
则a与b的关系是()
A.a=bB.a>bC.a<bD.不能确定
2、两个体积相同的密闭容器A、B,在A中充入SO2和O2各1mol,在B中充入SO2和O2各2mol,加热到相同温度,有如下反应2SO2(g)+O2(g)
2SO3(g),对此反应,下述不正确的是()
A.反应速率B>AB.SO2的转化率B>AC.平衡时各组分含量B=AD.平衡时容器的压强B>A
3、一定量混合气体在密闭容器中发生如下反应:
xA(气)+yB(气)
nC(气),达到平衡后,测得A气体的浓度为0.5mol/L。
保持温度不变将容器的容积扩大1倍,再达平衡时,测得A气体的浓度为0.3mol/L,则下列叙述中正确的是()
A、x+y 4、一定温度下,在一个体积可变的密闭容器中加入2molH2和2molN2,建立如下平衡: N2(g)+3H2(g) 2NH3(g)相同条件下,若向容器中再通入1molH2和,1molN2又达到平衡.则下列说法正确的是() A.NH3的百分含量不变B.N2的体积分数增大C.N2的转化率增大D.NH3的百分含量增大 5、某温度下的密闭容器中发生如下反应: 2M(g)+N(g) 2E(g),若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molM和1molN的混合气体,则达平衡时M的转化率为() A.20%B.40%C.60%D.80% 参考答案: 1、A2、C3、D4、A5、C
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 关于 化学平衡 转化 求解 问题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
