 人教版九年级化学第六单元测试题.docx
人教版九年级化学第六单元测试题.docx
- 文档编号:4699594
- 上传时间:2022-12-07
- 格式:DOCX
- 页数:10
- 大小:288.07KB
人教版九年级化学第六单元测试题.docx
《人教版九年级化学第六单元测试题.docx》由会员分享,可在线阅读,更多相关《人教版九年级化学第六单元测试题.docx(10页珍藏版)》请在冰豆网上搜索。
人教版九年级化学第六单元测试题
人教版九年级化学第六单元测试题
姓名:
________班级:
________成绩:
________
一、单选题
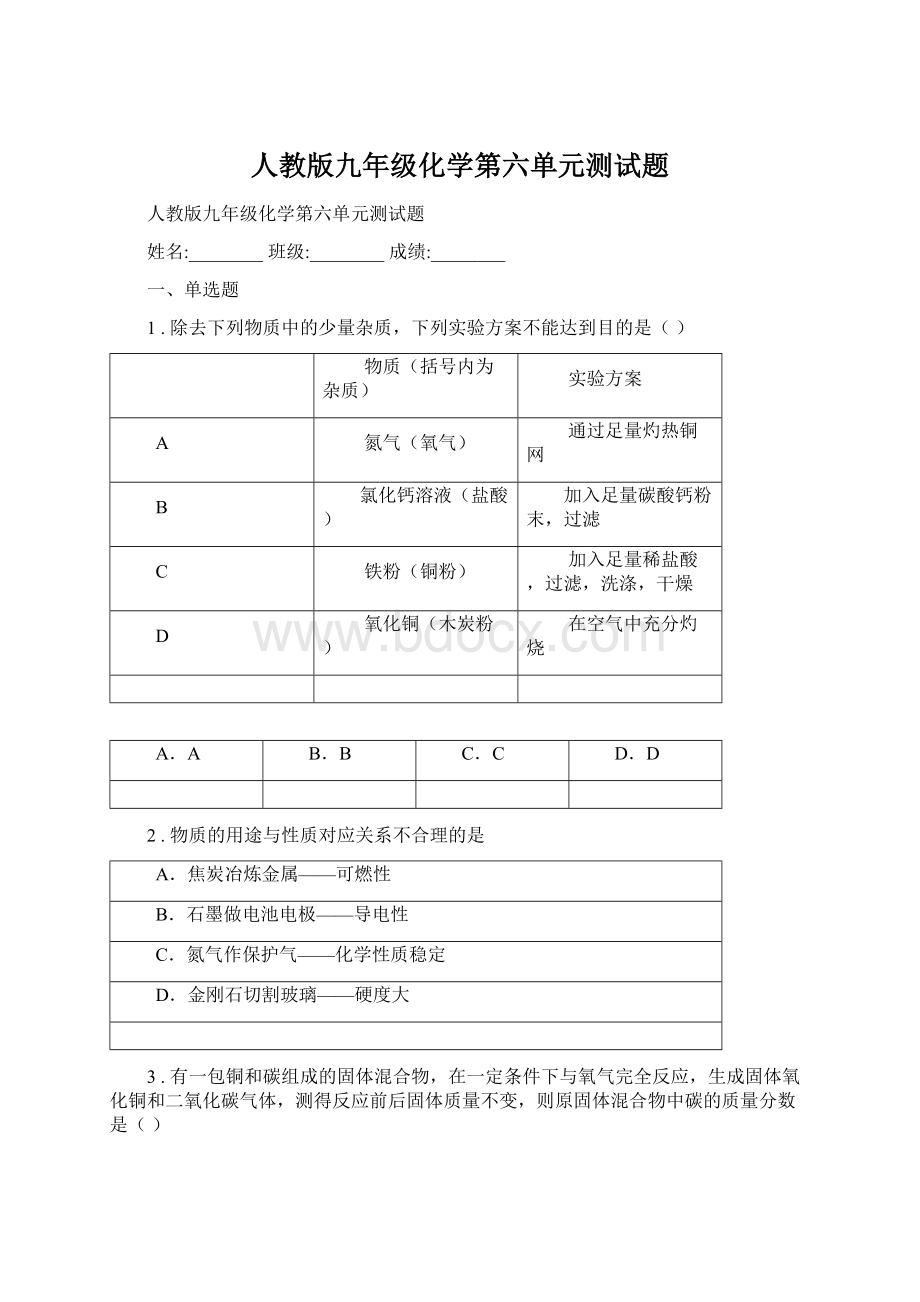
1.除去下列物质中的少量杂质,下列实验方案不能达到目的是()
物质(括号内为杂质)
实验方案
A
氮气(氧气)
通过足量灼热铜网
B
氯化钙溶液(盐酸)
加入足量碳酸钙粉末,过滤
C
铁粉(铜粉)
加入足量稀盐酸,过滤,洗涤,干燥
D
氧化铜(木炭粉)
在空气中充分灼烧
A.A
B.B
C.C
D.D
2.物质的用途与性质对应关系不合理的是
A.焦炭冶炼金属——可燃性
B.石墨做电池电极——导电性
C.氮气作保护气——化学性质稳定
D.金刚石切割玻璃——硬度大
3.有一包铜和碳组成的固体混合物,在一定条件下与氧气完全反应,生成固体氧化铜和二氧化碳气体,测得反应前后固体质量不变,则原固体混合物中碳的质量分数是()
A.15%
B.20%
C.32%
D.无法确定
4.下列做法错误的是
A.
检验装置的气密性
B.
称量氢氧化钠固体
C.
稀释浓硫酸
D.
蒸发结晶
5.下列有关木炭、一氧化碳、甲烷的说法错误的是
A.都可做燃料
B.都是有机化合物
C.都含有碳元素
D.完全燃烧都有CO2生成
6.能鉴别空气、氧气、二氧化碳三瓶气体的方法是()
A.闻气味
B.带火星木条
C.澄清石灰水
D.伸入燃着的木条
7.下列有关氧气的认识,正确的是()
A.在1.01×105Pa,-218.4℃,氧气变为白色的雪花状固体
B.空气中的氧气主要来自于植物的光合作用
C.分离液态空气能制得液氧,说明液氧的沸点比液氮低
D.鱼、虾等能在水中生存,说明氧气易溶于水
8.NO在常温下是一种气体,难溶于水,密度比空气略大,能跟空气中的氧气迅速起反应生成NO2气体.现要收集一瓶NO气体,应采用的收集方法是()
A.只能用排水法
B.向上排空气法
C.排水法或向上排空气法
D.向下排空气法
9.“变废为宝,资源循环,持续发展”是科学家在当今环境问题上的最新构想之一。
例如:
燃料
燃烧产物
燃料,这样既可解决能源问题,又能消除污染。
则上述构想中两个转化过程()
A.均为物理变化
B.①为物理变化,②为化学变化
C.均为化学变化
D.①为化学变化,②为物理变化
10.下表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是
甲
乙
丙
丁
A
Zn
Fe
Cu
CuSO4
B
C
CO
CO2
CaCO3
C
H2O2
H2O
O2
MgO
D
CO2
CaCO3
H2O
O2
A.A
B.B
C.C
D.D
11.除去二氧化碳中混有的少量一氧化碳,应采取的方法是
A.点燃混合气体
B.把混合气体通入澄清的石灰水中
C.把混合气体通过足量的灼热氧化铜
D.把混合气体通入足量的水中
二、填空题
12.化学用语是学习化学的重要工具
(1)写出下列微粒的化学符号:
①2个氢原子 ;②5个硫离子 ;
③3个钙离子 ;④保持氮气化学性质的最小粒子 ;
⑤海洋中含量最高的元素 ;⑥n个铵根离子 。
(2)用下列字母序号填空:
A活性炭 B碳酸 C镁 D二氧化碳 E氧气 F一氧化碳
① 可做冰箱除臭剂;
② 可用于制作照明弹,它在空气中燃烧发出耀眼的白光;
③汽水中含有的一种酸是 ;
④ 可用作温室气体肥料;
⑤供给动植物呼吸的是 ;
⑥有毒的气体是___________。
(3)写出下列反应的文字或符号表达式
①铁丝在氧气中燃烧 ,基本反应类型是______________反应;
②高锰酸钾制氧气_______________________,基本反应类型是______________反应;
③实验室制备二氧化碳的反应__________________________。
13.能源、环境与人类的生活息息相关。
(1)写出天然气燃烧的化学方程式_____
(2)点燃天然气等可燃性气体前,要先_____,以免发生爆炸
(3)液氨有望成为新一代绿色能源。
氨气在纯氧中燃烧,生成空气中含量最多的气体和一种氧化物,同时放出大量热。
写出该反应的化学方程式_____
三、实验题
14.为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计出了下列4种实验装置,请回答下列问题:
(1)选择任意一种实验装置,简述出现的实验现象,解释产生该实验现象的原因:
选择的实验装置是_____________.实验现象为:
_________________.
产生该实验现象的原因是:
_______________________________________________.
(2)某同学质疑上述实验设计,该同学质疑的依据是:
________________________.
(3)在原实验的基础上,请你设计实验证明CO2和NaOH肯定发生了化学反应._________________________.
15.用集气瓶可完成多种实验。
请根据如下实验装置示意图,回答有关问题:
(1)写出仪器①的名称_____________;
(2)实验装置I中进行反应的化学方程式是_____________;
(3)实验室可选用装置II收集氢气的原因是____________;
(4)要达到装置图III所示实验的目的,需在原装置中改进的是_______________;
(5)为确保实验IV能安全进行,你认为在装置IV中加以改进的是_____________。
16.某化学兴趣小组利用如图装置进行有关实验,请按要求填空:
(1)若物质X为CuO,则玻璃管内的实验现象为______。
(2)若物质X为Fe2O3,则玻璃管内发生的化学方程式是______。
(3)实验开始时要先通入CO,后加热目的是______。
(4)该套装置有一处明显的缺陷是______。
(5)某炼铁厂用含杂质20%的赤铁矿(主要成分是氧化铁)冶炼生铁。
求200t这种矿石炼出含杂质4%的生铁______t?
(相对原子质量Fe:
56 O:
16)
四、简答题
17.中国古代文献记载了丰富的化学知识。
(1)我国是最早生产钢铁的国家之一。
“百炼成钢”是指将生铁转化为钢,该过程发生的变化属于___________(填“物理变化”或“化学变化”)。
(2)黑火药是我国的“四大发明”之一,爆炸时发生的主要反应如下,请完成配平(在方框内配上计量数,计量数“1”也要写):
___KNO3+___S+___C
___K2S+___N2↑+___CO2↑。
(3)我国是最早采用湿法冶铜的国家。
文献记载“胆铜法”:
用铁与“胆水”(含CuSO4)反应获得铜。
写出反应的化学方程式:
_______。
(4)古诗“投泥泼水愈光明”:
在高温条件下,炭与水蒸气反应得到一氧化碳和另一种可燃性气体。
写出反应的化学方程式:
_______。
18.据报道,全球每年浪费掉的粮食约有1000亿吨,其中,约300亿吨是加工过的食品。
如图是一包烤花生的图片,图中的脱氧剂在食品防腐保鲜,特别是对延长含高油脂食品的保质期有着重要作用。
请回答下列问题:
(1)脱氧剂的作用原理是脱氧剂中的铁粉与氧气、水发生反应生成氢氧化铁,写出该反应的化学方程式________________,据此判断脱氧剂对食品具有防腐保鲜作用的原因是________(填序号)。
a.脱氧剂具有杀菌、消毒的作用
b.脱氧剂吸收水分,使食品保持干燥
c.脱氧剂吸收氧气,防止食品发生缓慢氧化
(2)铁是应用最广泛的金属材料,写出工业上炼铁原理的化学方程式:
________;
(3)我们日常生活中使用的清洁球,就是用不锈钢丝制作的,最好不要用来擦洗铝锅,其原因是________________。
(4)据统计,我国每年因金属腐蚀造成的经济损失约占国民生产总值的2%—4%,防止金属腐蚀具有重要意义。
答出一种防止金属腐蚀的措施________。
19.“氧循环”、“水循环”和“碳循环”是三大重要循环。
(1)自然界“氧循环”过程中消耗氧气的主要途径是动植物的呼吸和________。
(2)自然界“水循环”的主要变化过程与另外两种循环有本质的区别,从微观角度看,主要原因是:
___________。
(3)自然界“碳循环”的部分循环途径如图所示。
①含碳单质的矿物燃烧的符号表达式为_______;
②海水吸收CO2反应的符号表达式是_________;该反应与绿色植物吸收CO2相比,反应物相同而产物不同的原因是________。
20.南海是中国四大海域中最大、最深、自然资源最为丰富的海域,南海不但资源丰富,还是亚太地区海运的“咽喉要道”,这里有世界上最繁忙的航线,因此引起周边国家的窥视。
(1)海水晒盐属于混合物分离操作的是_____________(填序号);
A.蒸馏
B.蒸发
C.过滤
D.沉淀
(2)南海油气资源丰富,石油加工可得到石油液化气(假设主要成分为C4H10);小明家欲将石油液气灶改为天然气(主要成分为CH4)灶具,他应将空气管口_________(填“增大”或“减小”);
(3)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序是________;
(4)生铁和钢是世界上用量最大的_______(填“金属材料”或“合成材料”)。
五、推断题
21.甲、乙、丙、丁是常见的化合物,它们有如图所示转化关系(部分物质已略去),甲是实验室常用燃料,其相对分子质量为46的有机物;乙是最常见的溶剂;丁是白色难溶固体,可做补钙剂。
则甲的化学式为_____;反应③的化学方程式为_____;试剂A中溶质在生产或生活中的一种用途是_____。
六、计算题
22.常温下,将6克大理石投入100克稀盐酸中,恰好完全反应(大理石中的杂质既不溶于水,也不与酸反应),称得反应后剩余物的质量为103.8克。
问:
(1)碳酸钙中钙元素的质量分数是___________;
(2)反应后生成CO2气体的质量是__________克;
(3)大理石中碳酸钙的质量分数是_______?
(结果精确到0.1%)
参考答案
一、单选题
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
二、填空题
1、
2、
三、实验题
1、
2、
3、
四、简答题
1、
2、
3、
4、
五、推断题
1、
六、计算题
1、
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版 九年级 化学 第六 单元测试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
