 金属及其化合物 单元提纲.docx
金属及其化合物 单元提纲.docx
- 文档编号:4398660
- 上传时间:2022-12-01
- 格式:DOCX
- 页数:13
- 大小:101.71KB
金属及其化合物 单元提纲.docx
《金属及其化合物 单元提纲.docx》由会员分享,可在线阅读,更多相关《金属及其化合物 单元提纲.docx(13页珍藏版)》请在冰豆网上搜索。
金属及其化合物单元提纲
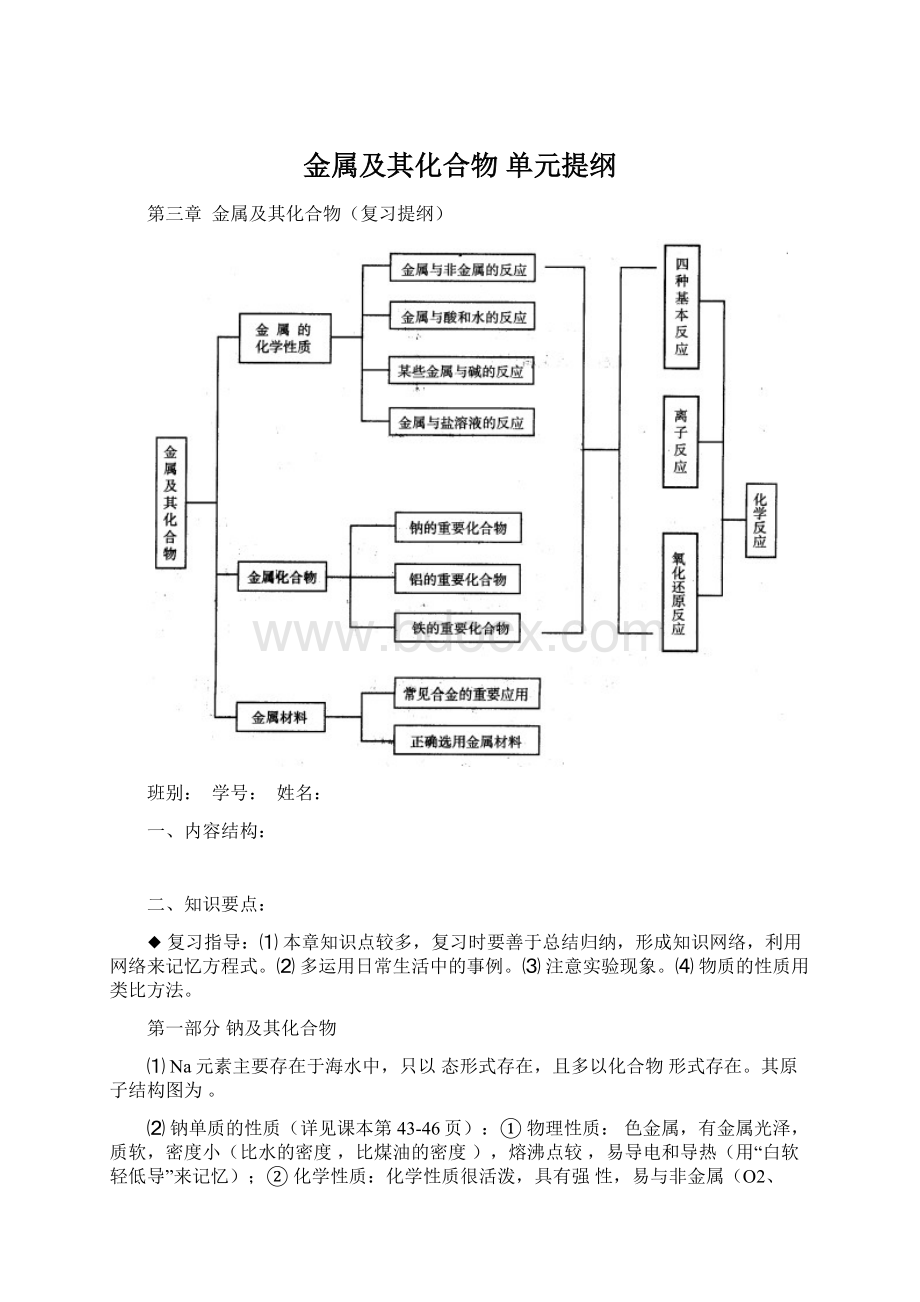
第三章金属及其化合物(复习提纲)
班别:
学号:
姓名:
一、内容结构:
二、知识要点:
◆复习指导:
⑴本章知识点较多,复习时要善于总结归纳,形成知识网络,利用网络来记忆方程式。
⑵多运用日常生活中的事例。
⑶注意实验现象。
⑷物质的性质用类比方法。
第一部分钠及其化合物
⑴Na元素主要存在于海水中,只以态形式存在,且多以化合物形式存在。
其原子结构图为。
⑵钠单质的性质(详见课本第43-46页):
①物理性质:
色金属,有金属光泽,质软,密度小(比水的密度,比煤油的密度),熔沸点较,易导电和导热(用“白软轻低导”来记忆);②化学性质:
化学性质很活泼,具有强性,易与非金属(O2、Cl2)、水和酸溶液反应,钠在反应中只作剂;③保存方法:
钠是危险化学品,须密封保存,实验室中常把钠保存在中(因为钠易与空气和水反应,钠的密度比大,可沉在底部,起到的作用);④灭火方法:
钠等活泼金属着火时,不能用水或泡沫灭火器灭火,须用来灭火;⑤用途:
在核工业上钠可用作传热介质。
在电力工业上用于制钠灯。
⑶氧化钠的性质(详见课本第51页):
①物理性质:
色粉末;②化学性质:
化学性质很活泼,不稳定存在,是一种性氧化物,具有其通性;③保存方法:
Na2O是危险化学品,须密封保存。
⑷过氧化钠的性质(详见课本第51、52页):
①物理性质:
色粉末;②化学性质:
化学性质很活泼,具有强性,易与水和CO2反应,Na2O2在反应中一般既作剂又作剂;③保存方法:
Na2O2是危险化学品,须密封保存;④灭火方法:
Na2O2着火时,不能用或灭火器灭火,须用干燥砂土来灭火;⑤用途:
常用在缺乏空气的场合,如矿井、坑道、潜水、宇宙飞船等方面,以供人们呼吸应急用(即作为呼吸面具使用)。
⑸碳酸钠的性质(详见课本第52页):
①俗名:
和;②物理性质:
色晶体,溶于水(溶解过程会热),粉末遇水生成结晶水合物,晶体在干燥空气里易失水变成粉末;③化学性质:
热稳定性,能使酚酞溶液变,呈性;能与酸反应生成CO2,可与CO2反应生成NaHCO3。
④用途:
食用碱。
⑹碳酸氢钠的性质(详见课本第52页):
①俗名:
;②物理性质:
色晶体,溶于水(溶解度比Na2CO3);③化学性质:
热稳定性,能使酚酞溶液变,呈性;能与酸反应生成CO2,可与碱反应生成Na2CO3。
④用途:
食用碱、发酵粉成分、胃药成分、灭火剂(不能用于活泼金属着火时)等。
⑺Na元素的焰色:
色
第二部分铝及其化合物
⑴Al元素是自然界中分布最广的元素,地壳中铝的含量仅次于和。
通常以态形式存在。
其原子结构图为。
⑵铝单质的性质(详见课本第44、47页):
①物理性质:
色金属,有金属光泽,密度较小,是一种典型轻金属,熔沸点不高,延展性好,易导电和导热,溶于水;②化学性质:
化学性质活泼,具有性,易与非金属(O2、Cl2)反应;可与稀酸(盐酸或稀硫酸)、强碱溶液反应生成盐,同时放出氢气(是一种典型的金属);铝在冷的或中会被钝化,铝在反应中只作剂;③用途:
铝合金因轻硬,不易被腐蚀等优良性能被广泛应用于飞机、汽车、火车、船舶、导弹、宇宙飞船、人造卫星等制造工业;铝还是导线用材(因其性好);铝是制造机器活塞、热交换器、饭锅和电熨斗的理想材料(因其性好);铝易于加工,广泛用于包装香烟、糖果,作易拉罐等。
⑶氧化铝的性质(详见课本第54页):
①物理性质:
溶于水,熔点,硬度,仅次于金刚石和石英砂(碳化硅)(铝不易被腐蚀的原因?
因为表面有Al2O3有效保护地内层金属);②化学性质:
典型的两性氧化物,可溶于也可溶于(铝制品不宜用来蒸煮或长时间存放酸性、碱性或咸的食物);③用途:
自然界存在的α型氧化铝称为刚玉,混有少量杂质可使刚玉带有各种色泽,称为宝石,如红宝石和蓝宝石,可用磨料(因其硬度大)和耐火材料(因其熔点高)。
⑷氢氧化铝的性质(详见课本第54页):
①物理性质:
色絮状物质(所以有吸附性,可作净水剂),溶于水;②化学性质:
是典型的两性氢氧化物,它既能溶于
生成铝盐溶液,又能溶于生成偏铝酸盐溶液;③实验室制法:
用铝盐(硫酸铝)和氨水制备,方程式:
或用偏铝酸盐(偏铝酸钠)和CO2制备,方程式:
;④用途:
净水剂(现在用铁盐取代)和胃酸中和剂(因其碱性)。
第三部分铁及其化合物
⑴Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,常以氧化物形式存在。
⑵铁单质的性质(详见课本第46页):
①物理性质:
银白色金属,纯铁相对较软,有良好的延展性和导热性,能导电,能被磁化,又可去磁;②化学性质:
纯铁化学性质比较活泼,是一种良好的剂,含杂质的铁在潮湿空气里逐渐生锈(易被腐蚀),铁红热时能与水蒸气反应生成和,铁易溶于稀酸中(生成价铁),但在浓硫酸或浓硝酸中由于表面发生钝化而不能溶解,铁加热时能与Cl2反应(生成价铁);③工业制法:
常用焦炭、铁矿石(如赤铁矿:
主要成分是Fe2O3)和石灰石为原料炼得,方程式:
④用途:
炼钢,钢合金是使用最广泛的合金。
⑶氧化物的性质(详见课本第55、56页):
①FeO是色粉末,不稳定,在空气里受热可氧化成,它是一种性氧化物,具有其通性;②Fe2O3是色粉末,俗称,常用作红色油漆和涂料,它是一种性氧化物,具有其通性;③Fe3O4是具有性色晶体,俗称;
⑷氢氧化亚铁的性质(详见课本第56页):
①物理性质:
色粉末;②化学性质:
化学性质很活泼,具有强性,不能在空气中稳定存在,是一种不溶性弱碱,具有其通性;③实验室制法:
现象是先看到色沉淀,迅速变为色,最终变为色,方程式:
⑸氢氧化铁的性质(详见课本第56页):
①物理性质:
色粉末;②化学性质:
能在空气中稳定存在,是一种不溶性弱碱,具有其通性;③实验室制法:
现象是看到色沉淀,方程式:
⑹亚铁盐的性质(详见课本第57页):
①物理性质:
溶液呈色;②化学性质:
具有性,能与剂(如氯水、硝酸等)反应生成铁盐,所以亚铁盐一般容易变质,须密封保存,其水溶液一般现配现用,须加入过量铁粉存放,可与可溶性碱反应生成氢氧化亚铁;③检验方法:
先加入溶液,看不到明显现象,再加入氯水,看到溶液变色,方程式:
⑺铁盐的性质(详见课本第57页):
①物理性质:
溶液通常呈色;②化学性质:
具有性,能与剂(如铁粉、铜等金属)反应生成亚铁盐,可与可溶性碱反应生成氢氧化铁;③检验方法:
加入溶液,看到溶液变色。
第四部分其他知识
⑴焰色反应(详见课本第53页):
很多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这在化学上叫,这一性质可利用来。
在实验室中做焰色反应,必须用洗净的铁丝或铂丝蘸取溶液,在外焰上灼烧(操作方法)。
其中钠元素的焰色是色,钾元素的焰色透过蓝色钴玻璃观察是色。
⑵合金(详见课本第60页):
①定义:
合金是指在金属中加热熔合某些金属或非金属制得具有金属特征的金属材料,它是物;②物理性质:
一般硬度大,延展性好,但熔点于它的成分金属;③常见合金:
铜合金(青铜(我国使用最早的合金)、黄铜、白铜等)、钢合金(碳素钢、合金钢等)、铝合金(硬铝等)
金属和非金属比较
(l)从原子结构来看,金属元素的原子最外层电子数较少,一般小于4;而非金属元素的原子最外层电子数较多,一般大于4。
(2)从化学性质来看,在化学反应中金属元素的原子易失电子,表现出还原性,常做还原剂。
非金属元素的原子在化学反应中易得电子,表现出氧化性,常做氧化剂。
(3)从物理性质来看,金属与非金属有着较多的差别,主要是:
①一般说来金属单质具有金属光泽,大多数金属为银白色;非金属单质一般不具有金属光泽(也有具有金属光泽的,如晶体硅),颜色也是多种多样。
②金属除汞在常温时为液态外,其他金属单质常温时都呈固态;非金属单质在常温时多为气态,也有的呈液态(溴)或固态(碳、硅、碘等)。
③一般说来,金属的密度较大,熔点较高;而非金属的密度较小,熔点较低。
④金属大都具有延展性,能够传热、导电;而非金属没有延展性,不能够传热、导电。
必须明确上述各点不同,都是“一般情况”或“大多数情况”,而不是绝对的。
第三章金属及其化合物(化学反应归纳)
班别:
学号:
姓名:
注意:
在横线上写出对应化学方程式,如是离子反应请再写出离子方程式,如是氧化还原反应请标明氧化剂和还原剂。
一、金属的通性
⑴金属活动性顺序表;、、、、、、
、、、、、、、、
⑵与非金属反应:
Ⅰ与O2反应(大多数金属都会与O2在不同条件反应);
1银白色的钠在空气中会变暗:
2钠在空气中燃烧呈黄色火焰,生成淡黄色固体:
3铁在纯氧中燃烧,火光四射,生成黑色固体:
4金属铝性质活泼,但不易被腐蚀:
5灼热的红铜会变黑:
Ⅱ与Cl2反应
1加热的钠块放入Cl2瓶中,剧烈燃烧,生成白烟:
2加热的铁丝放入Cl2瓶中,剧烈燃烧,生成棕褐色烟:
3加热的铜丝放入Cl2瓶中,剧烈燃烧,生成棕黄色烟:
⑶与水反应(只有很活泼金属才会反应,如钠。
某些金属在高温条件下可反应,但不生成碱)
(规律:
活泼金属+H2O→H2↑+碱)
1金属钠着火时不能用水灭火,是因为:
2往灼热的还原铁粉中通入水蒸气
⑷与非氧化性酸溶液(指盐酸和稀硫酸)反应
(规律:
(排在H前的)金属+H+→H2↑+盐)
1钠与盐酸反应比钠与水反应更剧烈:
2在活性炭粉中混有铝粉,常用盐酸溶液除去:
3在实验室里,要制备不易变质的FeSO4溶液,常用稀硫酸与过量铁粉反应:
4在实验室里,要制备H2常用锌块与稀硫酸反应:
⑸与氧化性酸溶液(指硝酸和浓硫酸)反应
(规律:
大多数金属(除金、铂外)+氧化性酸→盐+水+其他产物)
注意:
和在冷的浓硫酸和浓硝酸中会钝化,没有此类型反应。
1铜与足量浓硫酸混合加热,铜块会全部溶解:
2铜与稀硫酸不反应,但向里面加入KNO3后,铜会逐渐溶解:
3铜与浓硝酸混合,生成红棕色气体:
⑹与盐溶液反应
(规律:
排在前面的金属+后面金属盐→新盐+后面的金属)
注意:
排在Mg前的金属(指、、)不会从盐溶液中置换出弱的金属,它们与盐溶液反应,其实质是先与水反应,产物再与盐反应。
1农药波尔多液(成分CuSO4溶液)不能用铁制容器盛放:
2铝丝伸入AgNO3溶液中,可生成银树:
⑺与FeCl3(指Fe3+)溶液反应
(规律:
金属(除钾钙钠铂金外)+FeCl3→新的金属盐+FeCl2)
1刻印印刷电路(铜箔复合体)时,要用FeCl3溶液作为腐蚀液:
2把铁粉放入过量FeCl3溶液中,铁粉可全部溶解,但无气体放出:
二、碱性氧化物的通性(Na2O、CaO、MgO、CuO、FeO、Fe2O3)
⑴溶于水并与水反应(规律:
碱性氧化物+水→碱)只有Na2O和CaO能发生此反应
1Na2O能与水剧烈反应:
2人们常把生石灰放入石灰池里,再倒入水可见到水蒸气沸腾(此反应放出的热量可煮熟鸡蛋):
⑵与强酸溶液反应(规律:
碱性氧化物+H+→H2O+盐)
1人们常用稀盐酸除掉铁锈:
2SiO2中混有的生石灰,常用盐酸溶液除去:
3活性炭中混有的CuO,常用盐酸溶液除去:
4MgO熔点高,常用作耐火材料,但它不耐酸,常在酸雨地区受到腐蚀:
⑶在高温条件下与酸性氧化物反应(略,见第四章“酸性氧化物的通性”)
⑷与具有还原性的气体(H2、CO)反应(规律:
碱性氧化物+气体→金属+另一产物)
1将氢气流通过灼热的氧化铜,可生成红色物质:
2CO2中混有CO时,常把气体通过灼热的氧化铜除去:
3钢铁工业常用燃烧焦炭不完全生成CO还原赤铁矿(主要成分是Fe2O3)制得生铁:
三、碱的通性
⑴分类:
(写化学式)
1强碱:
、、、(微溶)
2弱碱:
其他的碱(包括氨水)
3可溶性碱:
、、、
4不溶性碱:
其他的碱。
其固体(沉淀)颜色:
红褐色:
,蓝色:
,白色但很快变为灰绿色,最终变成红褐色:
,白色:
⑵与酸碱指示剂反应:
能使紫色石蕊试液或红石蕊试纸变,使无色酚酞试液变
⑶中和反应:
与酸溶液反应(规律:
碱+酸→H2O+盐)
强酸与强碱反应的离子反应:
H++OH ̄=H2O(除Ba(OH)2与H2SO4反应外)
1向滴有酚酞的NaOH溶液加入盐酸,红色会逐渐变红直至消失:
2Ba(OH)2与H2SO4反应:
3做完Fe(OH)3胶体实验的试管会沾有不溶于水的物质,可用稀盐酸溶液洗净:
⑷与酸性气体(Cl2、CO2、SO2等)或酸性氧化物反应:
(规律:
碱+酸性氧化物→H2O+盐)
1将Cl2通入NaOH溶液,可制得漂白液:
2CO中混有CO2时,常把气体通过足量的NaOH溶液以除去:
3制备有毒气体SO2,须把尾气通入足量的NaOH溶液吸收除去,以免污染环境:
4把过量的CO2通入足量的NaOH溶液,可生成小苏打溶液:
⑸可溶性碱与某些盐反应:
(规律:
可溶性碱+某性盐→新盐+不溶性碱)
1在实验室里,要制备Fe(OH)3沉淀,常用FeCl3溶液和NaOH溶液反应:
2在实验室里,要制备Fe(OH)2沉淀,常用FeSO4溶液和NaOH溶液反应:
3在实验室里,要制备Al(OH)3沉淀,常用AlCl3溶液和氨水反应:
4在粗盐提纯中,为除去杂质MgCl2,常加入过量NaOH溶液:
⑸不溶性碱和氨水受热易分解:
(规律:
不溶性碱(氨水)
氧化物(NH3)+H2O)
1洗净Fe(OH)3沉淀后,灼烧可得到红棕色的铁红:
2把Al(OH)3沉淀加热:
3钠与CuSO4溶液反应时,可发现蓝色沉淀周围出现黑色固体:
4在实验室中要制取少量氨气,可用加热浓氨水的方法:
四、钠及其化合物:
⑴钠是很活泼的金属,能与O2在常温下发生反应,所以钠必须保存在煤油中
⑵钠在空气中能剧烈燃烧,必须远离火源放置
⑶在有酚酞的水里加入一小块钠,可以看到“红师傅游泳”
⑷在盐酸里加入一小块钠,可以看到钠剧烈反应,最后消失
⑸Na2O是活泼金属的碱性氧化物,可以与水剧烈反应
⑹Na2O是典型的碱性氧化物,可以与酸剧烈反应
⑺Na2O是典型的碱性氧化物,可以与酸性氧化物反应
⑻Na2O2是钠燃烧后的产物,可以与水剧烈反应
⑼Na2O2可作为呼吸面具中提供氧气的来源
⑽Na2CO3可与一些碱反应生成沉淀,生成NaOH
⑾在NaOH溶液中通入少量的CO2
⑿Na2CO3固体中混有NaHCO3,可采用加热的方法除去
Na2CO3溶液中混有NaHCO3,可滴入适量NaOH溶液以除去
⒀在饱和的Na2CO3溶液通入CO2或在Na2CO3溶液中加入Ca(HCO3)2,可以看到有白色晶体生成
⒁在Na2CO3溶液中加入稀盐酸,可以看到有气泡生成
⒂NaHCO3呈弱碱性,可作为胃药来中和胃酸
五、铝及其化合物:
⑴铝虽然性质活泼,但不像铁易被腐蚀,是因为其表面能生成一层致密的氧化膜
⑵铝制容器不耐酸
⑶铝制容器也不耐碱
⑷Al2O3是一种金属氧化物,能溶于酸溶液
⑸Al2O3是一种典型的两性氧化物,还能溶于强碱溶液
⑹Al(OH)3呈弱碱性,可作为胃药来中和胃酸
⑺Al(OH)3是一种典型的两性氢氧化物,能溶于强碱溶液中
⑻Al(OH)3是一种不溶性碱,加热易分解
⑼实验室里常用AlCl3溶液和氨水来制备Al(OH)3
⑽在实验室里也可往NaAlO2溶液中通入CO2来制备Al(OH)3
注意:
Al3+和AlO2 ̄能发生反应,在溶液中不能大量共存。
六、铁及其化合物:
⑴铁丝在纯氧中加热可生成黑色磁性氧化铁
往灼热的还原铁粉中通入水蒸气
⑵可用铁与稀盐酸反应来制取氢气
⑶加热的铁丝放入Cl2瓶中,剧烈燃烧,生成棕褐色烟
⑷FeO不稳定,但是碱性氧化物,能与酸反应
⑸铁锈是碱性氧化物,可以酸除去
⑹在实验室里,要制备Fe(OH)2沉淀,可用FeCl2溶液和NaOH溶液反应
⑺Fe(OH)2沉淀不能稳定存在于空气中,会从白色转变为灰绿色最后变成红褐色
⑻在实验室里,要制备Fe(OH)3沉淀,常用FeCl3溶液和NaOH溶液反应
⑼Fe(OH)3是一种碱,能与酸反应
⑽Fe(OH)3是不溶性弱碱,受热易分解
⑾Fe2+具有还原性,在FeCl2溶液中加入氯水可反应
⑿FeCl2溶液很容易变质,实验室中常加入铁粉以防变质
七、Na2CO3和NaHCO3比较
碳酸钠
碳酸氢钠
俗名
纯碱或苏打
小苏打
色态
白色晶体
细小白色晶体
水溶性
易溶于水,溶液呈碱性使酚酞变红
易溶于水(但比Na2CO3溶解度小)溶液呈碱性(酚酞变浅红)
热稳定性
较稳定,受热难分解
受热易分解
2NaHCO3
Na2CO3+CO2↑+H2O
与酸反应
CO32 ̄+H+
HCO3 ̄
HCO3 ̄+H+
CO2↑+H2O
HCO3 ̄+H+
CO2↑+H2O
相同条件下放出CO2的速度NaHCO3比Na2CO3快
与碱反应
Na2CO3+Ca(OH)2
CaCO3↓+2NaOH
反应实质:
CO32 ̄与金属阳离子的复分解反应
NaHCO3+NaOH
Na2CO3+H2O
反应实质:
HCO3 ̄+OH ̄=H2O+CO32 ̄
与H2O和CO2的反应
Na2CO3+CO2+H2O
2NaHCO3
CO32 ̄+H2O+CO2
HCO3 ̄
不反应
与盐反应
CaCl2+Na2CO3
CaCO3↓
+2NaCl
Ca2++CO32 ̄
CaCO3↓
不反应
主要用途
玻璃、造纸、制皂、洗涤
发酵、医药、灭火器
转化关系
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 金属及其化合物 单元提纲 金属 及其 化合物 单元 提纲
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
 中国移动网络题库模板无线GSM网络优化.xls
中国移动网络题库模板无线GSM网络优化.xls
 电力工程基础课件-孙丽华-第二版-第7章.ppt
电力工程基础课件-孙丽华-第二版-第7章.ppt
