 届高考化学单元考点复习题5.docx
届高考化学单元考点复习题5.docx
- 文档编号:4271386
- 上传时间:2022-11-28
- 格式:DOCX
- 页数:10
- 大小:118.63KB
届高考化学单元考点复习题5.docx
《届高考化学单元考点复习题5.docx》由会员分享,可在线阅读,更多相关《届高考化学单元考点复习题5.docx(10页珍藏版)》请在冰豆网上搜索。
届高考化学单元考点复习题5
单元测试5物质结构元素周期律
(满分:
100分考试时间:
90分钟)
一、选择题 (共16小题,每小题3分)
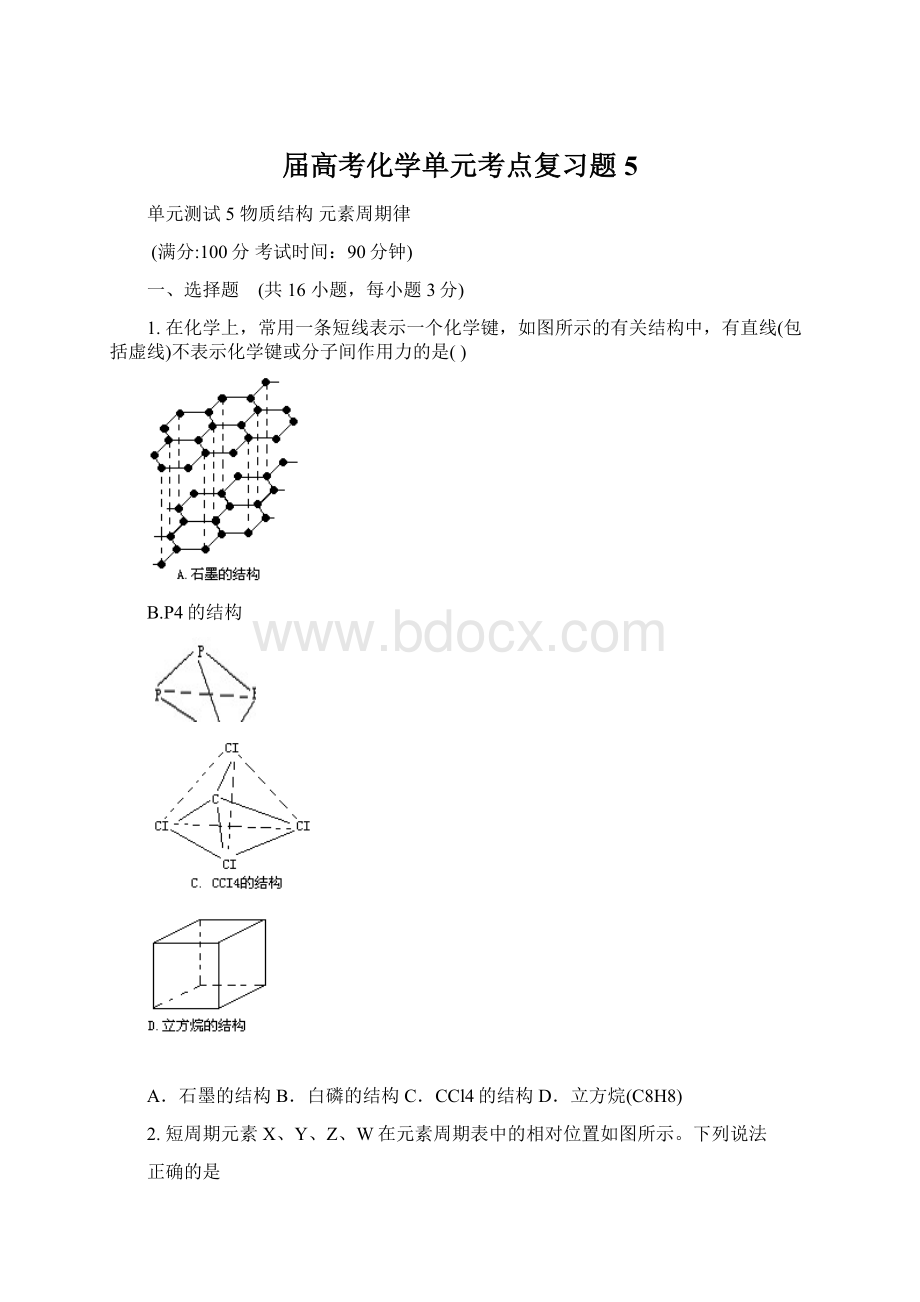
1.在化学上,常用一条短线表示一个化学键,如图所示的有关结构中,有直线(包括虚线)不表示化学键或分子间作用力的是()
B.P4的结构
A.石墨的结构B.白磷的结构C.CCl4的结构D.立方烷(C8H8)
2.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。
下列说法
正确的是
A.元素Z位于元素周期表中第3周期第ⅠA族
B.原子半径的大小顺序为:
rW>rZ>rY>rX
C.Y、W元素的氢化物,其化学式都为H2R
D.离子Y2-和Z3+的核外电子数和电子层数都相同
3.北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60的形成的球碳盐K3C60。
实验测知该物质属于离子晶体,具有良好的超导性。
下列关于K3C60的组成和结构的分析中正确的是
A.K3C60中既有离子键,又有极性键
B.1molK3C60中含有的离子数目为63×6.02×1023
C.该晶体在熔融状态下能导电
D.该物质的化学式可写为KC20
4.35Cl和37Cl是氯元素的两种核素,下列说法正确的是
A.35Cl2与37Cl2互为同分异构体
B.35Cl与37Cl的原子结构示意图不同
C.通过化学变化可以实现35Cl与37Cl间的相互转化
D.常温常压下,1.12LH35Cl与1.12LH37Cl所含原子总数相等
5.下列叙述中,错误的是
A.离子化合物中可能含有非极性键
B.分子晶体中的分子内不含有离子键
C.原子晶体中可能含有非极性键
D.分子晶体中的分子内一定有共价键
6.美国科学家宣称发现了普通盐水在无线电波照射下可燃烧,有望解决用水作人类能源的重 大问题。
无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火, 氢原子就会在该种频率下持续燃烧。
上述中“结合力”实质是
A.分子间作用力 B.氢键 C.非极性共价键 D.极性共价键
7.核电是一种高效能源,也是一种高危能源。
例如会泄露出
,当达一定浓度时,会对人体有伤害。
中质子数比中子数少:
A.131B.53C.25D.78
8.下列有关微粒性质的排序中,正确的是
A.元素的非金属性:
S>Cl>P>Si
B.元素的原子半径:
N C.离子半径: Al3+>Mg2+>Na+ D.沸点: HCl 9.下列判断中一定正确的是 A.若R2-和M+的电子层结构相同,则原子序数: M>R B.若X、Y是同主族气态氢化物,且相对分子质量: X>Y,则沸点: X>Y C.若M、N是同主族非金属元素,且电子层数: M>N,则非金属性: M>N D.若X、Y属于同周期元素,且原子序数: X>Y,则最高正价: X>Y 10.几种短周期元素的原子半径及主要化合价如下表: 元素代号 X Y Z W V 原子半径/nm 0.090 0.118 0.075 0.073 0.102 主要化合价 +2 +3 +5、+3、-3 -2 +6、-2 下列叙述不正确的是 A.X、Z、W位于同周期,Y与V位于同周期 B. 与 的核外电子数相等 C.Y与W形成的化合物具有两性 D.Z的氢化物可与V的最高价氧化物的水溶液反应生成盐 11.已知金属元素X的+1价阳离子最外层有2个电子,该阳离子有6个电子层。 由此推知下列说法中正确的是() A、X元素位于元素周期表的第六周期第ⅣA族B、X元素的还原性比铝元素强 C、X(OH)3和Al(OH)3一样是两性氢氧化物D、离子半径X3+>X+ 12.下列关于Na、Mg、Al、Si、P、S、Cl的比较: ①它们的原子核对最外层电子的引力逐渐减弱;②非金属性逐渐增强,金属性逐渐减弱;③Na、Mg、Al的阳离子氧化性逐渐增强,P、S、Cl的阴离子还原性逐渐减弱;④最高价氧化物对应的水化物碱性逐渐减弱,酸性逐渐增强;⑤只有Al的氧化物、氢氧化物能与HCl、HClO4和NaOH反应;⑥Si、P、S、Cl的氢化物稳定性逐渐减弱。 其中正确的是() A.6句B.5句C.4句D.3句 13.X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z的最外层屯子数是内层电子总数的3倍。 下列有关叙述正确的是 A.X肯定为碱金属元素 B.稳定性: Y的氢化物>Z的氢化物 C.X、Y两元素形成的化合物一定为离子化合物 D.Y、Z两元素形成的化合物熔点较低 14.已知A+.B2+.C-.D2-为同周期主族元素的离子,则下列叙述正确的是 A.离子半径: D>C>B>A B.原子序数: D>C>B>A C.原子半径: A>B>C>D D.最高价氧化物的水化物碱性: A>B,酸性: C>D 15.下表物质与其所含化学键类型、所属化合物类型完全正确的一组是 选 项 A B C D 物 质 CO2 MgCl2 HCl NaOH 所含化学键类型 共价键 离子键、共价键 离子键 离子键、共价键 所属化合物类型 共价化合物 离子化合物 离子化合物 共价化合物 16.下列事实与氢键有关的是() A.水加热到很高的温度都难以分解 B.水结成冰体积膨胀 C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 D.HF、HCl、HBr、HI的热稳定性依次减弱 二、非选择题 (共5小题,共52分) 17.(10分) (1)已知四种短周期元素形成的离子 、 、 、 具有相同的电子层结构。 ①M、N、R、W的原子序数由大到小的顺序是。 ②M、N、R、W的原子半径由大到小的顺序是。 ③ 、 、 、 的离子半径由大到小的顺序是。 (2)原子序数大于4的主族元素A和B的离子分别为 和 已知它们的核外电子排布相同,据此推断: ①A和B所属周期数之差为(填具体数字)。 ②A和B的核电荷数之差为(用含m或n的式子表示)。 ③B和A的族序数之差为。 18.(10分)A+、B+、C-、D、E五种微粒(分子或离子),每个微粒均含有10个电子。 已知: ①A++C- D+E↑②B++C- 2D 请回答以下问题: (1)C-离子含有的化学键为__________________ (2)具有相同空间构型的微粒是__________________和__________________ (3)分别写出A+和D反应,B+和E反应的离子方程式。 A++D: __________________B++E: __________________ 19.(10分)短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中Q所处的周期序数是其主族序数的一半,请回答下列问题: ⑴T的原子结构示意图为_____________。 ⑵原子的得电子能力: Q______W(填“强于”或“弱于”)。 ⑶原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________。 ⑷W的单质与其最高价氧化物对应的水化物的浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_______________。 ⑸R有多种氧化物,其中甲的相对分子质量最小。 在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___________。 20.(12分)X、Y、Z三种短周期元素,它们的原子序数之和为16。 X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: 一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10。 请回答下列问题: (1)X元素在周期表中的位置是_____________________________。 (2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在_____________。 (3)①C在一定条件下反应生成A的化学方程式是__。 ②X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐。 该盐的水溶液pH7(填“大于”、“小于”、“等于”),其原因是(写出离子方程式)。 (4)已知Y单质与Z单质生成C的反应是可逆反应,△H<0。 将等物质的量的Y、Z两种单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。 下列说法正确的有。 a.达到化学平衡时,正反应速率与逆反应速率相等 b.反应过程中,Y单质的体积分数始终为50% c.达到化学平衡时,Y、Z两种单质在混合气体中的物质的量之比为1: 1 d.达到化学平衡的过程中气体平均相对分子质量减小 e.达到化学平衡后,升高温度,C的体积分数增大 21.(12分)X、Y、Z为三种短周期元素,核电荷数依次增大,且X、Y、Z三种元素的原子核外电子层数之和为5。 已知X是原子结构最简单的元素,Y元素原子最外电子层上的电子数是其电子数的2倍、Z元素是植物生长的重要营养元素。 请回答下列问题: (1)推断X、Y、Z的元素: X________,Y_________,Z__________(写元素符号)。 (2)Y元素的单质中有一种称为足球稀的分子Y ,它可能最易发生的反应是______。 A.消去反应B.取代反应C.加成反应D.聚合反应 (3)Z与X可形成多种化合物,其中ZX 的电子式为________________。 (用推断出的X、Z的元素符号表示) (4)最近科学家们合成了由Z元素形成的Z ,电子式为 则n值____________________。 (5)Z的最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙。 ①甲的浓度溶液与Y元素的单质共热的化学反应方程式为_____________________。 ②丙对水的电离起____________作用(填“抑制”、“促进”或“不影响”),原因是(用离子方程式表示)_______________________________; ③在一定条件下,将乙放入固定容积的密闭容器中使其发生分解反应,已知 ,达到平衡状态后,改变其中一个条件X,Y随X的变化符合图中曲线的是___________(选填字母) a.当X表示温度时,Y表示乙的物质的量 b.当X表示压强时,Y表示乙的转化率 c.当X表示反应时间时,Y表示混合气体的密度 (6)若X的单质的燃烧热为MKJ ,试写出其单质在空气中燃烧的热化学方程式: __________________________。 答案 一、选择题 1.C 2.D 3.C 4.D 5.D 6.D 7.C 8.D 9.A 10.B 11.B 12.C 13.D 14.D 15.A 16.B 二、非选择题 17.答案: (1)①N>M>R>W ②M>N>W>R ③ (2)①1②m+n③8-m-n 18. (1)共价键 (2)NH3,H3O+, (3)NH4++H2O≒NH3·H2O+H+.NH3+H3O+= +H2O 19.⑴ ⑵弱于⑶2H2O2 2H2O+O2↑ ⑷S+2H2SO4(浓) 3SO2↑+2H2O⑸NaNO2. 20. (1)第2周期VIA族 (2)氢键 (3)①4NH3+5O2====4NO+6H2O②小于NH4++H2ONH3·H2O+H+ (4)ab 21. (1)HC (2)C(1分) (3) (4)1 (5)① ②促进 ③ab(6) 或其他合理答案
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 单元 考点 复习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
