 专题17离子浓度大小比较三年高考化学试题附解析.docx
专题17离子浓度大小比较三年高考化学试题附解析.docx
- 文档编号:4255754
- 上传时间:2022-11-28
- 格式:DOCX
- 页数:12
- 大小:395.69KB
专题17离子浓度大小比较三年高考化学试题附解析.docx
《专题17离子浓度大小比较三年高考化学试题附解析.docx》由会员分享,可在线阅读,更多相关《专题17离子浓度大小比较三年高考化学试题附解析.docx(12页珍藏版)》请在冰豆网上搜索。
专题17离子浓度大小比较三年高考化学试题附解析
专题17离子浓度大小比较
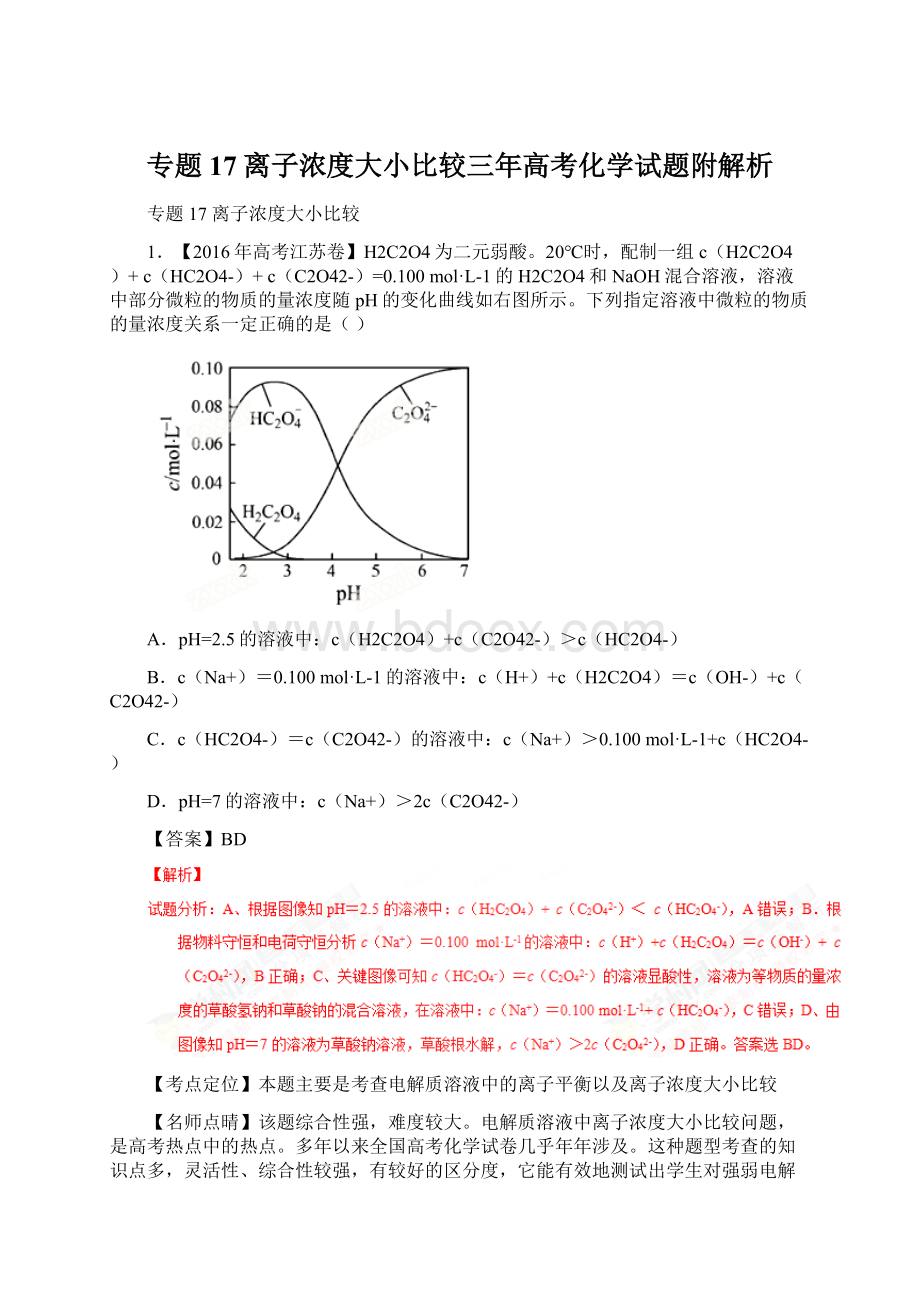
1.【2016年高考江苏卷】H2C2O4为二元弱酸。
20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如右图所示。
下列指定溶液中微粒的物质的量浓度关系一定正确的是()
A.pH=2.5的溶液中:
c(H2C2O4)+c(C2O42-)>c(HC2O4-)
B.c(Na+)=0.100mol·L-1的溶液中:
c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-)
C.c(HC2O4-)=c(C2O42-)的溶液中:
c(Na+)>0.100mol·L-1+c(HC2O4-)
D.pH=7的溶液中:
c(Na+)>2c(C2O42-)
【答案】BD
【考点定位】本题主要是考查电解质溶液中的离子平衡以及离子浓度大小比较
【名师点晴】该题综合性强,难度较大。
电解质溶液中离子浓度大小比较问题,是高考热点中的热点。
多年以来全国高考化学试卷几乎年年涉及。
这种题型考查的知识点多,灵活性、综合性较强,有较好的区分度,它能有效地测试出学生对强弱电解质、电离平衡、水的电离、pH、离子反应、盐类水解等基本概念的掌握程度以及对这些知识的综合运用能力。
围绕盐类水解的类型和规律的应用试题在高考中常有涉及。
解决这类题目必须掌握的知识基础有:
掌握强弱电解质判断及其电离,盐类的水解,化学平衡理论(电离平衡、水解平衡),电离与水解的竞争反应,以及化学反应类型,化学计算,甚至还要用到“守恒”来求解。
解题的关键是运用物料守恒、电荷守恒和质子守恒原理计算相关离子浓度大小。
2.【2016年高考四川卷】向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol 0.015时发生的反应是: 2NaAlO2+CO2+2H2O=2Al(OH)3↓+Na2CO3。 下列对应关系正确的是() 选项 n(CO2)/mol 溶液中离子的物质的量浓度 A 0 c(Na+)>c(AlO2-)+c(OH-) B 0.01 c(Na+)>c(AlO2-)>c(OH-)>c(CO32-) C 0.015 c(Na+)>c(HCO3-)>c(CO32-)>c(OH-) D 0.03 c(Na+)>c(HCO3-)>c(OH-)>c(H+) 【答案】D 【解析】 试题分析: 向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,首先进行的反应为氢氧化钠和二氧化碳反应生成碳酸钠和水,0.02mol氢氧化钠消耗0.01mol二氧化碳,生成0.01mol碳酸钠;然后偏铝酸钠和二氧化碳反应生成氢氧化铝和碳酸钠,0.01mol偏铝酸钠消耗0.005mol二氧化碳,生成0.005mol碳酸钠;再通入二氧化碳,二氧化碳和碳酸钠反应生成碳酸氢钠,消耗0.015mol二氧化碳,生成0.03mol碳酸氢钠。 A、未通入二氧化碳时,根据溶液中的电荷守恒有c(Na+)+c(H+)=c(AlO2-)+c(OH-),c(Na+)<c(AlO2-)+c(OH-),错误;B、当通入的二氧化碳为0.01mol时,则溶液为含有0.01mol碳酸钠和0.01mol偏铝酸钠的混合液,因为碳酸酸性强于氢氧化铝,所以偏铝酸根离子水解程度比碳酸根离子强,则偏铝酸根离子浓度小于碳酸根离子浓度,错误;C、当通入的二氧化碳为0.015mol时溶液中含有0.015mol碳酸钠,离子浓度的关系为c(Na+)>c(CO32-)>c(OH-)c(HCO3-),故错误;D、当通入二氧化碳的量为0.03mol时,溶液为碳酸氢钠溶液,溶液显碱性,离子浓度关系为c(Na+)>c(HCO3-)>c(OH-)>c(H+),故正确。 【考点定位】考查电解质溶液中的离子平衡,钠、铝及其化合物的性质 【名师点睛】本题将元素化合物知识与电解质溶液中离子浓度大小比较综合在一起考查,熟练掌握相关元素化合物知识,理清反应过程,结合相关物质的用量正确判断相关选项中溶液的成分是解题的关键。 电解质溶液中微粒浓度大小比较要抓住两个平衡: 电离平衡和盐类的水解平衡,抓两个微弱: 弱电解质的电离和盐类的水解是微弱的,正确判断溶液的酸碱性,进行比较。 涉及等式关系要注意电荷守恒式、物料守恒式和质子守恒式的灵活运用。 3.【2016年高考天津卷】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是() A.三种酸的电离常数关系: KHA>KHB>KHD B.滴定至P点时,溶液中: c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) C.pH=7时,三种溶液中: c(A-)=c(B-)=c(D-) D.当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) 【答案】C 【解析】 【考点定位】考查中和滴定图像、弱电解质的电离平衡、离子浓度大小比较 【名师点晴】本题考查了酸碱混合时的定性判断、弱电解质的电离平衡、离子浓度大小比较等。 在判断溶液中微粒浓度大小的比较时,要重点从三个守恒关系出发,分析思考。 (1)两个理论依据: ①弱电解质电离理论: 电离微粒的浓度大于电离生成微粒的浓度。 例如,H2CO3溶液中: c(H2CO3)>c(HCO3-)≫c(CO32-)(多元弱酸第一步电离程度远远大于第二步电离)。 ②水解理论: 水解离子的浓度大于水解生成微粒的浓度。 例如,Na2CO3溶液中: c(CO32-)>c(HCO3-)≫c(H2CO3)(多元弱酸根离子的水解以第一步为主)。 (2)三个守恒关系: ①电荷守恒: 电荷守恒是指溶液必须保持电中性,即溶液中所有阳离子的电荷总浓度等于所有阴离子的电荷总浓度。 例如,NaHCO3溶液中: c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)。 ②物料守恒: 物料守恒也就是原子守恒,变化前后某种元素的原子个数守恒。 例如,0.1mol·L-1 NaHCO3溶液中: c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol·L-1。 ③质子守恒: 由水电离出的c(H+)等于由水电离出的c(OH-),在碱性盐溶液中OH-守恒,在酸性盐溶液中H+守恒。 例如,纯碱溶液中c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)。 质子守恒的关系式也可以由电荷守恒式与物料守恒式推导得到。 解答本题时,能够从图像的起始点得出三种酸的相对强弱是解题的关键。 4.【2015浙江理综化学】40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如下图所示。 下列说法不正确的是() A.在pH=9.0时,c(NH4+)>c(HCO )>c(NH2COOˉ)>c(CO32-) B.不同pH的溶液中存在关系: c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COOˉ)+c(OHˉ) C.随着CO2的通入, 不断增大 D.在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成 【答案】C 【解析】A、在pH=9.0时,作直线垂直于横坐标,从图上可直接看得出: c(NH4+)>c(HCO )>c(NH2COOˉ)>c(CO32-),A正确;B、根据电荷守恒可得: c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COOˉ)+c(OHˉ),B正确;C、 = ,Kb不变,c(NH4+)不断增大,则比值不断减小,C不正确;D、从图上看,pH降低过程中,有含NH2COOˉ的中间产物生成,D正确。 答案选C。 【考点定位】本题主要是考查电解质溶液中离子浓度大小关系,电荷守恒关系,图像分析应用等。 【名师点晴】本题从知识上考查了电解质溶液。 涉及弱电解质的电离和盐类的水解、离子浓度的大小比较、外加各类物质对电离平衡、水解平衡的影响。 在比较离子浓度的大小关系时经常要用到物料守恒、电荷守恒、质子守恒这三大守恒关系。 考察了学生对知识理解、综合运用能力,对离子浓度大小的比较的方法积三大守恒的掌握情况。 这道高考题为一道中档题,创新性较强。 5.【2015四川理综化学】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。 下列关于滤液中的离子浓度关系不正确的是() A. <1.0×10-7mol/L B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) C.c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-) D.c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-) 【答案】C 【考点定位】电解质溶液 【名师点睛】电解质溶液中离子浓度大小比较问题,是高考热点中的热点。 多年以来全国高考化学试卷几乎年年涉及。 这种题型考查的知识点多,灵活性、综合性较强,有较好的区分度,它能有效地测试出学生对强弱电解质、电离平衡、水的电离、pH、离子反应、盐类水解等基本概念的掌握程度以及对这些知识的综合运用能力。 围绕盐类水解的类型和规律的应用试题在高考中常有涉及。 考查的重点内容有: 1、弱电解质的电离平衡(主要考查: 电解质、非电解质的判断;某些物质的导电能力大小比较;外界条件对电离平衡的影响及电离平衡的移动;将电离平衡理论用于解释某些化学问题;同浓度(或同pH)强、弱电解质溶液的比较等等。 );2、水的电离程度影响的定性判断与定量计算;3、盐溶液蒸干灼烧后产物的判断;4、溶液中离子浓度大小的比较等。 6.【2015山东理综化学】室温下向10mL0.1mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA溶液pH的变化曲线如图所示。 下列说法正确的是() A.a点所示溶液中c(Na+)>c(A—)>c(H+)>c(HA) B.a、b两点所示溶液中水的电离程度相同 C.pH=7时,c(Na+)=c(A—)+c(HA) D.b点所示溶液中c(A—)>c(HA) 【答案】D 【考点定位】本题通过分析图像的分析、酸碱中和反应进行的程度,结合弱电解质的电离平衡和盐类的水解规律,考查了离子浓度比较、水的电离程度的比较。 【名师点睛】本题难度较大,综合性较强,涉及到电解质水溶液中离子浓度的等量关系、大小关系以及水的电离程度等知识和规律。 解答本题时应正确分析图像,根据酸碱中和反应,分析出溶液的溶质,根据酸碱性和弱电解质的电离平衡和盐类的水解规律,考查了考生灵活运用所学知识解决实际问题的能力。 7.【2015安徽理综化学】25℃时,在10mL浓度均为0.1mol/LNaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是() A.未加盐酸时: c(OH-)>c(Na+)=c(NH3·H2O) B.加入10mL盐酸时: c(NH4+)+c(H+)=c(OH-) C.加入盐酸至溶液pH=7时: c(Cl-)=c(Na+) D.加入20mL盐酸时: c(Cl-)=c(NH4+)+c(Na+) 【答案】B 【考点定位】本题重点考查溶液中水的电离和离子的水解,比较溶液中离子浓度的大小,物料守恒,电荷守恒和质子守恒原理的应用。 【名师点睛】溶液中离子浓度大小比较,是全国高考的热点题型之一,重复率达100%,因为这类题目涉及的知 识点多,难度大,区分度高。 解决这类题目必须掌握的知识基础有: 掌握强弱电解质判断及其电离,盐类的 水解,化学平衡理论(电离平衡、水解平衡),电离与水解的竞争反应,以及化学反应类型,化学计算,甚至还要 用到"守恒"来求解。 解题的关键是运用物料守恒、电荷守恒和质子守恒原理计算相关离子浓度大小。 8.【2015江苏化学】室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是() A.向0.10mol·L-1NH4HCO3溶液中通入CO2: c(NH4+)=c(HCO3-)+c(CO32-) B.向0.10mol·L-1NaHSO3溶液中通入NH3: c(Na+)>c(NH4+)>c(SO32-) C.0.10mol·L-1Na2SO3溶液通入SO2: c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] D.0.10mol·L-1CH3COONa溶液中通入HCl: c(Na+)>c(CH3COOH)=c(Cl-) 【答案】D 【解析】A、两者不反应,根据溶液呈现电中性,c(NH4+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),因为pH=7,c(H+)=c(OH-),即c(NH4+)=c(HCO3-)+2c(CO32-),故错误;B、HSO3- H++SO32-,NH3和H+反应,生成亚硫酸钠和亚硫酸铵,水解的程度是微弱的,c(Na+)>c(SO32-)=c(NH4+),故错误;C、Na2SO3+SO2+H2O=2NaHSO3,pH=7,反应后溶液的溶质Na2SO3、NaHSO3,根据物料守恒: 2c(Na+)=3[c(SO32-)+c(HSO3-)+c(H2SO3)],故错误;D、CH3COONa+HCl=CH3COOH+NaCl,溶液pH=7,反应后的溶质: NaCl、CH3COOH、CH3COONa,电离和水解相等,即: c(Na+)>c(CH3COOH)=c(Cl-),故正确。 【考点定位】考查离子浓度大小比较中电荷守恒、物料守恒等知识。 【名师点睛】涉及离子浓度大小比较,常用规律: 电荷守恒、质子守恒、物料守恒、水解程度和弱电解质电离程度微弱,然后分析反应后溶液中溶质有哪些物质,分析是电离为主还是水解为主,这需要根据题目所给信息进行判断,此类题中等难度,要求学生学会分析问题的能力。 9.【2014年高考海南卷】室温下,用0.l00mol/LNaOH溶液分别滴定20.00mL0.100mol/L的盐酸和醋酸,滴定曲线如图所示。 下列说法正确的是 A.II表示的是滴定醋酸的曲线 B.pH=7时,滴定醋酸消耗的V(NaOH)小于20mL C.V(NaOH)=20.00mL时,两份溶液中c(Cl-)=C(CH3COO-) D.V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>C(CH3COO-)>c(H+)>c(OH-) 【答案】B 【解析】A、相同浓度的盐酸和醋酸,由于盐酸是一元强酸,在水溶液中完全电离,醋酸是一元弱酸,在水溶液中部分电离。 所以溶液的pH醋酸的大,盐酸小。 因此 表示的是醋酸, 表示的是盐酸。 错误。 B、NaOH是强碱,HCl是强酸,当pH=7时,二者恰好反应,物质的量相等,所以n(NaOH)=20ml。 若与醋酸反应的NaOH的体积也是20ml.则得到的是醋酸钠。 醋酸钠是强碱弱酸盐,水解是溶液显碱性,因此若要使pH=7时,则滴加的体积就要少于20ml。 因此滴定消耗的V(NaOH),酸小醋于20mL。 正确。 C、任何溶液都符合电荷守恒。 、质子守恒、物料守恒。 在醋酸溶液中加入20mlNaOH溶液时,醋酸根离子会发生水解反应,所以除了存在醋酸分子外,还存在醋酸根离子。 根据物料守恒,可得c(Cl-)=c(Na+)=C(CH3COO-)+C(CH3COOH)。 错误。 D、V(NaOH)=10.00mL时,得到是醋酸和醋酸钠等浓度的混合溶液。 由于在等浓度、等体积的醋酸与醋酸钠的混合溶液中,醋酸分子的电离作用大于醋酸钠盐的水解作用,所以根据物料守恒和电荷守恒可得: 溶液中C(CH3COO-)>c(Na+)>c(H+)>c(OH-)。 错误。 【考点定位】本题以常见的酸: 盐酸、醋酸与常用的强碱溶液混合时溶液中微粒的浓度变化来通过图像的展示来考查三大守恒、盐的水解作用。 考查了学生的知识掌握、综合分析、灵活应用能力,综合性很强。 【名师点睛】本题考查图像法在酸碱中和滴定中的应用;考查了盐的水解、酸的电离、比较溶液中微粒浓度的大小的三个守恒知识。 解答本题,首先应该掌握物质酸的相对强弱,了解在浓度相同时电离产生的离子浓度的大小。 然后看其与与碱混合发生反应时,酸碱相对物质的量的多少、溶液中的溶质的种类、电解质的电离程度与产生的盐的水解程度的相对大小。 最后对选项中的问题根据题意进行解答。 10.【2014年高考安徽卷第11题】室温下,下列溶液中粒子浓度大小关系正确的是() A.Na2S溶液: c(Na+)>c(HS-)>c(OH-)>c(H2S) B.Na2C2O4溶液中: c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) C.Na2CO3溶液: c(Na+)+c(H+)=2c(CO32-)+c(OH-) D.CH3COONa和CaCl2混合溶液: c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) 【答案】B 【考点定位】本题主要是考查电解质溶液,涉及盐类水解,三大守恒关系的应用 【名师点晴】本题是高考中的热点题型和高频点,侧重对学生灵活应用基础知识解决实际问题的能力培养。 意在考查学生分析问题、解决问题的能力,属于中等难度试题的考查,答题的关键是灵活应用电荷守恒、物料守恒以及质子守恒,题目难度中等。 11.【2014年高考江苏卷第14题】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是() A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合: c(Na+)=c(Cl-)>cCH3COO-)>c(OH-) B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7): c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-) C.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合: c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) D.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸): 2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) 【答案】AC 【解析】A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积恰好反应混合生成醋酸和氯化钠,醋酸电离溶液显酸性,则c(Na+)=c(Cl-)>cCH3COO-)>c(OH-),正确;B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),这说明溶液显碱性,因此氨水的电离程度大于铵根的水解程度,则c(NH4+)>c(Cl-)>c(NH3·H2O)>c(OH-),不正确;C、0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合,则根据物料守恒可知 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),正确;D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸),二者恰好反应生成草酸酸氢钠和氯化钠,则根据电荷守恒可知溶液中2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),不正确。 【考点定位】本题主要是考查溶液中离子浓度的关系判断 【名师点晴】本题以微粒浓度大小的比较、微粒浓度的等式关系判断为载体。 考察学生对溶液中各种平衡的理解和对电荷守恒、物料守恒、质子守恒等等式的应用,考察学生的理论应用能力。 本题的解题要点为溶液中微粒浓度的关系,首先要明确溶液的溶质,存在哪些微粒,存在哪些平衡,多平衡存在时以哪个平衡为主等,然后明确溶液中的电荷守恒、物料守恒、质子守恒等三个等式。 关键是判断溶液中的平衡。 12.【2014年高考四川卷第6题】下列溶液中粒子的物质的量浓度关系正确的是() A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中: c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) B.20ml0.1mol/LCH3COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中: c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中: c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中: c(OH-)>c(H+)+c(CH3COOH) 【答案】B 【考点地位】本题主要是考查水溶液中的离子平衡以及溶液中离子浓度大小比较 【名师点晴】本题属于溶液中离子平衡方面的考查,侧重于弱电解质的电离及盐类水解,题目难度较大。 该类试题重点考查了学生对知识理解、综合运用能力,对离子浓度大小的比较的方法及三大守恒的掌握情况。 意在考查学生分析、归纳、总结问题的能力。 选项C是易错点,注意反应后酸碱过量问题的判断。 13.【2014年高考天津卷第5题】下列有关电解质溶液中粒子浓度关系正确的是() A.pH=1的NaHSO4溶液: c(H+)=c(SO42-)十c(OH-) B.含有AgCl和AgI固体的悬浊液: c(Ag+)>c(C1-)=c(I-) C.CO2的水溶液: c(H+)>c(HCO3-)=2c(CO32-) D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] 【答案】A 【解析】 试题分析: 根据电解质溶液中的电荷守恒、物料守恒、弱电解质的电离平衡和沉淀溶解平衡规律分析离子浓度关系。 A、根据电荷守恒,pH=1的NaHSO4溶液存在: c(Na+)+c(H+)=2c(SO42‾)+c(OH‾),因为c(Na+)=c(SO42‾),所以c(H+)=c(SO42‾)+c(OH‾),正确;B、含有AgCl和AgI固体的悬浊液: c(Ag+)>c(Cl‾)>c(Br‾),错误;C、H2CO3的第一步电离大于第二步电离,所以c(H+)>c(HCO3‾)>c(CO32‾),但c(HCO3‾)不等于c(CO32‾),错误;D、NaHC2O4和Na2C2O4的物质的量的相等,NaHC2O4根据物料守恒可得: c(Na+)=c(HC2O4-)+c(C2O42-)+c(H2C2O4),Na2C2O4根据物料守恒可得: c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)],所以溶液中2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)],错误。 理解、运用各种守恒规律分析、判断,如NaHC2O4和Na2C2O4分别根据物料守恒得出守恒关系,然后得出正确的结论。 【考点地位】本题主要是考查溶液中离子浓度大小比较,涉及弱电解质的电离、盐类水解、溶解平衡等 【名师点晴】本题通过NaHSO4溶液、AgCl和AgI、CO2的水溶液和含等物质的量的NaHC2O4和Na2C2O4的溶液考查了电荷守恒、物料守恒、弱电解质的电离平衡和沉淀溶解平衡,根据守恒规律进行离子浓度比较,考查了学生运用所学规律解决问题的能力。 选项D是易错点。 14.【2013年高考四川卷第5题】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表: 实验编号 起始浓度/(mol·L-1) 反应后溶液的pH c(HA) c(KOH) ①
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题 17 离子 浓度 大小 比较 三年 高考 化学试题 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
