 硫酸铝钾与氢氧化钡反应.docx
硫酸铝钾与氢氧化钡反应.docx
- 文档编号:418780
- 上传时间:2022-10-09
- 格式:DOCX
- 页数:11
- 大小:151.74KB
硫酸铝钾与氢氧化钡反应.docx
《硫酸铝钾与氢氧化钡反应.docx》由会员分享,可在线阅读,更多相关《硫酸铝钾与氢氧化钡反应.docx(11页珍藏版)》请在冰豆网上搜索。
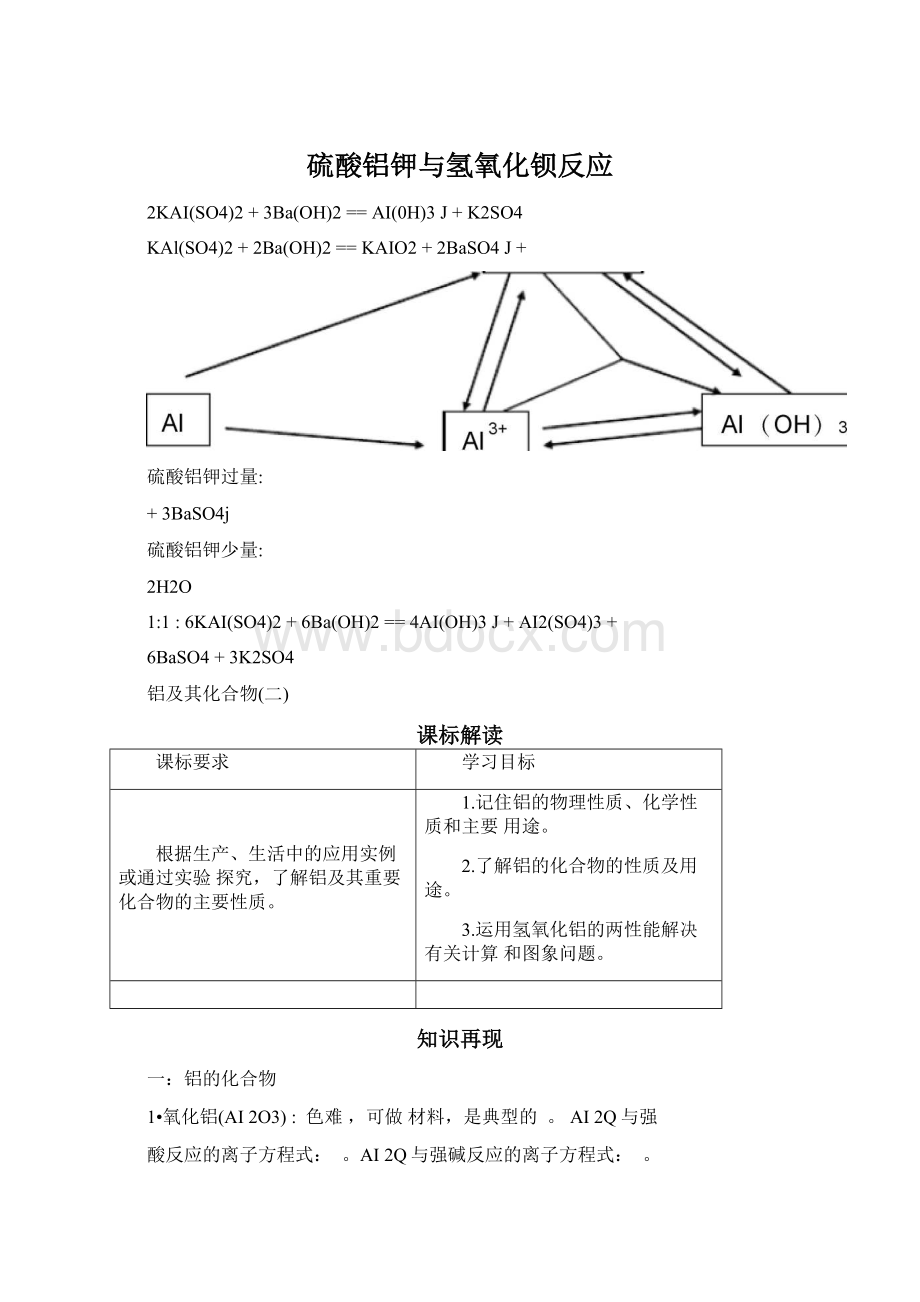
硫酸铝钾与氢氧化钡反应
2KAI(SO4)2+3Ba(OH)2==AI(0H)3J+K2SO4
KAl(SO4)2+2Ba(OH)2==KAIO2+2BaSO4J+
硫酸铝钾过量:
+3BaSO4j
硫酸铝钾少量:
2H2O
1:
1:
6KAI(SO4)2+6Ba(OH)2==4AI(OH)3J+AI2(SO4)3+
6BaSO4+3K2SO4
铝及其化合物
(二)
课标解读
课标要求
学习目标
根据生产、生活中的应用实例或通过实验探究,了解铝及其重要化合物的主要性质。
1.记住铝的物理性质、化学性质和主要用途。
2.了解铝的化合物的性质及用途。
3.运用氢氧化铝的两性能解决有关计算和图象问题。
知识再现
一:
铝的化合物
1•氧化铝(AI2O3):
色难,可做材料,是典型的。
AI2Q与强
酸反应的离子方程式:
。
AI2Q与强碱反应的离子方程式:
。
2.氢氧化铝[AI(OH)3]:
色状物,是典型的。
氢氧化铝的电离方程式:
;当向AI(OH)3中加入强酸时,平衡向移动;当向AI(OH)3中加入强碱时,平衡向移动。
实验室制备AI(OH)3时,选用铝盐和氨水作用而不选氢氧化钠溶液
的原因是。
写出实验室制备氢氧化铝的化学方程式。
O
4.十二水合硫酸铝钾俗名明矶,是色晶体,在水中的电离方程式
;明矶能够净水其离子方程式为
.铝的化合物的相互转化关系,掌握重要的方程式
AI(OH)4
(1)向1LO.1mol/L的氯化铝溶液中逐滴滴加氢氧化钠溶液,写出各步反应的方
程式及离子方程式,并画出生成氢氧化铝的物质的量与所加氢氧化钠的物
质的量的关系图像。
,
(2)向偏铝酸钠(含溶质1mol)溶液中逐滴滴加盐酸,写出各步反应的化学方
程式及离子方程式,并画出氢氧化铝的物质的量与所加HCI的物质的量的
关系图像。
,
(3)(3)向偏铝酸钠溶液中通入二氧化碳,生成氢氧化铝沉淀及碳酸氢钠,写
出各步反应的方程式及离子方程式。
,
(4)(4)向氢氧化钠溶液(含溶质1mol)中逐滴滴加氯化铝溶液,边加边振荡,
发生的现象是,写出有关反应的化学方程式及离子方程式
,并画出生成氢氧化铝的物质的量与所加氯化铝的物质的
量的关系图像。
(5)(5)向含HCIImol的盐酸溶液中逐滴滴加偏铝酸钠溶液,边加边振荡,
发生的现象为,写出有关反应的化学方程式及离子方程式
,,并画出生成氢氧化,并画出生成氢氧化,并画出生成氢氧化铝的物质的量与所加HCI的物质的量的关系图像。
典题解悟
[例1].向明矶[KAI(SO4)2•12H2O]溶液中逐滴加入Ba(OH)2溶液至过量.
(1)
乳(沉淀ymoi
n[Ba(OH》]/mol
写出可能发生的有关反应的离子方程式.
(2)在图中,纵坐标表示生成沉淀的物质的量,横坐标表
示加入Ba(OH)2的物质的量.试在图中画出当溶液中明矶为1
mol时,生成的每一种沉淀的物质的量随Ba(OH)2物质的量变
化的曲线(在曲线上标明沉淀的化学式).
(3)当向aL物质的量浓度为Mmol/L的明矶溶液中滴加
物质的量浓度为nmol/L的Ba(OH)2溶液bL,用含a,MN的表达式表示:
1当b满足条件时,沉淀的总物质的量为最大值.
2当b满足条件时,沉淀的质量为最大值.
Ba(OH)。
的物质的量分别在0〜
【解析】⑴设溶液中明矶的物质的量为1mol.则当滴加的
1.5mol和1.5mol〜2.0mol时,所发生的反应的化学方程式和离子方程式分别为:
2KAl(SO4)2+3Ba(OH)2=KaSQ+3BaSO+2AI(OH)3J①
K2SO4+2AIQH)3+Ba(OH)2=2KAIQ+BaSQJ+4H2O②
(2)从化学方程式可以看出,生成BaSQ的物质的量随Ba(OH)2的量的增加而增加,生成
AI(OH)3的物质的量随Ba(OH)2的量的增加而发生先增加后减少直至完全溶解的变化过程.
(3)
3mol2mol
2
由方程式①知,当加入了1.5molBa(OH)2时,生成沉淀的物质的量为
=2.5mol质量为1.5molx233g/moI+1molx78g/mol=427.
1
程式②知,当继续滴加0.5molBa(0H)2时,沉淀的物质的量将减少1moix=0.5mol,
2
沉淀的质量却增加虿0.5molx233g/mol—78g=38.5g.所以,把明矶溶液中AI廿恰好沉淀完全时,生成沉淀的总的物质的量最大,把SO2-沉淀完全时,生成沉淀的质量最大.
【点拨】沉淀包括两部分,氢氧化铝和硫酸钡,氢氧化铝能溶于过量的碱溶液中,而硫酸钡不溶于过量的碱溶液。
[例2]向100mL2mol•L-的AICI3溶液中,逐滴加入NaOH溶液100mL时产生沉淀为7.8g,则加入NaOH溶液的物质的量浓度是()
A.1mol•LB.1.5mol•L
C.3mol•L-D.7mol•L-
【解析】7.8gAl(OH)3的物质的量为0.1mol。
AlCl3逐滴加入NaOH溶液有关反应为:
Al+3OH=Al(OH)3J
A1(OH)3+Ol=A1O-+2HO
(1)NaOH不足
设参加反应的NaOH的物质的量为n(NaOH
Al+3OH=Al(OH)3J
31
n(NaOH)0.1mol
n(NaOH)=0.3mol
c(NaOH)=0.3mol/0.1L=3mol•L-
(2):
NaOH过量
Al3+全部沉淀为AI(OH)3,过量的NaOH溶解部分的Al(OH)3,只余0.1molAl(OH)3沉淀。
设使Al3+全部沉淀需NaOH的物质的量为n1(NaOH)
溶解部分Al(OH)3需NaOH的物质的量为n2(NaOH)
Al3++3OH=Al(OH)3J
131
0.2moln1(NaOH)0.2mol
n1(NaOH)=0.6mol
Al(OH)3+OH=A1O2+2H2O
11
0.1moln2(NaOH)
n2(NaOH)=0.1molc(NaOH)=7mol•L-
【点拨】向AlCl3溶液中,逐滴加入NaOH溶液先生成氢氧化铝沉淀,继续滴加,沉淀会溶解。
夯实双基
1.向含有amolA1C1的溶液中加入含bmolKOH的溶液,生成沉淀的物质的量可能是()
①amol②bmol③仝mol④bmol⑤0mol⑥(4a-6)tool
T3
A.①②④⑤⑥B①③④⑤⑥C.①②③⑤⑥D.①③⑤
2.现有200mLMgCl2和A1CP的混合溶液,其中c(Mg)=0.2mol/L,c(C1-)=1.3mol/L,要使M『转化为Mg(OH)a,并使M『、Al3+分离开来,至少用4mol/LNaOH溶液多少毫升?
3•将金属钠投入氯化铝溶液中,下列有关叙述一定正确的是()
(A)一定有气体放出(B)最后一定有沉淀生成,且有气体放出
(C)一定有金属铝生成(D)溶液最后不一定澄清,但有气体放出
4.在MgSO和Al2(SO4)3的混合溶液中,[Al]=0.4mol/L,[SO4-]=0.9mol/L,则[Mg]最接
近于()
(A)0.5mol/L(B)0.4mol/L(C)0.3mol/L(D)0.2mol/L
5.向含有0.1mol明矶的溶液中逐滴加入含有0.2molBa(OH)2的溶液中,下面判断正确的应
是()
3+2
(A)先出现沉淀而后全部溶解(B)当Al和SO-全部沉出所得沉淀量最大
(C)最后只有BaSO沉淀(D)最后生成0.1molAl(OH)3和0.2molBaSO4
6.某混合溶液中含有MgCb的浓度为2mol/L,含AlCl3的浓度为3mol/L,将此溶液200mL
中Mg+转化为Mg(OH).沉淀分离出来,至少需要1.6mol/L的NaOH溶液的体积是()
(A)3.2L(B)2L(C)1.5L(D)1.8L
7.同量Al2(SQ)3分别与适量下列溶液反应,可能生成沉淀的物质的量最大的是(),
沉淀质量最大的是()
(A)NH3•H2O(B)NaAlO2(C)NaOH(D)Ba(OH2
8.在下列操作中最终能产生沉淀的是()
(A)向NaOH溶液中滴加Al2(SO)3溶液至过量(B)向NaAIQ溶液中滴加盐酸至过量
(C)向石灰水中滴加磷酸至过量(D)向AgNO溶液中滴加氨水至过量
9.有100毫升3摩/升的NaOH溶液和100毫升1摩/升的AlCl3溶液。
(a)将NaOH溶液逐滴
滴加到AlCl3溶液中,边滴边振荡,直到滴完;(b)将AlCl3溶液逐滴滴加到NaOH溶液中,
现象相同,沉淀质量不相等现象不相同,沉淀质量不相等
()
边滴边振荡,直至滴完。
对上述两处实验过程,说法正确的是()
(A)现象相同,沉淀质量相等(B)
(C)现象不相同,沉淀质量相等(D)
10.下列反应加入过量试剂仍能保持透明溶液的是
(A)在硫酸铝溶液中滴加过量氨水
(B)在氯化镁溶液中滴加过量的烧碱溶液
(C)在偏铝酸钠溶液中加入过量盐酸
(D)在氯化钙溶液中通入过量的二氧化碳
11.向一种混合溶液中加入过量氨水得到白色沉淀和无色溶液,过滤后再向沉淀中加入过量
烧碱溶液,沉淀部分溶解,经过滤得无色溶液,则该混合溶液中含有阳离子的组合是()
亠亠22亠2亠
(A)Ag、Na、Mg(B)Ag、Cu、Mg
(C)Ag、Mg、Al3'(D)Cu2、Mg、Al3
12.下列各实验操作过程中,能发生AI3++3AIO2-+6HO=4AI(OH)3J离子反应的是()
(1)向铝盐溶液中不断滴入烧碱溶液直至过量
(2)向偏铝酸盐溶液中不断滴入盐酸直至过量
(3)向烧碱溶液中不断滴入铝盐溶液直至过量
(4)向盐酸中不断滴入偏铝酸盐溶液直至过量
(A)只有⑴、
(2)(B)只有⑶(C)只有⑶、(4)(D)都未发生上述离子反应
13.下列各组反应中,最后得到Al(OH)3沉淀的是()
(A)将Al2Q固体粉末加到沸水中
(B)将CO气体通入NaAIQ溶液中
C)将过量金属钠投入到NaAIQ溶液中
(D)向200毫升1摩/升NaOH溶液中加入50毫升1摩/升的AICI3溶液
14.
下列物质:
①NaHCO②AI(OH)3,③NHHS,④K2SQ,⑤AgNO中既能跟盐酸反应又能跟氨水反应的是()。
18、工业上用电解冰晶石(NasAIFO和氧化铝的熔融混合物冶炼金属铝,白云石(CaCO•MgCO)
是一种含镁的矿物,下列物质的主要成分不属于复盐的是()
(A)明矶(B)冰晶石(C)光卤石(D)白云石
19.准确称取6g铝土矿样品(含A12Q、FaC3、SiO0放人盛有100mL某浓度硫酸溶液的烧
杯中,
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 硫酸铝 氢氧化钡 反应
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《稻草人》精彩读书笔记精选多篇.docx
《稻草人》精彩读书笔记精选多篇.docx
