 上海初中化学第六单元常见的金属和盐教案习题带答案图解读.docx
上海初中化学第六单元常见的金属和盐教案习题带答案图解读.docx
- 文档编号:3818537
- 上传时间:2022-11-25
- 格式:DOCX
- 页数:8
- 大小:163.65KB
上海初中化学第六单元常见的金属和盐教案习题带答案图解读.docx
《上海初中化学第六单元常见的金属和盐教案习题带答案图解读.docx》由会员分享,可在线阅读,更多相关《上海初中化学第六单元常见的金属和盐教案习题带答案图解读.docx(8页珍藏版)》请在冰豆网上搜索。
上海初中化学第六单元常见的金属和盐教案习题带答案图解读
第六单元:
常见的金属和盐第一节:
奇光异彩的金属
考点一:
金属材料一、金属材料
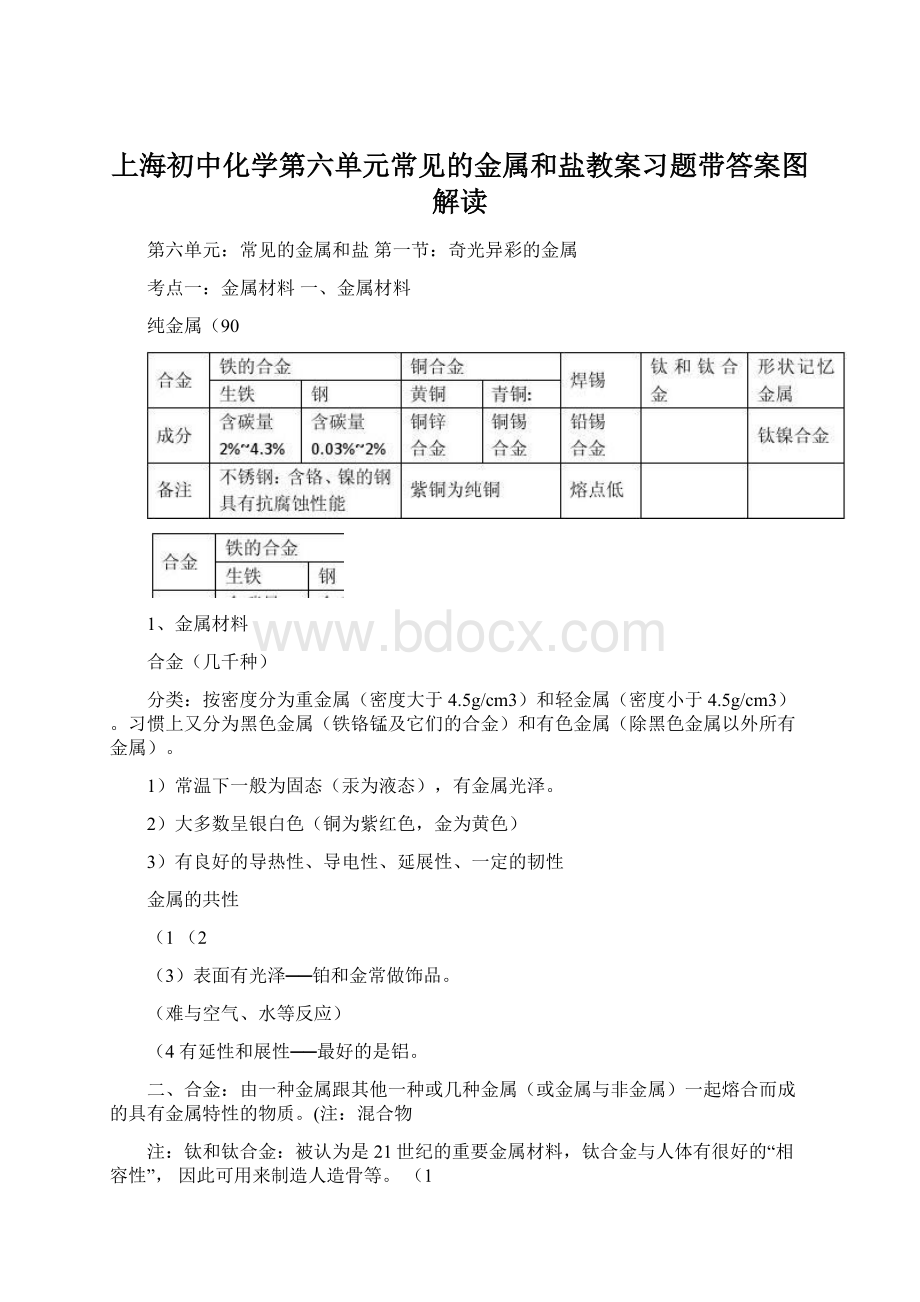
纯金属(90
1、金属材料
合金(几千种)
分类:
按密度分为重金属(密度大于4.5g/cm3)和轻金属(密度小于4.5g/cm3)。
习惯上又分为黑色金属(铁铬锰及它们的合金)和有色金属(除黑色金属以外所有金属)。
1)常温下一般为固态(汞为液态),有金属光泽。
2)大多数呈银白色(铜为紫红色,金为黄色)
3)有良好的导热性、导电性、延展性、一定的韧性
金属的共性
(1(2
(3)表面有光泽──铂和金常做饰品。
(难与空气、水等反应)
(4有延性和展性──最好的是铝。
二、合金:
由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
(注:
混合物
注:
钛和钛合金:
被认为是21世纪的重要金属材料,钛合金与人体有很好的“相容性”,因此可用来制造人造骨等。
(1
优点(
(3)抗腐蚀性能好
考点二、金属的化学性质一、金属的化学性质
1、大多数金属可与氧气的反应
点燃
2Mg+O2
2MgO2Mg+O22MgO注:
MgO:
白色固体
点燃
4Al+3O2
2Al2O34Al+3O22O3注:
Al2O3:
白色固体
点燃
3Fe+2O2Fe3O42Cu+O2
△
2CuO注:
CuO:
黑色固体
注意:
①、虽然铝在常温下能与氧气反应,但是在铝表面生成了一层致密的氧化铝薄膜,从而阻止了反应的进行,所以铝在常温下不会锈蚀。
②、“真金不怕火炼”说明金即使在高温时也不能与氧气反应,金的化学性质极不活泼。
2、金属+酸→盐+H2↑置换反应(条件:
活动性:
金属>H)
H2SO4+MgMgSO4+H2↑2HCl+MgMgCl2+H2↑
现象:
反应剧烈,有大量气泡产生,液体仍为无色
3H2SO4+2AlAl2(SO43+3H2
↑2AlCl3+3H2↑
现象:
反应剧烈,有大量气泡产生,液体仍为无色
H2SO4+ZnZnSO4+H2↑2HCl+ZnZnCl2+H2↑
现象:
反应比较剧烈,有大量气泡产生,液体仍为无色
H2SO4+FeFeSO4+H2↑2HCl+FeFeCl2+H2↑
现象:
反应比较缓慢,有气泡产生,液体由无色变为浅绿色
当一定质量的金属与足量的稀盐酸(或硫酸)反应时,产生的氢气质量与金属质量的关系:
M(H2=
3、金属+盐→另一金属+另一盐置换反应(条件:
参加反应的金属>化合物中金属元素)Fe+CuSO4==Cu+FeSO4(“湿法冶金”原理现象:
铁钉表面有红色物质出现,液体由蓝色变为浅绿色2Al+3CuSO4Al2(SO43+3Cu
现象:
铝丝表面有红色物质出现,液体由蓝色变为无色
Cu+2AgNO3Cu(NO32+2Ag
现象:
铜丝表面有银白色物质出现,液体由无色变为蓝色。
注意:
①CuSO4溶液:
蓝色FeSO4、FeCl2溶液:
浅绿色②Fe在参加置换反应时,生成+2价的亚铁盐。
二、置换反应
1、概念:
由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应2、特点:
反应物、生成物都两种;物质种类是单质与化合物三、常见金属活动性顺序:
KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu
金属活动性由强逐渐减弱在金属活动性顺序里:
(1)金属的位置越靠前,它的活动性就越强
(2)位于氢前面的金属能置换出盐酸、稀硫酸中的氢元素(不可用浓硫酸、硝酸)(3)位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来。
(除K、Ca、Na)1、金属与酸反应
金属活动性由强到弱的顺序:
镁>锌>铁>铜2、金属与盐溶液反应
金属活动性由强到弱的顺序:
锌>铁>铜>银
1.波尔多液是一种农业上常用的杀菌剂,它是由硫酸铜、石灰加水配制而成,为3应用:
○
什么不能用铁制容器来配制波尔多液?
2.○不法商贩常常用铝制的假银元坑害消费者,小明在市场上买了一枚银元,请你用化学方法帮他鉴别这枚银元的真假。
考点三、金属资源的保护和利用一、铁的冶炼
1、原理:
在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
高温3CO+Fe2O3
2Fe+3CO2
2、现象:
红色粉末逐渐变为黑色,产生的气体能使澄清的石灰水变浑浊。
3,实验中需注意:
①先通CO再加热的目的:
排出装置内的空气,以免加热时CO与空气混合,可能会发生爆炸。
②实验完毕后继续通入CO的目的;防止氧化铁被还原成铁后,在较高的温度下重新被氧化③尾气的处理:
因为CO有毒,所以尾气中的CO气体要经过处理,变成无毒的气体。
可点燃使其生成无毒的二氧化碳气体。
4、原料:
铁矿石、焦炭、石灰石、空气常见的铁矿石有磁铁矿(主要成分是Fe3O4)、赤铁矿(主要成分是Fe2O3)5、石灰石的作用:
除去铁矿石中的二氧化硅二、含杂质化学反应的计算
含杂质的物质质量与纯物质质量的转化:
纯物质的质量=含杂质的物质质量×纯物质的纯度三、铁的锈蚀
(1)铁生锈的条件是:
铁与O2、水接触(铁锈的主要成分:
Fe2O3·XH2O)(铜生铜绿的条件:
铜与O2、水、CO2接触。
铜绿的化学式:
Cu2(OH2CO3)
(2)防止铁制品生锈的措施:
①保持铁制品表面的清洁、干燥
②表面涂保护膜:
如涂油、刷漆、电镀、烤蓝等③改变铁的单一结构,制成不锈钢
(3)铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气反应,因此铁制品可以全部被锈蚀。
因而铁锈应及时除去。
(4)铝与氧气反应生成致密的氧化铝薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
四、金属资源的保护和利用:
①防止金属腐蚀
1③合理开采矿物④寻找金属的代用
2
第二节:
盐和肥料
考点一、生活中常见的盐
盐的分类:
二、精盐提纯——去除不溶性杂质,得到的精盐中还含有氯化镁、氯化钙等可溶性杂质。
1、
三、碳酸钠、碳酸氢钠、碳酸钙的化学性质
1、碳酸钠的化学性质:
这两个反应可用检
(1)与酸的反应:
2HCl+Na2CO3
2NaCl+CO2↑+H2O
(2)与碱溶液的反应;Ca(OH2+Na2CO3CaCO3↓+2NaOH验NaOH是否变质
2、碳酸氢钠的化学性质:
与酸的反应;HCl+NaHCO3H2O+NaCl+CO2↑
碳酸根离子的鉴别:
-
澄清石灰CO32稀HCl
碳及碳的化合物、两种碱的相互转化:
-
检验溶液中存在CO32的方法:
-
⑴加入稀HCl,若有无色气泡产生,则有存在CO32
-
⑵加入石灰水或Ba(OH2溶液,若液体变浑浊,则有存在CO32
-
⑶加入CaCl2或Ca(NO32溶液,若液体变浑浊,则有存在CO32四、盐的性质
(一)、酸、碱、盐的溶解性
123
氯化物除AgCl难溶外,其余多数均可溶;
碳酸盐除碳酸钾、碳酸钠、碳酸铵可溶,其余都难溶。
注:
BaSO4、AgCl不溶于水,也不溶于酸。
、
(二)、盐的化学性质1、盐(可溶)+金属1→金属2+新盐(金属1比金属2活泼,K、Ca、Na除外)反应类型:
置换反应Fe+CuSO4==Cu+FeSO4(“湿法冶金”原理2Al+3CuSO4Al2(SO43+3CuCu+2AgNO3Cu(NO32+2Ag2、盐+酸→新盐+新酸(满足复分解反应的条件)反应类型:
复分解反应H2SO4+BaCl2CuBaSO4↓+2HCl(注BaSO4沉淀:
白色,不溶于稀硝酸)Cu2HCl+Na2CO32NaCl+CO2↑+H2OCuOCO2↑+CaCl2+H2O2HCl+CaCO3O+O+CuH2O+NaCl+CO2↑HCl+NaHCO3CuHCl+AgNO3HNO3+AgCl↓(注AgCl沉淀:
白色,不溶于稀硝酸)+2HCu+3、盐+碱→新盐2H新碱(反应物需都可溶,且满足复分解反应的条件)O+CuO+反应类型:
复分解反应O2HC2NaOH+CuSO4Cu(OH2↓+Na2SO4现象:
出现蓝色沉淀ClOCl2H+(注:
CuSO4溶液:
蓝色Cu(OH2沉淀:
蓝色)+2H3NaOH+FeCl3lCuOFe(OH3↓+3NaCl现象:
出现红褐色沉淀Cu2HCu(注:
FeCl3溶液:
黄色Fe(OH3沉淀:
红褐色)Cl2HCCuOCa(OH2+Na2CO3Cl+CaCO3↓+2NaOH现象:
澄清石灰水变浑浊CuC4、盐+盐→两种新盐(反应物需都可溶,且满足复分解反应的条件)Cl2ClCl2CuCuO反应类型:
复分解反应lCu+l22HC+NaCl+AgNO3AgCl↓+NaNO3现象:
出现白色沉淀+Cu+BaSO↓+2NaClCl2Na2SO4+BaCl2现象:
出现白色沉淀4+CuC2HCCuO五、复分解反应Cl2l3H2CuO23H23H1、概念:
由两种化合物互相交换成分,生成另外两种化合物的反应2Cl+2HCl2+l+2、特点:
首尾交换,各元素的化合价不变+CuCO++OO3H2l3H22CuC3、复分解反应的类型+3Hl22HC2HC23HOOOlCuC+l23H24、条件:
生成物:
有沉淀或有气体或有水生成时,复分解反应才可以发生。
lOl2+反应物:
有酸酸必溶,无酸碱盐溶3HCuC2O由于初中常见的酸是可溶性的,因此:
CuC金属氧化物+酸→盐2+水3Hl2碱+酸→盐+水O+l2酸→另一种盐+CO2+H2ORHCO3/RCO3++O一些盐的用途3H21.食盐(NaCl)3H2工业原料、农业选种、融化积雪、消毒O2.硫酸铜(CuSO4)O湿法炼铜、配制波尔多液(与熟石灰)3.明矾(KAl(SO42·2O)作净水的凝聚剂12H这三种复分解反应一定能发生
六、特殊离子鉴别:
离子种类Cl--SO42检验方法(所加试剂)先加AgNO3溶液,再加稀HNO3先加Ba(NO32(或BaCl2)溶液,再加稀HNO3先滴加稀HCl,再将气体通入澄清的石灰水中滴加无色酚酞试液滴加紫色石蕊试液先加碱溶液(溶液)加热,再用湿润的蓝色石蕊试纸试验现象产生白色沉淀产生白色沉淀有无色气泡产生,石灰水变浑浊试液变红试液变红有无色气体产生,试纸变蓝CO32OHH+--NH4+考点二、化学肥料一、农家肥料:
营养元素含量少,肥效慢而持久、价廉、能改良土壤结构二、化学肥料(氮肥、钾肥、磷肥)铵态氮肥(NH42SO4、NH4HCO4、NH4NO3、NH4Cl氮肥硝态氮肥KNO3有机态氮肥CO(NH22钾肥KNO3、KCl、草木灰化学肥料磷肥Ca(H2PO42复合肥料KNO3微量元素肥料肥料农家肥料1、氮肥⑴作用:
促进植物茎、叶生长茂盛、叶色浓绿(促苗)。
缺氮:
叶黄⑵、常用氮肥:
含N量NH4HCO317.7%NH4NO335%(NH42SO421.2%NH4Cl26.2%CO(NH2246.7%NH3H2ONaNO3⑶、生物固氮:
豆科植物的根瘤菌将氮气转化为含氮的化合物而吸收.使用注意事项易分解,施用时深埋易爆,结块不可用铁锤砸长期使用会使土壤酸化、板结长期使用会使土壤酸化、板结含氮量最高的氮肥(有机物)加水稀释后施用不稳定,易放出NH3↑铵态氮肥防晒防潮,且均不能与碱性物质(如草木灰、熟石灰等)混合施用®(4).碳酸氢铵受热易分解:
NH4HCO3¾¾¾NH3↑+CO2↑+H2O加热(5.铵态氮肥不宜和碱性物质混用:
(NH42SO4+Ca(OH2→CaSO4+2NH3↑+2H2O──铵盐的检验方法
2、钾肥⑴作用:
促使作物生长健壮、茎杆粗硬,抗倒伏(壮秆)。
缺钾:
叶尖发黄KCl⑵常用钾肥草木灰:
农村最常用钾肥(主要成分为K2CO3),呈碱性K2SO4:
长期使用会使土壤酸化、板结3、磷肥⑴作用:
促进植物根系发达,穗粒增多,饱满(催果),抗旱抗寒,促进作物提早成熟缺磷:
生长迟缓,产量降低,根系不发达⑵常用磷肥磷矿粉Ca3(PO42钙镁磷肥(钙和镁的磷酸盐)过磷酸钙Ca(H2PO42和CaSO4不能与碱性物质混合施用。
如草木灰、熟石灰。
重过磷酸钙Ca(H2PO42⒋复合肥:
含N、P、K中的两种或三种KNO3NH4H2PO4不能与碱性物质混合施用(NH42HPO4三、使用化肥、农药对环境的影响1、使用化肥、农药对环境的影响
(1)土壤污染:
重金属元素、有毒有机物、放射性物质
(2)大气污染:
NO2、NH3、H2S、SO2(3)引起水体污染:
N、P过多,导致水体富营养化,赤潮、水华等现象2、合理使用化肥
(1)根据土壤情况和农作物种类选择化肥
(2)、农家肥和化肥合理配用四、氮、磷、钾三种化肥的区别方法氮肥看外观加水灼烧加Ca(OH2白色晶体全部溶于水可燃烧,熔化起泡冒烟放出氨气不燃烧,跳动、爆裂声不放出氨气钾肥磷肥灰白色粉末大多数不溶于水五、NH4+的检验试剂:
碱(NaOH、Ca(OH2等)、湿润的红色石蕊试纸NH4NO3+NaOH=NaNO3+NH3↑+H2O
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 上海 初中化学 第六 单元 常见 金属 教案 习题 答案 图解
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
