 化学元素周期表初中.docx
化学元素周期表初中.docx
- 文档编号:3685833
- 上传时间:2022-11-24
- 格式:DOCX
- 页数:18
- 大小:35.40KB
化学元素周期表初中.docx
《化学元素周期表初中.docx》由会员分享,可在线阅读,更多相关《化学元素周期表初中.docx(18页珍藏版)》请在冰豆网上搜索。
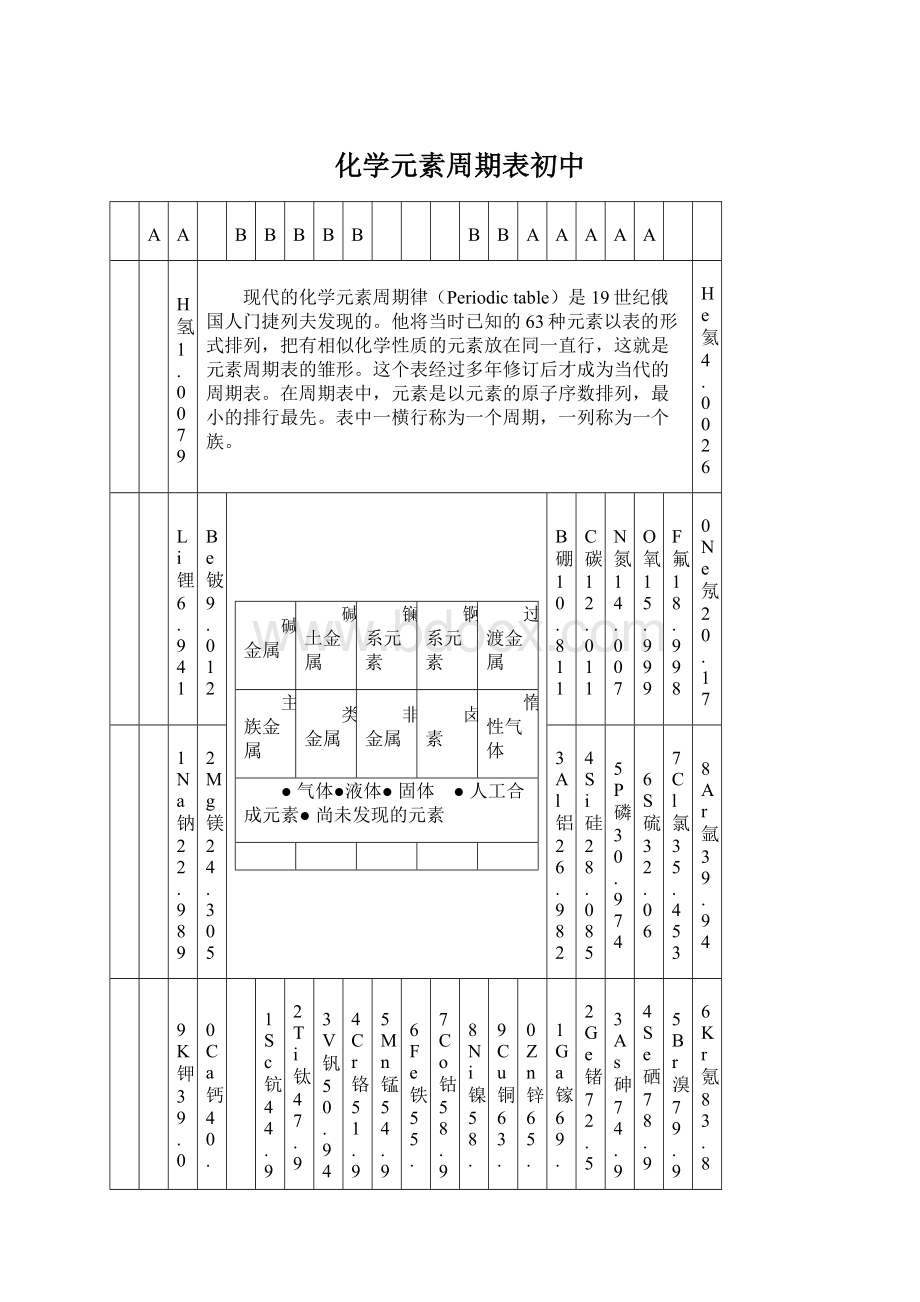
化学元素周期表初中
ⅠA
ⅡA
ⅢB
ⅣB
ⅤB
ⅥB
ⅦB
Ⅷ
ⅠB
ⅡB
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
1
1 H
氢
1.0079
现代的化学元素周期律(Periodictable)是19世纪俄国人门捷列夫发现的。
他将当时已知的63种元素以表的形式排列,把有相似化学性质的元素放在同一直行,这就是元素周期表的雏形。
这个表经过多年修订后才成为当代的周期表。
在周期表中,元素是以元素的原子序数排列,最小的排行最先。
表中一横行称为一个周期,一列称为一个族。
2 He
氦
4.0026
2
3 Li
锂
6.941
4 Be
铍
9.012
碱金属
碱土金属
镧系元素
锕系元素
过渡金属
主族金属
类金属
非金属
卤素
惰性气体
●气体●液体●固体 ●人工合成元素●尚未发现的元素
5 B
硼
10.811
6 C
碳
12.011
7 N
氮
14.007
8 O
氧
15.999
9 F
氟
18.998
10Ne
氖
20.17
3
11 Na
钠
22.989
12 Mg
镁
24.305
13 Al
铝
26.982
14 Si
硅
28.085
15 P
磷
30.974
16 S
硫
32.06
17Cl
氯
35.453
18Ar
氩
39.94
4
19 K
钾
39.098
20 Ca
钙
40.08
21 Sc
钪
44.956
22Ti
钛
47.9
23 V
钒
50.9415
24 Cr
铬
51.996
25 Mn
锰
54.938
26 Fe
铁
55.84
27 Co
钴
58.9332
28 Ni
镍
58.69
29 Cu
铜
63.54
30 Zn
锌
65.38
31 Ga
镓
69.72
32 Ge
锗
72.5
33 As
砷
74.922
34Se
硒
78.9
35Br
溴
79.904
36Kr
氪
83.8
5
37Rb
铷
85.467
38 Sr
锶
87.62
39 Y
钇
88.906
40Zr
锆
91.22
41 Nb
铌
92.9064
42 Mo
钼
95.94
43 Tc
锝
99
44 Ru
钌
101.07
45 Rh
铑
102.906
46 Pd
钯
106.42
47 Ag
银
107.868
48 Cd
镉
112.41
49 In
铟
114.82
50 Sn
锡
118.6
51 Sb
锑
121.7
52Te
碲
127.6
53 I
碘
126.905
54Xe
氙
131.3
6
55Cs
铯
132.905
56 Ba
钡
137.33
71Lu镥
174.96
72Hf
铪
178.4
73 Ta
钽
180.947
74 W
钨
183.8
75 Re
铼
186.207
76 Os
锇
190.2
77 Ir
铱
192.2
78Pt
铂
195.08
79 Au
金
196.967
80 Hg
汞
200.5
81 Tl
铊
204.3
82 Pb
铅
207.2
83 Bi
铋
208.98
84Po
钋
(209)
85At
砹
(201)
86Rn
氡
(222)
7
87Fr
钫
(223)
88 Ra
镭
226.03
103Lr铹
260
104Rf
钅卢
(261)
105Db
钅杜(262)
106Sg
钅喜(263)
107Bh
钅波(262)
108Hs
钅黑(265)
109Mt
钅麦(266)
110Ds
钅达(269)
111Rg
钅仑
(272)
112
Uub
(285)
113
Uut
(284)
114
Uuq
(289)
115Uup
(288)
116Uuh
(292)
117
Uus
118
Uuo
57La
镧
138.905
58Ce
铈
140.12
59Pr
镨
140.91
60Nd
钕
144.2
61Pm
钷
147
62Sm
钐
150.4
63Eu
铕
151.96
64Gd
钆
157.25
65Tb
铽
158.93
66Dy
镝
162.5
67Ho
钬
164.93
68Er
铒
167.2
69Tm
铥
168.934
70Yb
镱
173.0
89Ac
锕
227.03
90Th
钍
232.04
91Pa
镤
231.04
92U
铀
238.03
93Np
镎
237.05
94Pu
钚
244
95Am
镅
243
96Cm
锔
247
97Bk
锫
247
98Cf
锎
251
99Es
锿
254
100Fm
镄
257
101Md
钔
258
102No
锘
259
化学元素周期表
百科名片
化学元素周期表
化学元素周期表是1869年俄国科学家门捷列夫(DmitriMendeleev)首创的,他将当时已知的63种元素依原子量大小并以表的形式排列,把有相似化学性质的元素放在同一行,就是元素周期表的雏形。
在周期表中,元素是以元素的原子序排列,最小的排行最先。
表中一横行称为一个周期,一列称为一个族。
目录[显示]
起源简介
化学元素周期表
现代化学的元素周期律是1869年的德米特里·伊万诺维奇·门捷列夫首创的。
1913年英国科学家莫色勒利用阴极射线撞击金属产生X射线,发现原子序越大,X射线的频率就越高,因此他认为核的正电荷决定了元素的化学性质,并把元素依照核内正电荷(即质子数或原子序数)排列,经过多年
元素周期表
修订后才成为当代的周期表。
常见的元素周期表为长式元素周期表。
在长式元素周期表中,元素是以元素的原子序排列,最小的排行最先。
表中一横行称为一个周期,一列称为一个族,最后有两个系。
除长式元素周期表外,常见的还有短式元素周期表,螺旋元素周期表,三角元素周期表等。
道尔顿提出科学原子论后,随着各种元素的相对原子质量的数据日益完善和原子价(化合价)概念的提出,就使元素相对原子质量与性质(包括化合价)之间的联系显露出来。
德国化学家德贝莱纳就提出了“三元素组”观点。
他把当时已知的54种元素中的15种,分成5组,每组的三种元素性质相似,而且中间元素的相对原子质量等于较轻和较重的两个元素相对原子质量之和的一半。
例如钙、锶、钡,性质相似,锶的相对原子质量大约是钙和钡的相对原子质量之和的一半。
法国矿物学家尚古多提出了一个“螺旋图”的分类方法。
他将已知的62种元素按相对原子质量的大小顺序,标记在绕着圆柱体上升的螺旋线上,这样某些性质相近的
元素恰好出现在同一母线上。
这种排列方法很有趣,但要达到井然有序的程度还有困难。
另外尚古多的文字也比较暧昧,不易理解,虽然是煞费苦心的大作,但长期未能让人理解。
英国化学家纽兰兹把当时已知的元素按相对原子质量大小的顺序进行排列,发现无论从哪一个元素算起,每到第八个元素就和第一一个元素的性质相近。
这很像音乐上的八度音循环,因此,他干脆把元素的这种周期性叫做“八音律”,并据此画出了标示元素关系的“八音律”表。
显然,纽兰兹已经下意识地摸到了“真理女神"的裙角,差点就揭示元素周期律了。
不过,条件限制了他做进一步的探索,因为当时相对原子质量的测定值有错误,而且他也没有考虑到还有尚未发现的元素,只是机械地按当时的相对原子质量大小将元素排列起来,所以他没能揭示出元素之间的内在规律。
他的“八音律”在英国化学学会上受到了嘲弄,主持人以不无讥讽的口吻问道:
“你为什么不按元素的字母顺序排列?
那样,也许会得到更加意想不到的美妙效果。
”德国化学家迈耶尔借鉴了德贝莱纳、纽兰兹等人的研究成果,从化合价和物理性质方面人手,去探索元素间的规律。
在他的《近代化学理论》一书中,刊登了元素周期表,表中列出了28个元素,他们按相对原子质量递增的顺序排列,一共分成六族,并给出了相应的原子价是4、3、2、1、1、2。
1868年,发表了第二张周期表,增加了24个元素和9个纵行,并区分了主族和副族。
迈耶尔的第三张元素周期表发表于1870年,他采用了竖式周期表的形式,并且预留了一些空位给有待发现的元素,但是表中没有氢元素。
可以说,迈耶尔已经发现了元素周期律。
[编辑本段]
周期表解读
表格说明
周期表的编排显示出不同元素的化学性质的周期性,在周期表中,元素按原子序(即原子核内的质子数目递增次序排列,并分为若干列和栏,在同一行中的称为同一周期,根据量子力学,周期对应着元素原子的电子排布,显示出该原子的已装填电子层数目。
沿着周期表向下,周期的长度逐渐上升,并按元素的电子排布划分出s区元素、p区元素、d区元素和f区元素。
而同一栏中的则称为同一族,同一族的元素有着相似的化学性质。
在印刷的周期表中,会列出元素的符号和原子序。
而很多亦会附有以下的资料,以元素X为例:
A:
质量数(Massnumber),即在数量上等于原子核(质子加中子)的粒子数目。
Z:
原子序数,即是质子的数目。
由于它是固定的,一般不会标示出来。
e:
净电荷,正负号写在数字后面。
n:
原子数目,元素在非单原子状态(分子或化合物)时的数目。
除此之外,部份较高阶的周期表更会列出元素的电子排布、电负性和价电子数目。
元素读音
第一周期元素:
1氢(qīng)2氦(hài)
元素周期表正确金属汉字写法
第二周期元素:
3锂(lǐ)4铍(pí)5硼(péng)6碳(tàn)7氮(dàn)8氧(yǎng)9氟(fú)10氖(nǎi)
第三周期元素:
11钠(nà)12镁(měi)13铝(lǚ)14硅(guī)15磷(lín)16硫(liú)17氯(lǜ)18氩(yà)
第四周期元素:
19钾(jiǎ)20钙(gài)21钪(kàng)22钛(tài)23钒(fán)24铬(gè)25锰(měng)26铁(tiě)27钴(gǔ)28镍(niè)29铜(tóng)30锌(xīn)31镓(jiā)32锗(zhě)33砷(shēn)34硒(xī)35溴(xiù)36氪(kè)
第五周期元素:
37铷(rú)38锶(sī)39钇(yǐ)40锆(gào)41铌(ní)42钼(mù)43锝(dé)44钌(liǎo)45铑(lǎo)46钯(bǎ)47银(yín)48镉(gé)49铟(yīn)50锡(xī)51锑(tī)52碲(dì)53碘(diǎn)54氙(xiān)
第六周期元素:
55铯(sè)56钡(bèi)57镧(lán)58铈(shì)59镨(pǔ)60钕(nǚ)61钷(pǒ)62钐(shān)63铕(yǒu)64钆(gá)65铽(tè)66镝(dī)67钬(huǒ)68铒(ěr)69铥(diū)70镱(yì)71镥(lǔ)72铪(hā)73钽(tǎn)74钨(wū)75铼(lái)76锇(é)77铱(yī)78铂(bó)79金(jīn)80汞(gǒng)81铊(tā)82铅(qiān)83铋(bì)84钋(pō)85砹(ài)86氡(dōng)
第七周期元素:
87钫(fāng)88镭(léi)89锕(ā)90钍(tǔ)91镤(pú)92铀(yóu)93镎(ná)94钚(bù)95镅(méi)96锔(jú)97锫(péi)98锎(kāi)99锿(āi)100镄(fèi)101钔(mén)102锘(nuò)103铹(láo)104鑪(lú)105𨧀(dù)106𨭎(xǐ)107𨨏(bō)108𨭆(hēi)109䥑(mài)110鐽(dá)111錀(lún)112鎶(gē)
外围电子层排布
外围电子层排布,括号指可能的电子层排布
1H1s12He1s2
3Li2s1
4Be2s2
5B2s22p1
6C2s22p2
7N2s22p3
8O2s22p4
9F2s22p5
10Ne2s22p6
11Na3s1
12Mg3s2
13Al3s23p1
14Si3s23p2
15P3s23p3
16S3s23p4
17Cl3s23p5
18Ar3s23p6
19K4s1
20Ca4s2
21Sc3d14s2
22Ti3d24s2
23V3d34s2
24Cr3d54s1
25Mn3d54s2
26Fe3d64s2
27Co3d74s2
28Ni3d84s2
29Cu3d104s1
30Zn3d104s2
31Ga4s24p1
32Ge4s24p2
33As4s24p3
34Se4s24p4
35Br4s24p5
36Kr4s24p6
37Rb5s1
38Sr5s2
39Y4d15s2
40Zr4d25s2
41Nb4d45s1
42Mo4d55s1
43Tc4d55s2
44Ru4d75s1
45Rh4d85s1
46Pd4d10
47Ag4d105s1
48Cd4d105s2
49In5s25p1
50Sn5s25p2
51Sb5s25p3
52Te5s25p4
53In5s25p5
54Xe5s25p6
55Cs6s1
56Ba6s2
57La5d16s2
58Ce4f15d16s2
59Pr4f36s2
60Nd4f46s2
61Pm4f56s2
62Sm4f66s2
63Eu4f76s2
64Gd4f75d16s2
65Tb4f96s2
66Dy4f106s2
67Ho4f116s2
68Er4f126s2
69Tm4f136s2
70Yb4f146s2
71Lu4f145d16s2
72Hf5d26s2
73Ta5d36s2
74W5d46s2
75Re5d56s2
76Os5d66s2
77Ir5d76s2
78Pt5d96s1
79Au5d106s1
80Hg5d106s2
81Tl6s26p1
82Pb6s26p2
83Bi6s26p3
84Po6s26p4
85At6s26p5
86Rn6s26p6
87Fr7s1
88Ra7s2
89Ac6d17s2
90Th6d27s2
91Pa5f26d17s2
92U5f36d17s2
93Np5f46d17s2
94Pu5f67s2
95Am5f77s2
96Cm5f76d17s2
97Bk5f97s2
98Cf5f107s2
99Es5f117s2
100Fm5f127s2
101Md(5f137s2)
102No(5f147s2)
103Lr(5f146d17s2)
104Rf(6d27s2)
105Db(6d37s2)
106Sg5f146d47s2
107Bh5f146d57s2
108Hs5f146d67s2
109Mt5f146d77s2
110Ds5f146d97s1
111Rg5f146d107s1
112Cn5f146d107s2
113Uut5f146d107s27p1
114Uuq5f146d107s27p2
115Uup5f146d107s27p3
116Uuh5f146d107s27p4
117Uus5f146d107s27p5
118Uuo5f146d107s27p6
[编辑本段]
蕴含规律
递变性规律
1原子半径
(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;
(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
注意:
原子半径在VIB族及此后各副族元素中出现反常现象。
从钛至锆,其原子半径合乎规律地增加,这主要是增加电子层数造成的。
然而从锆至铪,尽管也增加了一个电子层,但半径反而减小了,这是与它们对应的前一族元素是钇至镧,原子半径也合乎规律地增加(电子层数增加)。
然而从镧至铪中间却经历了镧系的十四个元素,由于电子层数没有改变,随着有效核电荷数略有增加,原子半径依次收缩,这种现象称为“镧系收缩”。
镧系收缩的结果抵消了从锆至铪由于电子层数增加到来的原子半径应当增加的影响,出现了铪的原子半径反而比锆小的“反常”现象。
2元素变化规律
(1)除第一周期外,其余每个周期都是以金属元素开始逐渐过渡到非金属元素,最后以稀有气体元素结束。
(2)每一族的元素的化学性质相似
3元素化合价
(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);
(2)同一主族的元素的最高正价、负价均相同
(3)所有单质都显零价
4单质的熔点
(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;
(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增
5元素的金属性与非金属性
(1)同一周期的元素电子层数相同。
因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增;
(2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。
6最高价氧化物和水化物的酸碱性
元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
7非金属气态氢化物
元素非金属性越强,气态氢化物越稳定。
同周期非金属元素的非金属性越强,其气态氢化物水溶液一般酸性越强;同主族非金属元素的非金属性越强,其气态氢化物水溶液的酸性越弱。
8单质的氧化性、还原性
一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱;元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
元素周期律
元素周期表是元素周期律用表格表达的具体形式,它反映元素原子的内部结构和它们之间相互联系的规律。
元素周期表简称周期表。
元素周期表[1]有很多种表达形式,目前最常用的是维尔纳长式周期表。
元素周期表有7个周期,有16个族和4个区。
元素在周期表中的位置能反映该元素的原子结构。
周期表中同一横列元素构成一个周期。
同周期元素原子的电子层数等于该周期的序数。
同一纵行(第Ⅷ族包括3个纵行)的元素称“族”。
族是原子内部外电子层构型的反映。
例如外电子构型,IA族是ns1,IIIA族是ns2np1,O族是ns2np4,IIIB族是(n-1)d1·ns2等。
元素周期表能形象地体现元素周期律。
根
据元素周期表可以推测各种元素的原子结构以及元素及其化合物性质的递变规律。
当年,门捷列夫根据元素周期表中未知元素的周围元素和化合物的性质,经过综合推测,成功地预言未知元素及其化合物的性质。
现在科学家利用元素周期表,指导寻找制取半导体、催化剂、化学农药、新型材料的元素及化合物。
现代化学的元素周期律是1869年俄国科学家德米特里·伊万诺维奇·门捷列夫(DmitriIvanovichMendeleev)首先整理,他将当时已知的63种元素依原子量大小并以表的形式排列,把有相似化学性质的元素放在同一行,就是元素周期表的雏形。
利用周期表,门捷列夫成功的预测当时尚未发现的元素的特性(镓、钪、锗)。
1913年英国科学家莫色勒利用阴极射线撞击金属产生X射线,发现原子序越大,X射线的频率就越高,因此他认为核的正电荷决定了元素的化学性质,并把元素依照核内正电荷(即质子数或原子序)排列,经过多年修订后才成为当代的周期表。
当然还有未知元素等待我们探索.
这张表揭示了物质世界的秘密,把一些看来似乎互不相关的元素统一起来,组成了一个完整的自然体系。
位置规律
判断元素在周期表中位置应牢记的规律:
(1)元素周期数等于核外电子层数;
(2)主族元素的族数等于最外层电子数。
阴阳离子的半径大小辨别规律
由于阴离子是电子最外层得到了电子而阳离子是失去了电子
所以,总的说来(同种元素)
(1)阳离子半径<原子半径
(2)阴离子半径>原子半径
(3)阴离子半径>阳离子半径
(4)对于具有相同核外电子排布的离子,原子序数越大,其离子半径越小。
(不适合用于稀有气体)
[编辑本段]
意义与作用
1869年,门捷列夫发现了元素周期律和元素周期表,在元素周期律的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循。
现在,化学家们已经能利用各种先进的仪器和分析技术对化学世界进行微观的探索,并正在探索利用纳米技术制造出具有特定功能的产品,是化学在材料、能源、环境和生命科学等研究上发挥越来
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学元素 周期表 初中
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
