 高二第二次月考.docx
高二第二次月考.docx
- 文档编号:366124
- 上传时间:2022-10-09
- 格式:DOCX
- 页数:11
- 大小:109.24KB
高二第二次月考.docx
《高二第二次月考.docx》由会员分享,可在线阅读,更多相关《高二第二次月考.docx(11页珍藏版)》请在冰豆网上搜索。
高二第二次月考
高二第一学期第二次月考
化学试题(2015、01)
欢迎你参加这次测试,测试范围选修4所学内容,祝你取得好成绩!
本试卷分第Ⅰ卷选择题和第
卷非选择题,共100分,考试时间90分钟。
可能用到的相对原子质量:
H:
1C:
12O:
16S:
32Na:
23N:
14Cl:
35.5Mg:
24Fe:
56Cu:
64
第Ⅰ卷(共50分)
一、选择题(本题包括25个题,每小题2分,共50分;每小题只有一个正确选项。
)
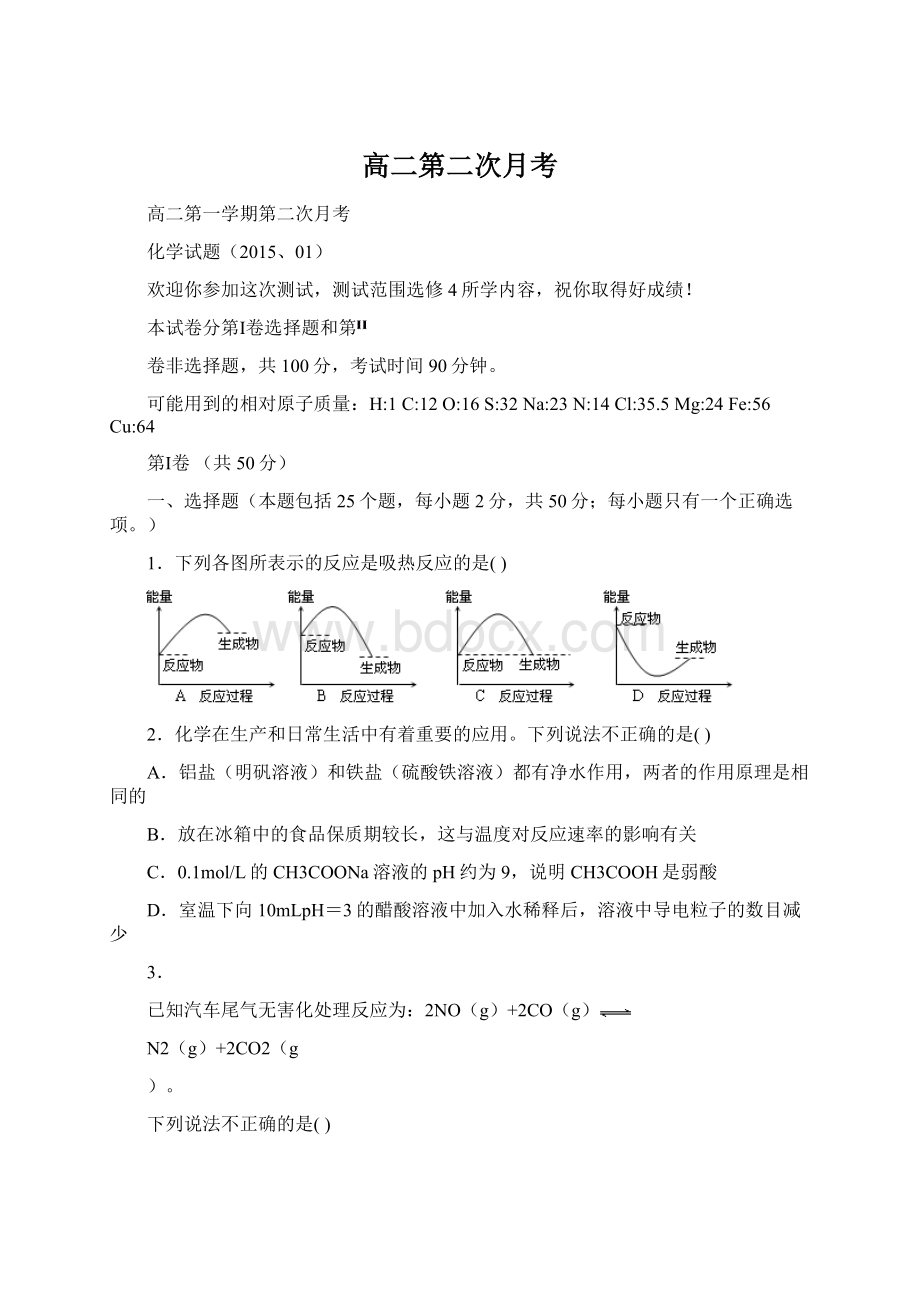
1.下列各图所表示的反应是吸热反应的是()
2.化学在生产和日常生活中有着重要的应用。
下列说法不正确的是()
A.铝盐(明矾溶液)和铁盐(硫酸铁溶液)都有净水作用,两者的作用原理是相同的
B.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
C.0.1mol/L的CH3COONa溶液的pH约为9,说明CH3COOH是弱酸
D.室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中导电粒子的数目减少
3.
已知汽车尾气无害化处理反应为:
2NO(g)+2CO(g)
N2(g)+2CO2(g
)。
下列说法不正确的是()
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高该反应的速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
4.下列离子方程式中,属于水解反应的是()
A.CH3COOH+H2O
CH3COO--+H3O+B.CO2+H2O
HCO3--+H+
C.CO32--+H2O
HCO3--+OH--D.HS--+H2O
S2--+H3O+
5.在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:
X(g)+2Y(g)
2Z(g),此反应达到平衡的标志是()
A.容器内压强不随时间变化B.υ正(X)=υ逆(Z)
C.容器内X、Y、Z的浓度之比为l:
2:
2D.单位时间消耗0.1molX同时生成0.2molZ
6.关于溶液的酸碱性说法正确的是()
A.c(H+)很小的溶液一定呈碱性B.pH=7的溶液一定呈中性
C.c(OH--)=c(H+)的溶液一定呈中性D.不能使酚酞试液变红的溶液一定呈酸性
7.关于浓度均为0.1mol/L的三种溶液:
①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是()
A.c(NH4+):
③>①B.水电离出的c(H+):
②>①
C.①和②等体积混合后的溶液:
c(H+)=c(OH--)+c(NH3·H2O)
D.①和③等体积混合后的溶液:
c(NH4+)>c(Cl--)>c(OH--)>c(H+)
8.下列事实均能说明醋酸是弱电解质的是()
①醋酸与水能以任意比互溶 ②醋酸溶液能导电 ③醋酸溶液中存在醋酸分子 ④0.1mol/L醋酸溶液的pH比0.1mol/L盐酸的pH大 ⑤醋酸能和碳酸钙反应放出CO2 ⑥大小相同的锌粒与相同物质的量浓度的盐酸和醋酸溶液反应,开始醋酸产生H2速率慢
A.②③⑥ B.④⑤⑥C.③④⑥D.①②③
9.
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
A.外电路的电流方向为:
X→外电路→Y
B.若两电极分别为铁和碳棒,则X为碳棒,Y为铁
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属,则它们的活动性顺序为X>Y
10.用NaOH滴定pH相同、体积相同的H2SO4、HCl、CH3COOH三种溶液,恰好中和时,所用相同浓度NaOH溶液的体积依次为V1、V2、V3,则这三者的关系是( )
A.V1>V2>V3B.V1 11.用0.1mol/LNaOH溶液滴定0.1mol/L盐酸溶液,如达到滴定终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05mL),继续加水至50mL,所得溶液的pH是( ) A.10B.9C.11.5D.12.5 12.常温下,一定浓度的某溶液,由水电离出的c(OH--)=10--4mol/L,则该溶液中的溶质可能是() A.Na2SO4B.CH3COOHC.NaOHD.CH3COOK 13.等浓度的下列溶液中,NH4+浓度最大的是() A.(NH4)2SO4B.NH4ClC.(NH4)2CO3D.NH4HCO3 14.室温下,用0.100mol/LNaOH溶液分别滴定20.00ml0.100mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是() A、Ⅱ表示的是滴定醋酸的曲线 B、PH=7时,滴定醋酸消耗V(NaOH)小于20ml C、V(NaOH)=20ml时,C(Cl—)=C(CH3COO—) D、V(NaOH)=10ml时,醋酸溶液中: C(Na+)>C(CH3COO—)>C(H+)>C(OH—) 15.相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HC1O说法正确的是() A.电离程度: HCN>HClO B.pH: HClO>HCN C.NaOH恰好完全反应时,消耗NaOH的物质的量: HClO>HCN D.酸根离子浓度: c(ClO--)>c(CN--) 16.25℃时,盐酸溶液的pH是4,氯化铵溶液的pH是5,盐酸与氯化铵溶液中水电离的c(H+)之比为() A.10: 1B.1: 10C.1: 105D.105: 1 17.已知: 25°C时, , 。 下列说法正确的是 A.25°C时,饱和 溶液与饱和 溶液相比,前者的 大 B.25°C时,在 的悬浊液中加入少量的 固体, 增大 C.25°C时, 固体在20ml0.01mol· 氨水中的Ksp比在20mL0.01mol· 溶液中的Ksp小 D.25°C时,在 的悬浊液中加入NaF溶液后,不可能有 生成 18.一定条件下,在一个容积为2L的密闭容器中加入0.8molA2气体和0.6molB2气体反应达平衡生成1molAB气体并释放出热量,反应中各物质的浓度随时间的变化情况如图所示。 下列说法不正确的是 A.图中a点的值为0.15B.该反应的平衡常数K=0.03 C.温度升高,平衡常数K值减小D.平衡时A2的转化率为62.5% 19.已知在298K时下述反应的有关数据: C(s)+1/2O2(g)=CO(g)△H1=-110.5kJ/mol C(s)+O2(g)=CO2(g)△H2=-393.5kJ/mol 则C(s)+CO2(g)=2CO(g)的△H为 A.283kJ/molB.-504kJ/mol C.-172.5kJ/molD.172.5kJ/mol 20.一定温度下,三种碳酸盐MCO3(M: Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。 已知: pM=-lgc(M),pc(CO32-)=-lgc(CO32-)。 下列说法正确的是() A.MgCO3、CaCO3、MnCO3的Ksp依次增大 B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO32-) C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) D.c点可表示MgCO3的过饱和溶液,且c(Mg2+)<c(CO32-) 21.常温下体积相同的下列四种溶液: ①pH=3的盐酸②pH=3的醋酸溶液③pH=11的氨水④pH=11的NaOH溶液。 下列说法中,正确的是() A.②和④混合,所得混合溶液的pH大于7 B.将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>① C.③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④ D.①和③混合,所得混合溶液中c(H+)+c(NH4+)=c(Cl-)+c(OH-) 22.己知Ksp(AgCl)=1.56×10-10、Ksp(AgBr)=7.7×10-13、Ksp(Ag2CrO4)=9.0×10-12。 某溶液中含有C1--,Br--和CrO42--浓度均为0.010mo1/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( ) A.C1--、Br--、CrO42--B.CrO42--、Br--、C1-- C.Br--、C1--、CrO42--D.Br--、CrO42--、C1-- 23.0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度大小顺序正确的是 A.c(Na+)>c(Cl-)>c(OH-)>c(H+)B.c(Na+)=c(Cl-)>c(H+)>c(OH-) C.c(Cl-)>c(Na+)>c(OH-)>c(H+)D.c(Na+)=c(Cl-)>c(OH-)>c(H+) 24.下列有关电解质溶液中粒子浓度关系正确的是( ) A.pH=1的NaHSO4溶液: c(H+)=c(S O )+c(OH-) B.含有AgCl和AgI固体的悬浊液: c(Ag+)>c(Cl-)=c(I-) C.CO2的水溶液: c(H+)>c(HCO )=2c(CO ) D.NaHCO3溶液: c(H+)+c(HCO )+c(CO )=c(OH-) 25.下列溶液中粒子的物质的量浓度关系正确的是() A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中: C(Na+)>c(CO32-)>c(HCO3-)>c(OH-) B.20ml0.1mol/LCH3COONa溶液与10ml0.1mol/LHCl溶液混合后溶液呈酸性,所得溶液中: C(CH3COO-)>c(Cl-) >c(CH3COOH)>c(H+) C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中: c(Cl-)+c(H+)>c(NH4+)>c(OH-) D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中: c(OH-)>c(H+)+c(CH3COOH) 第II卷非选择题 二、非选择题 26.(12分)I.常温下,两种溶液①0.1mol/LNH3·H2O ②0.1mol/LNH4Cl中: (1)溶液②呈 性(填“酸”、“碱”或“中”),其原因是 __________________(用离子方程式表示),其溶液中离子浓度按由大到小的顺序为。 (2)两种溶液中c(NH4+)的大小为 (填字母)。 A.两种溶液中c(NH4+)都等于0.1mol/LB.两种溶液中c(NH4+)都小于0.1mol/L C.NH4Cl溶液中c(NH4+)小于NH3·H2O溶液中c(NH4+) II.(3)Cu(OH)2在水溶液中存在着如下沉淀溶解平衡: Cu(OH)2(s) Cu2+(aq)+2OH--(aq),在常温下KSP=2×10--20.在常温下如果要生成Cu(OH)2沉淀,需要向0.02mol/L的CuSO4溶液中加入碱溶液来调整溶液的pH,使溶液的pH大于。 将CuCl2溶液加热蒸干并灼烧,所的物质为。 27.(12分)I.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作: A.在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解 B.在250mL容量瓶中定容成250mL烧碱溶液 C.用
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第二次 月考
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《稻草人》精彩读书笔记精选多篇.docx
《稻草人》精彩读书笔记精选多篇.docx
