 届高考中对物质结构与性质的考查角度研究.docx
届高考中对物质结构与性质的考查角度研究.docx
- 文档编号:3343542
- 上传时间:2022-11-21
- 格式:DOCX
- 页数:11
- 大小:618.69KB
届高考中对物质结构与性质的考查角度研究.docx
《届高考中对物质结构与性质的考查角度研究.docx》由会员分享,可在线阅读,更多相关《届高考中对物质结构与性质的考查角度研究.docx(11页珍藏版)》请在冰豆网上搜索。
届高考中对物质结构与性质的考查角度研究
高考中关于物质结构与性质的几个考查角度
一、数列的表达式问题
例:
(2019高考全国卷Ⅲ)直链的多磷酸盐是一种复杂磷酸盐,如:
焦磷酸钠、三磷酸钠等。
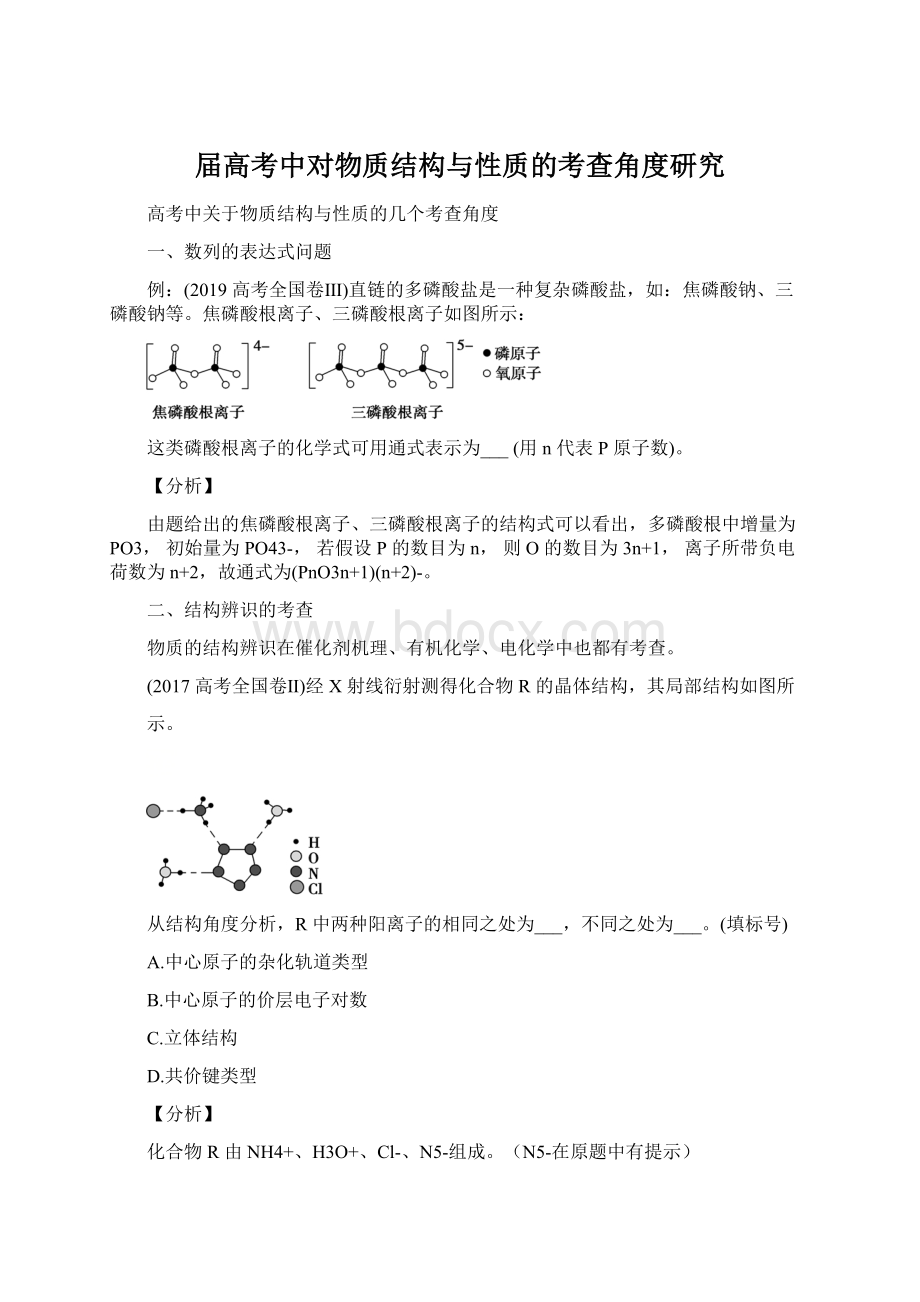
焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为___(用n代表P原子数)。
【分析】
由题给出的焦磷酸根离子、三磷酸根离子的结构式可以看出,多磷酸根中增量为PO3,初始量为PO43-,若假设P的数目为n,则O的数目为3n+1,离子所带负电荷数为n+2,故通式为(PnO3n+1)(n+2)-。
二、结构辨识的考查
物质的结构辨识在催化剂机理、有机化学、电化学中也都有考查。
(2017高考全国卷Ⅱ)经X射线衍射测得化合物R的晶体结构,其局部结构如图所
示。
从结构角度分析,R中两种阳离子的相同之处为___,不同之处为___。
(填标号)
A.中心原子的杂化轨道类型
B.中心原子的价层电子对数
C.立体结构
D.共价键类型
【分析】
化合物R由NH4+、H3O+、Cl-、N5-组成。
(N5-在原题中有提示)
三、晶体粒子配位数的考查
配位数的考查主要有金刚石或CaF2的4配位,NaCl或简单立方的6配位,CsCl、
CaF2或体心立方的8配位,面心立方或六方的12配位。
其中六方的12配位需要用六棱柱判断,如用下图中上面的面心的黄球来推理。
例:
(2020·高考全国卷Ⅱ)(CaTiO3的晶胞如图所示,Ca2+的配位数是___。
【分析】以Ca2+为中心的水平切面上有4个O2-与它距离相等,以Ca2+为中心的前后垂直切面上有4个O2-与它距离相等,以Ca2+为中心的左右垂直切面上有4个O2-与它距离相等,所以配位数为12。
四、晶胞中原子坐标问题的考查
下图为CuCl的晶胞。
原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为(0,
0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为___。
【分析】此晶胞与金刚石晶胞类似。
要解此题,需要对金刚石晶胞的结构非常理解。
D位于晶胞中右、前、下方的1/8晶胞的小立方体的体心位置。
D在x方向上处于3/4位置,在y方向上处于1/4位置,在z方向上处于1/4位置,故D的坐标参数为(3/4,1/4,1/4)。
五、轨道成键问题的考查
考查轨道的杂化方法、轨道的成键问题。
如σ键中的s-sσ键,s-pσ键,p-pσ键,spn杂化轨道-sσ键,spn杂化轨道-pσ键,spn杂化轨道-spm杂化轨道σ键,p-pπ键等。
1.SOCl2中S的___杂化轨道与O的2p轨道形成___键,S的3p轨道与O的2p
轨道形成___键。
【分析】SOCl2的电子式为
,价层电子对为3,sp2杂化,其杂化轨道与O只能形成σ键,S剩余的一个3p轨道与O的2p轨道形成π键。
2.CH3-CN中的C-C键是由___杂化轨道与___杂化轨道形成σ键。
【分析】
甲基上的C为sp3杂化,氰基上的C为sp杂化,所以由sp3杂化轨道与sp杂化轨道形成σ键。
六、杂化方式种类的考查
1.(2020高考山东等级考)一种Cd2+配合物的结构如图所示,该化合物中N的杂化方式有种。
【分析】
由于Cd2+带两个正电荷,可以推理出,左边为NO3-,结构为
,价层电子对数为3,杂化类型为sp2杂化。
右侧为NO2-,结构为
,价层电子对数为3,杂化类型为sp2
杂化。
上面和下面的
,价层电子对数为3,杂化类型为sp2杂化。
2.(2020高考全国卷Ⅲ)
(1)NH3BH3分子中,N-B化学键称为___键,其电子对由
___提供。
(2)氨硼烷在催化剂作用下水解释放氢气:
3NH3BH3+6H2O=3NH4++B3O63-+9H2↑,B3O63-的结构为
。
在该反
应中,B原子的杂化轨道类型由___变为___。
【分析】
(1)B原子最外层有3个电子,其与3个H原子形成共价键后,其价层电子对只有3对,还有一个空轨道;在NH3中,N原子有一个孤对电子,故在NH3BH3分子中,N-B键为配位键,其电子对由N原子提供。
(2)NH3BH3分子中,B原子的价层电子对数为4,故其杂化方式为sp3。
由B3O63-的结构信息可知,每个B原子只形成3个σ键,其中的B原子的杂化方式为sp2,因此,B原子的杂化轨道类型由sp3变为sp2。
七、大π键分析的考查
1.(2017高考全国卷Ⅱ)分子中的大π键可用符号Πmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π66),则下图中N5-中的大π键应表示为___。
【分析】
N5-的结构如图。
双键两边的4个N各提供1个电子形成大π键,带负电荷的N原子提供的p轨道的2个电子形成大π键,所以大π键应表示为Π56。
2.(2020高考山东等级考)B3N3H6(无机苯)的结构与苯类似,也有大π键。
下列关于
B3N3H6的说法错误的是()
A.其熔点主要取决于所含化学键的键能
B.形成大π键的电子全部由N提供
C.分子中B和N的杂化方式相同
D.分子中所有原子共平面
【分析】
B3N3H6的结构与苯类似,如上图,12个原子都在同一平面,也有大π键。
B原子最外层有3个电子,与3个原子形成共价键后,还有一个空轨道;在N原子最外层有5个电子,与3个原子形成共价键后,还有一个孤电子对。
对于大π键,B只能提供空轨道,N提供一个孤电子对,表示为Π66。
八、利用原子半径进行晶胞边长、原子间距计算的考查
1.(2019高考全国卷Ⅰ)图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。
图(b)是沿立方格子对角面取得的截图。
可见,Cu原子之间最短距离x=___pm,Mg原子之间最短距离y
=___pm。
【分析】由题图(b)可知,立方格子面对角线长为a√2pm,即为4个Cu原子直径之和,则Cu原子之间最短距离为a√2/4pm。
由题图(b)可知,若将每个晶胞分为8个小立方体,则Mg原子之间最短距离不是面上对角两点的距离,而是体心与顶点的距离,如下图所示。
y=(1/2)apm×√3×1/2=√3/4apm。
2.(2018高考全国卷Ⅲ)金属Zn晶体中的原子堆积方式如图所示,六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为___g·cm-3(列出计算式)。
【分析】六棱柱底边边长为acm,则六棱柱上下面的面积均为3√3/2a2cm2,则六棱柱的体积为3√3/2a2ccm3。
锌原子在六棱柱的顶点、上下面心和晶胞内,一个晶胞含锌原子个数为12×1/6
+2×1/2+3=6,因此一个晶胞中Zn的质量=65×6/NAg。
由此可知,Zn的密度为65×6/(NA×3√3/2a2c)g·cm-3。
九、空间位置相似性判断的考查
(2020高考全国卷Ⅱ,改)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH3+,其晶胞如图(b)所示。
其中Pb2+与图(a)中___的空间位置相同,CH3NH3+与与图(a)中___的空间位置相同。
【分析】
图(b)中I-位于面心上,每个Pb2+周围距离最近的有6个I-,Pb2+正好位于由6个I-形成的正八面体的体心位置。
图(a)中每个Ti4+周围距离最近的有6个O2-(需要考虑晶胞外的O2-),Ti4+也是正好位于由6个O2-形成的正八面体的体心位置。
图(b)中I-位于面心上,每个CH3NH3+周围距离最近的有12个I-(需要考虑晶胞外的I-),图(a)中每个Ca2+周围距离最近的有12个O2-,两者相似。
所以,Pb2+与Ti4+的空间位置相同,CH3NH3+与Ca2+的空间位置相同。
十、晶胞中正八面体空隙、正四面体空隙的观察与计算的考查
1.(2018高考全国卷Ⅱ)FeS2晶体的晶胞如图所示。
晶胞棱长为anm,晶胞中Fe2+
位于S22-所形成的正八面体的体心,该正八面体的边长为___nm。
【分析】本晶胞中对正八面体做了虚线描绘,观察起来比较容易。
分析晶胞结构可知,Fe2+位于棱心和体心,S22-位于顶点和面心,正八面体的边长即为两个面心点的距离,因此正八面体的边长为√2/2anm。
2.(2019高考全国卷Ⅰ)下图是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。
【分析】
如下图,四个红点形成的正四面体,里面填充了一个正四面体的Cu4。
四个红点形成的正四面体所对应的小立方体,是晶胞的八个小立方体中,体心未填充Mg的四个立方体中的一个。
晶胞的另外三个位置,也存在着这种结构。
如下图,六个红点形成的正八面体,里面也相当于填充了一个正四面体的Cu4。
3.Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、
6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。
Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,有___%的正八面体空隙没有填充阳离子。
【分析】
由图可知晶体结构中O2-数目为8×1/8+6×1/2=4个,根据Fe3O4的化学式,同时可以推理出晶胞中的Fe3+有2个,Fe2+有1个。
如图,结构中如1、3、6、7的O2-围成的正四面体空隙有8个。
Fe3O4中有一半的Fe3+填充到正四面体空隙中,则只有1个正四面体中有Fe3+。
若晶胞边长为a,则每个正四面体的体积为1/8a3-1/8a2×1/2a×1/3×4=1/24a3。
即这
个Fe3+占用了晶胞空间的1/24。
如图,结构中如3、6、7、8、9、12的O2-围成的正八面体空隙有1个。
正八面体的体积为1/2a2×1/2a×1/3×2=1/6a3。
另一半Fe3+和Fe2+填充在正八面体空隙中,则另1个Fe3+和Fe2+填充正八面体空隙中。
若这两个离子每个也占用了晶胞空间的1/24。
两个共占用了晶胞空间的1/12。
而正八面体占用晶胞空间的1/6,所以这两个离子占用了正八面体空间的50%。
4.
铬的一种氧化物的晶胞结构如图所示,其中氧离子与晶体镁堆积方式一致,铬离子在其八面体空隙中(如:
CrA在O1、O2、O3、O4、O5、O6构成的八面体空隙中)。
该晶胞有___%八面体空隙未填充阳离子。
【分析】此晶胞中O2-采用六方堆积方式。
根据题中利用O5、O6和O3、O4、与O1、形成正八面体,可以推理,利用中间3个O2-形成的三角形的另外两条边,分别与1和上面的两条边,形成另外两个正八面体,如下图。
在三个正八面体中,只有两个体心上有铬离子,所以有1/3的正八面体空隙未填充阳离子。
【练习】
1.Cr和Ca可以形成某种具有特殊导电性的复合氧化物,晶胞结构如图所示。
(1)该晶体的化学式为。
(2)若Ca与O的核间距离为xnm,则该晶体的密度为g·cm-3。
2.铜镍合金的立方晶胞结构如图所示,其中原子A的坐标参数为(0,1,0)。
(1)原子B的坐标参数为。
(2)若该晶体密度为dg·cm-3,则铜镍原子间最短距离为pm。
3.CaF2的晶胞为立方晶胞,结构如图所示:
(1)CaF2晶胞中,Ca2+的配位数为。
(2)“原子坐标参数”可表示晶胞内部各原子的相对位置,已知A、B两点的原子坐标参数如图所示,则C点的“原子坐标参数”为(___,,1/4)。
(3)晶胞中两个F-的最近距离为273.1pm,用NA表示阿伏加德罗常数的值,则晶胞的密度为g·cm-3(列出计算式即可)。
4.(2020高考山东等级考)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。
四方晶系CdSnAs2的晶胞结构如图所示。
晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标
x
y
z
Cd
0
0
0
Sn
0
0
0.5
As
0.25
0.25
0.125
(1)一个晶胞中有个Sn。
(2)找出距离Cd(0,0,0)最近的Sn(用分数坐标表示)。
(3)CdSnAs2晶体中与单个Sn键合的As有个。
【练习答案】
1.
(1)CaCrO3
(2)(7×1022)/(√2×x3×NA)
2.
(1)(1/2,0,1/2)
(2)√2/2×(251/dNA)1/3×1010
3.
(1)8
(2)3/43/4
(3)(4×78)/[NA(546.2×10-10)3]
4.
(1)4
(2)(0.5,0,0.25)、(0.5,0.5,0)(3)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 物质 结构 性质 考查 角度 研究
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
