 高中化学18弱电解质的电离平衡.docx
高中化学18弱电解质的电离平衡.docx
- 文档编号:3161348
- 上传时间:2022-11-18
- 格式:DOCX
- 页数:19
- 大小:147.76KB
高中化学18弱电解质的电离平衡.docx
《高中化学18弱电解质的电离平衡.docx》由会员分享,可在线阅读,更多相关《高中化学18弱电解质的电离平衡.docx(19页珍藏版)》请在冰豆网上搜索。
高中化学18弱电解质的电离平衡
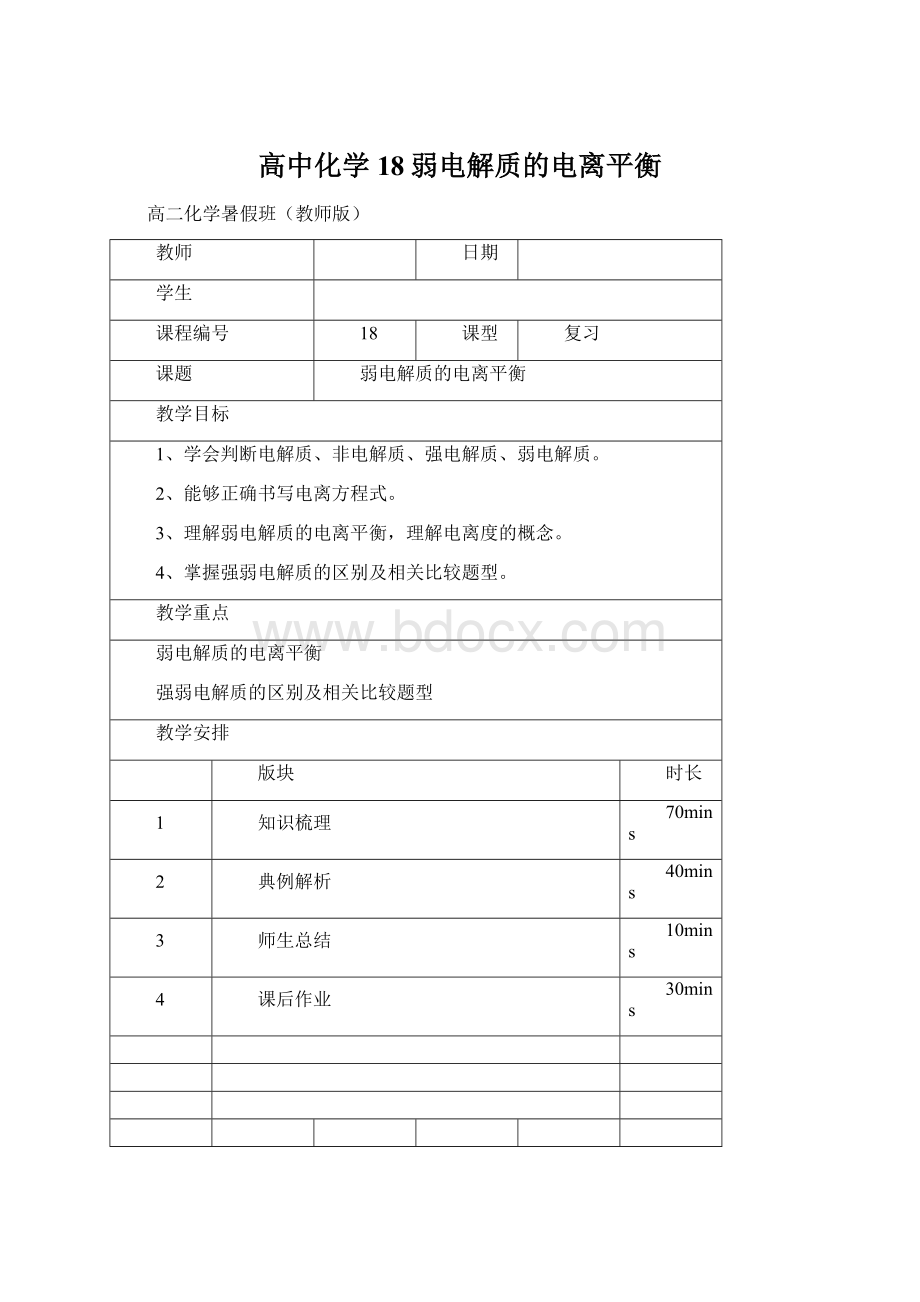
高二化学暑假班(教师版)
教师
日期
学生
课程编号
18
课型
复习
课题
弱电解质的电离平衡
教学目标
1、学会判断电解质、非电解质、强电解质、弱电解质。
2、能够正确书写电离方程式。
3、理解弱电解质的电离平衡,理解电离度的概念。
4、掌握强弱电解质的区别及相关比较题型。
教学重点
弱电解质的电离平衡
强弱电解质的区别及相关比较题型
教学安排
版块
时长
1
知识梳理
70mins
2
典例解析
40mins
3
师生总结
10mins
4
课后作业
30mins
一、电解质与非电解质的判断
1.定义
电解质
非电解质
定义
在水溶液或熔融状态下能够导电的化合物
凡是在水溶液里和熔融状态下都不能导电的化合物
常见物质与类别
所有的离子化合物和部分共价化合物:
酸、碱、盐、水、金属氧化物
全是_______化合物:
非金属氧化物、氨气及绝大多数的有机物
2.注意点
(1)单质、混合物既不是电解质也不是非电解质。
(2)电解质是纯净物,电解质溶液是混合物。
(3)CO2、SO2溶于水能够导电,但溶液中的离子不是他们本身电离所产生的,所以仍为_______
_________。
(4)有机物中只有有机酸是电解质,其他都不是。
【答案】共价非电解质
3.物质导电情况
共价化合物:
属于电解质的共价化合物只有在溶液中能导电。
离子化合物:
熔融状态和溶液中均能导电。
金属:
固体和熔融状态下均能导电。
【练一练】
1.下列物质中,属于电解质的是_____________,属于非电解质的是_______________。
A.二氧化硫B.氨气C.铜D.硫酸钡晶体
E.无水硫酸F.氯化氢气体G.饱和食盐水H.蔗糖
I.酒精水溶液J.熔融的氯化钠
【答案】DEFJ、ABH
2.下列物质在给定条件下能导电的是______________。
A.NaCl固体B.石墨C.熔融NaOHD.稀硫酸
E.HCl气体F.CuG.熔融的F
【答案】B、C、D、F、G
二、强电解质与弱电解质的判断
1.强弱电解质的比较
强电解质
弱电解质
定义
在水溶液中全部电离成离子的电解质
在水溶液中只有一部分电离成离子的电解质
电离程度
完全
部分
溶液里粒子
水合离子
水合分子、水合离子
常见物质
通常为
强酸:
HCl、H2SO4、HNO3等
强碱:
NaOH、KOH、Ba(OH)2等
绝大多数盐:
NaCl、CaCO3、CH3COONa等
通常为
弱酸:
CH3COOH、HF、HClO、H2S、H2CO3、H2SiO3、H4SiO4等
弱碱:
NH3·H2O、Cu(OH)2等
极少数盐、水
与常见物质类别的关系
离子化合物与某些共价化合物
某些共价化合物
2.电解质溶液的导电性与导电能力
溶液的导电能力取决于自由移动的离子的___________以及___________________。
注意点:
(1)电解质的强弱与溶解性无关
如:
NaCl溶液导电性强于AgCl溶液,但两溶液中的溶质都是强电解质
(2)电解质强弱与溶液的导电能力无关
如:
CH3COOH是弱电解质,BaSO4是强电解质
(3)电解质不一定导电,导电的不一定是电解质
如:
NaCl固体是强电解质,但不导电;如Cu能导电,但既不是电解质也不是非电解质。
【答案】浓度大小离子所带电荷的多少
【练一练】
1.判断下列物质中,属于强电解质的是_____________________,属于弱电解质的是_________
________________。
(1)NaCl
(2)NH3(3)Cl2(4)BaSO4(5)HCl(6)CH3COOH(7)HNO2(8)NaHCO3(9)Cu(OH)2(10)Cu(11)HF(12)HNO3(13)Al2(SO4)3(14)SO2
(15)无水乙醇(16)H2S(17)Na2O(18)H3PO4(19)蔗糖(20)盐酸
【答案】
(1)(4)(5)(8)(12)(13)(17)
(6)(7)(9)(11)(16)(18)
2.关于强、弱电解质的叙述正确的是()
A.强电解质都是离子化合物、弱电解质都是共价化合物
B.强电解质都是可溶性化合物,弱电解质都是难溶性化合物
C.强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子
D.强电解质水溶液的导电能力强,弱电解质的水溶液导电能力弱
【答案】C
三、弱电解质的电离平衡
1.定义
在一定条件下(如温度、浓度)下,当电解质分子离解成离子的速率和离子结合成分子的速率相等时,电离过程就达到了平衡状态。
2.特征
弱:
弱电解存在着电离平衡
等:
电解质分子离解成离子的速率和离子结合成分子的速率相等
定:
条件一定,分子与离子浓度一定
动:
动态平衡
变:
条件改变,平衡破坏,发生移动
吸:
弱电解质的电离是个吸热过程
3.电离平衡的移动
原理:
符合勒夏特列原理
影响因素
内因:
电解质本身的结构决定。
一般共价键极性越弱,电解质越弱,其电离程度越小。
常温下绝大多数0.1mol/L弱电解质的电离分子数不超过10%
外因:
a.浓度:
浓度越大,电离程度________,越稀越易电离。
在稀释溶液时,电离平衡向右移动,而离子浓度会___________。
b.温度:
温度越高,电离程度越________。
(弱电解质的电离是个_________过程)
c.同离子效应:
如在醋酸溶液中加入醋酸钠晶体,增大了CH3COO-浓度,平衡左移,电离程度减小;加入稀HCl,平衡也会左移。
d.能反应的物质:
如在醋酸溶液中加入锌或NaOH溶液,平衡右移,电离程度增大
4.电离度
(1)定义:
α=
×100%
=
×100%
=
×100%
(2)影响电离度的因素
A.内因:
电解质本身的性质,电解质越弱,电离度越小。
B.外因:
①对于同一弱电解质,溶液越稀,电离度越________。
②温度越高,电离度越________。
(电离过程一般都是吸热过程)
【答案】越小减小大吸热大大
【练一练】在一定条件下,0.1mol/L的氨水溶液中有下列平衡:
NH3·H2O
NH4++OH-改变下表所述条件,选用"增大,减少,不变"填写有关空格:
C(NH3·H2O)
C(NH4+)
C(OH-)
电离度
pH值
加入少量硫酸
加入少量烧碱
加固体氯化铵
加水稀释
【答案】
NH3·H2O
NH4+
OH-
电离度
pH值
加入少量硫酸
减少
增大
减少
增大
减小
加入少量烧碱
增大
减少
增大
减少
增大
加固体氯化铵
增大
增大
减少
减少
减小
加水稀释
减少
减少
减少
增大
减少
四、电离方程式的书写
1.规则
强等号、弱可逆、多元弱酸分步写、多元弱碱一步写
2.举例
写出下列物质在水溶液中的电离方程式:
①H2SO4:
②Ba(OH)2:
③CH3COOH:
④NH3.H2O:
⑤H2CO3:
⑥Na2CO3:
⑦NaHSO4:
⑧NaHCO3:
⑨Al(OH)3:
【答案】①H2SO4→2H++SO42-②Ba(OH)2→Ba2++2OH-
③CH3COOH
CH3COO-+H+④NH3.H2O
NH4++OH-
⑤H2CO3
H++HCO3-⑥Na2CO3→2Na++CO32-
⑦NaHSO4→Na++H++SO42-⑧NaHCO3→Na++HCO3-
⑨Al(OH)3
Al3++3OH-
五、一元强酸和一元弱酸的比较
比较对象
等物质的量浓度、等体积的盐酸(a)与醋酸(b)
相同PH、相同体积的盐酸(a)与醋酸(b)
c(H+)
PH
物质的量浓度
溶液导电性
中和NaOH的量
开始与金属反应产生H2的速率
与足量金属反应产生H2的体积
分别加该酸钠盐固体后的pH
【答案】
比较对象
等物质的量浓度、等体积的盐酸(a)与醋酸(b)
相同pH、相同体积的盐酸(a)与醋酸(b)
c(H+)
a>b
a=b
pH
a<b
a=b
物质的量浓度
a=b
a>b
溶液导电性
a>b
a=b
中和NaOH的量
a=b
a>b
开始与金属反应产生H2的速率
a>b
a=b
与足量金属反应产生H2的体积
a=b
a>b
【练一练】
1.下列关于盐酸与醋酸两种稀溶液的说法正确的是()
A.相同浓度的两溶液中c(H+)相同
B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠
C.pH=3的两溶液稀释100倍,pH都为5
D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小
【答案】B
2.当NaOH溶液与氨水的pH、体积都相同时,下列叙述正确的是()
A.两溶液的物质的量浓度相同
B.两溶液中的c(H+)相同
C.用同浓度盐酸中和时,消耗酸的体积相同
D.升高温度10℃,两者pH仍相等
【答案】B
知识点1:
弱电解质的电离平衡
【例1】向0.1mol/L的氨水中加入一定量的水,始终保持增大趋势的是()
A.NH3·H2O浓度B.OH-浓度
C.NH4+数目D.NH4+浓度
【难度】★★
【答案】C
变式1:
(双选)已知0.1mol/L的醋酸溶液中存在电离平衡:
CH3COOH
H++CH3COO-,要使溶液中的c(CH3COO-)/c(H+)值减小,可采取的措施是()
A.加少量烧碱溶液B.升高温度C.加少量冰醋酸D.加水
【难度】★★★
【答案】BD
变式2:
常温下0.1mol·L-1氨水溶液的pH=a,下列能使溶液pH=(a-1)的措施是()
A.将溶液稀释到原体积的10倍B.加入适量的氯化铵固体
C.加入等体积0.2mol/L盐酸D.通入氨气
【难度】★★
【答案】B
【方法提炼】
需要学生熟练掌握影响弱电解质电离平衡移动的因素,外在条件的改变会导致平衡如何移动,溶液中各微粒的浓度如何改变等等。
知识点2:
导电能力的判断
【例1】在两个溶液导电性实验装置中,分别注入30mL2mol/L的醋酸和20mL2mol/L的氨水,灯光明暗度相似,如果把这两种溶液相混合后再实验,则()
A.灯光变暗B.灯光变亮
C.灯光明暗程度不变D.灯光明暗程度变化不明显
【难度】★★
【答案】B
变式1:
常温时,浓度为0.1moL/L的一元某酸100mL,其[H+]为0.1moL/L,下列溶液中与其导电能力几乎一致的是()
A.1L0.1moL/LNaOH溶液B.200mL0.05moL/LNaNO3溶液
C.
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 18 电解质 电离 平衡
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
