 医疗器械注册产品真实性核查报告(格式文本).docx
医疗器械注册产品真实性核查报告(格式文本).docx
- 文档编号:30848676
- 上传时间:2024-02-15
- 格式:DOCX
- 页数:3
- 大小:19.30KB
医疗器械注册产品真实性核查报告(格式文本).docx
《医疗器械注册产品真实性核查报告(格式文本).docx》由会员分享,可在线阅读,更多相关《医疗器械注册产品真实性核查报告(格式文本).docx(3页珍藏版)》请在冰豆网上搜索。
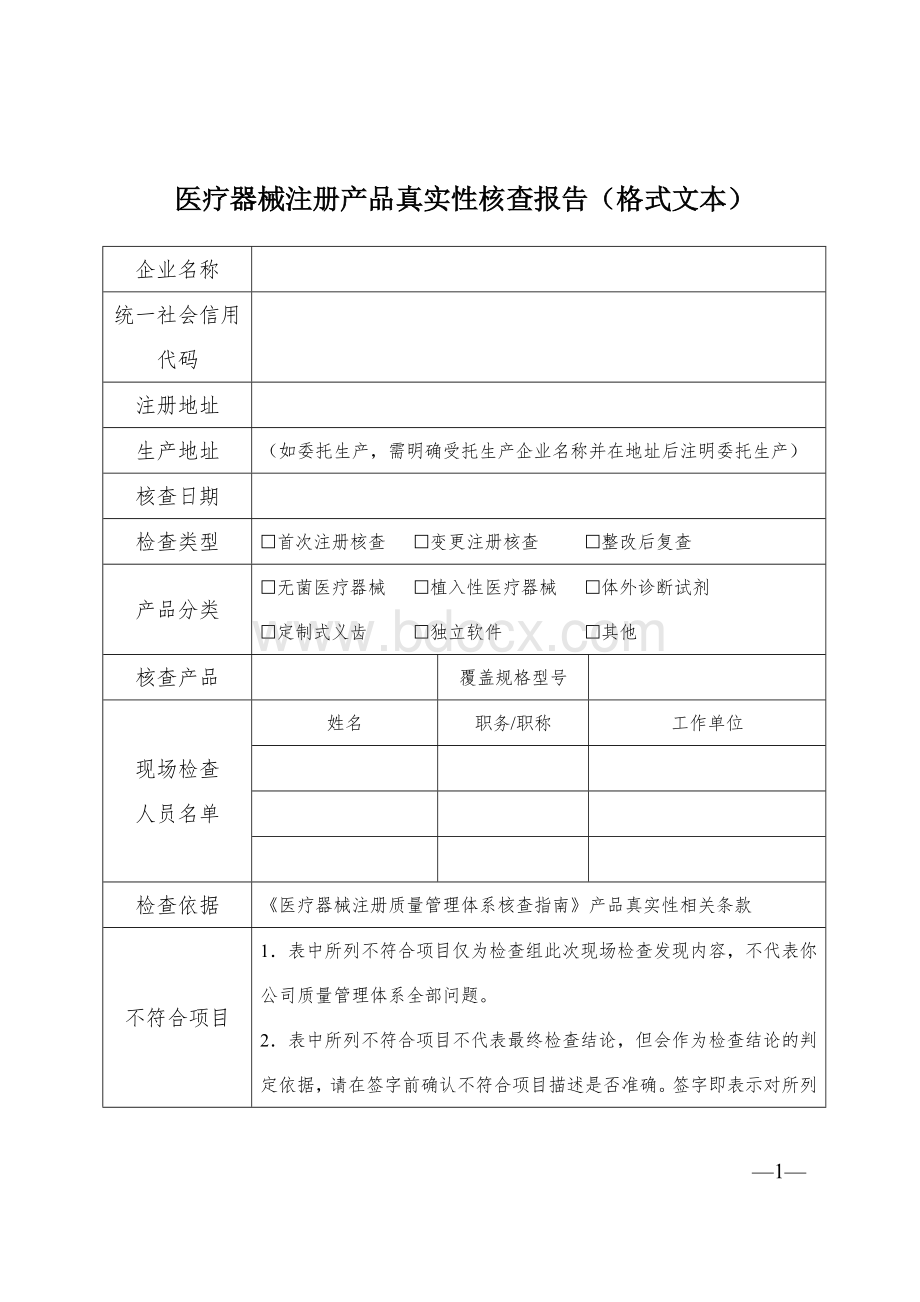
医疗器械注册产品真实性核查报告(格式文本)
企业名称
统一社会信用代码
注册地址
生产地址
(如委托生产,需明确受托生产企业名称并在地址后注明委托生产)
核查日期
检查类型
£首次注册核查£变更注册核查£整改后复查
产品分类
£无菌医疗器械£植入性医疗器械£体外诊断试剂
£定制式义齿£独立软件£其他
核查产品
覆盖规格型号
现场检查
人员名单
姓名
职务/职称
工作单位
检查依据
《医疗器械注册质量管理体系核查指南》产品真实性相关条款
不符合项目
1.表中所列不符合项目仅为检查组此次现场检查发现内容,不代表你公司质量管理体系全部问题。
2.表中所列不符合项目不代表最终检查结论,但会作为检查结论的判定依据,请在签字前确认不符合项目描述是否准确。
签字即表示对所列不符合项目的认可。
3.对不符合项目有异议的,可与检查组沟通,或向检查组织单位提交书面说明。
序号
条款号
不符合项描述
不符合项共项:
其中关键项项,一般项项。
产品真实性
核查情况
*4.10.1
注册检验产品,包括检验产品批号(编号/序列号等)及规格型号、检验时间、检验数量、检验依据、检验结论、关键原料和/或部件等信息、校准物质和/或质控物质、检验产品照片(含独立软件发布版本信息的照片)、标签等信息,应当与生产记录相符并可追溯。
是£否£
*4.10.2
临床试验产品,包括临床试验产品批号(编号/序列号等)及规格型号,应当与生产记录相符并可追溯。
是£否£
*4.10.3
生产的产品批次及生产批号或者产品编号、规格型号/包装规格、每批数量、注册检验产品和临床试验产品批号及数量、留样产品批号及数量、现存产品生产批号或者产品编号及数量、主要原材料批号及数量等应当可追溯。
是£否£
*4.10.4
应当保留用于产品生产的原材料采购记录,至少包括:
原材料品名、型号规格、批号、材质(牌号)、供应商(生产商)、质量标准及进货验收、采购凭证、出入库记录及台账等。
采购记录的相关信息应当与生产记录、注册检验报告相应内容相一致。
是£否£
*4.10.5
生产记录、过程检验原始记录、成品检验原始记录等应当符合设计输出文件要求。
是£否£
*4.10.6
如需留样,应当留存留样产品,并保留产品台账、留样观察记录。
是£否£
其他需要说明的情况
服务企业
检查组
建议
£真实性符合要求£真实性不符合要求
£限期整改
检查组成员
签字
组员
组长
观察员
企业确认
检查结果
企业负责人签字:
(加盖企业公章)
年月日
备注
—3—
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 医疗器械 注册 产品 真实性 核查 报告 格式 文本
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《铁皮石斛生产全产业链管控技术规范》(报批稿).docx
《铁皮石斛生产全产业链管控技术规范》(报批稿).docx
