 完整版常见阳离子的检验方法.docx
完整版常见阳离子的检验方法.docx
- 文档编号:3038484
- 上传时间:2022-11-17
- 格式:DOCX
- 页数:8
- 大小:17.37KB
完整版常见阳离子的检验方法.docx
《完整版常见阳离子的检验方法.docx》由会员分享,可在线阅读,更多相关《完整版常见阳离子的检验方法.docx(8页珍藏版)》请在冰豆网上搜索。
完整版常见阳离子的检验方法
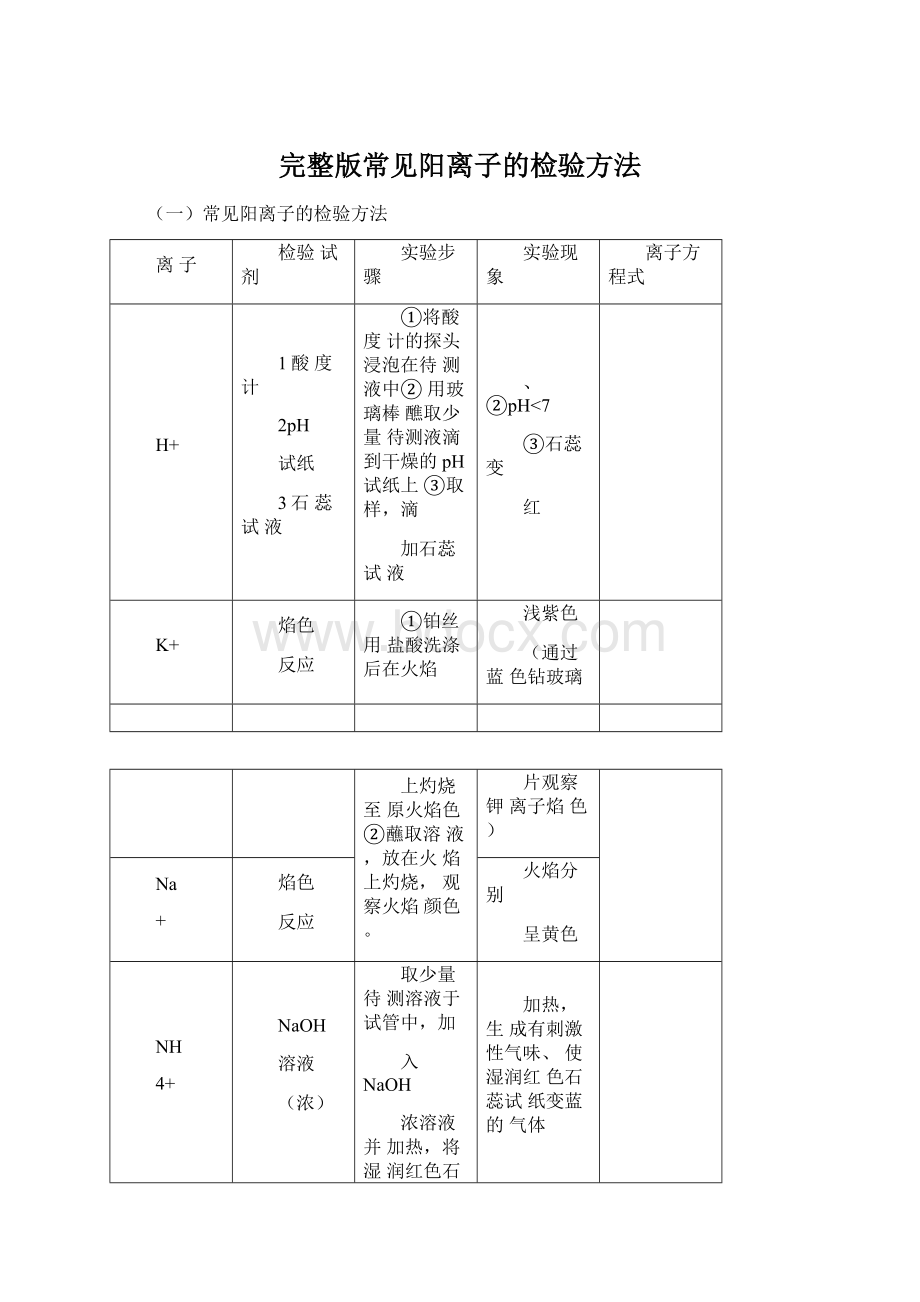
(一)常见阳离子的检验方法
离子
检验试剂
实验步骤
实验现象
离子方程式
H+
1酸度计
2pH
试纸
3石蕊试液
①将酸度计的探头浸泡在待测液中②用玻璃棒醮取少量待测液滴到干燥的pH试纸上③取样,滴
加石蕊试液
、②pH<7
③石蕊变
红
K+
焰色
反应
①铂丝用盐酸洗涤后在火焰
浅紫色
(通过蓝色钻玻璃
上灼烧至原火焰色②蘸取溶液,放在火焰上灼烧,观察火焰颜色。
片观察钾离子焰色)
Na
+
焰色
反应
火焰分别
呈黄色
NH
4+
NaOH
溶液
(浓)
取少量待测溶液于试管中,加
入NaOH
浓溶液并加热,将湿润红色石蕊试纸置于试管口
加热,生成有刺激性气味、使湿润红色石蕊试纸变蓝的气体
Ag
+
稀
HNO3
、稀盐酸(或
取少量待测溶液于试管中,加入稀
生成白色沉淀,不溶于稀
Ag++CI――
AgClJ
NaCI)
HNO3再
加入稀盐酸(或
NaCI)
HNO3
Ba
2+
①稀
H2SO
4或可
溶性硫酸盐溶液②稀
HNO3
取少量待测溶液于试管中,加入稀
H2SO4再加入稀
HNO3
产生白色沉淀,且沉淀不溶于稀
HNO3
Ba2++
SO42-=BaSO&
Fe
3+
KSCN
溶液
取少量待测溶液于试管中,加
入KSCN
溶液
变为血红
色溶液
Fe3++3SCN——
Fe(SCN)3
加苯酚
取少量待测溶液于试管中,加苯酚
溶液显紫色
淀粉
KI溶
液
滴加淀粉
KI溶液
溶液显蓝色
2Fe3++2l――
2Fe2++I2
加
NaOH
溶液
力口NaOH
溶
产生红褐色沉淀
Fe3++3OH――
Fe(OH)3J
离子
检验试剂
实验步骤
实验现象
离子方程式
Fe
2+
①KSCN溶液,新
制的氯水
①取少量待测溶液于试管中,加入
KSCN溶
①加入
KSCN溶液不显红色,加入少量新制
2Fe2++
CI2#FormatlmglD_1#2Fe3++2CI-Fe3++3SCN――Fe(SCN)3
液,新制的氯水
的氯水后,立即显红色。
②加
NaOH
溶液
②取少量待测溶液于试管中,加入
NaOH溶液并露置在空气中
②开始时生成白色
Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色
Fe(OH)3
沉淀。
Fe2++2OH—=Fe(OH)2J4Fe(OH)2十O2+2H2O=4Fe(
OH)3
③(无其它还原性物质如
SO32-)酸性
取少量待测溶液于试管中,加入酸性高锰酸钾溶液
加入酸性高锰酸钾溶液紫色褪去
高锰酸钾
AI3
+
NaOH
溶液
取少量待测溶液于试管中,逐滴加入
NaOH溶
液至过量
加入适量
NaOH溶液后生成白色沉
淀,该沉淀溶于过量NaOH溶液中
AI3++3OH――
AI(OH)3JAI(OH)3+OH——AIO2-+2H2O
Cu
2+
NaOH
溶液
取少量待测溶液于试管中,加
入NaOH
溶液
加入适量
NaOH溶
液后生成蓝色沉淀
Cu++2OH――
Cu(OH)2J
(二)常见阴离子的检验方法
离
检验试
实验步骤
实验现
离子方程式
子
剂
象
OH
1酸度
计
2pH
试纸③酚酞或石蕊试液
①将酸度计的探头浸泡在待测液中②用玻璃棒醮取少量待测液滴到干燥的pH试纸上③取样,滴加石蕊试液
2pH>7
3酚酞变红或石蕊变蓝
CO
32-
①BaCI
2溶液、
稀盐酸
取少量待测溶液于试管中,加入
BaCI2溶
液再向沉淀中加入
1•加入BaCI2溶液后生成白色
沉淀,沉淀溶于稀盐酸,
Ba2++CO32-=BaCO$BaCO3+2H+=Ba2++CO2f+H2O
稀盐酸。
并放出无色无味气体
②稀盐
酸、
Ca(OH)2溶液
取少量待测溶液于试管中,加入稀盐酸后放出的气体通入使澄清的
Ca(OH)2
溶液
2•加入稀盐酸后放出无色无味气体,通入澄清的
Ca(OH)
2溶液变浑浊
CO32-+2H+=H2O+CO2TCa2++2OH—+CO2=CaCO3;+H2O
SO
42-
BaCl2
溶液、稀硝酸或稀盐酸
取少量待测溶液于试管中,加入
BaCl2溶
液再向沉淀中加入
生成不溶于稀硝酸或稀盐酸的白色沉淀
Ba2++
SO42-=BaSO4;
稀盐酸。
SO
32-
①稀盐酸、品红溶液
取少量待测溶液于试管中,加入稀盐酸后放出的气体通入品红溶液
加入稀盐酸后放出的气体使品红溶液褪色
SO32-+2H+=H20+S02?
②BaCI
2溶液、
稀盐酸
取少量待测溶液于试管中,加入
BaCI2溶
液再向沉淀中加入稀盐酸。
加入
BaCI2溶
液后生成白色沉淀,沉淀溶于稀盐酸,并放出刺激性气味的
SO32-+2H+=H2
O+SO2?
气体
离子
检验试
剂
实验步骤
实验现
象
离子方程式
Cl
AgN03
溶液、稀硝酸或稀盐酸
取少量待测溶液于试管中,加入
AgNO3
溶液,再向沉淀中加入稀盐酸。
生成不溶于稀硝酸或稀盐酸的白色沉淀
Ag++CI――
AgClJ
Br
AgNO3
溶液、稀硝酸或稀盐酸
生成不溶于稀硝酸或稀盐酸的浅黄色沉淀
Ag++Br――
AgBrJ
I—
①AgNO3溶
液、稀
①生成
不溶于
稀硝酸
Ag++I――AglJ
硝酸
的黄色
沉淀
②新制氯水,淀粉溶液
取少量待测溶液于试管中,加入新制氯水,再加入淀粉溶液
②滴入新制
CI2,振
荡后再滴入淀粉溶液,变蓝
Ag++I—=AglJ2I-+CI2=I2+2CI-
I2遇淀粉变蓝
Cl
O-
HCl、淀粉-KI
取少量待测溶液于试管中,加入HCI溶液,然后加入淀粉-KI溶液
淀粉-KI
溶液变蓝
HCl、石
取少量待
测溶液于
石蕊先
变红后
心心
试管中,加入HCI溶液,然后加入石蕊试液
褪色
汪意:
1.若SO42-与Cl-同时检验,需注意检验顺序。
应先用
Ba(NO3)2溶液将SO42枪出,并滤去BaS04然后再用AgN03检验Cl-o
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。
因为稀硝酸能把SO32-氧化成SO42-o
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用
盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+o
4.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用
盐酸将Ag+检验出
5.若CO32千口HC03同时检验,应先用足量的BaCI2溶液将CO32枪出,静置,取上层清夜用Ba(0H)2或Ca(0H)2检出HCO3-
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 完整版 常见 阳离子 检验 方法
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
 水生态系统保护与修复-唐克旺2013全国水利风景区规划设计培训班课件.pps
水生态系统保护与修复-唐克旺2013全国水利风景区规划设计培训班课件.pps
