 第一学期生物化学实验教案 韩栓.docx
第一学期生物化学实验教案 韩栓.docx
- 文档编号:3014218
- 上传时间:2022-11-17
- 格式:DOCX
- 页数:28
- 大小:126.73KB
第一学期生物化学实验教案 韩栓.docx
《第一学期生物化学实验教案 韩栓.docx》由会员分享,可在线阅读,更多相关《第一学期生物化学实验教案 韩栓.docx(28页珍藏版)》请在冰豆网上搜索。
第一学期生物化学实验教案韩栓
生物化学实验教案
生物化学实验原理、方法和技术是生命科学等诸多学科的重要研究手段,是生物科学专业学生必修的基础实验课程。
它不仅是生物化学教学重要的组成部分,而且在培养学生分析和解决问题的能力、严谨的科学态度和独立工作的能力等方面,有着不可替代的作用。
按照生物科学专业教学计划的安排,并充分考虑实验室实验设备的现状以及学科发展的需要,本实验教学大纲主要以容易采摘及获得的动、植物材料为研究对象,围绕各类生物大分子的分离和测定,安排了一系列不同层次的实验项目,重点突出电泳、比色等常用的生化实验技术,所用的多为普通生化实验设备,一般无需大型精密仪器。
所选实验均系多年来在教学和科研中较为成熟的实验方法,适合初学者使用。
同时在实验选择上充分考虑到学科发展的成果,安排了一定比例的提高型实验。
通过实验,使学生了解、验证、巩固和加深理论课的基本知识,掌握生物化学常用的实验技术和方法。
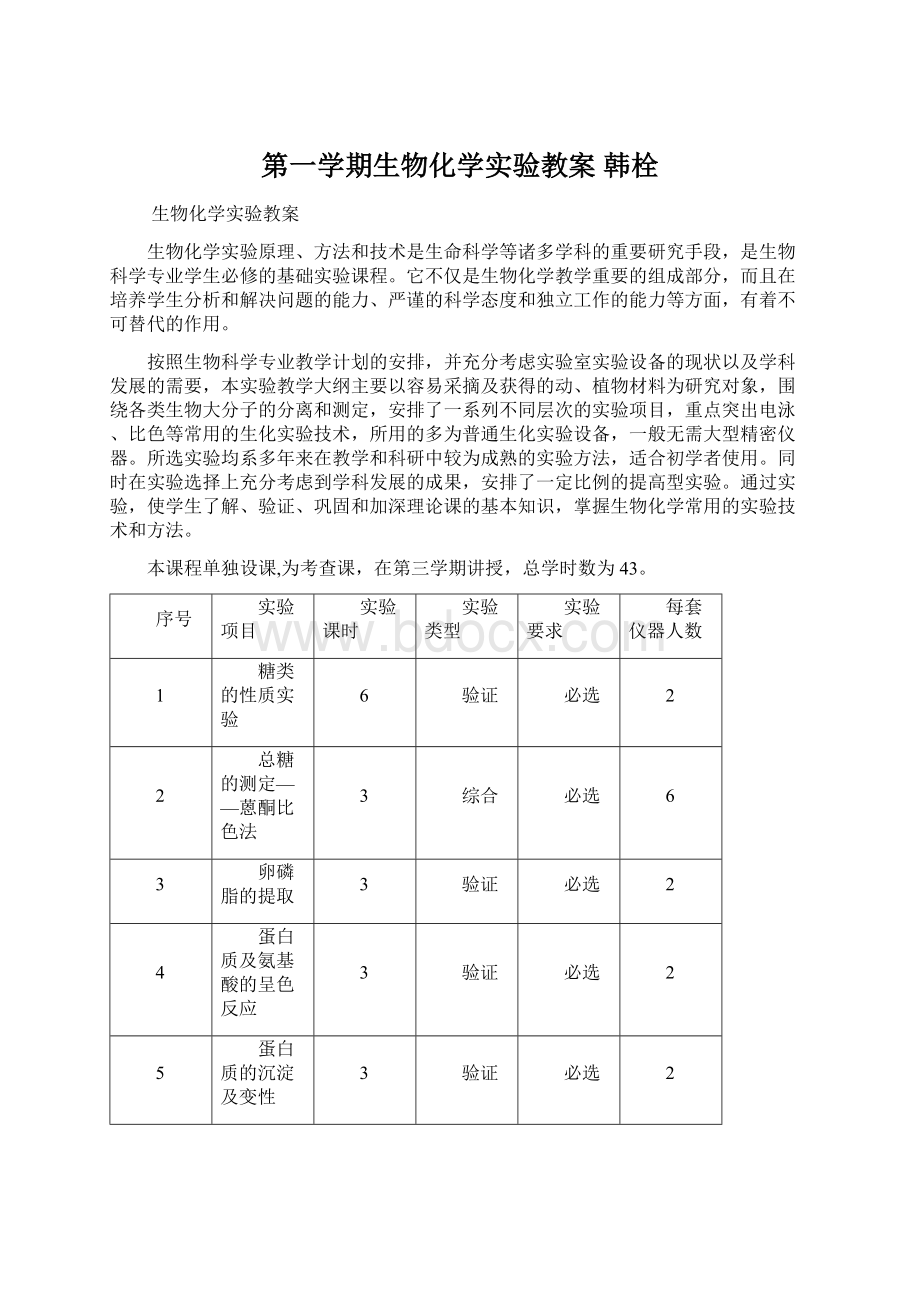
本课程单独设课,为考查课,在第三学期讲授,总学时数为43。
序号
实验项目
实验课时
实验类型
实验要求
每套仪器人数
1
糖类的性质实验
6
验证
必选
2
2
总糖的测定——蒽酮比色法
3
综合
必选
6
3
卵磷脂的提取
3
验证
必选
2
4
蛋白质及氨基酸的呈色反应
3
验证
必选
2
5
蛋白质的沉淀及变性
3
验证
必选
2
6
蛋白质的等电点测定
3
验证
必选
2
7
氨基酸的分离鉴定——纸层析法
3
验证
必选
2
8
酪蛋白的制备
3
验证
必选
6
9
蛋白质含量测定法
(一)Bradford法
3
综合
选修
6
10
蛋白质含量测定法
(二)紫外吸收法
3
综合
选修
6
11
定磷法测定核酸含量
3
验证
选修
6
12
蛋白质的透析
3
验证
选修
2
13
甲醛滴定法测定氨基氮
3
验证
选修
6
14
紫外吸收法测定核酸的含量
3
验证
选修
6
预实验基本操作
一.目的
1.熟悉实验室规则及常用生化仪器。
2.掌握各种仪器的正规操作。
3.清点洗刷实验用具。
一、实验内容
(一)
常用生化仪器
量器:
量筒、离心管、吸量管、容量瓶
玻璃仪器
容器:
烧杯、试管、锥形瓶、滴管
仪器:
离心机、水浴箱、电泳仪、分光光度计等
(二)玻璃仪器的洗涤
1、初用的玻璃仪器的清洗:
表面附有碱性物质,先用去污粉洗,再用自来水冲洗干净,然后浸于盐酸溶液浸泡过夜,再用自来水反复冲洗干净,最后用蒸馏水冲洗1-2次,80℃烤干备用。
2、使用过的玻璃仪器洗涤
(1)一般非计量玻璃仪器或粗容量仪器,如烧杯、试管、量筒等先用肥皂水刷洗,再用自来水冲洗干净,最后用蒸馏水冲洗1-2次,倒置晾干。
(2)量器,如滴定管、容量瓶等先用自来水冲洗,直至不挂水珠,再用蒸馏水冲洗1-2次,分干备用。
若冲洗后仍挂水珠,则将其晾干后浸于铬酸洗液浸泡数小时。
然后用自来水反复冲洗干净,再用蒸馏水冲洗1-2次,干燥备用。
(三)吸量管和微量移液器的使用
1.吸量管的使用(注意标签、选择容量大小合适的吸量管)
(1)正确拿法中指和拇指拿住吸管上端,食指顶住吸量管顶端
(2)取液用橡皮球吸液体至刻度上,眼睛看着液面上升;吸完后用食指顶住吸量管上端。
(3)调刻度吸量管与地面保持垂直,下口与试剂瓶接触,并成一角度;用食指控制液体下降至最上一刻度处;液体凹面、刻度和视线应在一水平面上。
(4)放液吸量管移入准备接受溶液的容器中,仍使其出口尖端接触器壁,并成一角度,吸量管仍保持垂直。
放开食指,使液体自动流出。
奥氏吸量管和刻度到底的吸量管应吹出尖端残留的液体。
移液管应最后靠壁15秒。
2.微量移液器的使用
调节体积选取钮至所需值,套上吸头,旋紧。
垂直持握移液器,用大拇指按下液体吸放钮至第1档,将吸头插入待吸溶液,松开大拇指使吸放钮回复原位。
将移液器移入准备接受液体的仪器,用大拇指再次按下液体吸放钮,至第1档后继续至第2档以排空液体。
3.练习吸量管的使用
取50ml锥形瓶加入未知酸5ml,酚酞指示剂1滴,摇匀,用0.01mol/LNaOH滴定,记录结果。
(无色酚酞遇酸不变色,遇碱变红。
)滴定时边滴边摇动锥形瓶。
(四)离心机的使用方法
离心机是利用离心力将悬浮液中的微粒从溶液中分离出来的一种仪器。
根据最高离心转速的不同可将离心机分为三种类型:
普通离心机,其最高转速一般在4000转/分至6000转/分;高速离心机,转速可达10000转/分至25000转/分;超速离心机,转速可超过50000转/分以上。
生化实验室常使用普通离心机。
普通离心机的使用方法:
1.使用前先检查变速旋钮是否在“0”位,外套管是否完整无损和垫有橡皮垫。
2.离心时先将待离心的物质转移到大小合适的离心管内,盛量不宜过多,占管的2/3体积为宜,以免溢出。
将此离心管放入外套管,再在离心管与外套管间加入缓冲用水。
3.将一对装有离心管的外套管在台称上平衡。
如不平衡可调整缓冲用水或离心物质的量。
4.将平衡好的套管,按对称方位放到离心机插孔中。
把不用的离心套管取出,盖严离心机盖。
5.接通电源,开启开关,平稳、缓慢移动调速手柄,至所需转速。
计时。
6.当达到离心所需时间后,将调速柄慢慢调回零位,关闭开关。
待离心机自动停止转动后,再打开离心机盖取出样品。
7.用完后,取出套管中橡皮垫洗净,冲洗外套管,倒置干燥。
实验一糖类的性质实验
(一)
糖类的颜色反应
[时间安排]:
3学时。
[目的类型]:
验证
[目的要求]:
1、了解糖类某些颜色反应的原理。
2、学习应用糖的颜色反应鉴别糖类的方法。
[实验原理]:
(一)α-萘酚反应(Molisch反应)。
糖在浓无机酸(硫酸、盐酸)作用下,脱水生成糠醛及糠醛衍生物,后者能与α-萘酚生成紫红色物质。
因为糠醛及糠醛衍生物对此反应均呈阳性,故此反应不是糖类的特异反应。
[器材、试剂]:
器材:
(1)试管及试管架
(2)滴管
试剂:
(1)莫氏(Molisch)试剂:
5%α-萘酚的酒精溶液1500mL称取α-萘酚5g,溶于
95%酒精中,总体积达100mL,贮于棕色瓶内。
用前配制。
(2)1%葡萄糖溶液100mL
(3)1%果糖溶液100mL
(4)1%蔗糖溶液100mL
(5)1%淀粉溶液100mL
(6)0.1%糠醛溶液100mL
(7)浓硫酸500mL
[重要实验步骤与教学设计]:
取5支试管,分别加入1%葡萄糖溶液、1%果糖溶液、
1%蔗糖溶液、1%淀粉溶液、0.1%糠醛溶液各1mL。
再向5支试管中各加入2滴莫氏试剂,充分混合。
斜执试管,沿管壁慢慢加入浓硫酸约1mL,慢慢立起试管,切勿摇动。
浓硫酸在试液下形成两层。
在二液分界处有紫红色环出现。
观察、记录各管颜色。
(二)间苯二酚反应(Seliwanoff反应)
[实验原理]:
在酸作用下,酮糖脱水生成羟甲基糠醛,后者再与间苯二酚作用生成红色物质。
此反应是酮糖的特异反应。
醛糖在同样条件下呈色反应缓慢,只有在糖浓度较高或煮沸时间较长时,才呈微弱的阳性反应。
在实验条件下蔗糖有可能水解而呈阳性反应。
[器材、试剂]:
器材:
试管及试管架、滴管、水浴锅
试剂:
(1)塞氏(Seliwanoff)试剂
0.05%间苯二酚-盐酸溶液 1000mL
称取间苯二酚0.05g溶于30mL浓盐酸中,再用蒸馏水稀释至100mL
(2)1%葡萄糖溶液100mL
(3)1%果糖溶液100mL
(4)1%蔗糖溶液100mL
[重要实验步骤与教学设计]:
取3支试管,分别加入1%葡萄糖溶液、1%果糖溶液、1%蔗糖溶液各0.5mL。
再向各管分别加入塞氏试剂5mL,混匀。
将3支试管同时放入沸水浴中,注意观察、记录各管颜色的变化及变化时间。
[实验注意事项]:
[实验后记]:
实验二糖类的性质实验
(二)
糖类的还原作用
[时间安排]:
3学时。
[目的类型]:
验证
[目的要求]:
学习几种常用的鉴定糖类还原性的方法及其原理。
[实验原理]:
许多糖类由于其分子中含有自由的或潜在的醛基或酮基,故在碱性溶液中能将铜、铋、汞、铁、银等金属离子还原,同时糖类本身被氧化成糖酸及其他产物。
糖类这种性质常被利用于检测糖的还原性及还原糖的定量测定。
本实验进行糖类的还原作用所用的试剂为斐林试剂和本尼迪克特试剂。
它们都是含Cu2+的碱性溶液,能使还原糖氧化而本身被还原成红色或黄色的Cu2O沉淀。
生成Cu2O沉淀的颜色之所以不同是由于在不同条件下产生的沉淀颗粒大小不同引起的,颗粒越小呈黄色,越大则呈红色。
如有保护性胶体存在时,常生成黄色沉淀。
[器材、试剂]:
器材:
1.试管及试管架 2.竹试管夹 3.水浴锅 4.电炉
试剂:
1.斐林(Fehling)试剂1000mL
甲液(硫酸酮溶液):
称取34.5g硫酸铜(CuSO4·5H2O)溶于500mL蒸馏水中。
乙液(碱性酒石酸盐溶液):
称取125g氢氧化钠和137g洒石酸钾钠溶于500mL蒸馏水中。
为了避免变质,甲、乙二液分开保存。
用前,将甲、乙二液等量混合即可。
2.本尼迪克特(Benedict)试剂1000mL
称取柠檬酸钠173g及碳酸钠(Na2CO3·H2O)100g加入600mL蒸馏水中,加热使其溶解,冷却,稀释至850mL。
另称取17.3g硫酸铜溶解于100mL热蒸馏水中,冷却,稀释至150mL。
最后,将硫酸铜溶液徐徐地加入柠檬酸钠-碳酸钠溶液中,边加边搅拌,混匀,如有沉淀,过滤后贮于试剂瓶中可长期使用。
(2)1%葡萄糖溶液100mL
(3)1%果糖溶液100mL
(4)1%蔗糖溶液100mL
(5)1%淀粉溶液100mL
(6)0.1%麦芽溶液100mL
[重要实验步骤与教学设计]:
先取1支试管加入斐林试剂约1mL,再加入4mL蒸馏水,加热煮沸,如有沉淀生成,说明此试剂已不能使用。
经检验,试剂合格后,再进行下述实验。
取5支试管,分别加入2mL斐林试剂,再向各试管分别加入1%葡萄糖溶液、1%果糖溶液、1%蔗糖溶液、1%麦芽糖溶液、1%淀粉溶液各1mL。
置沸水浴中加热数分钟,取出,冷却。
观察各管溶液的变化。
另取6支试管,用本尼迪克特试剂重复上述实验。
比较两种试法的结果。
[实验注意事项]:
[实验后记]:
实验三总糖的测定
[时间安排]:
3学时。
[目的类型]:
验证
[目的要求]:
1.学习蒽酮比色定糖法的原理和方法。
2.学习722型分光光度计的原理和操作方法。
[实验原理]:
蒽酮比色法是一个快速而简便的定糖方法。
蒽酮可以和游离的己糖或多糖中的己糖基,戊醛糖及己糖醛酸起反应,反应后溶液呈蓝绿色,在620nm处有最大吸收。
蒽酮可与其他一些糖类发生反应,但显现的颜色不同。
当样品中存有含较多色氨酸的蛋白质时,反应不稳定,呈现红色。
对于以上特定的糖类,反应较稳定。
本法多用于测定糖原含量,亦可用于测定葡萄糖含量。
[器材、试剂]:
器材:
无蛋白滤液或其他生物材料。
吸管1m1(×2)、5m1(×1)、0.1m1(×1)、0.5mL(×2)。
试管1.5×15cm(×7)。
7200型分光光度计.
水浴锅。
冰浴锅。
试剂:
1.蒽酮试剂:
取2g蒽酮溶于1,000ml80%(V/V)硫酸中,当日配制使用。
2.标准葡萄糖溶液:
(0.1mg/m1)100ml葡萄糖用蒸馏水定容至1000ml(可滴加几滴甲苯作防腐剂)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第一学期生物化学实验教案 韩栓 第一 学期 生物化学 实验 教案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
