 选修四 化学反应原理 第四章 电化学基础复习 带答案.docx
选修四 化学反应原理 第四章 电化学基础复习 带答案.docx
- 文档编号:30095483
- 上传时间:2023-08-04
- 格式:DOCX
- 页数:23
- 大小:251.34KB
选修四 化学反应原理 第四章 电化学基础复习 带答案.docx
《选修四 化学反应原理 第四章 电化学基础复习 带答案.docx》由会员分享,可在线阅读,更多相关《选修四 化学反应原理 第四章 电化学基础复习 带答案.docx(23页珍藏版)》请在冰豆网上搜索。
选修四化学反应原理第四章电化学基础复习带答案
选修四化学反应原理第四章电化学基础复习
一、电化学:
研究化学能电能的装置、过程和效率的科学
二、形成条件
原电池
电解池
自发的氧化还原反应
两个电极与电源相连
一般是活泼性不同的两电极
电解质溶液(或熔融盐)
形成闭合回路:
①电解质溶液(或熔融盐);②两电极直接或间接接触;③两电极插入电解质溶液中。
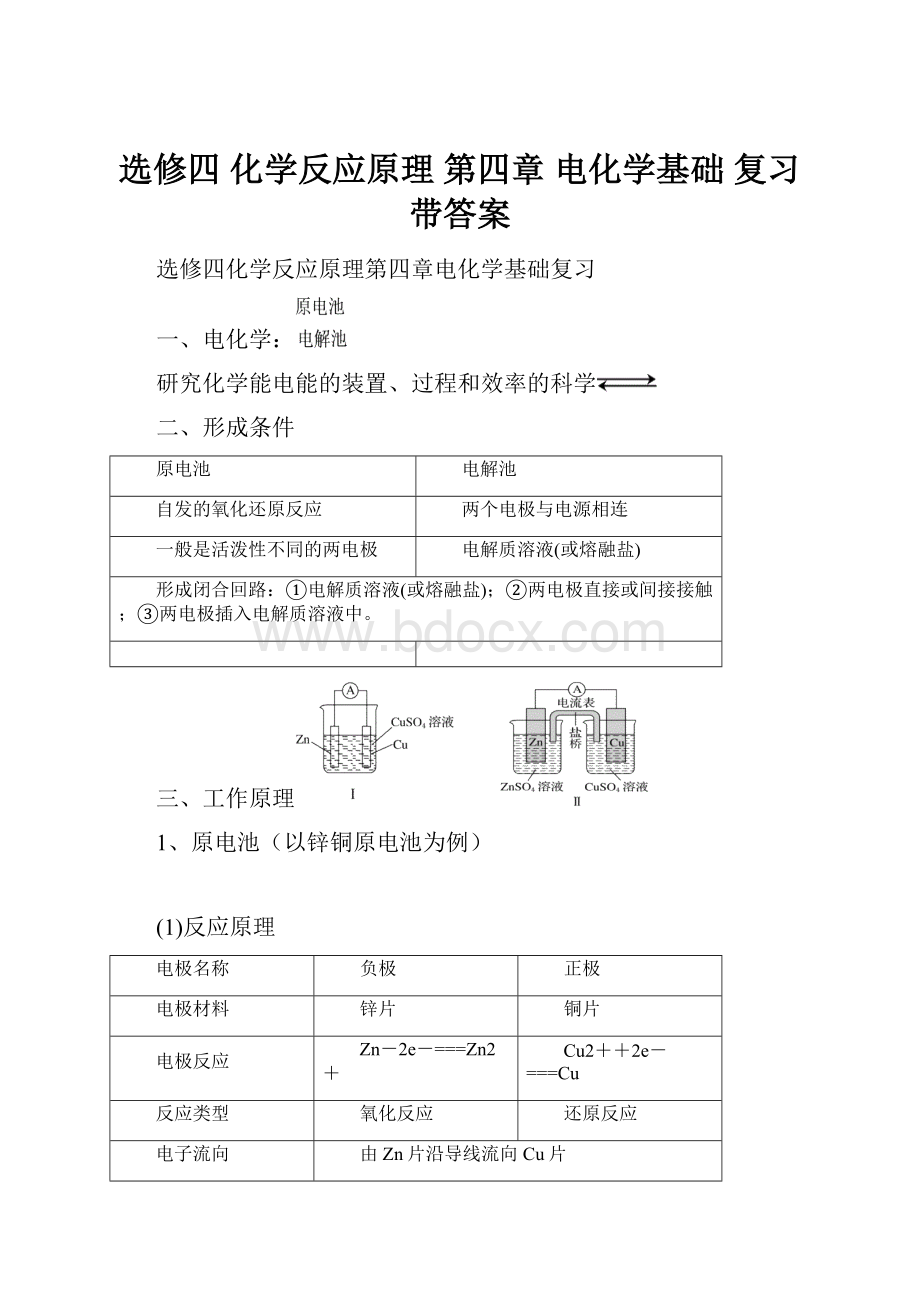
三、工作原理
1、原电池(以锌铜原电池为例)
(1)反应原理
电极名称
负极
正极
电极材料
锌片
铜片
电极反应
Zn-2e-===Zn2+
Cu2++2e-===Cu
反应类型
氧化反应
还原反应
电子流向
由Zn片沿导线流向Cu片
盐桥中离子移向
盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
(2)盐桥的组成和作用:
盐桥中装有饱和的KCl、KNO3等溶液和琼胶制成的胶冻。
作用:
①连接内电路,形成闭合回路;②平衡电荷,使原电池不断产生电流。
(3)图Ⅰ中部分Zn与Cu2+直接接触反应,这部分化学能转化成热能,使温度升高。
图Ⅱ中Zn与Cu2+不直接接触,不直接反应,所以仅是化学能转化成电能,电流稳定,且持续时间长,能量转化效率更高。
2、电解池(以电解CuCl2溶液为例)
1、放电顺序(注意阴极电极被保护、阳极活泼电极先放电)
阴极(氧化性):
Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+
阳极(还原性):
活泼电极>S2->I->Br->Cl->OH->含氧酸根离子(非还原性的)
注意:
结合题干信息、电解质等,合理判断放电产物
四、电极反应
方法步骤:
谁得失多少电子生成什么;得失电子与价态变化一致;电荷守恒;元素守恒
1、原电池
(1)判断电池正负极
(2)电极反应书写
①镁—铝电池(Al│KOH溶液│Mg)总反应:
负极:
;正极:
②锂电池(Li│LiAlCl4—SOCl2│石墨)总反应:
4Li+2SOCl2===SO2↑+4LiCl+S,则
负极:
正极:
③氢氧燃料电池(酸性、中性或碱性条件下)总反应式:
2H2+O2===2H2O都一样
负极:
2H2-4e-+4OH-===4H2O(碱性);2H2-4e-===4H+(酸性或中性);
正极:
O2+2H2O+4e-===4OH-(碱性或中性);O2+4H++4e-===2H2O(酸性)
④甲烷燃料电池(铂为两极、正极通入O2和CO2、负极通入甲烷、电解液有三种)
电解质
总反应
正负极反应
酸性溶液
CH4+2O2===CO2+2H2O
正极:
2O2+8e-+8H+===4H2O
负极:
碱性溶液
正极:
2O2+8e-+4H2O===8OH-
负极:
熔融碳酸盐
CH4+2O2===CO2+2H2O
注意:
正极要通入CO2和O2
正极:
负极:
CH4-8e-+4CO
===5CO2+2H2O
熔融氧化物
CH4+2O2===CO2+2H2O
正极:
负极:
CH4-8e-+4O2-===CO2+2H2O
试一试:
书写甲醇燃料电池在不同电解质条件下的电解反应
2、电解池
惰性电极电解规律
电解质及类别
电极反应式
电解物质
pH
复原
电解
水
H2SO4
含氧酸
阳极:
阴极:
4H++4e-===2H2↑
H2O
减小
加入
NaOH
强碱
阳极:
4OH--4e-===O2↑+2H2O
阴极:
Na2SO4
活泼金属的含氧酸盐
阳极:
阴极:
电解
电解
质
HCl
无氧酸
阳极:
2Cl--2e-===Cl2↑
阴极:
加入
CuCl2
不活泼金属的无氧酸盐
阳极:
2Cl--2e-===Cl2↑
阴极:
Cu2++2e-===Cu
CuCl2
加入
放H2
生碱
NaCl活泼金属的无氧酸盐
阳极:
2Cl--2e-===Cl2↑
阴极:
加入
CuSO4不活泼金属的含氧酸盐
阳极:
阴极:
2Cu2++4e-===2Cu
加入
(1)用惰性电极电解AgNO3溶液。
阳极:
________________________________;
总反应:
_________________________;阴极:
________________________________。
(2)用惰性电极电解MgCl2溶液阳极:
________________________________;
总反应:
_________________________;阴极:
________________________________。
(3)用铁作电极电解NaOH溶液阳极:
________________________________;
总反应:
_________________________;阴极:
________________________________。
(4)用Al作电极电解NaOH溶液阳极:
________________________________;
总反应:
_________________________;阴极:
________________________________。
(5)用Al作阳极,电解H2SO4溶液,铝材表面形成氧化膜。
阳极:
________________________________;
总反应:
_________________________;阴极:
________________________________。
(6)用惰性电极电解熔融MgCl2阳极:
________________________________;
总反应:
_________________________;阴极:
________________________________。
五、计算
1、类型:
电极产物定量计算、溶液PH、产物的量与电量关系(如比能量的比较)等
2、方法:
(1)根据总反应或电极反应计算
(2)根据电子守恒计算:
①串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数相等。
②用于混合溶液中电解的分阶段计算。
(3)列关系式计算如:
4e-~2Cl2(Br2、I2)~O2~2H2~2Cu~4Ag~
M(M为金属,n为价态)
六、应用
1、原电池
(1)金属活动性比较(略)
(2)加快反应速率例如在Zn与稀H2SO4反应时加入少量CuSO4能使产生H2的速率加快。
(3)设计电池:
化学电源
①一次电池碱性锌锰干电池总反应:
Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2
正极:
________________________________负极:
Zn+2OH--2e-==Zn(OH)2
锌银电池总反应:
Zn+Ag2O+H2O===Zn(OH)2+2Ag
负极:
____________________________正极:
___________________________
②二次电池(可充电电池)以铅蓄电池为例(Pb‖稀硫酸‖PbO2)
放电
充电
负极:
阴极:
正极:
阳极:
总反应:
③燃料电池(略)
(4)金属的电化学腐蚀(与化学腐蚀相比,强调“不纯金属或合金”、“电解质溶液”)
类型
析氢腐蚀
吸氧腐蚀
条件
水膜酸性较强
电极反应
负极
Fe-2e-===Fe2+
正极
总反应式
联系
________更普遍
生成铁锈:
___________________________________________________________________
(5)金属电化学防护:
牺牲阳极的阴极保护法(略)
2、电解池
(1)氯碱工业:
2Cl-+2H2O
2OH-+H2↑+Cl2↑
阳极:
2Cl--2e-===Cl2↑
阴极:
4H2O+4e-===2H2↑+4OH-
阳离子交换膜的作用:
只允许阳离子(Na+)通过,而阻止阴离子(Cl-、OH-)和分子(Cl2)通过,这样既能阻止H2和Cl2混合爆炸,又能避免Cl2和NaOH溶液作用生成的NaClO影响烧碱质量。
(2)电镀(以钥匙镀银为例如图)
①镀件作阴极,镀层金属银作阳极,电解质溶液是含镀层金属阳离子的盐溶液
②阳极:
Ag-e-===Ag+;阴极:
Ag++e-===Ag
③特点:
阳极溶解,阴极沉积,电镀液的浓度不变。
(3)电解精炼铜
①阳极为粗铜,阴极为纯铜,电解质溶液是含Cu2+的盐溶液
②阳极:
Zn-2e-===Zn2+、Fe-2e-===Fe2+、Ni-2e-===Ni2+、
Cu-2e-===Cu2+;阴极:
Cu2++2e-===Cu
(4)电冶金如冶炼铝阳极:
6O2--12e-==3O2↑;阴极:
4Al3++12e-===4Al
(5)金属电化学防护:
外加电流的阴极保护法(略)
《电化学基础》复习题
( )1.有关电化学知识的描述正确的是
A.CaO+H2O==Ca(OH)2反应放热,故可把该反应设计成原电池,将化学能转化为电能
B.某原电池反应为Cu+2AgNO3==Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液
C.原电池的两极一定是由活动性不同的两种金属组成
D.从理论上讲,任何能自发进行的氧化还原反应都可设计成原电池
( )2.X、Y、Z、M、N代表五种金属,有以下反应:
①Y与M用导线连接放入稀硫酸中,M上冒气泡;
②M、N为电极,与N的盐溶液组成原电池,电子从M流出,经外电路,流入N极;
③Z+2H2O(冷水)===Z(OH)2+H2↑;
④水溶液中,X+Y2+===X2++Y。
则这五种金属的活动性由强到弱的顺序为
A.Z>X>Y>M>NB.Z>Y>X>M>N
C.Z>X>Y>N>MD.X>Y>M>N>Z
( )3.下列有关电化学知识的说法中正确的是
A.电池放电时,导线中电子由负极流向正极,溶液中阴离子向正极移动
B.电池充电时,电池负极应该接在直流电源的正极上
C.电解池工作时,阴极接电源负极,一般是还原性较强的离子得到电子
D.原电池工作时,可能会伴随着热能变化
( )4.2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。
下列叙述错误的是
A.a为电池的正极
B.电池充电反应为LiMn2O4===Li1-xMn2O4+xLi
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
( )
5.如图装置模拟电解原理在工业上的应用。
下列正确的是
A.氯碱工业中,X电极上反应式是4OH--4e-===2H2O+O2↑
B.电解精炼铜时,Z溶液中的Cu2+浓度不变
C.在铁片上镀铜时,Y是纯铜
D.制取金属镁时,Z是熔融的氯化镁
( )6.如图所示,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为
A.②①③④⑤⑥B.⑤④③①②⑥C.⑤④②①③⑥D.⑤③②④①⑥
( )7.利用右图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。
下列说法不正确的是
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a处溶液的pH增大,b处溶液的pH减小
D.a、b两处具有相同的电极反应式:
Fe-2e-===Fe2+
( )8.下列与金属腐蚀有关的说法正确的是
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,钢铁轮船外壳连接一块金属A(铜块)可以减缓船体外壳腐蚀速度
( )9.下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO
+2I-+2H+⇋AsO
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。
甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
下列叙述中正确的是
A.甲组操作时,电流表(A)指针发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C2作正极
D.乙组操作时,C1上发生的电极反应为I2+2e-===2I-
( )
10.甲醇燃料电池容易携带、容易存储等优点,目前被认为将会替代传统的电池成为携带型设备的主要电源。
如图是甲醇的质子交换膜型燃料电池模型,下列正确的是
A.Y极为电池的负极
B.X电极反应:
CH3OH+H2O-6e-===CO2+6H+
C.若常温下用该电池电解100mLKCl溶液至pH=12时,质子交换膜迁移的A为0.01mol
D.空气以20%为氧气计算,X极每消耗1mol甲醇,Y极必消耗168L空气中的氧气
( )
11.人工光合作用能够借助太阳能用CO2和水制备化学原料,如图是通过人工光合作用制备HCOOH的原理示意图,下列说法中正确的是
A.催化剂a处通CO2气体,催化剂b处加水
B.催化剂a处发生的反应为2H2O+4e-===O2↑+4H+
C.该电池的电解质溶液可采用HCOOH溶液
D.在合成HCOOH的过程中,电池内部的H+的物质的量浓度不发生改变
( )12.下图左,甲为直流电源,乙为用含有酚酞的饱和食盐水浸透的滤纸,丙为电镀槽。
断开K后,发现乙上c点附近显红色;闭合K,可实现铁上镀锌,电路中通过0.002NA个电子。
以下判断正确的是
A.a为负极B.d上发生还原反应C.e为锌板D.f极的质量增加0.056g
13.用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如上图右所示(电极材料为石墨)。
(1)图中a极要连接电源的_____极,C口流出的物质是________。
(2)SO
放电反应______________________
(3)电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:
___________________________________________________________。
14.常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是______________,溶液中的H+向________极移动,t1时,原电池中电子流动方向发生改变,其原因是____________________________________。
15.使用氯化钠作原料可以得到多种产品。
(1)实验室用惰性电极电解100mL0.1mol·L-1NaCl溶液,若阴、阳两极均得到112mL气体(标准状况),则所得溶液的物质的量浓度是______________(忽略溶液体积变化)。
(2)某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置。
对电源电极名称和消毒液的主要成分判断正确的是_____
A.a正极,b负极;NaClO和NaClB.a负极,b正极;NaClO和NaCl
C.a阳极,b阴极;HClO和NaClD.a阴极,b阳极;HClO和NaCl
(3)实验室中很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。
某同学利用上图装置,只更换一个电极,通过电解法制取较纯净的
Fe(OH)2沉淀,且较长时间不变色。
该同学换上的电解材料是______,总的反应式是________________________________________。
(4)若用锌锰干电池做电源,维持电流强度0.5A,工作5分钟,理论上消耗锌______g。
(已知F=96500C·mol-1)
16.[2015·重庆理综,11(5)]如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
(1)腐蚀过程中,负极是_____(填a、b或c);
(2)环境中的Cl-扩散到孔口,并与正极反应产物和负
极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离
子方程式为_______________________________________________;
(3)若生成4.29gCu2(OH)3Cl,则理论上耗氧体积为________L(标准状况)。
17.如下图1所示,用氢氧燃料电池分别电解CuSO4溶液、FeCl3溶液,其中A、B、D
电极材料均为石墨,C电极材料为铜。
工作一段时间后,断开K,此时电解池乙两极上产生的气体体积相同。
(1)甲中通入H2的电极反应式为_____________________________________________。
(2)乙装置中,产生气体在标状況下总体积为______mL,此时乙中溶液的PH=______(忽略水解,lg2=0.3),要使乙中CuSO4溶液恢复到原来的浓度,需要加入的物质是____________。
(3)丙装置中,溶液慢慢由黄色变成浅绿色,D电极发生的反应为__________________,溶液中金属阳离子的物质的量与电路中转移电子的物质的量变化关系如图2所示,则图中直线②表示的是________(填离子符号)的变化
四、电极反应
1、原电池
(2)电极反应书写
①镁—铝电池(Al│KOH溶液│Mg)总反应:
2Al+2OH-+2H2O===2AlO
+3H2↑
负极:
2Al+8OH--6e-===2AlO
+4H2O;正极:
6H2O+6e-===3H2↑+6OH-
②锂电池(Li│LiAlCl4—SOCl2│石墨)总反应:
4Li+2SOCl2===SO2↑+4LiCl+S,则
负极:
4Li-4e-===4Li+正极:
2SOCl2+4e-===SO2↑+S+4Cl-
③氢氧燃料电池(酸性、中性或碱性条件下)总反应式:
2H2+O2===2H2O都一样
负极:
2H2-4e-+4OH-===4H2O(碱性);2H2-4e-===4H+(酸性或中性);
正极:
O2+2H2O+4e-===4OH-(碱性或中性);O2+4H++4e-===2H2O(酸性)
④甲烷燃料电池(铂为两极、正极通入O2和CO2、负极通入甲烷、电解液有三种)
电解质
总反应
正负极反应
酸性溶液
CH4+2O2===CO2+2H2O
正极:
2O2+8e-+8H+===4H2O
负极:
CH4-8e-+2H2O===CO2+8H+
碱性溶液
CH4+2O2+2KOH===K2CO3+3H2O
正极:
2O2+8e-+4H2O===8OH-
负极:
CH4-8e-+10OH-===CO
+7H2O
熔融碳酸盐
CH4+2O2===CO2+2H2O
注意:
正极要通入CO2和O2
正极:
2O2+8e-+4CO2===4CO
负极:
CH4-8e-+4CO
===5CO2+2H2O
熔融氧化物
CH4+2O2===CO2+2H2O
正极:
2O2+8e-===4O2-
负极:
CH4-8e-+4O2-===CO2+2H2O
电解池电极反应书写参考答案:
惰性电极电解规律
电解质及类别
电极反应式
电解物质
pH
复原
电解
水
H2SO4
含氧酸
阳极:
2H2O-4e-===O2↑+4H+
阴极:
4H++4e-===2H2↑
H2O
减小
加入
H2O
NaOH
强碱
阳极:
4OH--4e-===O2↑+2H2O
阴极:
4H2O+4e-===2H2↑+4OH-
增大
Na2SO4
活泼金属的含氧酸盐
阳极:
2H2O-4e-===O2↑+4H+
阴极:
4H2O+4e-===2H2↑+4OH-
不变
电解
电解
质
HCl
无氧酸
阳极:
2Cl--2e-===Cl2↑
阴极:
2H++2e-===H2↑
HCl
增大
加入HCl
CuCl2
不活泼金属的无氧酸盐
阳极:
2Cl--2e-===Cl2↑
阴极:
Cu2++2e-===Cu
CuCl2
加入
CuCl2
放H2
生碱
NaCl活泼金属的无氧酸盐
阳极:
2Cl--2e-===Cl2↑
阴极:
4H2O+4e-===2H2↑+4OH-
NaCl、H2O
增大
加入
HCl
放O2
生酸
CuSO4不活泼金属的含氧酸盐
阳极:
2H2O-4e-===O2↑+4H+
阴极:
2Cu2++4e-===2Cu
CuSO4、H2O
减小
加入
CuO或
CuCO3
(1)2H2O-4e-===O2↑+4H+4Ag++4e-===4Ag4Ag++2H2O
4Ag+O2↑+4H+
(2)2Cl--2e-===Cl2↑2H2O+2e-===H2↑+2OH-
Mg2++2Cl-+2H2O
Mg(OH)2↓+Cl2↑+H2↑
(3)Fe-2e-+2OH-==Fe(OH)22H2O+2e-==H2↑+2OH-Fe+2H2O
Fe(OH)2+H2↑
(4)2Al-6e-+8OH-==2AlO
+4H2O 6H2O+6e-==3H2↑+6OH-
2Al+2H2O+2OH-
2AlO
+3H2↑
(5)2Al-6e-+3H2O===Al2O3+6H+6H++6e-===3H2↑2Al+3H2O
Al2O3+3H2↑
(6)2Cl--2e-===Cl2↑Mg2++2e-===MgMg2++2Cl-
Mg+Cl2↑
六、应用
(3)设计电池:
化学电源
①一次电池碱性锌锰干电池总反应:
Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2
正极:
2MnO2+2H2O+2e-===2MnOOH+2OH-负极:
Zn+2OH--2e-==Zn(OH)2
锌银电池总反应:
Zn+Ag2O+H2O===Zn(OH)2+2Ag
负极:
Zn+2OH--2e-===Zn(OH)2正极:
Ag2O+H2O+2e-===2Ag+2OH-
②二次电池(可充电电池)以铅蓄电池为例(Pb‖稀硫酸‖PbO2)
放电
充电
负极:
Pb(s)+SO
(aq)-2e-===PbSO4(s)
阴极:
PbSO4(s)+2e-===Pb(s)+SO
(aq)
正极:
PbO2(s)+4H+(aq)+SO
(aq)+2e-===PbSO4(s)+2H2O(l)
阳极:
PbSO4(s)+2H2O(l)-2e-===PbO2(s)+4H+(aq)+SO
(aq)
Pb(s)+PbO2(s)+2H2SO4(aq)
2PbSO4(s)+2H2O(l)
(4)金属的电化学腐蚀(与化学腐蚀相比,强调“不纯金属或合金”、“电解质溶液”)
类型
析氢腐蚀
吸氧腐蚀
条件
水膜酸性较强
水膜酸性很弱或呈中性
电极反应
负极
Fe-2e-===Fe2+
正极
2H++2e-===H2↑
O2+2H2O+4e-===4OH-
总反应式
Fe+2H+===Fe2++H2↑
2Fe+O2+2H2O===2Fe(OH)2
联系
吸氧腐蚀更普遍
生成铁锈:
4Fe(OH)2+O2+2H2O==
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 选修四 化学反应原理 第四章 电化学基础 复习 带答案 选修 化学反应 原理 第四 电化学 基础 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
