 y高中化学方程式总汇.docx
y高中化学方程式总汇.docx
- 文档编号:30007316
- 上传时间:2023-08-04
- 格式:DOCX
- 页数:34
- 大小:454.44KB
y高中化学方程式总汇.docx
《y高中化学方程式总汇.docx》由会员分享,可在线阅读,更多相关《y高中化学方程式总汇.docx(34页珍藏版)》请在冰豆网上搜索。
y高中化学方程式总汇
高中化学方程式总汇
说明:
①无★为基本反应,全体同学必须掌握;
②★为较高要求反应,基础较好同学应该掌握;
③★★方程式基础较好同学应该了解。
(一)卤族元素
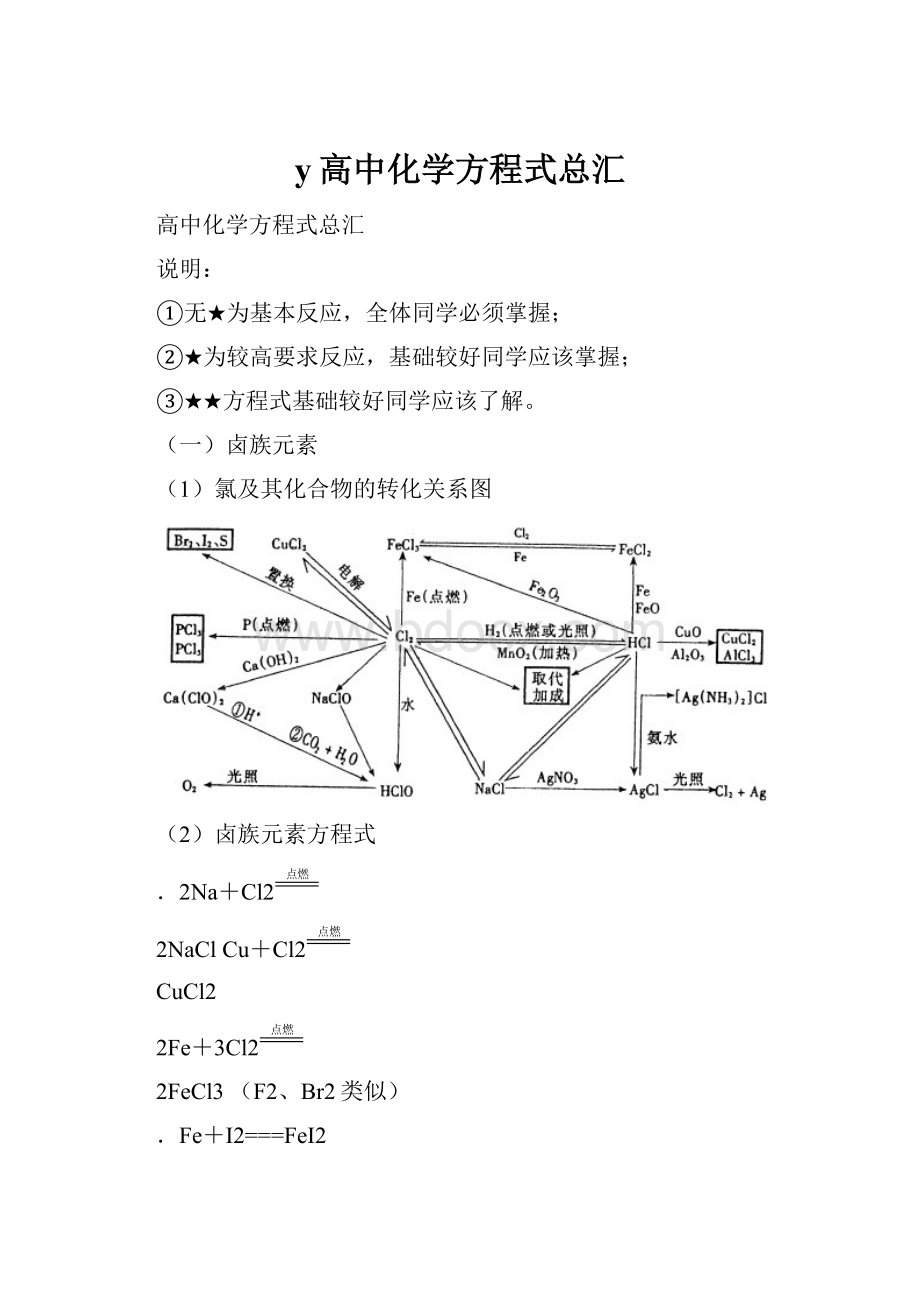
(1)氯及其化合物的转化关系图
(2)卤族元素方程式
.2Na+Cl2
2NaClCu+Cl2
CuCl2
2Fe+3Cl2
2FeCl3(F2、Br2类似)
.Fe+I2===FeI2
.Cl2+H2
2HCl
.3Cl2+2P
2PCl35Cl2+2P
2PCl5
.Cl2+H2O
H++Cl-+HClO2HClO===2HCl+O2↑(见光加快)
.Cl2+2OH-===Cl-+ClO-+H2O(吸收Cl2)
.2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O(工业上制漂白粉)
.★3Cl2+6KOH(浓)
KClO3+5KCl+3H2O
.Ca(ClO)2+CO2+H2O===CaCO3↓+2HClO(日常漂白、消毒原理)
.Ca(ClO)2+2HCl(稀)===CaCl2+2HClO(工业漂白原理)
.★★3Cl2+2NH3(不足)===N2+2HCl
.★★3Cl2+8NH3(过量)===N2+6NH4Cl
.Cl2+2Br-===2Cl-+Br2Cl2+2I-===2Cl-+I2Br2+2I-===2Br-+I2
.Cl2+SO2+H2O===4H++SO42-+2Cl-(Br2、I2类似)
.Cl2+H2S===2H++2Cl-+S↓
.MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O(实验室制Cl2)
.★Ca(ClO)2+4HCl(浓)===CaCl2+Cl2↑+2H2O(实验室制Cl2)
.★2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O(实验室制Cl2)
.★★KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O(实验室制Cl2)
.★★K2Cr2O7+14HCl(浓)===2KCl+2CrCl3+3Cl2↑+7H2O(实验室制Cl2)
.★NaCl+H2SO4(浓)
NaHSO4+HCl↑(实验室制HCl)
.★2NaCl+H2SO4(浓)
Na2SO4+2HCl↑(实验室制HCl)
.H2+F2===2HFH2+Br2
2HBrH2+I2
2HI
.Ag++Cl-===AgCl↓(白色)Ag++Br-===AgBr↓(淡黄色)
Ag++I-===AgI↓(黄色)
.★2HCl+F2===2HF+Cl2(颜色变深)
.2F2+2H2O===4HF+O2
.Si+4F2===SiF4Si+4HF===SiF4↑+2H2↑
.SiO2+4HF===SiF4↑+2H2O
.2AgX===2Ag+X2(X=Cl、Br、I)
(二)氧族元素
(1)生成氧气的反应
.2H2O
2H2↑+O2↑
.2KClO3
2KCl+3O2↑
.2KMnO4
K2MnO4+MnO2+O2↑
.2HgO
2Hg+O2↑
.4HNO3
4NO2↑+O2↑+2H2O
.2HClO
2HCl+O2↑
.2F2+2H2O===4HF+O2
.2H2O2
2H2O+O2↑
.2Na2O2+2CO2===2Na2CO3+O2
.2Na2O2+2H2O===4NaOH+O2↑
.2Al2O3(熔融)
4Al+3O2↑
(2)与O3有关的反应
.2O3===3O23O2
2O3
.★★O3+2KI+H2O===2KOH+I2+O2
(3)H2O2的性质
.2H2O2
2H2O+O2↑
.★SO2+H2O2===H2SO4
.★2Fe2++H2O2+H+===2Fe3++2H2O
.★2MnO4-+5H2O2+6H+===2Mn2++5O2↑+8H2O
(4)硫及其化合物的转化关系图
(5)硫元素的性质
①单质的性质
.2Na+S
Na2SFe+S
FeS2Cu+S
Cu2S
.★2Al+3S
Al2S3★★Al2S3+6H2O===2Al(OH)3↓+3H2S↑
.★Hg+S===HgS★2Ag+S===Ag2S
.H2+S
H2SH2+Se
H2Se(H2+Te不能直接化合)
.★★S+2KNO3+3C
K2S+N2↑+3CO2↑(黑火药燃烧)
.★3S+6KOH
2K2S+K2SO3+3H2O(洗硫)
.S+O2
SO2
.S+2H2SO4(浓)
3SO2↑+2H2O★S+6HNO3(浓)===H2SO4+6NO2↑+2H2O
②H2S的性质
.H2S
H2+S
.2H2S+O2(不足)
2S+2H2O2H2S+3O2(过量)
2SO2+2H2O
.H2S+X2===2HX+S↓ S2-+X2===2X-+S↓(X=Cl、Br、I)
.★H2S+CuSO4===CuS↓+H2SO4★H2S+CuCl2===CuS↓+2HCl
.★H2S+(CH3COO)2Pb===PbS↓+2CH3COOH
.★H2S+H2SO4(浓)===S↓+SO2↑+2H2O★3H2S(过量)+H2SO4(浓)===4S↓+4H2O
★H2S+3H2SO4(浓,过量)===4SO2↑+4H2O
.★FeS(s)+2HCl(稀)===FeCl2+H2S↑★FeS(s)+H2SO4(稀)===FeSO4+H2S↑
(实验室制H2S)
③SO2、H2SO3、SO32-的性质
.SO2+2H2S===3S+2H2OH2SO3+2H2S===3S↓+3H2O
SO32-+2S2-+6H+===3S↓+3H2O(SO32-、S2-碱性可大量共存,酸性不能大量共存)
.2SO2+O2
2SO32H2SO3+O2===2H2SO4(缓慢)
2SO32-+O2===2SO42-(迅速)还原性:
SO2<H2SO3<SO32-
.SO2+Na2O===Na2SO3★SO2+Na2O2===Na2SO4
.SO2+NaOH(不足)===NaHSO3SO2+2NaOH(过量)===Na2SO3+H2O
.Na2SO3+SO2+H2O===2NaHSO3
.2SO2+Ca(OH)2(不足)===Ca(HSO3)2SO2+Ca(OH)2(过量)===CaSO3↓+H2O
.★2NaHCO3+SO2===Na2SO3+2CO2↑+H2O
.★Na2CO3+SO2===Na2SO3+CO2
.SO2+H2O
H2SO3H2SO3
H++HSO3-
.SO2+X2+2H2O===H2SO4+2HXH2SO3+X2+H2O===H2SO4+2HX
SO32-+X2+H2O===SO42-+2H++2X-(X=Cl、Br、I)
.2Fe3++SO2+2H2O===2Fe2++4H++SO42-
.SO2+NH3·H2O===NH4HSO3
.4FeS2+11O2
2Fe2O3+8SO2
.★Na2SO3+H2SO4(1:
1)===Na2SO4+SO2↑+H2O(实验室制SO2)
④SO3、浓H2SO4的性质
.SO3+H2O===H2SO4
.Fe(Al)+H2SO4(浓)
钝化
.Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.Al+6H2SO4(浓)
Al2(SO4)3+3SO2↑+6H2O
.Fe+6H2SO4(浓)
Fe2(SO4)3+3SO2↑+6H2O
.C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.★★2NaX(s)+H2SO4(浓)
Na2SO4+2HX↑(X=F、Cl)
.★2HI+H2SO4(浓)
I2+SO2↑+2H2O(HBr类似)
(三)碳族元素
(1)碳、硅及其化合物的转化关系图
(2)碳、硅元素方程式
.CH4+2O2
CO2+2H2O
.2C+O2
2COC+O2
CO2
.C+CuO
Cu+COC+2CuO
2Cu+CO2
.C+H2O
CO+H2CO+H2O
CO2+H2
.C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
.★★C+2S
CS2
.★3C+CaO
CaC2+CO↑(制电石)
.2CO+O2
2CO2
.3CO+Fe2O3
2Fe+3CO2
.CO2+2Mg
2MgO+C
.CO2(少量)+Ca(OH)2===CaCO3↓+H2O
.2CO2(过量)+Ca(OH)2===Ca(HCO3)2离子方程式:
CO2+OH-===HCO3-
.CO2+BaCl2(aq)
不反应
.CO2(少量)+H2O+Na2SiO3===H2SiO3↓+Na2CO3
离子方程式:
CO2+H2O+SiO32-===H2SiO3↓+CO32-
.★2CO2(过量)+2H2O+Na2SiO3===H2SiO3↓+2NaHCO3
.CO2(少量)+H2O+Ca(ClO)2===CaCO3↓+2HClO
.★2CO2(过量)+2H2O+Ca(ClO)2===Ca(HCO3)2+2HClO
离子方程式:
CO2+H2O+ClO-===HCO3-+HClO
.CO2+H2O+Na2CO3===2NaHCO3
.向纯碱溶液中缓慢逐滴加入稀盐酸至过量:
Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2↑
.Na2CO3+Ca(OH)2===CaCO3↓+2NaOHCO32-+Ca2+===CaCO3↓
.NaHCO3+HCl===NaCl+H2O+CO2↑
.NaHCO3+NaOH===Na2CO3+H2O
.★NaHCO3(少量)+Ca(OH)2===H2O+CaCO3↓+NaOH
离子方程式:
HCO3-+Ca2++OH-===H2O+CaCO3↓
.★2NaHCO3+Ca(OH)2(少量)===2H2O+CaCO3↓+Na2CO3
离子方程式:
2HCO3-+Ca2++2OH-===2H2O+CaCO3↓+CO32-
.★Ca(HCO3)2+NaOH(少量)===H2O+CaCO3↓+NaHCO3
离子方程式:
Ca2++HCO3-+OH-===H2O+CaCO3↓
.★Ca(HCO3)2(少量)+2NaOH===2H2O+CaCO3↓+Na2CO3
离子方程式:
Ca2++2HCO3-+2OH-===2H2O+CaCO3↓+CO32-
.Si+2F2===SiF4Si+4HF===SiF4↑+2H2↑
.Si+2NaOH+H2O===Na2SiO3+2H2↑
.Si+O2
SiO2
.★Si+C
SiC
.SiO2+2C
Si+2CO
.★★Si与Cl2加热:
Si+2Cl2
SiCl4
.SiO2+4HF===SiF4↑+2H2O
.SiO2+CaO
CaSiO3
.SiO2+2NaOH===Na2SiO3+H2O
.工业制玻璃的两个反应:
SiO2+Na2CO3
Na2SiO3+CO2↑
SiO2+CaCO3
CaSiO3+CO2↑
.由SiO2制硅酸:
SiO2+Na2CO3
Na2SiO3+CO2↑
Na2SiO3+2HCl===H2SiO3↓+2NaCl
Na2SiO3+2CO2+2H2O===H2SiO3↓+2NaHCO3
(四)氮族元素
(1)氮及其化合物的转化关系图
(2)氮元素的方程式
①氮气的性质
.N2+3H2
2NH3
.N2+O2
2NO
.N2+3Mg
Mg3N2★Mg3N2+6H2O===3Mg(OH)2+2NH3↑
②NO、NO2的性质
.2NO+O2===NO22NO2(g)
N2O4(g);ΔH>0
.3NO2+H2O===2HNO3+NO
.4NO+3O2+2H2O===4HNO34NO2+O2+2H2O===4HNO3
.★★2NO2+2NaOH===NaNO3+NaNO2+H2O(硝酸工业尾气吸收)
.★★NO2+NO+2NaOH===2NaNO2+H2O(硝酸工业尾气吸收)
③NH3、NH3·H2O的性质
.NH3+H2O
NH3·H2O
NH4++OH-
.NH3+HCl===NH4Cl(白烟)NH3+HNO3(浓)===NH4NO3(白烟)
.2NH3+H2SO4===(NH4)2SO4(无白烟)
.NH3+CO2+H2O===NH4HCO32NH3+CO2+H2O===(NH4)2CO3
.★★CaCl2+8NH3===CaCl2·8NH3(CaCl2不能干燥NH3)
.AlCl3+3NH3·H2O===Al(OH)3↓+3NH4Cl[Al(OH)3不溶于过量的氨水]
.FeCl3+3NH3·H2O===Fe(OH)3↓+3NH4Cl
.AgNO3+NH3·H2O===AgOH↓+NH4NO3
.AgOH+2NH3·H2O===[Ag(NH3)2]OH+2H2O
.4NH3+5O2
4NO+6H2O★4NH3+3O2(纯)
2N2+6H2O
.★★8NH3+6NO2
7N2+12H2O★★4NH3+6NO
5N2+6H2O
.★★2NH3(不足)+3Cl2===N2+6HCl★★8NH3(过量)+3Cl2===N2+6NH4Cl(白烟)
.★★2NH3+3CuO
N2+3Cu+3H2O
④铵盐的性质
.NH4Cl
NH3+HCl
.NH4HCO3
NH3↑+CO2↑+H2O↑(NH4)2CO3
2NH3↑+CO2↑+H2O↑
.2NH4Cl(s)+Ca(OH)2
CaCl2+2NH3↑+2H2O(实验室制NH3)
.铵盐和强碱在溶液中反应:
NH4+(稀)+OH-(稀)===NH3·H2ONH4+(浓)+OH-(浓)===NH3↑+H2O
NH4++OH-
NH3↑+H2O
⑤HNO3、NO3-(H+)的性质
.4HNO3
4NO2↑+O2↑+2H2O
.CuO+2HNO3===Cu(NO3)2+H2O
.Fe2O3+6HNO3===2Fe(NO3)3+3H2O
.★FeO+4HNO3(浓)===Fe(NO3)3+NO2↑+2H2O
.★3FeO+10HNO3(稀)===3Fe(NO3)3+NO↑+5H2O
.Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
.3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
.Fe+6HNO3(浓)
Fe(NO3)3+3NO2↑+3H2O
.Fe(少量)+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O
.3Fe(过量)+8HNO3(稀)===3Fe(NO3)2+2NO↑+4H2O
.C+4HNO3(浓)===CO2↑+4NO2↑+2H2O
.★S+6HNO3(浓)===H2SO4+6NO2↑+2H2O
.工业上制HNO3:
4NH3+5O2
4NO+6H2O2NO+O2===NO2
3NO2+H2O===2HNO3+NO
.★NaNO3(s)+H2SO4(浓)
NaHSO4+HNO3↑(实验室制HNO3)
.NO3-的检验:
晶体或浓溶液(稀溶液先浓缩)与浓H2SO4、Cu共热,若产生红棕色气体,证明有NO3-。
★NaNO3(s)+H2SO4(浓)
NaHSO4+HNO3↑
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
.★6I-+2NO3-+8H+===3I2+2NO↑+4H2O
.★3H2S+2NO3-+2H+===3S↓+2NO↑+4H2O
.★3S2-+2NO3-+8H+===3S↓+2NO↑+4H2O
.★3SO32-+2NO3-+2H+===3SO42-+2NO↑+H2O
(3)磷及其化合物的转化关系图
(4)磷及其化合物的性质
.白磷(P4)
红磷(白磷有毒,红磷无毒)
.4P+5O2
2P2O5★4P+3O2
2P2O3
.2P+5Cl2
2PCl5(白烟)2P+3Cl2
2PCl3(白雾)
.P2O5+3H2O
2H3PO4★P2O5+H2O(冷)===2HPO3(有毒)
.H3PO4+NaOH===NaH2PO4+H2O
.H3PO4+2NaOH===Na2HPO4+2H2O
.H3PO4+3NaOH===Na3PO4+3H2O
.★★H3PO4(浓)+NaBr(s)
NaH2PO4+HBr↑(实验室制HBr)
.★★H3PO4(浓)+KI(s)
KH2PO4+HBr↑(实验室制HI)
(五)碱金属元素
(1)钠及其化合物的转化关系图
(2)碱金属元素方程式
1.单质的反应
.4Li+O2
2Li2O
.4Na+O2===2Na2O2Na+O2
Na2O22Na2O+O2
2Na2O2
.★K+O2
KO2(Rb、Cs与O2反应生成更复杂的化合物)
.★2Na+H2
2NaH★NaH+H2O===NaOH+H2↑
.2Na+S===Na2S
.2Na+2H2O===2NaOH+H2↑(浮、熔、游、响)
.2Na+2HCl===2NaCl+H2↑
.2Na+2H2O+CuSO4===Cu(OH)2↓+Na2SO4+H2↑
.2Na+2C2H5OH
2C2H5ONa+H2↑
.2NaCl(熔融)
2Na+Cl2↑(工业上制Na)
2.Na2O、Na2O2的反应
.Na2O+CO2===Na2CO32Na2O2+2CO2===2Na2CO3+O2
.Na2O+H2O===2NaOH2Na2O2+2H2O===4NaOH+O2↑
.Na2O+2HCl===2NaCl+H2O★2Na2O2+4HCl===4NaCl+2H2O+O2↑
.★Na2O2+SO2===Na2SO4★★Na2O2+CO
Na2CO3
3.NaOH的反应
①与氧化物反应
.CO2+NaOH(不足)===NaHCO3CO2+2NaOH(过量)===Na2CO3+H2O
.SO2+NaOH(不足)===NaHSO3SO2+2NaOH(过量)===Na2SO3+H2O
.SiO2+2NaOH===Na2SiO3+H2O
.★★2NO2+2NaOH===NaNO3+NaNO2+H2O
★★NO2+NO+2NaOH===2NaNO2+H2O
②与酸反应
.2NaOH+H2SO4===Na2SO4+2H2O
.NaOH+H3PO4===H2O+NaH2PO42NaOH+H3PO4===2H2O+Na2HPO4
3NaOH+H3PO4===3H2O+Na3PO4
③与两性物质反应
.Al2O3+2NaOH===2NaAlO2+H2O
.Al(OH)3+NaOH===NaAlO2+2H2O
④与盐反应
.2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
.2NaOH+MgSO4===Mg(OH)2↓+Na2SO4
.2NaOH+(NH4)2SO4===Na2SO4+2NH3·H2O(在溶液中)
.2NaOH(s)+(NH4)2SO4(s)
Na2SO4(s)+2NH3↑+2H2O
.Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑(实验室制NH3)
.★Ca(HCO3)2+2NaOH(过量)===2H2O+CaCO3↓+Na2CO3
.★Ca(HCO3)2+NaOH(不足)===H2O+CaCO3↓+NaHCO3
.★Mg(HCO3)2+4NaOH(过量)===Mg(OH)2↓+2Na2CO3+2H2O
⑤与某些单质反应
.2Al+2NaOH+2H2O===2NaAlO2+3H2↑
.Si+2NaOH+H2O===Na2SiO3+2H2↑
.Cl2+2NaOH===NaCl+NaClO+H2O
.★3S+6NaOH
2Na2S+Na2SO3+3H2O(洗硫)
4.Na2CO3、NaHCO3的反应
①与酸反应
.Na2CO3+HCl===NaHCO3+NaCl
.NaHCO3+HCl===NaCl+H2O+CO2↑(NaHCO3与盐酸反应更剧烈)
.Na2CO3+2HCl===2NaCl+H2O+CO2↑
②与酸性氧化物反应
.Na2CO3+CO2+H2O===2NaHCO3
.Na2CO3(饱和)+CO2+H2O===2NaHCO3↓(NaHCO3比Na2CO3溶解度小)
.Na2CO3+SiO2
Na2SiO3+CO2↑
.★2NaHCO3(过量)+SO2===Na2SO3+2CO2↑+H2O
.★NaHCO3(不足)+SO2===NaHSO3+CO2↑
.★2Na2CO3+SO2+H2O===2NaHCO3+Na2SO3
.★Na2CO3+SO2===Na2SO3+CO2↑
.★Na2CO3+2SO2+H2O===2NaHSO3+CO2↑
③与碱反应
.NaHCO3+NaOH===H2O+Na2CO3
.★NaHCO3(不足)+Ca(OH)2===H2O+CaCO3↓+NaOH
.★2NaHCO3(过量)+Ca(OH)2===2H2O+CaCO3↓+Na2CO3
.Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
④与盐反应
.Na2CO3+CaCl2===CaCO3↓+2NaCl
.Na2CO3+BaCl2===BaCO3↓+2NaCl
.NaHCO3与CaCl2、BaCl2不反应(用于区别CO32-、HCO3-)
.NaHCO3+NaHSO4===Na2SO4+H2O+CO2↑
⑤热稳定性
.2NaHCO3
Na2CO3+H2O+CO2↑(Na2CO3受热不分解)
.CaCO3
CaO+CO2↑(MgCO3、BaCO3类似)
(六)镁、铝、铁、铜元素
(1)镁、钙及其化合物的转化关系图
(2)镁及其化合物的性质
1.单质的还原性
.2Mg+O2
2MgO
.3Mg+N2
Mg3N2★Mg3N2+6H2O===3Mg(OH)2+2NH3↑
.Mg+Cl2
MgCl2★Mg+S
MgS
.2Mg+CO2
2MgO+C
.Mg+2H2O
Mg(OH)2+H2↑
.Mg+2H+===Mg2++H2↑
.★
总反应:
Mg+2NH4+===Mg2++2NH3↑+H2↑
2.化合物的性质
.MgO+2H+===Mg2++H2O
.★MgO+H2O===Mg(OH)2
.Mg(OH)2
MgO+H2O
.Mg(OH)2+2H+===Mg2++2H2O
.Mg2++2OH-===Mg(OH)2↓
.Mg2++2NH3·H2O===Mg(OH)2↓+2NH4+
.MgCl2(熔融)
Mg+Cl2↑
★.MgCl2+2H2O
Mg(OH)2↓+H2↑+Cl2↑
★.MgSO4+Ca(OH)2===Mg(OH)2↓+CaSO4↓
★★.MgCO3+H2O
Mg(OH)2↓+CO2↑
★★.Mg(HCO3)2
Mg(OH)2↓+2CO2↑
.Mg(HCO3)2+2Ca(OH)2===Mg(OH)2↓+2CaCO3↓+2H2O
(3)铝及其化合物的转化关系图
(4
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 方程式 总汇
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
