 专题七铁铜及其重要化合物a.docx
专题七铁铜及其重要化合物a.docx
- 文档编号:30005701
- 上传时间:2023-08-04
- 格式:DOCX
- 页数:18
- 大小:362.06KB
专题七铁铜及其重要化合物a.docx
《专题七铁铜及其重要化合物a.docx》由会员分享,可在线阅读,更多相关《专题七铁铜及其重要化合物a.docx(18页珍藏版)》请在冰豆网上搜索。
专题七铁铜及其重要化合物a
【教学标题】专题七:
铁、铜及其重要化合物
【教学目标】
1、了解铁单质及化合物的颜色.状态及性质。
2、.通过合金材料了解铜及化合物的性质。
二、铁、铜及其重要化合物
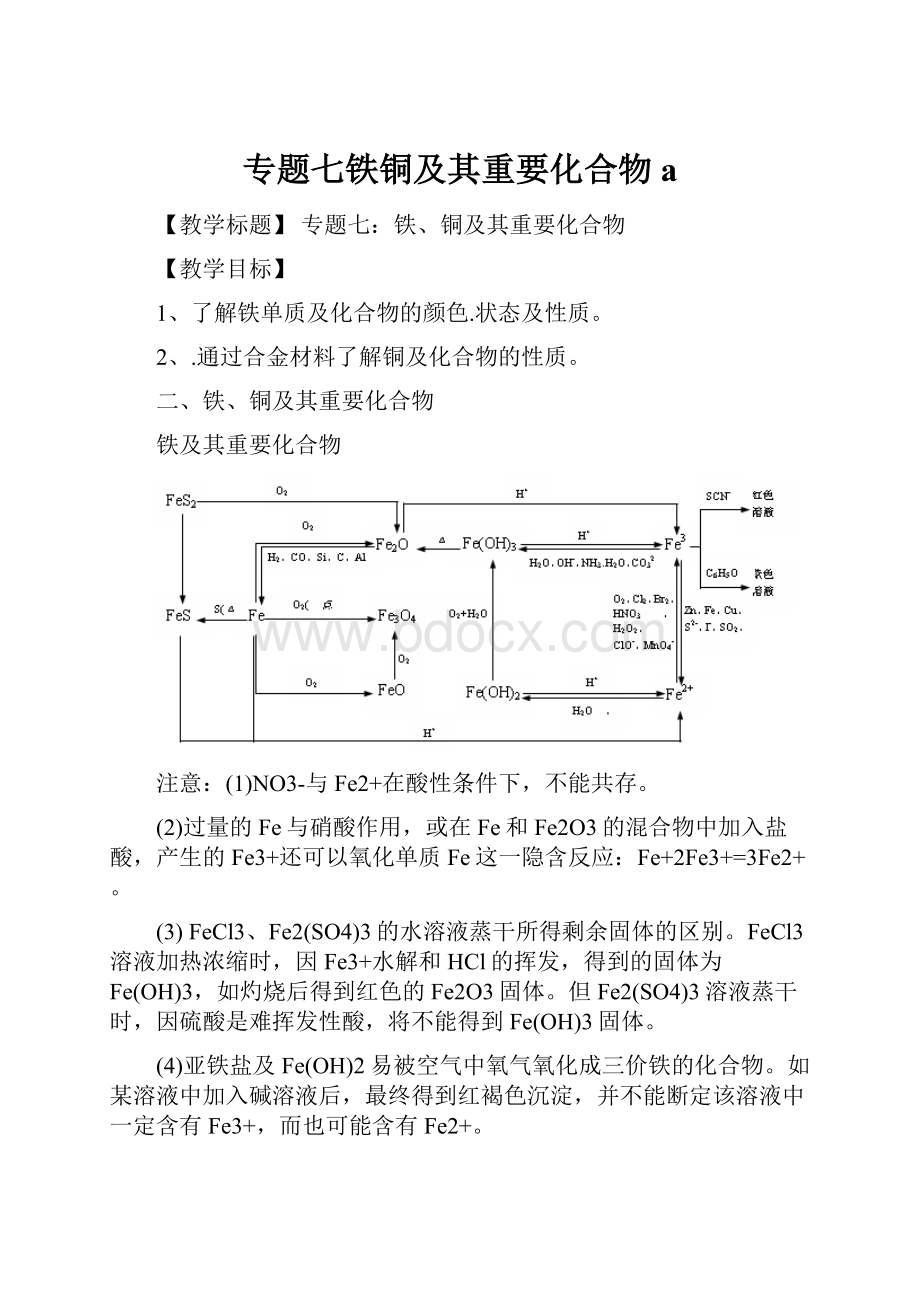
铁及其重要化合物
注意:
(1)NO3-与Fe2+在酸性条件下,不能共存。
(2)过量的Fe与硝酸作用,或在Fe和Fe2O3的混合物中加入盐酸,产生的Fe3+还可以氧化单质Fe这一隐含反应:
Fe+2Fe3+=3Fe2+。
(3)FeCl3、Fe2(SO4)3的水溶液蒸干所得剩余固体的区别。
FeCl3溶液加热浓缩时,因Fe3+水解和HCl的挥发,得到的固体为Fe(OH)3,如灼烧后得到红色的Fe2O3固体。
但Fe2(SO4)3溶液蒸干时,因硫酸是难挥发性酸,将不能得到Fe(OH)3固体。
(4)亚铁盐及Fe(OH)2易被空气中氧气氧化成三价铁的化合物。
如某溶液中加入碱溶液后,最终得到红褐色沉淀,并不能断定该溶液中一定含有Fe3+,而也可能含有Fe2+。
(5)铁单质与强氧化性物质反应时,也有生成二价铁化合物的可能性。
反应中若铁为足量,最终铁元素将以二价铁形式存在,因为2Fe3++Fe=3Fe2+。
1、稀硝酸(过量)单质
氧气:
_________________________硫:
_______________________
氯气:
________________________水蒸气:
_____________________
非氧化性酸_____________________浓硫酸_______________________
Fe与稀硝酸(硝酸过量)____________________________________________
稀硝酸(铁过量)-__________________________________________-
硫酸铜溶液_____________________氯化铁溶液__________________
2.铁的氧化物的比较
化学式
FeO
Fe2O3
Fe3O4
俗称
—
铁红
磁性氧化铁
色态
黑色粉末
红棕色粉末
黑色晶体
价态
+2
+3
1/3正2价,2/3正3价
水溶性
不溶
不溶
不溶
与酸的反应
FeO+2H+===Fe2++H2O
遇氧化性酸生成Fe3+盐
Fe2O3+6H+===2Fe3++3H2O
Fe3O4+8H+===Fe2++2Fe3++4H2O
遇氧化性酸生成Fe3+盐
与CO的反应
高温
FexOy+yCO===xFe+yCO2
3.Fe(OH)2与Fe(OH)3的比较
Fe(OH)2
Fe(OH)3
颜色状态
白色固体
红褐色固体
水溶性
不溶
不溶
稳定性
易氧化为Fe(OH)3,空气中加热得不到FeO
较稳定:
∆
Fe(OH)3==Fe2O3+3H2O
与酸的反应
Fe(OH)2+2H+===Fe2++3H2O
Fe(OH)3+3H+===Fe3++3H2O
制法
在隔绝O2的条件下Fe2+与碱反应
Fe3+与碱反应
相互转化关系:
4Fe(OH)2+O2+3H2O==4Fe(OH)3
4.Fe2+和Fe3+的比较
Fe2+
Fe3+
水合离子颜色
浅绿色
棕黄色
氧化还原性
既有氧化性,又有还原性
只有氧化性
水解性
Fe2++2H2O=Fe(OH)2+2H+
Fe3++3H2O←→Fe(OH)3+3H+
与碱的反应
Fe2++2OH—===Fe(OH)2↓
Fe3++3OH—===Fe(OH)3↓
5.检验Fe3+.常用方法有:
(1)向未知溶液滴入少量KSCN溶液呈血红色。
(2)向未知溶液滴入少量苯酚溶液呈紫色。
(3)向未知溶液中滴入少量NaOH溶液呈红褐色。
6.检验Fe2+.是向未知溶液滴入少量KSCN溶液呈无色,继续滴入少量氯水呈血红色。
【例1】(2010全国卷1)能正确表示下列反应的离子方程式是()
A.将铜屑加入
溶液中:
B.将磁性氧化铁溶于盐酸:
C.将氯化亚铁溶液和稀硝酸混合:
D.将铁粉加入稀硫酸中:
【例2】(2010上海卷)由5molFe2O3、4molFe3O4和3molFeO组成的混合物,加入纯铁1mol并在高温下和Fe2O3反应。
若纯铁完全反应,则反应后混合物中FeO与Fe2O3的物质的量之比可能是()
A.4:
3B.3:
2C.3:
1D.2:
l
【例3】(2009广东)钢铁生锈过程发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2;②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③2Fe(OH)3=Fe2O3+3H2O。
下列说法正确的是()
A.反应①、②中电子转移数目相等B.反应①中氧化剂是氧气和水
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
【例4】(2010四川理综卷)四川攀枝花蕴藏丰富的钒、钛、铁资源。
用钛铁矿渣(主要成分为TiO2、FeO、Fe2O3,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的主要步骤如下:
请回答下列问题:
(1)硫酸与二氧化钛反应的化学方程式是_______________。
(2)向滤液I中加入铁粉,发生反应的离子方程式为:
______________、______
(3)在实际生产过程中,向沸水中加入滤液Ⅲ,使混合液pH达0.5,钛盐开始水解。
水解过程中不断通入高温水蒸气,维持溶液沸腾一段时间,钛盐充分水解析出水合二氧化钛沉淀。
请用所学化学平衡原理分析通入高温水蒸气的作用:
__________________________________________________________________。
过滤分离出水合二氧化钛沉淀后,将滤液返回的主要目的是充分利用滤液中的钛盐、___________、_________、_______(填化学式),减少废物排放。
(4)A可用于生产红色颜料(Fe2O3),其方法是:
将556akgA(摩尔质量为278g/mol)溶于水中,加入适量氢氧化钠溶液恰好完全反应,鼓入足量空气搅拌,产生红褐色胶体;再向红褐色胶体中加入3336bkgA和112ckg铁粉,鼓入足量空气搅拌,反应完成后,有大量Fe2O3附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。
若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料_______________________kg。
[过手练习]
一、性质判断题
1、向FeCl3溶液中加入Mg(OH)2:
3Mg(OH)2+2Fe3+==2Fe(OH)3+3Mg2+()
2、生铁中含有碳,抗腐蚀能力比纯铁弱()
3、因为Fe3+有强氧化性,所以FeCl3溶液可用于回收废旧电路板中的铜()
4、Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置化反应()
二、选择题
1.下列关于铁的叙述正确的是( )
①铁能被磁铁吸引,但纯铁易锈蚀 ②在人体的血红蛋白中含有铁元素 ③不能通过化合反应生成FeCl2和Fe(OH)3 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与硝酸反应的产物仅是Fe(NO3)3
A.①③ B.②④C.②⑤D.④⑥
2.将下列四种铁的化合物溶于稀盐酸,滴加KSCN溶液没有颜色变化,再加入氯水即呈红色的是( )
A.FeSB.Fe2O3C.FeCl3D.Fe3O4
3.下列离子方程式书写正确的是( )
A.FeO固体放入稀硝酸溶液中:
FeO+2H+===Fe2++H2O
B.过量的铁粉与稀硝酸溶液反应:
Fe+4H++NO
===Fe3++NO↑+2H2O
C.向氢氧化亚铁中加入足量的稀硝酸:
Fe(OH)2+2H+===Fe2++2H2O
D.向Fe(OH)3中加入氢碘酸:
2Fe(OH)3+6H++2I-===2Fe2++I2+6H2O
4.(2011·山东高考)Al、Fe、Cu都是重要的金属元素。
下列说法正确的是( )
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中均只生成氧化物
C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al
5.某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示:
现对A、B、C、D作出的如下推断中,不正确的是( )
A.盐A一定是FeBr3B.浅黄色沉淀B是AgBr
C.滤液C中一定含Fe3+D.D溶液中有Fe(SCN)3
6.(2012·东莞一次联考)下列中学常见实验的现象或表述正确的是( )
A.过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加KSCN溶液,溶液显红色
B.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可
D.向CuSO4溶液中滴入过量NaOH溶液充分反应后,将混合液体倒入蒸发皿中加热一会,然后冷却、过滤,滤纸上的物体为“蓝色固体”
7(2011·上海)高铁酸钾(K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质()
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌
8.FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
A.加入KSCN溶液一定不变红色B.溶液中一定含Fe2+
C.溶液中一定含Cu2+D.剩余固体中一定含铜
9.(2011·福建高考)下表各选项中,不能利用置换反应通过Y得到W的一组化合物是()
选项
化合物
A
B
C
D
Y
CO2
Fe2O3
C2H5OH
FeCl3
W
MgO
Al2O3
C2H5ONa
CuCl2
10.(2011·潍坊模拟)某地污水中含有Zn2+、Hg2+、Fe3+、Cu2+四种阳离子。
甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下:
甲:
乙:
丙:
下列判断正确的是()
A.三种实验方案中都能制得纯净的铜
B.乙方案中加过量铁粉可以将四种阳离子全部还原
C.甲方案中的反应涉及置换、分解、化合、复分解四种反应类型
D.丙方案会产生环境污染
11.跟27克Al反应相应的稀HNO3溶液中最多可溶解Fe的质量为()
A.28gB.56gC.84gD.27g
12.5.6g铁粉加入含0.3mol
的溶液中,充分反应后,下列说法中正确的是()
A.Fe全部被氧化B.Fe部分被氧化
C.Fe3+全部被还原D.Fe3+部分被还原
三、非选择题
1.A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为液体,C为气体。
D、E、F、G、H、X均为化合物,其中X是一种无氧强酸,E为黑色固体,H在常温下为液体。
它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
(1)写出化学式:
A________、D________、E________、X________。
(2)在反应①~⑦中,不属于氧化还原反应的是________(填编号)。
(3)反应⑥的离子方程式为_________________________________________。
(4)反应⑦的化学方程式为_______________________________________;
该反应中每消耗0.3mol的A,可转移电子________mol。
(5)写出D的溶液与小苏打溶液、D的溶液中通入少量SO2反应的离子方程式:
________________________________________________
2.Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,铁及其化合物在生活、生产中有广泛应用。
请回答下列问题:
(1)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO3Fe+4CO2,若有1molFe3O4参加反应,转移电子的物质的量是________mol。
(2)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是__________________________________。
(3)某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。
请回答下列问题:
①各装置的正确连接顺序为(填写装置代号)A→________→_____→_____→D。
②装置C的作用是__________________________________________________。
③反应开始后,B中硬质玻璃管内的现象为_________________________;
可以检验生成物中含有Fe3+的试剂是________(填写试剂名称)。
3.(2011·全国卷Ⅱ)如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。
已知:
①反应C+G==B+H能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和E可以发生反应:
2E+I==2F+D,F中E元素的质量分数为60%。
回答问题:
(1)①中反应的化学方程式为___________________
(2)化合物I的电子式为___;
(3)1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方程式和计算过程);____________________________________、_________________________________________________________________。
(4)C与过量NaOH溶液反应的离子方程式为________________________
反应后溶液与过量化合物I反应的离子方程式为__________________
(5)E在I中燃烧观察到的现象是____________________________________。
4.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。
某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。
探究过程如下:
查阅资料:
Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
提出假设
假设1:
红色粉末是Fe2O3假设2:
红色粉末是Cu2O
假设3:
红色粉末是Fe2O3和Cu2O的混合物
设计探究实验取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
(1)若假设1成立,则实验现象是________________________________
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。
你认为这种说法合理吗?
________。
简述你的理由(不需写出反应的方程式)________________________。
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是________,写出发生反应的离子方程式____________________
_________________________________________________________________
探究延伸经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(4)实验小组欲用加热法测定Cu2O的质量分数,取ag固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为________。
(5)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
物质
Cu(OH)2
Fe(OH)2
Fe(OH)3
开始沉淀pH
6.0
7.5
1.4
沉淀完全pH
13
14
3.7
实验室有下列试剂可供选择:
A、氯水B、H2O2C、NaOH D、Cu2(OH)2CO3
实验小组设计如下实验方案:
试回答:
①试剂1为________,试剂2为________(填字母)。
②固体X的化学式为______________。
③操作Ⅰ为________________。
铜及其重要化合物
1、Cu与氧气、硫、氯气、氯化铁溶液等的反应电解
2、2Cu+O2+CO2+H2O==Cu2(OH)2CO32CuSO4+2H2O==2Cu+O2+2H2SO4
注意:
1、铜在潮湿的空气中最終不是生成CuO,而是铜綠(Cu2(OH)2CO3)
2、常用灼热的铜粉除去N2中的O2,灼热的CuO除去CO2中的CO
3、Cu和一定的浓HNO3反应,产生的是NO2和NO的混合气体,当Cu有剩余,再加入稀H2SO4,Cu继续溶解。
4、新制Cu(OH)2悬浊液常用来检验醛基
【例1】(2010全国卷1)下列叙述正确的是()
A.Li在氧气中燃烧主要生成
B.将SO2通入
溶液可生成
沉淀
C.将CO2通入次氯酸钙溶液可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
【例2】(2009广东化学)出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。
下列说法正确的是()
A.锡青铜的熔点比纯铜高B.在自然环境中,锡青铜中的锡对铜起保护作用
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
【过手练习】
一、性质判断
1、向硫酸铜溶液中加入镁条时有气体生成,该气体是H2()
2、用铜作电极电解CuSO4溶液:
2Cu2++2H2O==2Cu+O2+4H+()
3、过量的铜与浓硝酸反应有一氧化氮生成()
4、Al、Fe、Cu的单质放置在空气中均只生成氧化物()
二、非选择题
1.[2012·新课程理综]由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转化为低价氧化物。
该过程中两个主要反应的化学方程式是、,反射炉内生成炉渣的主要成分是;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。
转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。
冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式是、
;
(3)粗铜的电解精炼如右图所示。
在粗铜的电解过程中,粗铜板是图中电极(填图中的字母);在电极d上发生的电极反应为________________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的纯存在形式和位置为。
2.碱式碳酸铜可表示为:
xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种。
(1)现采用氢气还原法,请回答如下问题:
写出xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式_____
____________________________________________;
试验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→()()→()()→()()→()()→()()→(l)
③称取23.9g某碱式碳酸铜样品,充分反应后得到12.7g残留物,生成4.4g二氧化碳和7.2g水。
该样品的结晶水质量为g,化学式为;
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?
请说明理由。
_______________________________
_________________________________________________________________________。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题 七铁铜 及其 重要 化合物
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
