 整理zzzzzzzzzzzz奥赛晶体结构题.docx
整理zzzzzzzzzzzz奥赛晶体结构题.docx
- 文档编号:29963350
- 上传时间:2023-08-03
- 格式:DOCX
- 页数:40
- 大小:2.50MB
整理zzzzzzzzzzzz奥赛晶体结构题.docx
《整理zzzzzzzzzzzz奥赛晶体结构题.docx》由会员分享,可在线阅读,更多相关《整理zzzzzzzzzzzz奥赛晶体结构题.docx(40页珍藏版)》请在冰豆网上搜索。
整理zzzzzzzzzzzz奥赛晶体结构题
晶体结构题
一(2004年全国高中学生化学竞赛决赛6分)氢是
重要而洁净的能源。
要利用氢气作能源,必须解决
好安全有效地储存氢气问题。
化学家研究出利用合
金储存氢气,LaNi5是一种储氢材料。
LaNi5的晶体
结构已经测定,属六方晶系,晶胞参数a=511pm,
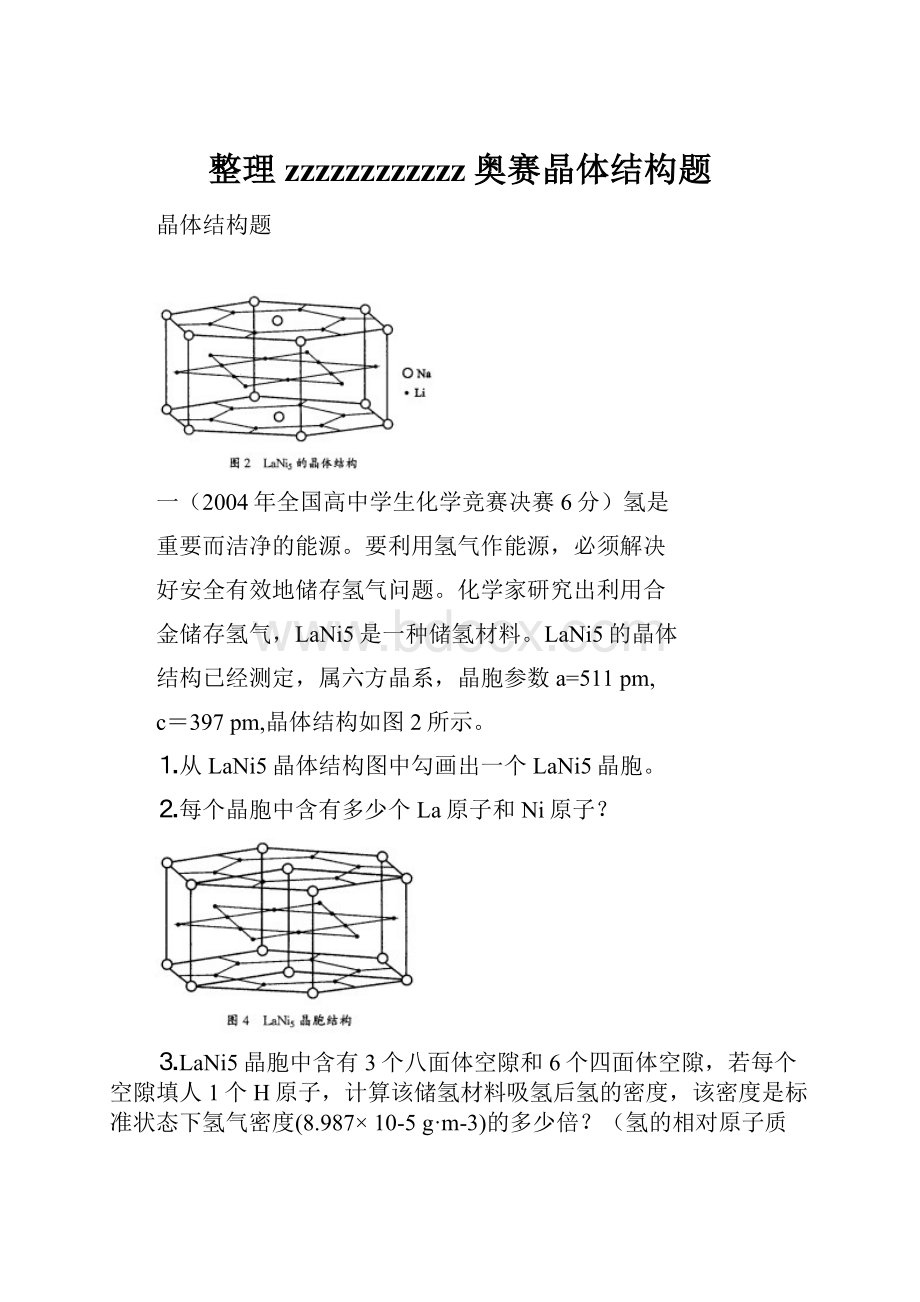
c=397pm,晶体结构如图2所示。
⒈从LaNi5晶体结构图中勾画出一个LaNi5晶胞。
⒉每个晶胞中含有多少个La原子和Ni原子?
⒊LaNi5晶胞中含有3个八面体空隙和6个四面体空隙,若每个空隙填人1个H原子,计算该储氢材料吸氢后氢的密度,该密度是标准状态下氢气密度(8.987×10-5g·m-3)的多少倍?
(氢的相对原子质量为1.008;光速c为2.998×108m·s-1;忽略吸氢前后晶胞的体积变化)。
解:
⒈晶胞结构见图4。
⒉晶胞中含有 1 个La原子
和 5 个Ni原子
⒊计算过程:
六方晶胞体积:
V=a2csin120°
=(5.11×10-8)2×3.97×10-8×31/2/2
=89.7×10-24cm3
氢气密度
是氢气密度的1.87×103倍。
二.(2006年全国高中学生化学竞赛决赛理论试题1)在酸化钨酸盐的过程中,钨酸根WO42-可能在不同程度上缩合形成多钨酸根。
多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含一个中心W原子和六个配位O原子的钨氧八面体WO6通过共顶或共边的方式形成。
在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2W12O40]6-。
在下面三张结构图中,哪一张是仲钨酸根的结构?
简述判断理由。
(a)
(b)
(c)
解:
提示:
考察八面体的投影图,可以得到更清楚地认识。
三.(2006年全国高中学生化学竞赛决赛理论试题4)轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,它的生产以白云石(主要成分是碳酸镁钙)为原料。
右图是省略了部分原子或离子的白云石晶胞。
[1]写出图中标有1、2、3、4、5、6、7的原子或离子的元素符号。
[2]在答题纸的图中补上与3、5原子或离子相邻的其他原子或离子,再用连线表示它们与Mg的配位关系。
解:
四.(2006年全国高中学生化学竞赛决赛理论试题7)沸石分子筛是重要的石油化工催化材料。
下图是一种沸石晶体结构的一部分,其中多面体的每一个顶点均代表一个T原子(T可为Si或Al),每一条边代表一个氧桥(即连接两个T原子的氧原子)。
该结构可以看成是由6个正方形和8个正六边形围成的凸多面体(称为β笼),通过六方柱笼与相邻的四个β笼相连形成的三维立体结构,如下图所示:
1.完成下列问题:
[1]若将每个β笼看作一个原子,六方柱笼看作原子之间的化学键,上图可以简化成什么结构?
在答题纸的指定位置画出这种结构的图形。
[2]该沸石属于十四种布拉维点阵类型中的哪一种?
指出其晶胞内有几个β笼。
[3]假设该沸石骨架仅含有Si和O两种元素,写出其晶胞内每种元素的原子数。
[4]已知该沸石的晶胞参数a=2.34nm,试求该沸石的晶体密度。
(相对原子质量:
Si:
28.0O:
16.0)
2.方石英和上述假设的全硅沸石都由硅氧四面体构成,下图为方石英的晶胞示意图。
Si-O
键长为0.162nm∠AED=109o28’
[1]求方石英的晶体密度。
[2]比较沸石和方石英的晶体密度来说明沸石晶体的结构特征。
3.一般沸石由负电性骨架和骨架外阳离子构成,利用骨架外阳离子的可交换性,沸石可以作为阳离子交换剂或质子酸催化剂使用。
下图为沸石的负电性骨架示意图:
请在答题纸的图中画出上图所示负电性骨架结构的电子式(用“∙”表示氧原子提供的电子,用“⨯”表示T原子提供的电子,用“*”表示所带负电荷提供的电子)。
解:
3
五.(2004年全国高中学生化学竞赛决赛4题)日本的白川英树等于1977年首先合成出带有金属光泽的聚乙炔薄膜,发现它具有导电性。
这是世界上第一个导电高分子聚合物。
研究者为此获得了2000年诺贝尔化学奖。
(1)写出聚乙炔分子的顺式和反式两种构型。
再另举一例常见高分子化合物,它也有顺反两种构型(但不具有导电性)。
(2)若把聚乙炔分子看成一维晶体,指出该晶体的结构基元。
(3)简述该聚乙炔塑料的分子结构特点。
(4)假设有一种聚乙炔由9个乙炔分子聚合而成,聚乙炔分子中碳—碳平均键长为140pm。
若将上述线型聚乙炔分子头尾连接起来,形成一个具有很好对称性的大环轮烯分子,请画出该分子的结构。
π电子在环上运动的能量可由公式
给出,式中h为普朗克常数(6.626×10-34J·s),me是电子质量(9.109×10-31kg),l是大环周边的长度,量子数n=0,士1,士2,…计算电子从基态跃迁到第一激发态需要吸收的光的波长。
(5)如果5个或7个乙炔分子也头尾连接起来,分别形成大环轮烯分子,请画出它们的结构。
(6)如果3个乙炔分子聚合,可得到什么常见物质。
并比较与由5、7、9个乙炔分子聚合而成的大环轮烯分子在结构上有什么共同之处。
(7)预测由3、5、7、9个乙炔分子聚合而成的化合物是否都具有芳香性?
作出必要的说明。
解:
(1)
(顺式)
(反式)
(顺式)天然橡胶
(反式)杜仲胶
(2)-CH=CH-CH=CH-
(3)聚乙炔的结构单元是CH,每个碳原子轨道都
是sp2杂化,形成了三个共平面的,夹角约120°的杂化轨
道,这些轨道与相邻的碳氢原子轨道键合构成了平面型的
结构框架。
其余未成键的PZ轨道与这一分子平面垂直,
它们互相重叠,形成长程的π电子共轭体。
(4)
(5)
(6)苯,都有3个顺式双键(苯看作单双键)
(7)[6]轮烯(苯)、[14]轮烯、[18]轮烯都具有芳香性;
[10]轮烯不具有芳香性。
[10]轮烯虽然π电子也满足4n+2,
但环内的2个氢原子的相对位置破坏了环的平面性。
六.(中国化学会第20届全国高中学生化学竞赛试题第8题(9分))超硬材料氮化铂略
七.(中国化学会第20届全国高中学生化学竞赛试题第11题)磷化硼是一种受到高度关注的耐磨涂料略
八.(中国化学会2003年全国高中学生化学竞赛试题第6题12分)2003年3月日本筑波材料科学国家实验室一个研究小组发现首例带结晶水的晶体在5K下呈现超导性。
略
九.(中国化学会2005年全国高中学生化学竞赛试题第2题12分)“爱因斯坦振荡器”的独立振荡原子与温度关系的模型。
略
十.(中国化学会2005年全国高中学生化学竞赛试题第8题12分)LiCl和KCl同属NaCl型晶体,略
十一.(第38届国际化学奥林匹克竞赛理论试题)Fe3O4(磁铁矿)本身是一种含有Fe2+、Fe3+的混合氧化物,属于AB2O4(尖晶石)型化合物。
其中氧离子作面心立方最密堆积。
下图示出了氧离子(灰球)的堆积形式与二价A离子、三价B离子的代表性位置。
墨球代表一个正四面体中心,白球代表一个正八面体中心。
1.在一个AB2O4单元中,铁离子有多少个可填充的正八面体空隙?
图中某些空隙是被相邻的单元共同拥有的。
解:
正八面体空隙4个;
AB2O4可采用常式与反式尖晶石结构。
在常式尖晶石中,两个B离子分别占据两个八面体空隙;一个A离子占据一个正四面体空隙。
在反式尖晶石结构中,两个B离子中的一个占据正四面体空隙,另一个B离子和A离子占据正八面体空隙。
2.在Fe3O4中,有百分之几的可填充的正四面体空隙被Fe2+或Fe3+占据?
解:
1/8;
3Fe3O4属于反式尖晶石结构,请画出在晶体场中Fe2+的分裂形式并填入电子。
电
子成对能大于八面体场分裂能。
解:
十二.(中国化学会第20届全国高中学生化学决赛竞赛试题第4题)
晶体硼的基本结构单元都是由硼原子组成的正二十面 体的原子晶体,其中含有20个等边三角形和一定数目的顶角,每个顶角上各有一个原子,试观察右边图形,回答:
(1) 这个基本结构单元由 12 个硼原子组成,
键角是 60 ,共含有 30 个B-B键。
(2) 在每个B-B键长的三分之一处切掉所有的硼原子,形成的是 32 面体。
如果在此新形成的多面体的每个顶点上换上碳原子,就是一种新的微粒,其化学式为 C60 。
截角二十面體,F=32(正五邊形×12、正六邊形×20);V=60;E=90
解:
十三.(中国化学会第20届全国高中学生化学决赛竞赛试题第2题)
解:
十四.(中国化学会2001年全国高中学生化学竞赛(省级赛区)试题第5题)今年3月发现硼化镁在39K呈超导性,略
十五.(中国化学会2001年全国高中学生化学竞赛(省级赛区)试题10题)最近有人用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,略
十六.(中国化学会2001年全国高中学生化学竞赛(省级赛区)试题第11题)研究离子晶体,常考察以一个离子为中心时,其周围不同距离的离子对它的吸引或排斥的静电作用力。
设氯化钠晶体中钠离子跟离它最近的氯离子之间的距离为d,以钠离子为中心,则:
1第二层离子有个,离中心离子的距离为d,它们是离子。
2已知在晶体中Na+离子的半径为116pm,Cl-离子的半径为167pm,它们在晶体中是紧密接触的。
求离子占据整个晶体空间的百分数。
3纳米材料的表面原子占总原子数的比例极大,这是它的许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰等于氯化钠晶胞的大小和形状,求这种纳米颗粒的表面原子占总原子数的百分比。
4假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞边长的10倍,试估算表面原子占总原子数的百分比。
解:
1)12,
,钠
2晶胞体积V=[2×(116pm+167pm)]3=181×106pm3
离子体积v=4x(4/3)π(116pm)3+4x(4/3)π(167pm)3=104×106pm3
v/V=57.5%(1分)(有效数字错误扣1分,V和v的计算结果可取4位,其中最后1位为保留数字,不扣分。
)
3表面原子为8(顶角)+6(面心)+12(棱中心)=26
总原子数为8(顶角)+6(面心)+12(棱中心)+1(体心)=27
表面原子占总原子数26/27×100%=96%(1分)
注:
26和27均为整数值,比值26/27是循环小数0.962,取多少位小数需根据实际应用而定,本题未明确应用场合,无论应试者给出多少位数字都应按正确结果论。
4计算分两个步骤:
步骤一:
计算表面原子数。
可用n=2、3的晶胞聚合体建立模型,得出计算公式,用以计算n=10。
例如,计算公式为:
[8]+[(n-1)×12]+[n×12]+[(n-1)2×6]+[n2x6]+[(n-1)×n×2×6]
顶角棱上棱交点棱上棱心面上棱交点面上面心面上棱心
n=10,表面原子总数为2402(2分)
步骤二:
计算晶胞聚合体总原子数:
n3×8+[8]×7/8+[(n-1)×12]×3/4+[n×12]×3/4+[(n-1)2×6]/2+[n2×6]/2+[(n-1)×n×2×6]/2
=8000+7+81+90+243+300+540
=9261(2分)
表面原子占总原子数的百分数:
(2402/9261)×100%=26%(1分)(总5分)
(注:
本题计算较复杂,若应试者用其他方法估算得出的数值在26%左右2个百分点以内可得3分,3个百分点以内可得2分,其估算公式可不同于标准答案,但其运算应无误。
本题要求作估算,故标准答案仅取整数,取更多位数不扣分。
)
十七.(中国化学会2000年全国高中学生化学竞赛(省级赛区)试题第4题)理想的宏观单一晶体呈规则的多面体外形。
略
十八.(中国化学会2000年全国高中学生化学竞赛(省级赛区)试题第5题)最近发现一种由钛原子和碳原子构成的气态团簇分子,略
十九.(中国化学会2000年全国高中学生化学竞赛(省级赛区)试题第9题)最近,我国一留美化学家参与合成了一种新型炸药,它跟三硝基甘油一样抗打击、抗震,但一经引爆就发生激烈爆炸,略
二十.(中国化学会2000年全国高中学生化学竞赛(省级赛区)试题第11题)已经探明,我国南海跟世界上许多海域一样,海底有极其丰富的甲烷资源。
其总量超过已知蕴藏在我国陆地下的天然气总量的一半。
据报导,这些蕴藏在海底的甲烷是高压下形成的固体,是外观像冰的甲烷水合物。
1.试设想,若把它从海底取出,拿到地面上,它将有什么变化?
为什么?
它的晶体是分子晶体、离子晶体还是原子晶体?
你作出判断的根据是什么?
(2分)
2.已知每1立方米这种晶体能释放出164立方米的甲烷气体,试估算晶体中水与甲烷的分子比(不足的数据由自己假设,只要假设得合理均按正确论)。
(6分)
【答案】
1.从海底取出的甲烷水合物将融化并放出甲烷气体,因为该晶体是分子晶体,甲烷分子和水分子都是由有限数目的原子以共价键结合的小分子,水分子和甲烷分子之间范德华力,而水分子之间是范德华力和氢键。
(2分)
2.假设甲烷气体体积是折合成标准状况下的数据,则1m3水合物中有甲烷164m3÷22.4m3/kmol=7.32kmol;假设甲烷水合物固体中的水的密度为1g/cm3,则其中有水1m3×1000kg/m3÷18kg/mol=55.56kmol;因此有:
CH4︰H2O=7.32kmol︰55.6kmol=1︰7.6。
甲烷水合物的组成可能是6CH4·46H2O(6分)
【说明】
以上是最简单的参考答案,设密度为1g/cm3也可包含甲烷,只要答案为CH4·6~9H2O,均可按满分计。
但设密度为0.9g/cm3又包含甲烷则不能认为是合理的(岂不会漂到海面上来?
另外,必须给出解题时的假设,否则不能得满分。
)
二十一.(中国化学会2003年全国高中学生化学竞赛(省级赛区)试题第9题) 钒是我国丰产元素,储量占全球11%,略
二十二.(中国化学会2004年全国高中学生化学竞赛(省级赛区)试题第5题)(18分)晶体的最小重复单位是晶胞,晶胞一般为平行六面体(立方晶格为立方体)。
NaCl属立方面心晶格,在NaCl晶胞中8个顶点各有一个Na+(顶点处的微粒为8个晶胞共有),6个面心处各有一个Na+(面心处的微粒为两个晶胞共有),故我们说Na+形成立方面心晶格,而在该晶胞的12条棱的中点处各有一个Cl-(棱心处的微粒为4个晶胞共有),在该立方晶胞的体心处还有一个Cl-(立方体内的微粒为一个晶胞独有),故Cl-也形成立方面心晶格。
⒈按上述微粒数的计算规则,则一个NaCl晶胞中有____个Na+,____个Cl-。
(每空1分)
⒉KCl和NaCl的晶格型式相同。
已知Na+离子的半径是Cl-离子的0.5倍,而又是K+离子的0.7倍,计算:
KCl晶胞和NaCl晶胞的边长之比;KCl和NaCl晶体的密度之比。
(相对原子质量:
K:
39,Na:
23,Cl:
35.5)(4分)
⒊将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在每两个不共面的“小立方体”中心处各放置一个C原子便构成了金刚石的一个晶胞,则一个金刚石的晶胞中有________个C原子。
(1分)
⒋计算金刚石的密度。
(已知C原子的半径为7.7×10-11m,相对原子质量:
12(4分)
⒌白硅石SiO2属AB2型共价键晶体。
若将金刚石晶胞中的所有C原子换成Si原子,同时在每两个相邻的Si原子(距离最近的两个Si原子)中心联线的中点处增添一个O原子,则构成SiO2晶胞,故SiO2晶胞中有_______个Si原子,______个O原子,离O原子最近的Si原子有_______个,离Si原子最近的O原子有_______个。
(每空1分)
⒍干冰(固态CO2)属于分子晶体。
若把每个CO2分子抽象为一个质点(微粒),则其晶胞也属于立方面心晶格,故一个干冰晶胞中有_________个CO2,在干冰分子中,原子之间靠_________________结合,CO2分子之间靠______________结合。
(每空1分)
解:
1、44
2、解:
(1)已知rNa+=0.5rCl-,rNa+=0.7rk+,于是可得:
0.7rk+=0.5rCl-
故akCl:
aNaCl=8:
7=1.14
(2)由于NaCl:
M胞=4(23+35.5),p=M/VNA,而V=aNaCl3
KCl:
M’胞=4(39+35.5),p’=M’/V’NA,而V’=aKCl3
所以,p’:
P=0.853
3、8
4、ρ=3.54(g.cm-3)
5、81624
6、4共价键范德华力
二十三.(中国化学会94年全国高中学生化学竞赛决赛试题第3题)
二十四.(中国化学会95年全国高中学生化学竞赛决赛试题第6题)
二十五.(中国化学会96年全国高中学生化学竞赛决赛试题第9题)
解:
二十六2008决赛
答案
二十七2009决赛
答案
二十八2010决赛
二十九98决赛
黄铜矿是最重要的铜矿,全世界约三分之二的铜是由它提炼的。
回答下列问题:
1.图6为黄铜矿的晶胞,计算该晶胞中各种原子的数目,
写出黄铜矿的化学式。
2.在黄铜矿晶胞中,化学和空间环境都相同的硫原子、
铁原子、铜原子各有几个?
在黄铜矿晶胞中含几个结构基元
(周期性重复的最小单位)?
每个结构基元代表什么?
3.在高温下,黄铜矿晶体中的金属离子可以发生迁移。
若铁原子与铜原子发生完全无序的置换,可将它们视作等
同的金属原子,请画出它的晶胞。
每个晶胞中环境相同的
硫原子有几个?
4.在无序的高温型结构中,硫原子作什么类型的堆积,
金属原子占据什么类型的空隙,该类型空隙被金属原子占据
的分数是多少?
5.实验表明,CuGaS2和Cu2FeSnS4与黄铜矿的结构类型相同,a=52.4pm,c=103.0pm
请据此推测黄铜矿中铜和铁的氧化态。
答案
(评判分:
30分)
1.4Fe,4Cu,8S(3分);化学式CuFeS2(2分);
2.2个结构基元(8分);结构基元为Cu2Fe2S4(2分);
3.晶胞为原晶胞的一半(如图,黑点代表Cu1/2Fe1/2的统计原子)(5分);每个晶胞有4个环境相同的硫原子(2分);
4.硫原子作立方面心堆积,金属原子占据四面体空隙,占据的分数为50%(6分).
5.Cu+1;Fe+3(2分)黄铜矿的无序结构图
三十01决赛
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体。
这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体。
固体电解质取代液体电解质,可以做成全固态电池及其它传感器、探测器等,在电化学、分析化学等领域的应用日益广泛。
银有α、β、和γ等多种晶型。
在水溶液中Ag+与I-沉淀形成的是γ-AgI和β-AgI的混合物,升温至136℃全变为β-AgI,至146℃全变为α-AgI。
α-AgI是一种固体电解质,导电率为1.31Ω-1·cm-1(注:
强电解质水溶液的导电率为10-3~1Ω-1·cm-1)。
4-1γ-AgI和β-AgI晶体的导电性极差。
其中γ-AgI晶体属立方晶系,其晶胞截面图如下所示。
图中实心球和空心球分别表示Ag+和I-,a为晶胞边长。
试指出γ-AgI晶体的点阵型式和Ag+、I-各自的配位数(已知通常I-的半径为220pm,Ag+的半径为100--150pm)。
4-2α-AgI晶体中,I-离子取体心立方堆积,Ag+填充在其空隙中。
试指出α-AgI晶体的晶胞中,八面体空隙、四面体空隙各有多少?
4-3为何通常Ag+离子半径有一个变化范围?
4-4实验发现,α-AgI晶体中能够迁移的全是Ag+,试分析Ag+能够发生迁移的可能原因。
答案
4-1点阵型式:
面心立方CN+=4CN-=4
4-2八面体空隙:
6个;四面体空隙:
12个
4-3在不同的晶体中,Ag+离子占据不同空隙,按正负离子相互接触计算的Ag+离子半径自然有一个变化范围。
4-4要点:
(1)四面体空隙与八面体空隙相连,四面体空隙与四面体空隙通过三角形中心相连,构成三维骨架结构的开放性“隧道”供Ag+迁移;
(2)有大量空隙(Ag+与空隙之比为1∶9)可供Ag+迁移;
(3)用适当的理论(如极化理论)说明Ag+容易发生迁移。
(注:
迁移的激活能为0.05eV)
三十一02决赛
(一)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图一所示,图中用虚线标出了石墨的一个六方晶胞。
4-1.试确定该晶胞的碳原子个数。
4-2.写出晶胞内各碳的原子坐标。
4-3.已知石墨的层间距为334.8pm,C-C键长为142pm,计算石墨晶体的密度。
(二)石墨可用作锂离子电池的负极材料,充电时发生下述反应:
Li1-xC6+xLi++xe-→LiC6
其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
4-4.图二给出了一个Li+沿C轴投影在A层上的位置,试在图上标出与该离子临近的其它六个Li十的投影位置。
4-5.在LiC6中,Li+与相邻石墨六元环的作用力属何种键型?
4-6.某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式,画出它的晶胞(C轴向上)。
(三)锂离子电池的正极材料为层状结构的LiNiO2。
已知LiNiO2中Li+和Ni3+均处于氧离子组成的正八面体体心位置,但处于不同层中。
4-7.将化学计量的NiO和LiOH在空气中加热到700℃可得LiNiO2,试写出反应方程式。
小8.写出LiNiO2正极的充电反应方程式。
49.锂离子完全脱嵌时LiNiO2的层状结构会变得不稳定,用铝取代部分镍形成LiNi1-yAlyO2可防止锂离子完全脱嵌而起到稳定结构的作用,为什么?
图一
答案
4—14个(1分)
4—2(0,0,0),(0,0,l/2),(l/3,2/3,0),(2./3,1/3,1/2)
4—32.27g·cm-3(体积计算1分,密度计算1分,共2分)
4—4见附图1(l分)
4—5离子键或静电作用(1分)
4—6LiC2晶胞见附图2(1+2分)
4—74NiO+4LiOH+O2==4LiNiO2+2H2O(1分)
4—8LiNiO2==Li1-xNiO2+xLi++xe-(1分)
4—9Al3+无变价,因此与之对应的Li十不能脱嵌。
(1分)
三十二05决赛
答案
三十三08(22届)初赛备用
第6题(12分)LiMO2(M为过渡金属)晶体是良好的导电材料,属六方晶系。
其中Li在晶胞的顶点,三个M原子在六棱柱的三个不相邻的三角形的中线上并位于1/2的高度上,O原子也在这条中线上但高度分别为1/4和3/4。
6-1试画出LiMO2的一个晶
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 整理 zzzzzzzzzzzz 晶体结构
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
