 届高考化学考前冲刺提分训练以化工工艺流程综合考查元素化合物知识答案+详解课后复习总结.docx
届高考化学考前冲刺提分训练以化工工艺流程综合考查元素化合物知识答案+详解课后复习总结.docx
- 文档编号:29941313
- 上传时间:2023-08-03
- 格式:DOCX
- 页数:12
- 大小:137.72KB
届高考化学考前冲刺提分训练以化工工艺流程综合考查元素化合物知识答案+详解课后复习总结.docx
《届高考化学考前冲刺提分训练以化工工艺流程综合考查元素化合物知识答案+详解课后复习总结.docx》由会员分享,可在线阅读,更多相关《届高考化学考前冲刺提分训练以化工工艺流程综合考查元素化合物知识答案+详解课后复习总结.docx(12页珍藏版)》请在冰豆网上搜索。
届高考化学考前冲刺提分训练以化工工艺流程综合考查元素化合物知识答案+详解课后复习总结
——以化工工艺流程综合考查元素化合物知识
【提分训练】
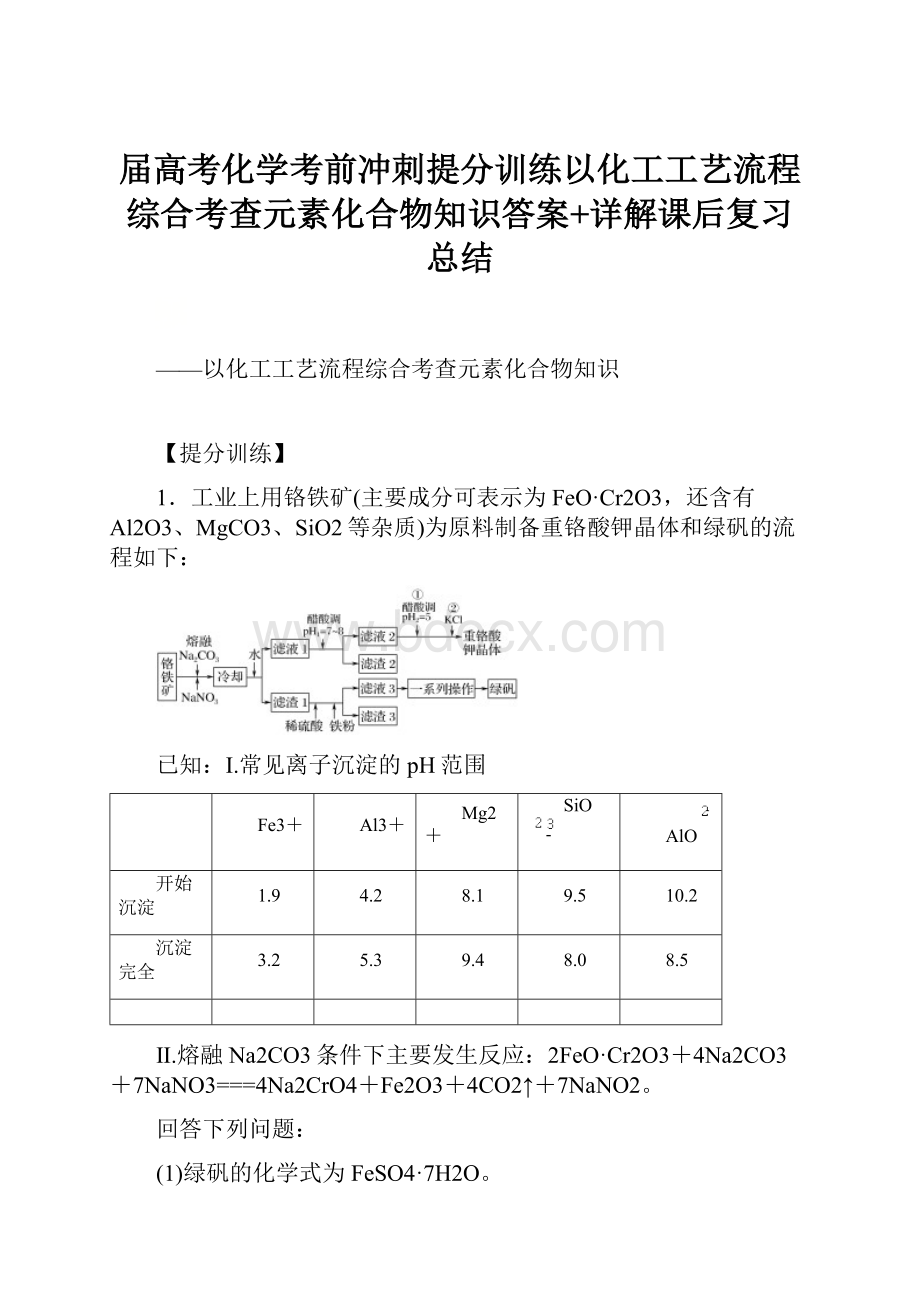
1.工业上用铬铁矿(主要成分可表示为FeO·Cr2O3,还含有Al2O3、MgCO3、SiO2等杂质)为原料制备重铬酸钾晶体和绿矾的流程如下:
已知:
Ⅰ.常见离子沉淀的pH范围
Fe3+
Al3+
Mg2+
SiO
AlO
开始沉淀
1.9
4.2
8.1
9.5
10.2
沉淀完全
3.2
5.3
9.4
8.0
8.5
Ⅱ.熔融Na2CO3条件下主要发生反应:
2FeO·Cr2O3+4Na2CO3+7NaNO3===4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
回答下列问题:
(1)绿矾的化学式为FeSO4·7H2O。
(2)滤液1中除含有Na2CrO4、NaNO2和过量的Na2CO3、NaNO3外,还含有NaAlO2和Na2SiO3,则熔融Na2CO3条件下发生的副反应有Na2CO3+Al2O3
2NaAlO2+CO2↑和Na2CO3+SiO2
Na2SiO3+CO2↑(用化学方程式表示)。
(3)滤渣2的主要成分为H2SiO3和Al(OH)3(填写化学式)。
(4)用醋酸调节pH2=5的目的为将CrO
转化为Cr2O
;若pH调节的过低,NO
可被氧化为NO
,其离子方程式为Cr2O
+3NO
+8H+===2Cr3++3NO
+4H2O。
(5)调节pH2后,加入KCl控制一定条件,可析出K2Cr2O7晶体的可能理由是在该条件下K2Cr2O7的溶解度最低,更易分离。
(6)流程中的一系列操作为蒸发浓缩、冷却结晶、过滤。
解析:
(1)绿矾的化学式为FeSO4·7H2O。
(2)生成NaAlO2和Na2SiO3的化学方程式为Na2CO3+Al2O3
2NaAlO2+CO2↑和Na2CO3+SiO2
Na2SiO3+CO2↑。
(3)调pH1=7~8,是为了得到沉淀H2SiO3和Al(OH)3。
(4)用醋酸调节pH2=5的目的是将CrO
转化为Cr2O
;若pH调节的过低会发生Cr2O
+3NO
+8H+===2Cr3++3NO
+4H2O。
(5)调节pH2后,加入KCl控制一定条件,可过滤出K2Cr2O7晶体的可能理由是在该条件下K2Cr2O7的溶解度最低。
(6)溶液中除了含有硫酸亚铁外,还含有少量其他杂质,例如硫酸镁。
所以从溶液中得到晶体的方法为蒸发浓缩、冷却结晶、过滤。
2.碳酸锂(相对分子质量为74)广泛应用于化工、冶金、陶瓷、医药、制冷、焊接、锂合金等行业。
制备流程如下:
已知:
①锂辉石的主要成分为Li2O·Al2O3·4SiO2;②碳酸锂的溶解度(g·L-1)见下表。
温度/℃
0
10
20
30
40
50
60
80
100
Li2CO3
1.54
1.43
1.33
1.25
1.17
1.08
1.01
0.85
0.72
(1)硫酸化焙烧工业反应温度控制在250~300℃,主要原因是温度低于250_℃,反应速率较慢;温度高于300_℃,硫酸挥发较多;同时,硫酸用量为理论耗酸量的115%左右,硫酸如果加入过多则ABC(填字母)。
A.增加酸耗量
B.增加后续杂质的处理量
C.增加后续中和酸的负担
(2)水浸时,需要在搅拌下加入石灰石粉末的主要作用是除去多余的硫酸,同时调整pH,除去大部分杂质。
(3)“沉锂”需要在95℃以上进行,主要原因是温度越高,碳酸锂溶解度越小,可以增加产率。
过滤碳酸锂所得母液中主要含有Na2SO4,还可能含有Na2CO3、Li2CO3。
解析:
(1)若温度过低,反应速率慢,若温度过高,则浓H2SO4沸腾,挥发较多。
(2)加入CaCO3一是和多余H2SO4反应,二是调节pH除去大部分杂质。
(3)由表格中数据可知,温度越高,Li2CO3溶解度越小,故沉锂在95℃以上进行可增加产率。
过滤后的母液中除Na2SO4外还可能有Na2CO3、Li2CO3。
3.(2018·新课标全国卷Ⅱ)我国是世界上最早制得和使用金属锌的国家。
一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子
Fe3+
Fe2+
Zn2+
Cd2+
开始沉淀的pH
1.5
6.3
6.2
7.4
沉淀完全的pH
2.8
8.3
8.2
9.4
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为2ZnS+3O2
2ZnO+2SO2。
(2)滤渣1的主要成分除SiO2外还有PbSO4;氧化除杂工序中ZnO的作用是调节溶液的pH,若不通入氧气,其后果是无法除去杂质Fe2+。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为Cd2++Zn===Cd+Zn2+。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为Zn2++2e-===Zn;沉积锌后的电解液可返回溶浸工序继续使用。
解析:
(1)在焙烧过程中ZnS和O2反应生成ZnO和SO2。
(2)溶液中的Pb2+与SO
不能共存生成PbSO4沉淀,SiO2不溶于H2SO4,即滤渣1中含SiO2和PbSO4。
氧化除杂过程中O2能将溶液中Fe2+氧化生成Fe3+,加入ZnO能调节溶液的pH,促进Fe3+完全水解。
由题表知Fe2+、Zn2+开始沉淀和沉淀完全时的pH非常接近,若不通入O2使Fe2+氧化为Fe3+,加入ZnO后无法除去Fe2+,会影响Zn的纯度。
(3)根据题中信息可知还原除杂工序中涉及的离子反应为Cd2++Zn===Cd+Zn2+。
(4)结合图示可知电解ZnSO4溶液时生成Zn,即电解时Zn2+在阴极被还原,电极反应式为Zn2++2e-===Zn。
沉积Zn后的电解液中主要含有H2SO4,可返回溶浸工序中继续使用。
4.工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。
其工艺流程如下:
[查阅资料]
①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质;
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
请回答:
(1)操作①的名称是过滤,“水浸”后的溶液呈碱性。
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为4Cr(OH)3+4Na2CO3+3O2===4Na2CrO4+4CO2+6H2O。
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为AlO
+H++H2O===Al(OH)3↓。
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为2CrO
+2H+===Cr2O
+H2O。
解析:
(1)操作①是从溶液中分离出滤渣,操作①的名称是过滤;水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等都为强碱弱酸盐,水解后呈碱性。
(2)焙烧氧化过程中有氧气参加反应,可知还应生成水,反应的化学方程式为4Cr(OH)3+4Na2CO3+3O2===4Na2CrO4+4CO2+6H2O。
(3)水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质,加入硫酸调节溶液的pH可得到Zn(OH)2、Al(OH)3沉淀,NaAlO2加入酸生成Al(OH)3沉淀的离子方程式为AlO
+H++H2O===Al(OH)3↓。
(4)Na2CrO4转化成Na2Cr2O7的离子方程式为2CrO
+2H+===Cr2O
+H2O。
5.石墨在材料领域有重要应用。
某初级石墨中含有SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。
为了提纯和综合利用初级石墨,设计工艺流程如图所示:
(注:
SiCl4的沸点是57.6℃,题中金属氯化物的沸点均高于150℃)
(1)已知1mol石墨完全转化为金刚石需要吸收1.9kJ的能量。
请写出石墨转化为金刚石的热化学方程式:
C(石墨,s)===C(金刚石,s) ΔH=+1.9kJ·mol-1。
(2)向反应器中通入Cl2前,需通一段时间的N2。
高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。
80℃冷凝的目的是将MgCl2、FeCl3、AlCl3等金属氯化物冷凝为固体,从而与SiCl4分离。
由活性炭得到气体Ⅱ的反应的化学方程式为2C+SiO2+2Cl2
SiCl4+2CO(或2C+SiO2
Si+2CO↑、Si+2Cl2
SiCl4)。
(3)向固体Ⅲ中加入过量NaOH溶液得到溶液Ⅳ的反应的离子方程式为Al3++4OH-===AlO
+2H2O。
(4)用化学反应原理解释得到沉淀Ⅴ的过程中加入乙酸乙酯和加热的作用:
溶液Ⅳ中NaAlO2水解显碱性,乙酸乙酯消耗NaAlO2水解生成的NaOH,促进NaAlO2水解生成Al(OH)3;加热促进水解,加快反应速率。
1kg初级石墨最多可获得沉淀Ⅴ的质量为0.078kg。
解析:
(1)书写热化学方程式时,要注意热化学方程式中化学计量数的含义、物质的聚集状态、焓变的正负及单位。
(2)通入Cl2进行高温反应后,石墨中的Al2O3、Fe2O3和MgO等金属氧化物均转变为相应的氯化物。
活性炭与SiO2在高温下反应生成Si和CO,Si与Cl2在高温下反应生成SiCl4,SiCl4的沸点是57.6℃,题中金属氯化物的沸点均高于150℃,在80℃冷凝可将MgCl2、FeCl3、AlCl3等金属氯化物冷凝为固体,从而与气态SiCl4分离。
气体Ⅱ是SiCl4和CO的混合物。
(3)固体Ⅲ中含MgCl2、FeCl3、AlCl3,加入过量NaOH溶液后,Mg2+、Fe3+转化为氢氧化物沉淀,Al3+转化为AlO
进入溶液Ⅳ中。
(4)溶液Ⅳ中含有AlO
,沉淀Ⅴ是Al(OH)3。
溶液Ⅳ中的NaAlO2水解使溶液显碱性,乙酸乙酯在碱性条件下能彻底水解,可消耗NaAlO2水解生成的NaOH,促进NaAlO2水解生成Al(OH)3;水解过程吸热,加热可促进水解,同时也可加快反应速率。
初级石墨中含5.1%的Al2O3,1kg初级石墨中,n(Al2O3)=1000g×5.1%÷102g·mol-1=0.5mol,不考虑转化过程中Al元素的损失,则最多可生成1molAl(OH)3沉淀,其质量为0.078kg。
【课后总结】
1.题型分析
工艺流程题是近几年高考的热考题型,工艺流程题的结构分题头、题干和题尾三部分。
题头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括副产品);题干主要用流程图形式将原料到产品的主要生产工艺流程表示出来;题尾主要是根据生产过程中涉及的化学知识设计成一系列问题,构成一道完整的化学试题。
此类试题集综合性、真实性、开放性于一体,包含必要的操作名称、化工术语或文字说明,考查知识面广、综合性强、思维容量大。
题干的呈现形式多为流程图、表格和图象;设问角度一般为操作措施、物质成分、化学反应、条件控制的原因和产率计算等,能力考查侧重于获取信息的能力、分析问题的能力、语言表达能力和计算能力;涉及到的化学知识有基本理论、元素化合物和实验基础知识等。
2.考查内容
(1)原材料的预处理
酸浸
加酸,使可溶性离子进入溶液,不溶物通过过滤除去
水浸
与水接触反应或溶解
水洗
除去水溶性杂质
浸出
固体加水(酸)溶解得到离子
研磨
将固体粉碎,增大表面积,加快反应速率
煅烧
使物质在高温下氧化、分解
碱洗
除去油污或者氧化膜
(2)反应条件控制
加热
加快反应速率;加速固体溶解;使平衡向吸热方向移动
降温
防止物质在高温时溶解;使化学反应速率下降;使化学平衡向放热的方向移动
续表
控温
温度过高,物质会分解或会挥发;温度过低,物质无法挥发或者反应
趁热过滤
防止某物质降温时会析出晶体
冰水洗涤
洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗
酸性氛围
防止金属阳离子水解
pH控制
控制溶液的酸碱性使某些金属离子形成氢氧化物沉淀
(3)产品的分离和提纯
①把握物质提纯的“6种”常用方法
看目的
选方法
除去可溶性杂质
水溶法
除去碱性杂质
酸溶法
除去酸性杂质
碱溶法
除去还原性或氧化性杂质
氧化还原法
除去受热易分解或易挥发的杂质
加热灼烧法
除去酸性Cu2+溶液中的Fe3+等
调pH法
②物质分离常用方法
过滤——基本操作:
一贴二低三靠。
结晶——当溶液为单一溶质时:
a.所得晶体不带结晶水。
如NaCl、KNO3等的结晶过程:
溶解、过滤、蒸发结晶。
b.所得晶体带结晶水。
如胆矾等的结晶过程:
将滤液蒸发浓缩、冷却结晶、过滤。
当溶液为两种以上溶质时:
a.要得到溶解度受温度影响小的溶质时:
浓缩结晶,趁热过滤;b.要得到溶解度受温度影响大的溶质时:
蒸发浓缩、冷却结晶,过滤。
重结晶:
蒸发浓缩、冷却结晶,过滤(重复操作)。
洗涤——向过滤器中的滤渣加蒸馏水至浸没滤渣,静置;取洗涤后小烧杯中的最后一次洗涤液,滴加试剂(如AgNO3检验氯离子或者BaCl2检验硫酸根离子),若无沉淀产生,则证明洗涤干净。
干燥——在干燥器隔绝空气的条件下低温烘干。
灼烧——固体在坩埚中进行加热。
分液——下层液体从下口放出;上层液体从上口倒出。
重复操作2~3次——保证实验的准确性。
(4)工业要求
是否污染环境、原子经济性、节约资源、安全性、资源再生。
3.解答无机化工流程试题的程序
(1)基本步骤。
①从题干中获取有用信息,了解生产的产品。
②整体浏览一下流程,基本辨别出预处理、反应、提纯、分离等阶段。
③分析流程中的每一步骤,从几个方面了解流程:
A.反应物是什么;B.发生了什么反应;C.该反应造成了什么后果,对制造产品有什么作用。
抓住一个关键点:
一切反应或操作都是为获得产品而服务的。
④从问题中获取信息,帮助解题。
(2)解题思路。
明确整个流程及每一部分的目的→仔细分析每步反应发生的条件以及得到的产物的物理或化学性质→结合基础理论与实际问题思考→注意答题的模式与要点。
(1)解题策略
解题步骤
解题策略
首尾呼应、
找出主线
①对照原料和产品,确定核心反应和核心辅料
②依核心反应,明确流程主线、支线和除杂任务
分段剖析、
明析细节
③以核心辅助原料为准,把流程划分为原料预处理、核心反应和产品分离提纯三个阶段
④依箭头指向,分析每一环节中物质流入和流出的意义、控制反应条件的作用,融通对流程的整体分析
⑤某些暂时琢磨不透的环节,可“跳过去”而“难得糊涂”,如有必要,可“顺藤摸瓜”或带着问题回头来进行有针对性的分析
由易到难、
破解答案
⑥先易后难:
先回答与工艺流程非密切相关的问题,确保易拿的分数先拿,增强答题信心
⑦变换角度:
从基本理论、绿色化学观点、经济角度、安全生产等多角度答题
⑧对棘手问题:
不忘尝试从题给信息中寻找答案
(2)物质判断:
主线主产品,副线副产品,回头为循环。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 考前 冲刺 训练 化工 工艺流程 综合 考查 元素 化合物 知识 答案 详解 课后 复习 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
