 沪教版九年级化学探究制取氧气需要的催化剂探究专题.docx
沪教版九年级化学探究制取氧气需要的催化剂探究专题.docx
- 文档编号:29734282
- 上传时间:2023-07-26
- 格式:DOCX
- 页数:15
- 大小:300.24KB
沪教版九年级化学探究制取氧气需要的催化剂探究专题.docx
《沪教版九年级化学探究制取氧气需要的催化剂探究专题.docx》由会员分享,可在线阅读,更多相关《沪教版九年级化学探究制取氧气需要的催化剂探究专题.docx(15页珍藏版)》请在冰豆网上搜索。
沪教版九年级化学探究制取氧气需要的催化剂探究专题
探究制取氧气需要的催化剂
1.学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:
氧化铜[CuO]能否起到类似MnO2的催化剂作用呢?
于是进行了以下探究。
(猜想)
Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质都不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质都发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后_____________________________________。
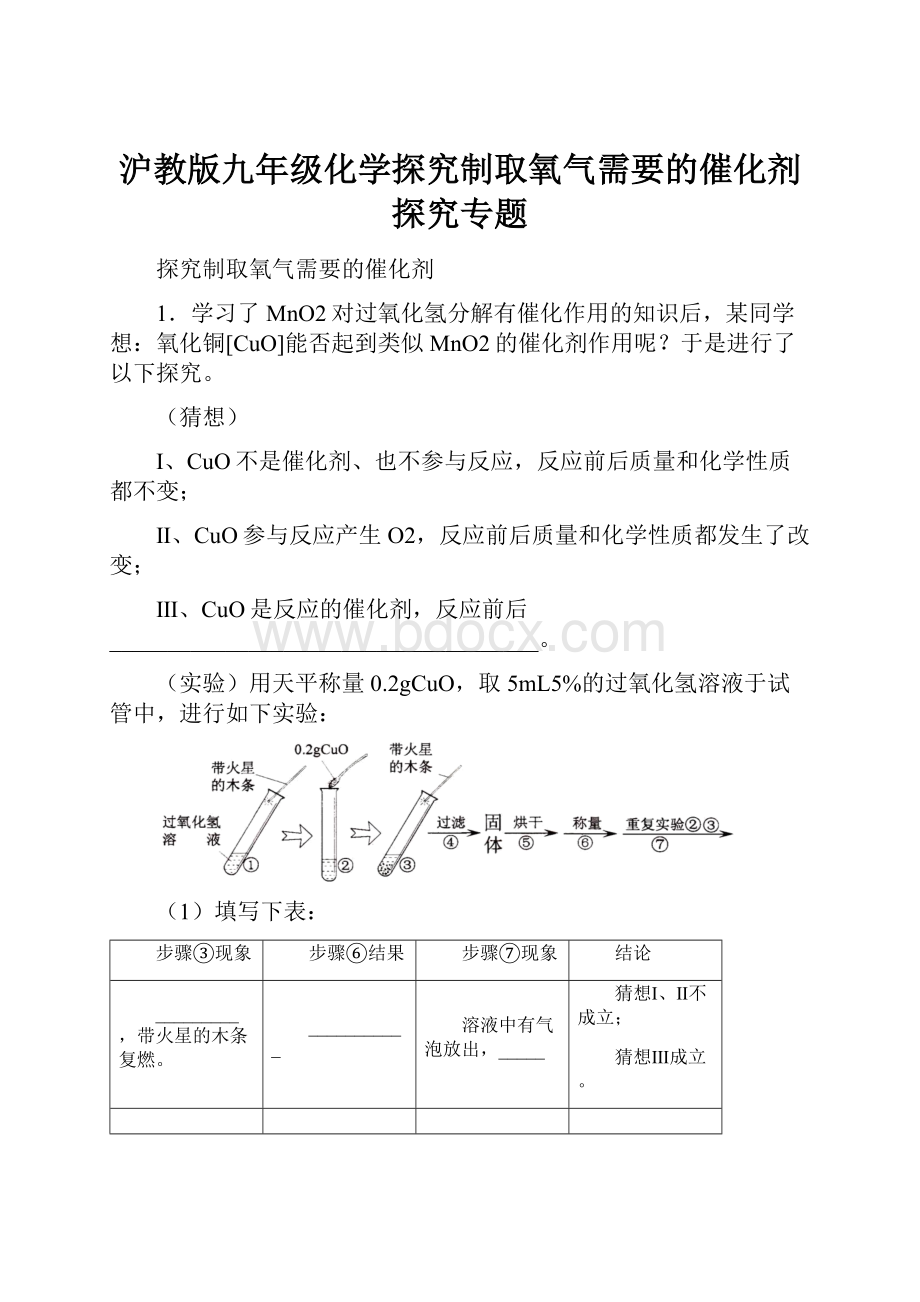
(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
步骤③现象
步骤⑥结果
步骤⑦现象
结论
_________,带火星的木条复燃。
___________
溶液中有气泡放出,_____
猜想Ⅰ、Ⅱ不成立;
猜想Ⅲ成立。
(2)过氧化氢能被CuO催化分解放出O2的符号表达式为_____________________________。
(实验拓展):
(3)某同学想比较二氧化锰和氧化铜对过氧化氢分解的催化效果,他需要对某些变量进行控制,其中包括有:
_____________________________________________________________。
(至少三点)
2.小玲同学在探究二氧化锰在过氧化氢分解中作催化剂中,设计了以下探究实验。
请根据题意答题
(1)实验报告
实验步骤
用带火星的木条检验时的现象
I.向试管①中倒入5mL30%的过氧化氢溶液
不复燃
Ⅱ.给试管①稍微加热,如图甲
不复燃
Ⅲ.向试管②中加入5mL30%的
过氧化氢溶液和少量二氧化锰
产生大量气泡,带火星的木条复燃
(2)小玲在步骤Ⅱ的装置中,加装了一个U形管(如图乙装置)后,带火星的木条较易复燃。
利用图甲装置做实验时,带火星的木条难复燃的原因是_________________________________;改用乙装置后带火星的木条能够复燃,装置中冰水的作用是_________________________________。
(3)小玲由此还想到了一个问题:
能使带火星的木条复燃的气体一定是纯氧气吗?
小玲设计的实验如下:
如丙图所示,按下表所示比例,用排水法收集部分氧气,分别得到五瓶空气和氧气的混合气体,进行木条复燃的实验。
实验编号
空气体积分数%
排水积分数%
带火星的木条复燃情况
1
85
15
火星稍变亮,不复燃
2
80
20
火星明亮,时燃时不燃
3
75
25
复燃
4
70
30
复燃
5
50
50
复燃
通过以上实验,可以得出的结论是___________________________________________________。
(4)小玲通过步骤Ⅲ得出二氧化锰能加快过氧化氢分解的结论,但小玮同学提出质疑:
过氧化氢溶液由水和过氧化氢组成,也可能是二氧化锰加快水的分解产生氧气。
请你设计一个实验证明小玮的猜想_________________________________________________(请写出操作步骤和实验现象)。
3.为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
(1)请写出实验室中H2O2制取氧气反应的符号表达式_________________________________。
(定性研究)
(2)如图甲,可通过观察______________________________________来定性比较两者的催化效果。
(定量研究)
(3)如图乙,实验中注射器的作用是____________________________。
要定量比较两者的催化效果,可测量生成等体积气体所需的___________________________________________。
(深入研究)
(4)老师认为该研究小组证明FeCl3溶液或CuSO4溶液可作H2O2制取氧气的催化剂的实验,除了要探究上述问题外,还应对它们在化学反应前后的_________________和__________________进行实验探究。
4.某化学兴趣小组对“氧化铜能否作过氧化氢分解的催化剂“进行了探究
(实验探究)
实验编号
实验操作
实验现象
实验分析或结论
实验分析
实验结论
①
有少量气泡;木条不复燃
过氧化氢能分解,但是
_______________
氧化铜是过氧化氢分解的催化剂
②
__________________
氧化铜能加快过氧化氢分解
(1)写出实验②中反应的符号表达式:
_____________________________________________。
(交流反思)实验过程中加入到两支试管里的过氧化氢溶液应满足的要求有______________________。
①体积相同②浓度相同③温度相同
(2)小明同学认为仅由上述实验还不能完全得出表内的“总结”,他补充设计了以下两个探究实验
实验一:
称量反应后固体质量,并与反应前的称量数据作比较,其目的是________________。
实验二:
另取5mL5%的过氧化氢溶液于试管中,再向其中加入实验②反应后的固体剩余物,如图1所示,其目的是证明___________________________________________________。
(实验拓展)小红同学用MnO2、CuO两种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球探究分解过氧化氢溶液制取氧气的适宜催化剂。
实验操作:
取30粒含MnO2的海藻酸钠微球,采用图1装置进行实验。
改用另一种微球,分别重复上述实验,得到图2的锥形瓶内压强随时间变化的曲线图。
(3)每次实验时,海藻酸钠微球数应相同的原因是__________________________________。
(4)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是______________________。
(5)从实验曲线看,催化效果较好、反应温和的催化剂是______________________________。
5.小明通过实验发现氧化铜也能作过氧化氢分解的催化剂,为比较氧化铜和二氧化锰对过氧化氢分解的催化效果,某研究小组进行了如下探究:
(1)(定性探究)
如图甲,可通过观察_____________________________来定性比较两者的催化效果。
(2)写出过氧化氢在氧化铜的催化作用下发生的反应的符号表达式_____________________________。
(3)(定量探究)为了定量比较两者的催化效果,实验时小红用图乙所示装置做对照实验,以生成40mL气体为标准,其他可能影响实验的因素均已忽略,设计了下列三组实验。
实验序号
5%过氧化氢溶液
其他物质质量
待测数据
①
20mL
②
20mL
氧化铜0.5g
③
20mL
二氧化锰0.5g
实验前检查图乙装置气密性的方法是___________________________________________。
(4)上述实验应测量的“待测数据”是指____________________________________。
(5)实验②比实验①的待测数据”更_______________(填“大”、“小”、“不确定”)。
(6)要比较氧化铜和二氧化锰对过氧化氢分解的催化效果,还可以测量_________________________。
6.实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气。
I、写出该反应的符号表达式____________________________________________。
II、小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
(完成实验)按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
实验编号
实验药品
分解温度(℃)
①
KClO3
580
②
KClO3、MnO2(质量比1∶1)
350
③
KClO3、CuO(质量比1∶1)
370
④
KClO3、Fe2O3(质量比1∶1)
390
(分析数据、得出结论)
(1)由实验______与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是______________________。
(反思)
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和_________不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证:
__________________________________________________________________________。
7.(探究活动一)为探究催化剂的种类对氯酸钾分解速率的影响,甲同学设计如表对比实验:
氯酸钾的质量
催化剂的种类
MnO2的质量
反应条件
收集45.0mLO2所需的时间(S)
Ⅰ
3.0g
MnO2
1.0g
混合加热
21
Ⅱ
xg
CuO
1.0g
混合加热
48
(1)表Ⅱ中x的值应为________;通过分析上表数据,可以得出的实验结论是:
在相同的条件下,KCLO3在MnO2作催化剂比CuO作催化剂的分解速率__________(选填“快”或“慢”)
(探究活动二)为探究双氧水浓度对过氧化氢分解速率的影响,乙同学设计以下实验:
[进行实验]
室温下,选用50.0g不同溶质质量分数的双氧水(1%、2%和4%)分别与0.1g二氧化锰进行实验(如图1,固定夹持仪器略去).
(2)MnO2在H2O2分解前后其质量和__________没有发生改变。
(3)按下图装置图1进行实验,在装药品前应检查该装置的气密性,具体做法是关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后______________则证明该装置气密性良好。
[数据处理]
(4)乙同学进行实验后,获得的相关实验数据记录如表所示:
双氧水的质量
双氧水的浓度
MnO2的质量
温度
相同时间(10S)内产生O2体积(mL)
Ⅰ
50.0g
1%
0.1g
20℃
9
Ⅱ
50.0g
2%
0.1g
20℃
16
Ⅲ
50.0g
4%
0.1g
20℃
31
①本实验中,测量O2体积的装置也可以选用如图2的哪套装置来代替_____(填编号)。
②分析上表数据,可以得出不同浓度的双氧水对过氧化氢分解速率影响的结论是:
____________。
[拓展延伸]
(5)丙同学认为用图3装置进行实验,通过比较__________也能探究双氧水浓度对过氧化氢分解速率的影响。
(6)暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见如图,集气瓶中原有37mL的水).以下对此改进实验的叙述,试计算此实验测出氧气的体积分数约是______?
8.某兴趣小组同学对实验室制备氧气的条件进行探究实验。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计对比实验:
Ⅰ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热;
Ⅱ.将xg氯酸钾与1.0g氧化铜均匀混合加热。
在相同温度下,比较两组实验产生氧气的快慢。
Ⅰ中反应的符号表达式是__________________________________,Ⅱ中x的值应为_______。
(2)乙探究了影响双氧水分解速度的某种因素。
实验数据记录如下:
双氧水的质量(g)
双氧水的浓度
二氧化锰的质量(g)
相同时间内产生氧气的体积(mL)
Ⅰ
50.0
1%
0.1
9
Ⅱ
50.0
2%
0.1
16
Ⅲ
50.0
4%
31
①取用二氧化锰的仪器是_________________,实验Ⅲ中,加入二氧化锰的质量为________g。
②实验结论:
在相同条件下,___________________________________,双氧水分解得越快。
9.化学实验小组同学在实验室用过氧化氢溶液制氧气。
(1)用过氧化氢和二氧化锰反应的化学方程式为:
_________________________________________。
(2)同学们发现反应时有白雾产生,用如下两个装置来找原因,其目的是:
____________________。
同时又展开了下列思考与探究:
(3)催化剂MnO2的用量对反应速率是否有影响呢?
他们做了这样一组实验:
每次均用30mL10%的H2O2溶液,采用不同质量MnO2粉末做催化剂,测定各次收集到500mL氧气所用的时间,结果如下:
(其它实验条件均相同)
实验次序
1
2
3
4
5
6
7
8
9
10
MnO2粉末用量(克)
0.1
0.2
0.3
0.4
0.5
0.6
0.7
0.8
0.9
1.0
所用时间(秒)
17
8
6
3
2
2
2
2
2
2
请根据表中数据回答,MnO2粉末的用量对反应速率的影响是________________________________。
(4)H2O2溶液的溶质质量分数对反应速率是否有影响呢?
小组同学又做了一组实验:
每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验。
记录数据如下:
(实验均在20℃室温下进行,其它实验条件均相同)
实验次序
1
2
3
4
5
6
7
8
H2O2溶液溶质质量分数
1%
3%
5%
10%
15%
20%
25%
30%
MnO2粉末用量(克)
0.2
0.2
0.2
0.2
0.2
0.2
0.2
0.2
收集到540mL气体时所用时间(秒)
660
220
205
80
25
9
4
3
分析表中数据可得出的结论是____________________________________________。
(3)实验反思:
MnO2颗粒的大小对反应速率是否有影响?
请设计实验证明(语言叙述,不用画装置图)______________________________________________________________。
10.某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。
为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:
用26mgMnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:
用5mL1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。
(解释与结论)
(1)过氧化氢溶液制取氧气的化学方程式为_________________________________。
(2)实验1得到的结论是____________________________________。
实验2的目的是____________。
欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比_______________。
(简要的写出实验设想)
(3)小组同学通过互联网得知:
多种物质能催化过氧化氢的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42﹣),稀硫酸中含有三种粒子(H2O、H+、SO42﹣)为了进一步探究CuSO4,溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H2O,他们的理由是_____________________________________________。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
实验步骤
实验现象
结论
a取一支试管加入5mL5%过氧化氢溶液,然后加入2﹣3滴稀硫酸
溶液几乎没有
气泡放出
验证明,起催化作用的是_______________。
b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2﹣3滴硫酸铜溶液
溶液中有大量气泡放出
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是______________________________________________、__________________________________________。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?
__________________________。
理由是___________________________________________________________。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 沪教版 九年级 化学 探究 制取 氧气 需要 催化剂 专题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
