 电位滴定.docx
电位滴定.docx
- 文档编号:29651871
- 上传时间:2023-07-25
- 格式:DOCX
- 页数:10
- 大小:163.37KB
电位滴定.docx
《电位滴定.docx》由会员分享,可在线阅读,更多相关《电位滴定.docx(10页珍藏版)》请在冰豆网上搜索。
电位滴定
测量仪器与参比电极
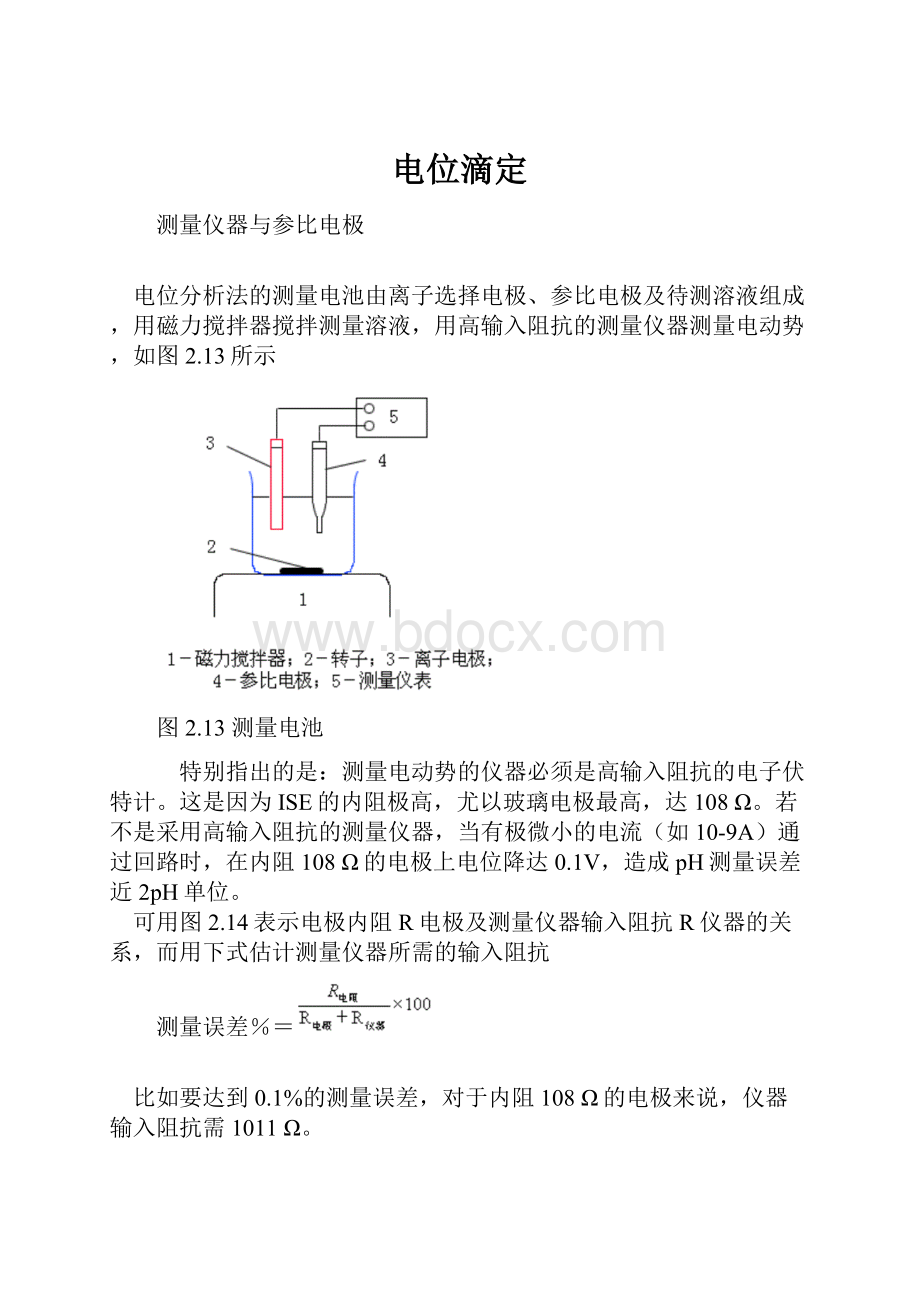
电位分析法的测量电池由离子选择电极、参比电极及待测溶液组成,用磁力搅拌器搅拌测量溶液,用高输入阻抗的测量仪器测量电动势,如图2.13所示
图2.13测量电池
特别指出的是:
测量电动势的仪器必须是高输入阻抗的电子伏特计。
这是因为ISE的内阻极高,尤以玻璃电极最高,达108 Ω。
若不是采用高输入阻抗的测量仪器,当有极微小的电流(如10-9A)通过回路时,在内阻108 Ω的电极上电位降达0.1V,造成pH测量误差近2pH单位。
可用图2.14表示电极内阻R电极及测量仪器输入阻抗R仪器的关系,而用下式估计测量仪器所需的输入阻抗
测量误差%=
比如要达到0.1%的测量误差,对于内阻108 Ω的电极来说,仪器输入阻抗需1011 Ω。
参比电极:
要求:
可逆性、重现性、稳定性;
类型:
氢电极、Ag/AgCl、Hg/Hg2Cl2(甘汞电极);
最常使用的是饱和甘汞电极(SCE)。
该电极25℃时电位为0.2438V,稳定性很好,但使用温度不能超过80℃。
否则Hg2Cl2发生歧化反应。
甘汞电极测量时温度滞后现象较为严重。
图2.14测量仪器的输入阻抗
活度与浓度
Nernst方程式表示的是电极电位与离子活度之间的关系式,而对于分析化学来说,测定的是离子浓度而不是活度,活度与浓度的关系为:
γ为活度系数,由溶液的离子强度所决定。
所以电位方程式变换为:
为此,在系列的测量中必须使γ基本不变,才不会影响测定系列的结果,在电位分析法中通过加入总离子强度调节缓冲剂(TISAB)来实现的。
在实际工作中,TISAB所含的成分有三个作用:
控制一定的离子强度,控制一定的测量酸度,含有络合剂可掩蔽干扰离子。
直接电位法
1.直接比较法--也称直读法
如测量离子A,组成电池为:
则
先测定标准溶液pAs的电动势Es,再测未知溶液pAx的电动势Ex
得到
(阳离子为+,阴离子为-)
在实际测量中,需用两个不同浓度的标准溶液pAs1、pAs2,且pAs1 2.标准曲线法--适于大批量且组成较为简单的试样分析 配制一系列(一般为5个)与试样溶液组成相似的标准溶液Ci,与试样溶液同样加入TISAB,分别测量E(或φ)。 绘制E~lgCi(或E~pCi)标准曲线,由未知试样溶液所测的Ex从曲线中求得Cx。 3.标准加入法--也称添加法 将小体积――Vs(一般为试液的1/50~1/100)而大浓度――Cs(一般为试液的100~50倍)的待测组分标准溶液,加入到一定体积的试样溶液中,分别测量标准加入前后的电动势,从而求出Cx。 可分为单次标准加入法和连续标准加入法两种。 (1)单次标准加入法 按照上述测量电池的构成图示式,对于阳离子的测量来说先测量体积为Vx的试样溶液的电动势Ex,则 再加入浓度为Cs,体积为Vs的标准溶液后测定 ,则 (标准加入前后测量溶液的组份基本不变) 则 整理后得到 (S为ISE的实际响应斜率,而非 ) 当Vs< 若是测定阴离子,则 ,而Cx的结果表达式和上式一样。 因此,测定阴阳离子的统一式为 (2)连续标准加入法--格兰(Gran)作图法 在测定过程中,连续多次(3~5次)加入标准溶液,多次测定E值,按照上述电池的图示式,对于阴离子测量来说,每次E值为 变换整理后得: 所以 与 成线性关系。 图2.15连续标准加入法曲线 每次加入Vs(累加值),测出一个E值,并计算出 的值,绘制 ~Vs曲线,如图2.15所示,延长直线交于Vs轴的Vs'(呈负值), 即 : 也就是: 所以: (对于阳离子,则前面函数式中指数项的指数为负值,即 及 其余不变) 上述的计算是很复杂的,1969年格兰作图法用于直接电位法。 格兰作图法是采用一种半反对数的格兰坐标纸,直接作E~Vs曲线,结果的计算公式同上。 使用格兰坐标纸时要注意到: ―― 坐标纸的纵坐标是以10%体积变化率校正的半反对数,规定一价离子的响应斜率为58mV,而10E/S以105/58为单位设计,即纵坐标每大格为5mV。 ―― 横坐标以Vx取100mV设计,每大格为1mL(若Vx取50mL,每格Vs为0.5mL)。 ―― 若ISE的响应斜率S不是58mV,应进行空白试验。 格兰作图法如图2.16所示 4.直接电位法的误差 直接电位法测定浓度结果的误差主要由电动势E的测量误差引起的。 或 则相对误差 或 (E的单位为伏特) 若E测量误差为±0.1mv时,测定一价离子的浓度相对误差为±0.4%,二价离子为±0.8%。 电位滴定法的原理和装置 电位滴定法与直接电位法的不同在于,它是以测量滴定过程中指示电极的电极电位(或电池电动势)的变化为基础的一类滴定分析方法。 滴定过程中,随着滴定剂的加入,发生化学反应,待测离子或与之有关的离子活度(浓度)发生变化,指示电极的电极电位(或电池电动势)也随着发生变化,在化学计量点附近,电位(或电动势)发生突跃,由此确定滴定的终点。 因此电位滴定法与一般滴定分析法的根本不同是确定终点的方法不同。 电位滴定法的装置由四部分组成,即电池、搅拌器、测量仪表、滴定装置,如图2.17所示。 滴定终点的确定 滴定终点的确定: 有作图法和二级微商计算法两种 1.作图法 ―― 作φ~V曲线(即一般的滴定曲线),以测得的电位φ(或电动势E)对滴定的体积V作图得到图2.18(a)的曲线,曲线的突跃点(拐点)所对应的体积为终点的滴定体积Ve。 ―― 作△φ/△V~V曲线(即一级微分曲线),对于滴定突跃较小或计量点前后滴定曲线不对称的,可以用△φ/△V(或△E/△V)对△V相应的两体积的平均值(即 )作图,得到图2.18(b)的曲线,曲线极大值所对应的体积为Ve。 ―― 作△2φ/△V2~V曲线(即二级微商曲线),以△2φ/△V2(或△2E/△V2)对二次体积的平均值(即 )作图,得到图2.18(c)曲线,曲线与V轴交点,即△2φ/△V2=0所对应的体积为Ve。 ―― 作△V/△φ~V曲线,只要在计量点前后取几对数据,以△V/△φ对V作图,可得到两条直线,图2.18(d)所示,其交点所对应的体积为Ve。 2.二级微商计算法 从二级微商曲线可见,当△2φ/△V2的两个相邻值出现相反符号时,两个滴定体积V1,V2之间,必有△2φ/△V2=0的一点,该点对应的体积为Ve。 用线性内插法求得φe、Ve: 自动电位的滴定 以前及目前还有不少使用自动电位滴定的装置如图2.19所示。 在滴定管末端连接可通过电磁阀的细乳胶管,此管下端接上毛细管。 滴定前根据具体的滴定对象为仪器设置电位(或pH)的终点控制值(理论计算值或滴定实验值)。 滴定开始时,电位测量信号使电磁阀断续开关,滴定自动进行。 电位测量值到达仪器设定值时,电磁阀自动关闭,滴定停止。 现代的自动电位滴定已广泛采用计算机控制。 计算机对滴定过程中的数据自动采集、处理,并利用滴定反应化学计量点前后电位突变的特性,自动寻找滴定终点、控制滴定速度,到达终点时自动停止滴定,因此更加自动和快速。 滴定类型及指示电极的选择 ∙酸碱滴定: 可以进行某些极弱酸(碱)的滴定。 指示剂法滴定弱酸碱时,准确滴定的要求必需 ≥10-8,而电位法只需大于等于10-10;电位法所用的指示电极为pH玻璃电极。 ∙氧化还原滴定: 指示剂法准确滴定的要求是滴定反应中,氧化剂和还原剂的标准电位之差必需△φo≥0.36V(n=1),而电位法只需大于等于0.2V,应用范围广;电位法采用的指示电极一般采用零类电极(常用Pt电极)。 ∙络合滴定: 指示剂法准确滴定的要求是,滴定反应生成络合物的稳定常数必需是 ≥6,而电位法可用于稳定常数更小的络合物;电位法所用的指示电极一般有两种,一种是Pt电极或某种离子选择电极,另一种却是Hg电极(实际上是第三类电极)。 ∙沉淀滴定: 电位法应用比指示剂法广泛,尤其是某些在指示剂滴定法中难找到指示剂或难以进行选择滴定的混合物体系,电位法往往可以进行;电位法所用的指示电极主要是离子选择电极,也可用银电极或汞电极。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 电位 滴定
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
