 九年级化学竞赛资料工业流程图.docx
九年级化学竞赛资料工业流程图.docx
- 文档编号:29573425
- 上传时间:2023-07-24
- 格式:DOCX
- 页数:20
- 大小:581.27KB
九年级化学竞赛资料工业流程图.docx
《九年级化学竞赛资料工业流程图.docx》由会员分享,可在线阅读,更多相关《九年级化学竞赛资料工业流程图.docx(20页珍藏版)》请在冰豆网上搜索。
九年级化学竞赛资料工业流程图
2016-2017化学竞赛专题辅导资料---工艺流程题
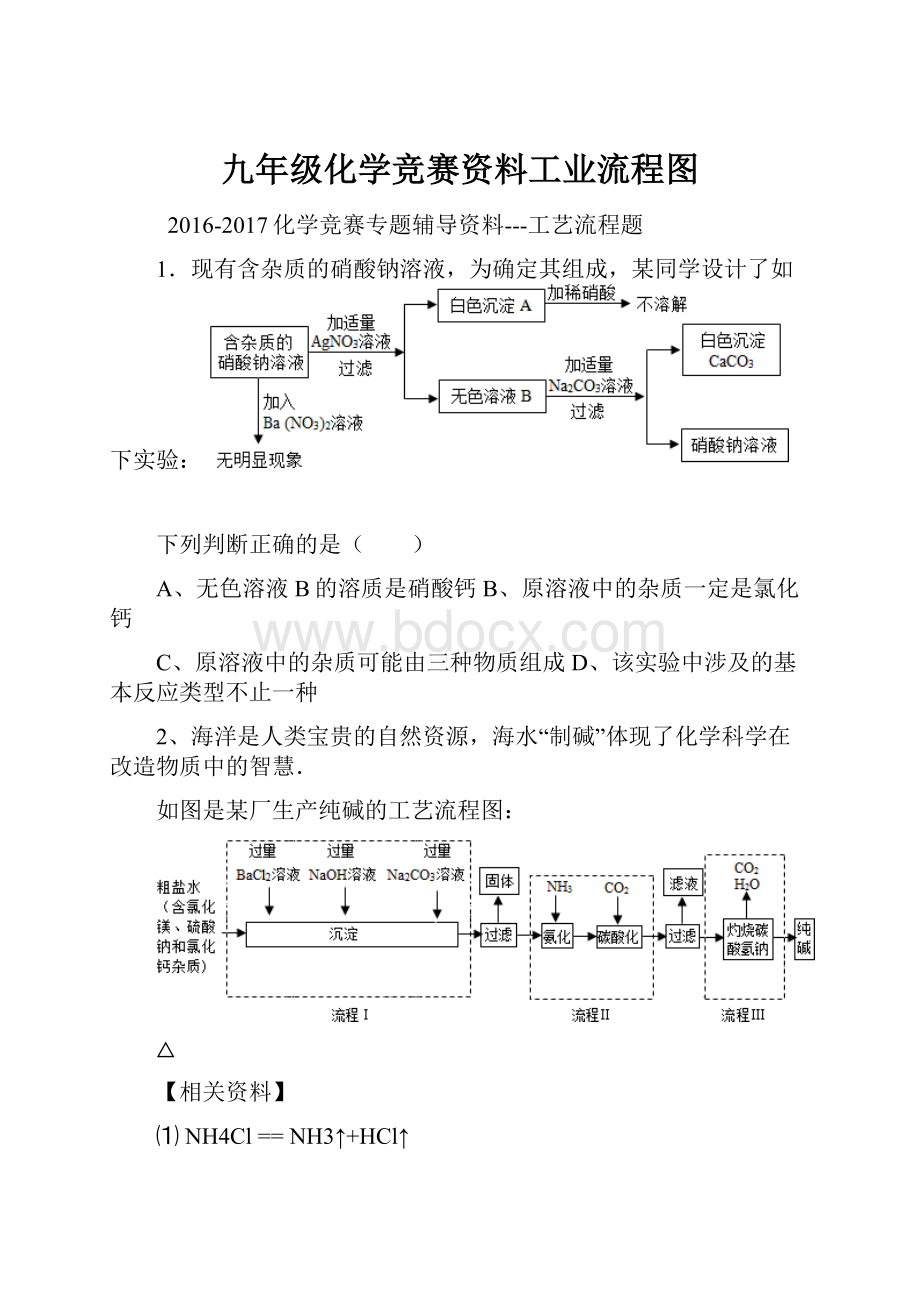
1.现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验:
下列判断正确的是( )
A、无色溶液B的溶质是硝酸钙B、原溶液中的杂质一定是氯化钙
C、原溶液中的杂质可能由三种物质组成D、该实验中涉及的基本反应类型不止一种
2、海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧.
如图是某厂生产纯碱的工艺流程图:
△
【相关资料】
⑴NH4Cl==NH3↑+HCl↑
⑵已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
物质
NaCl
NaHCO3
NH4Cl
NH3
CO2
溶解度
36.0g
9.6g
37.2g
710
0.9
请完成下列问题:
(1)该厂最终产品有 (填物质名称);
(2)流程I中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是 (填字母序号);
A.加入三种溶液的顺序不能调整B.加入三种溶液将粗盐水中的SO42﹣、Mg2+、Ca2+转化为沉淀C.按流程I所加溶液的顺序除杂,过滤后得到四中沉淀
(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化氨,氨气在制碱过程中的作用是 ;
(4)写出流程Ⅲ中发生反应的化学方程式 .
(5)滤液中含有的溶质有(至少写两种)
(6)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是。
海底矿产资源“可燃冰”,其主要成分是水合甲烷晶体(CH4·nH2O),若水合甲烷晶体中CH4的质量分数为10%,则水合甲烷晶体的化学式为。
3、粗盐中含泥沙、氯化钙、氯化镁等杂质,某同学自制的简易净水器中放置物质的顺序错误,使
净水效果不理想。
(1)请按由上到下的顺序重新排列________(填字母)。
调整后净化的盐水仍含可溶性杂质,他设计了下面的除杂流程:
(2)步骤①②都需要进行__________操作,步骤④需要进行操作。
(3)已知试剂X是碱溶液,则沉淀I为_______(写化学式),下列碱溶液不符合要求的是______(填序号)。
A.氢氧化钠溶液B.氢氧化钡溶液C.氢氧化钾溶液D.氢氧化钙溶液
(4)步骤②除去氯化钙的反应方程式是__________;步骤③中发生中和反应的化学方程式是。
4、Na2SO4是制造纸张、药品、染料稀释剂等的重要原料。
某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图所示。
(1)加入NaOH溶液可除去的阳离子是(填离子符号),其反应的化学方程式为:
.。
若添加的NaOH溶液和Na2CO3溶液过量,可加入适量(填名称)除去。
(2)操作a的名称是,该操作中需要用到的玻璃仪器有烧杯、玻璃棒、。
(3)溶液M中的溶质是Na2SO4和杂质NaCl,观察题21—2图的溶解度曲线,则操作b是:
先将溶液M蒸发浓缩,再降温结晶、过滤。
降温结晶的最佳温度范围是℃以下,因为Na2SO4的溶解度。
5、以氯化钾和硫酸亚铁为原料生产硫酸钾和氧化铁(铁红颜料),其主要流程如下,请认真观察工艺流程,回答下列问题:
(1)铁红的化学式是 ;
(2)FeSO4与NH4HCO3反应生成FeCO3、(NH4)2SO4、H2O和CO2,其反应的化学方程式是 ;
(3)硫酸酸化是为了除去过量的NH4HCO3,反应后逸出的气体是 ;
(4)沉淀池Ⅱ中溶质有KCl、K2SO4、H2SO4,还含有 .
6、七水硫酸镁(MgSO4•7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在湿热干燥空气中易失去结晶水,工业上将白云石(主要成分为MgCO3,CaCO3)碳烧成粉,用于制取MgSO4•7H2O,工艺流程如图所示.
(1)煅烧过程中,MgCO3转化为MgO的基本反应类型是 ;
(2)写出MgO与H2SO4反应的化学方程式:
;
(3)操作a的名称为 ;
(4)将分离后的母液循环利用的目的是 ;
(5)干燥得成品时,需要控制的条件是 .
7、FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.
实验一:
(如图1)
(1)写出步骤①中发生的化学方程式 ,此反应的基本类型是 .
(2)步骤②中的操作a名称是 ;步骤③中加入稀盐酸的目的是 .
实验二:
该实验小组同学通过查阅资料,又进行了另一种尝试.
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3Cu(OH)2
开始沉淀的pH1.94.7
沉淀完全的pH3.26.7
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (数值范围)比较合适.
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整:
,把试纸显示的颜色与标准比色卡比较,读出该溶液的pH.
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理.
A.稀硝酸B.稀硫酸C.稀盐酸D.稀醋酸.
8、过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法.
已知:
温度过高过氧化物会分解生成氧化物和氧气.
方法1:
由Ca(OH)2为原料最终反应制得,其制备流程如图1:
查阅资料:
沉淀完全后,让初生成的沉淀与母液一起放置一段时间,这个过程称为“陈化”。
其作用的是:
1,去除沉淀中包藏的杂质。
2,让沉淀晶体生长增大晶体粒径,并使其粒径分布比较均匀。
方法2:
由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如图2:
(1)方法1中搅拌的目的是 .请将搅拌过程中发生反应的化学方程式补充完整:
CaC12+H2O2+2NH3•H2O+6 ═CaO2•8H2O↓+2NH4Cl.制备过程中除水外可循环使用的物质是 (填化学式).
(2)方法2中气体X是 ,实验室常用 溶液来吸收.煅烧后的反应是化合反应,也能生成CaO2•8H2O,反应的化学方程式为 .该反应需控制温度在0~2℃,可将反应器放置在 ,获得的CaO2产品中主要含有的固体杂质是 (填化学式).
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能 .
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2•8H2O的反应符合“绿色化学”的是 (填“方法1”或“方法2”).
9、硫酸工业的部分生产流程如下:
SO2
SO3→H2SO4
某硫酸生产厂以黄铁矿(主要成分为FeS2)为原料生产硫酸,首先将矿石粉吹入沸腾炉里燃烧,制得SO2,其反应可表示为:
□FeS2+□O2=□Fe2O3+□SO2.
(1)配平矿石粉在沸腾炉中燃烧的反应方程式.
(2)若以SO2为原料生产硫酸,其过程中的反应均为化合反应,写出其反应的化学方程式:
SO2→SO3:
_________ ;SO3+ _________ →H2SO4:
_________ .
(3)SO2→SO3的反应过程中,V2O5的作用是:
_________ .
(4)沸腾炉的炉渣主要成分为Fe2O3,可变废为宝用于炼铁.写出高炉炼铁主要反应的化学方程式:
.
(5)市售硫酸多为98%的浓硫酸,实验室常将浓硫酸稀释成稀硫酸使用.稀释操作时,必须将 _________ ,否则会造成危险.
10、下图是氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图,根据要求回答问题。
(1)铁的另两种常见氧化物的化学式是、。
(2)加水溶解过程中,在实验室里通常要使用的玻璃仪器有烧杯和,操作A的名称
是。
(3)副产品P是,由溶液N获得该副产品的操作顺序是b→→→d。
a.过滤b.加热浓缩c.冷却结晶d.晶体加热至完全失去结晶水
△
(4)通空气时的化学方程式是4Fe(OH)2+2H2O+O2===4Fe(OH)3,由沉淀M获得Fe3O4的过程中发生的反应为Fe(OH)2+2Fe(OH)3===Fe3O4+4H2O,控制“一定量空气”的目的是,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为。
(相对分子质量:
Fe(OH)2—90,Fe(OH)3—107)
11、某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程。
【工艺流程及原理】
沉淀池中发生的主要化学反应为:
CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
【讨论交流】
(1)操作a的名称是,若在实验室进行此操作,用到的玻璃仪器除玻璃棒、烧杯外,还需要。
(2)经操作a后得到的固体物质在煅烧炉中高温分解生成X和Y两种物质,该工艺中,Y被作为原料之一循环利用。
Y的化学式为。
(3)沉淀池中也可能生成少量NH4HCO3,该反应的化学方程式为。
【硫酸铵化肥等级测定】
(1)判断(NH4)2SO4化肥中有无NH4HCO3:
取少量试样溶于水,滴加足量的,无气泡产生,则可判断该化肥中不存在NH4HCO3。
(2)化肥中氮元素含量的测定(已确定该化肥中不存在NH4HCO3杂质):
优等品
合格品
氮(N)含量
≥21.0%
≥20.5%
查阅资料:
①已知:
(NH4)2SO4+2NaOH
Na2SO4+2NH3↑+2H2O,氨气极易溶于水,其水溶液为氨水。
氨水呈碱性,不稳定,易挥发。
②工业判断硫酸铵化肥等级指标如下:
实验设计:
按右图所示装置进行实验。
(1)实验过程中,往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3。
(2)烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是(填序号);
①水②浓HCl③稀H2SO4④NaOH溶液
烧杯中干燥管的作用是。
交流讨论:
实验小组的同学认为,用上述实验装置测得的结果可能会出现下列情况。
(1)甲同学认为:
应在实验装置A、B之间增加一个装有(填“浓硫酸"或“碱石灰”)的干燥装置,否则实验测得的硫酸铵化肥含氮量可能偏高。
(2)乙同学认为:
在实验装置A、B之间增加正确的干燥装置后进行实验,测得的硫酸铵化肥含氮量可能偏低,理由是。
实验测定:
经讨论后,他们改进了实验装置,排除了可能产生误差的因素,重新进行实验。
取硫酸铵化肥样品13.5g进行实验,测得B装置增重与反应时间的关系如右图所示。
请通过计算判断该化肥的等级。
计算过程:
该化肥的等级为品
12、某化工厂用石灰石和废铜屑等设计生产石青、波尔多液的工艺流程如下:
(1)X的化学式为。
(2)反应②中空气的作用是。
(3)石青的化学式为2CuCO3·Cu(OH)2,写出反应③的化学方程式。
(4)若反应④中硫酸铜、生石灰和水的化学计量数之比为1:
1:
1,则其化学方程式为。
参考答案:
(1)CO2;
(2)起氧化作用;(3)3CaCO3+3CuSO4+H2O
2CuCO3Cu(OH)2↓+CO2↑+3CaSO4;
(4)CuSO4+CaO+H2O=Cu(OH)2↓+CaSO4.
13、某校化学兴趣小组的同学开展了测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验。
他们设计了如下的实验方案:
(1)“操作1”的名称是___________,溶液M中的溶质(写化学式)。
(2)滴加CaCl2溶液应“过量”,否则会使测定的结果(填“偏大”或“偏小”),
确定CaCl2溶液是否过量的方法是___________________________________。
(3)该混合物中Na2CO3的质量分数是多少?
(写出解题过程,计算结果精确到0.1%)
参考答案:
(1)过滤;NaCl、CaCl2。
(2)偏小;取少量溶液M,滴入适量的碳酸钠,若有沉淀产生,则CaCl2溶液过量(其它正确的也可以)。
(3)
14、FeSO4•7H2O是一种重要的食品和饲料添加剂.某工业废渣主要成分是Fe2O3,还含有CaCO3和SiO2(既不溶于水也不溶于稀硫酸),实验室用此废渣制备FeSO4•7H2O的流程如图1:
请根据流程图回答下列问题:
(1)稀硫酸与粉末中的氧化铁反应的化学方程式为
(2)操作②所需要的玻璃仪器是:
烧杯、玻璃棒和 .
(3)经测定,滤渣中只含有CaSO4和SiO2,你认为实验室 (填“能”或者“不能”)用粉末状的石灰石与稀硫酸反应制二氧化碳.
(4)Fe与Fe2(SO4)3反应的化学方程式为 .
(5)硫酸亚铁的溶解度曲线如图2.待结晶完毕后,滤除晶体,用少量冰水洗涤2﹣3次.用冰水洗涤的目的是
Ⅰ、除去晶体表面附着的杂质;Ⅱ、 .
参考答案:
(1)Fe2O3+2H2SO4═Fe2(SO4)3+3H2O;
(2)漏斗;(3)能;
(4)Fe+Fe2(SO4)3═3FeSO4;
(5)用冰水洗涤可降低洗涤过程中绿矾的损耗.
15、有一种工业废水,其中含有大量的硫酸亚铁、少量硫酸铜和污泥。
某同学设计了一个既经济又合理的实验方案,制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜。
方案流程如下:
【查阅资料】FeSO4·7H2O受热易分解。
回答下列问题:
(1)步骤
中用到的玻璃仪器有烧杯、漏斗和____________。
(2)步骤
中需加入的物质是___________,目的是_________________________。
(3)步骤
中发生反应的化学方程式是_____________________________。
(4)步骤
的操作是蒸发浓缩、____________、过滤。
参考答案
(1)玻璃棒
(2)铁;将硫酸铜溶液中的铜全部置换出来;(3)Fe+H2SO4═FeSO4+H2↑(4)冷却结晶
16、控制化学反应的条件可以促进或抑制化学反应,更好使化学反应为人类造福.
(1)如图是科学家正在研究的二氧化碳循环利用技术:
①二氧化碳与氢气在催化剂、高温条件下,除生成甲醇(CH4O)外,还生成一种常温下为液态的化合物,写出反应的化学方程式 ,甲醇中碳元素的化合价为 .
②从图中分析得出的下列结论中,正确的是 (填序号)
A.该技术符合低碳经济的理念.
B.水生成氢气的过程中所用的催化剂一定是二氧化锰.
C.该技术有助于缓解全球面临的能源危机.
D.液化石油气、汽油、甲醇均有碳、氢、氧三种元素组成.
(2)汽油燃烧时氧气浓度越大,燃烧越剧烈,试从微观角度解释这是因为 (3)尿素[CO(NH2)2]对提高粮食产量具有重要的作用.人们控制条件可以使CO2和物质M发生反应:
CO2+2M═CO(NH2)2+H2O,物质M的化学式为 .
参考答案:
(1)①3H2+CO2==CH3OH+H2O﹣2②AC
(2)氧气浓度越大,一定体积内氧分子数目越多,氧气分子与汽油分子碰撞的次数越多,燃烧越剧烈(3)NH3
17、硬水受热后会产生水垢,水垢的主要成分是CaCO3和Mg(OH)2,其它成分不参与反应。
实验室由水垢制取纯净CaCl2固体的流程如下:
请按要求填空:
(1)酸A是人体胃酸的主要成分,酸A的化学式是;
(2)步骤②中生成沉淀的化学反应方程式是;
(3)步骤④加酸A的作用是;
(4)步骤⑤是利用的方法得到氯化钙固体。
参考答案:
(1)HCl
(2)Ca(OH)2+MgCl2==Mg(OH)2↓+CaCl2
(3)除去过量的氢氧化钙或中和过量的氢氧化钙(4)蒸发溶剂或蒸发结晶
18、工业上用铝土矿(主要成分是Al2O3以及少量Fe2O3、SiO2等)提取纯Al2O3作冶炼铝的原料。
提取的操作过程可以用以下流程图表示:
(提示,氢氧化铝沉淀在强碱性溶液中会溶解变成可溶性的盐(偏铝酸钠NaAlO2),这种盐的溶液在通入二氧化碳气体又会析出氢氧化铝沉淀)
(1)你认为第一部实验中过滤的目的是,得到的不溶物是(写化学式),写出滤液A中含有的溶质是,请写出其中任意一种溶质与过量NaOH溶液反应的方程式___________________________________________;第二步实验得到的沉淀物是
(2)步骤①步骤②都将用到同一种玻璃仪器是,在实验操作中的作用是
(3)实际操作过程中,步骤③后得到的沉淀进行加热可以得到纯净的氧化铝,写出的到氧化铝的方程式
参考答案:
⑴分离出不溶物SiO2SiO2A中的溶质是:
AlCl3、FeCl3、HCl
通电
方程式:
略沉淀物是:
Fe(OH)3⑵玻璃棒,作用是引流,防止液滴外溅
⑶2Al(OH)3====Al2O3+3H2O⑷2Al2O3====4Al+3O2
19、坐落于常熟的江苏常福电缆厂是一家以生产电缆类产品为主的企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:
零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.
甲同学根据已学知识,提出了一套回收方案:
乙同学在查阅资料后得知:
在通入空气并加热的务件下,铜可与稀硫酸在溶液中发生反应(方程式为:
2Cu+2H2SO4+O2
2CuSO4+2H2O),于是他提出了另一套方案:
(1)甲方案的②③三个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:
②;③.
(2)从环保角度对两套方案的不同部分进行比较,你认为(选填“甲”或“乙”)的方案更合理.理由是:
.
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是:
.丁又提出了疑问:
“如果铁过量,剩余的铁会混在红色粉末中,该用什么化学方法处理?
”.请提出你的想法.
(4)最后,老师肯定了同学们的积极思考,但同时指出:
方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.请写出使“绿矾”结晶的两种可能方法:
、(“绿矾”溶解度随温度升高而增大).
2015-2016化学竞赛专题辅导资料---工艺流程题参考答案
1、C
2、
(1) 碳酸钠、氯化铵
(2) BC
(3) 使溶液显碱性,有利于吸收二氧化碳,增大产率;
(4)2NaHCO3
Na2CO3+H2O+CO2↑;
(5)NaHCO3、NaCl、NH4Cl、NH4HCO3(四种中的任意两种)
3、
(1)(1分)BADC(错1个0分)
(2)(2分)过滤蒸发结晶(或蒸发,或蒸发浓缩)
(3)(2分)Mg(OH)2C
(4)(4分)CaCl2+Na2CO3==CaCO3↓+2NaClNaOH+HCl==NaCl+H2O
4、
(1)Mg2+;2NaOH+MgCl2═Mg(OH)2↓+2NaCl;稀硫酸;
(2)漏斗(或铁架台);
(3)30;在30℃以下比氯化钠小(或30℃以下硫酸钠的溶解度受温度影响比氯化钠大).
5、
(1)Fe2O3;
(2)FeSO4+2NH4HCO3=FeCO3+(NH4)2SO4+H2O+CO2↑ ;
(3)二氧化碳 ;(4)(NH4)2SO4 .
6、
(1)分解反应;
(2)MgO+H2SO4=MgSO4+H2O;(3)过滤;
(4)提高原料的利用率;(5)温度低于48.1℃
7、
(1)Fe+CuCl2=FeCl2+Cu,置换反应.
(2)过滤;除去过量的铁粉.
(3)2HCl+CuO=CuCl2+H2O;3.2﹣4.7
(4)在玻璃板上放一小片试纸,用玻璃棒蘸取待测液滴在pH上 (5)C
8、
(1)让药品混合均匀,充分接触,加快反应速率; H2O;NH4C1(填化学式).
(2)二氧化碳;氢氧化钠;Ca(OH)2+H2O2+6H2O=CaO2•8H2O;冰水混合物中;Ca(OH)2
(3)造成CaO2•8H2O分解;(4)方法2
9、
(1)4FeS2+11O2=2Fe2O3+8SO2
(2)SO2→SO3:
2SO2+O2=2SO3;SO3+ →H2SO4:
SO3+H2O=H2SO4
(3)催化作用(4)Fe2O3+3CO
2Fe+3CO2
(5)浓硫酸沿烧杯壁慢慢的倒入水中,并不断的用玻璃棒搅拌
10、
(1)FeO,Fe2O3
(2)玻璃棒;过滤(3)硫酸钠,c,a(4)使部分氢氧化亚铁转化成氢氧化铁,45:
:
107
11、【讨论交流】
(1)过滤;漏斗;CO2;(3)CO2+NH3+H2O=NH4HCO3
【硫酸铵化肥等级测定】
(1)盐酸(HCl)、硫酸(H2SO4)或硝酸(HNO3)等;
实验设计:
(2)③;防止倒吸;
交流讨论:
(1)碱石灰;
(2)缺少赶尽反应装置中残留氨气的装置(或有氨气残留在装置中)
计算过程:
解:
增重的3.4g为氨气的质最。
设13.5g样品中含有(NH4)2SO4的质量为x。
(NH4)2SO4+2NaOH
Na2SO4+2NH3↑+2H2O
13234
x3.4g
132:
34=x:
3.4g
解得:
x=13.2g
28/132×13.2g=2.8g
2.8g/13.5g×100%=20.7%
该化肥的等级为合格品
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 九年级 化学 竞赛 资料 工业 流程图
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
