 台州市椒江区泰来高复无机推断专题训练含答案.docx
台州市椒江区泰来高复无机推断专题训练含答案.docx
- 文档编号:2927189
- 上传时间:2022-11-16
- 格式:DOCX
- 页数:13
- 大小:219.51KB
台州市椒江区泰来高复无机推断专题训练含答案.docx
《台州市椒江区泰来高复无机推断专题训练含答案.docx》由会员分享,可在线阅读,更多相关《台州市椒江区泰来高复无机推断专题训练含答案.docx(13页珍藏版)》请在冰豆网上搜索。
台州市椒江区泰来高复无机推断专题训练含答案
台州市椒江区泰来高复无机推断专题训练(含答案)
(2011年1月21日星期五汪)
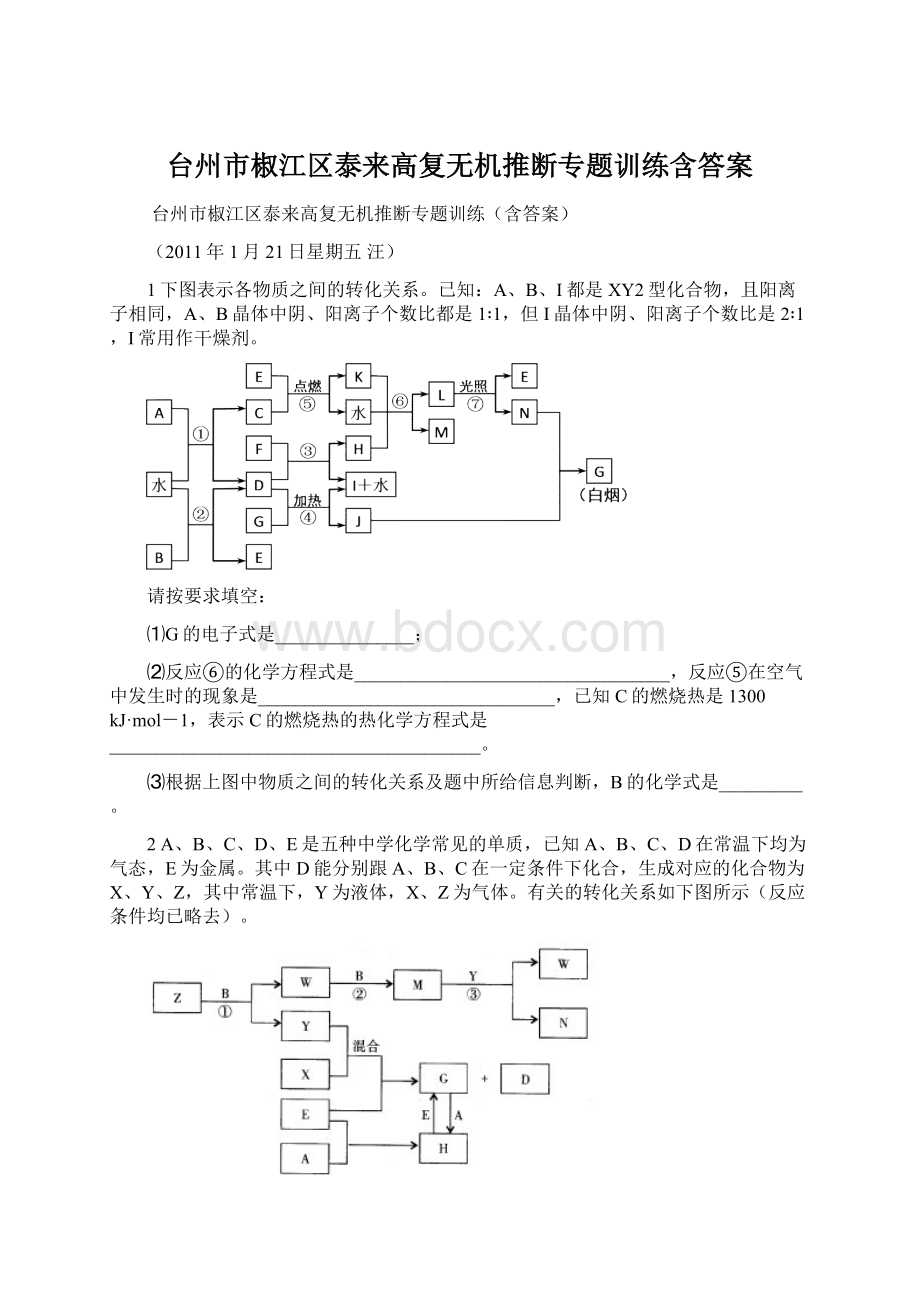
1下图表示各物质之间的转化关系。
已知:
A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
请按要求填空:
⑴G的电子式是_______________;
⑵反应⑥的化学方程式是__________________________________,反应⑤在空气中发生时的现象是________________________________,已知C的燃烧热是1300kJ·mol-1,表示C的燃烧热的热化学方程式是________________________________________。
⑶根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是_________。
2A、B、C、D、E是五种中学化学常见的单质,已知A、B、C、D在常温下均为气态,E为金属。
其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物为X、Y、Z,其中常温下,Y为液体,X、Z为气体。
有关的转化关系如下图所示(反应条件均已略去)。
回答下列问题:
⑴A的化学式为_______________;
⑵写出反应③的化学反应方程式___________________________________________;
⑶Z和W在催化剂作用下反应生成C和Y,这是一个很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为_______________________________;
⑷将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×
,则参加反应的E的质量为________g;
⑸将Z与N反应后的产物溶于水中,则常温该溶液的pH___7,其原因是(用离子方程式表示)___________________________________________。
3现有四种单质组成的合金A,为分析其成分,用此合金进行一系列实验,其过程及发生反应的现象如下图所示。
填写下列空白:
(1)A中含单质为为(写化学式);G的电子式为。
(2)写出A中的某单质与烧碱溶液反应的离子方程式________.
(3)写出固体F与硝酸反应的化学方程式,并标出电子转移的方向和数目
4:
根据下图中的反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
⑴单质L是__________________________
⑵化合物B是____________________
⑶图中除反应①以外,还有两个用于工业生产的反应,是________和________(填代号),它们的化学方程式分别是________________________________________和_____________________
5今将A、B、C、D四种固体投入水中,分别产生E、F、G、M四种气体,这四气体之间的反应如图所示:
I是一种遇空气变红棕色的气体,请填写下列空白:
A是_____________;B是_____________;C是_____________;D是_____________;
E是_____________;F是_____________;G是_____________;M是_____________。
6、如图所示A-J分别代表相关反应中的一种物质,已知A分解后得到等物质的量的B、C、D,图中有部分生成物未标出。
请填写以下空白
(1)B的电子式为_______________,D分子的空间构型为___________________-
(2)写出反应①、②的化学方程式:
①________________________________________________
②___________________________________________
(3)写出反应③的离子方程式_________________________________________________。
7.下图是无机物A~N在一定条件下的转化关系(部分产物及反应条件未列出)。
其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
N中只含有两种元素,N可作为工业生产C的原料。
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第__________周期_______族。
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_________(填写序号)。
(3)反应⑩的离子方程式是:
_____________。
(4)反应④的离子方程式是:
___________________________________。
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾).同时还生成KNO2和H2O。
该反应的化学方程式是:
________________________________________________________________(6)现有1molN参加反应,假设各步反应均完全,生成C的质量为490g,生成G的质量为224g,则反应①的化学方程式为_______________________。
8无机框图下图为中学化学中几种常见物质的转化关系(部分产物已略去)。
已知:
A、C、D是常见的气体单质,F气体极易溶于水,且液态常做致冷剂。
(1)写出化学式F,写出电子式G;
(2)鉴定G中阳离子的实验方法和现象__________________________________;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式、
。
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目。
9.下图是中学化学中常见物质之间的相互转化关系。
其中,X是气体单质,Y是液体化合物,Z是常见的碱且焰色反应为黄色;W、L是固体单质,K、I中含有相同的元素;反应①是高温下进行的工业上制取H的第一步反应。
请按要求填空:
(1)Y、Z的电子式分别为 Y、Z;
(2)写出下列反应的化学方程式:
①;
④;
⑨;
(3)反应⑩中生成1molL时,转移的电子数为。
10、根据下列框图关系填空。
已知反应①、③是工业生产中的重要反应,D、E常温下为气体、X常温下为五色液体,H与E相对分子质量之间的关系为:
Mr(H)-Mr(E)=34,又知C的焰色反应呈黄色。
(1)化合物B中所包含的化学键有___________________
(2)反应④的离子方程式:
________________________________
反应⑤的化学方程式:
________________________________
(3)已知每生成16gE,放出106.5kJ热量,则反应①的热化学方程式为:
11.下图中字母所代表的物质均为中学化学常见物质。
其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料;常温下C、D、H为气体单质。
单质E、M、N为金属,N是地壳中含量最大的金属元素。
Y是红褐色沉淀。
这些物质在一定条件下存在如下转化关系,其中有些反应物或生成物已经略去。
试回答下列问题:
⑴工业上,在电解A溶液的设备中将阴极区和阳极区用__________隔开,目的是
______________________________。
⑵Z→L反应的名称是_____,K的电子式为________。
⑶写出B→F的离子方程式____________________。
⑷写出K与CO2反应的化学方程式
_________________________________________________________。
⑸Y与NaClO和B混合溶液作用,是制备绿色水处理剂(Na2MO4)的一种方法,请写出有关反应的离子方程式
12、已知A为酸式盐,B为某二价主族金属(原子序数不超过20)的化合物,常温常压下C、D、F、G、I均呈气态,等物质的量A、B充分混合后加热能恰好完全反应。
图中反应条件(除加热)均已略去。
(1)写出A的化学式:
,B的电子式:
(2)写出下列反应的离子方程式:
①在A溶液中加入M
②向A的溶液中加入过量的NaOH溶液,并加热:
(3)如对气体G进行加压操作,产生的现象是:
发生反应的化学方程式
13、如图中A到J分别代表反应物中的一种常见物质,C、D、G在通常状态下是气体单质,其中C有刺激性气味,X、Y是常见的金属单质且X属于短周期元素。
W是由甲、乙两种元素按1:
1组成,其中甲元素的原子M层电子数是K层的一半,乙元素的原子最外层是次外层电子数的3倍。
参加反应的水和生成的水已从图中略去。
填写下列空白
(1)C是:
(化学式),Y元素在周期表中的位置是:
(2)用电子式表示W的形成过程:
(3)写出J+W+HO→G+A+H的离子方程式
设计实验分离F和H(写出加入试剂和操作方法)
14、在一定条件下(不需要添加别的反应物),经不同的化学反应,可实现如下图的各种反应。
其中,反应③、④、⑤属氧化还原反应,而反应 ①、②属非氧化还原反应。
X、F和Y为单质,且F是空气的主要组成成分之一,其余为化合物,据此请填空:
(1)物质A是 ,F是 ,X是 ,Y是 。
(2)写出反应②的化学方程式 。
15.已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。
现用A与石墨作电极,B的浓溶液作电解质,构成原电池。
有关物质之间的转化关系如下图:
(注意:
其中有些反应的条件及部分生成物被略去)
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
。
(2)从D溶液制备D的无水晶体的“操作a”为。
(3)反应②的化学方程式为 。
(4)反应⑤的化学方程式为 。
(5)原电池反应①中正极的电极反应式为。
16下图表示以NH4NO3和D物质为初始反应物发生的一系列变化。
在常温下,A为液体,F为不溶于水和碱溶液的白色固体,B、G和I为无色气体,G能使湿润的红色石蕊试纸变蓝。
请填空:
(1)D是_____________,E是___________,H是____________。
(2)写出下面反应的离子方程式:
④是_____________;⑤是_____________
17.下列物质均为中学化学常见物质转化关系图中,D为红棕色粉末反应条件及部分反应物、产物未全部说明
根据图示转化关系填写下列空白:
1写出下列物质的化学式A,B,G。
2C与D的混合物通常称填名称。
3写出下列化学方程式或离子方程式
I+JK离子方程式。
G+BH化学方程式。
答案
1.⑴
⑵Ca(ClO)2+CO2+H2O=CaCO3+2HClO火焰明亮并伴有浓烈黑烟
CH≡CH(g)+
O2(g)→2CO2(g)+H2O(l);ΔH=-1300kJ·mol-1⑶CaO2
2
(1)
(
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 台州市 椒江 泰来 无机 推断 专题 训练 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
